АЛГОРИТМ ВНУТРИАПТЕЧНОГО КОНТРОЛЯ ПРИ ЗАПОЛНЕНИИ ШТАНГЛАСА РЕЗОРЦИНОМ
• Работа с рецептом не проводится
Состоит в проверке исходных данных в «Журнале регистрации результатов контроля лекарственных средств на подлинность».
Состоит в проверке внешнего вида, запаха.
По приказу М3 РФ № 214 проводится качественный химический контроль при заполнении штангласа в ассистентской комнате.
• Контроль при отпуске
Больным не отпускается. Состоит в правильном оформлении штангласа. Штанглас должен быть оранжевого стекла, так как препарат легко окисляется на свету. На этикетке черными буквами по белому фону (препарат относится к общему списку) указано наименование лекарственного средства:
В помещении хранения на этикетке дополнительно указаны:
• номер серии завода-изготовителя;
• номер анализа контрольно-аналитической лаборатории;
В ассистентской комнате, кроме наименования, дополнительно указаны:
• подпись проверившего подлинность лекарственного средства;
• Оформление результатов контроля:
• записи в «Журнале регистрации результатов контроля лекарственных средств на подлинность»;
• номер анализа и подпись проверившего указать на этикетке шгангласа
ЗАНЯТИЕ 7
ВНУТРИАПТЕЧНЫЙ КОНТРОЛЬ МАЗИ САЛИЦИЛОВОЙ 2% — 30,0
Задачи
• Освоить внутриаптечный контроль мягких лекарственных форм.
• Изучить анализ салициловой кислоты.
Продолжительность занятия
2 академических часа (90 минут).
Вопросы для самоподготовки
• Внутриаптечный контроль мазей. Специфические показатели качества.
• Химический контроль салициловой кислоты. Способы извлечения действующего вещества из мазевой основы.
• Расчет. Оформление результатов контроля.
Материальное обеспечение
• раствор хлорида железа окисного;
• фталевый ангидрид (кристаллический).
Титрованные растворы и индикаторы:
• 0,1 моль/л раствор натрия гидроксида;
Посуда, приборы, оборудование:
• ручные весочки и разновес;
• химические стаканчики для титрования;
• мерные цилиндры на 10 мл;
• кусочки пергаментной бумаги.
Общие указания
Мазь — мягкая лекарственная форма, предназначенная для нанесения на кожу, раны или слизистые оболочки. Мазь состоит из основы и лекарственных веществ, равномерно в ней распределенных.
При анализе необходимо извлечь лекарственные вещества из мазевой основы. Чаще других используют следующие 2 способа извлечения действующих веществ:
• Основу растворяют в определенном растворителе. Например, жировые основы или углеводороды можно растворить в органических растворителях: хлороформе, эфире.
• Основу расплавляют на водяной бане, а действующее вещество извлекают подходящим растворителем: водой, спиртом, подкисленной водой и т.д. При охлаждении основа затвердевает, а полученный раствор действующих веществ сливают.
При органолептическом контроле мазей проверяют некоторые специфические показатели качества. Так, визуально определяют отсутствие расслаивания и механических включений. Однородность мазей проверяют по методике ГФ XI на биологическом микроскопе. В поле зрения микроскопа не должно быть частиц, размеры которых превышают нормы, установленные в частных статьях или другой нормативной документации.
Rp: Unguenli Acidi salicylici 2% — 30,0
D.S. Наносить на пораженные участки кожи.
Свойства
Светло-желтая однородная мазь, без запаха.
Подлинность
К 0,1 г мази прибавляют 2 мл воды и кипятят 1 минуту на водяной бане до расплавления основы. После охлаждения к водному извлечению добавляют 1-2 капли раствора хлорида окисного железа. Появляется фиолетовое окрашивание.
Количественное определение
Метод нейтрализации в спиртовой среде
0,5 I’ мази отвешивают на ручных весочках на кусочек пергаментной бумаги и помещают в стаканчик для титрования. Добавляют по 4—5 мл спирта и хлороформа, нейтрализованных по фенолфталеину, и нагревают на водяной бане при температуре 50-55°С в течение 10 минут.
После охлаждения прибавляют 2-3 капли фенолфталеина и титруют 0,1 моль/л раствором натрия гидроксида до розового окрашивания водного слоя.
1 мл 0,1 моль/л раствора натрия гидроксида соответствует 0,01381 г салициловой кислоты.
Хлороформ способствует растворению мазевой основы. Спирт не только растворяет салициловую кислоту, но и предотвращает гидролиз натрия салицилата.
Источник
ФЕНОЛЫ. АМИНОСПИРТЫ. ПРИЕМОЧНЫЙ КОНТРОЛЬ. ВНУТРИАПТЕЧНЫЙ КОНТРОЛЬ ПРИ ЗАПОЛНЕНИИ ШТАНГЛАСОВ И БЮРЕТОЧНЫХ УСТАНОВОК
Задачи
• Контроль и коррекция знаний по темам «Фенолы» и «Аминоспирты».
• Освоить приемочный контроль поступивших в аптеку лекарственных средств.
• Освоить внутриаптечный контроль при заполнении штангласов в помещениях хранения и в ассистентской.
Продолжительность занятия
2 академических часа (90 минут).
Вопросы для самоподготовки
• Общая характеристика фенолов и аминосниртов. Связь между химическим строением и действием на организм. Латинские, химические названия, получение, свойства, подлинность, испытания на чистоту, количественное определение, применение, хранение и отпуск резорцина, эфедрина гидрохлорида, адреналина и его препаратов.
• Приемочный контроль. Как поступают с лекарственными средствами в случае сомнения в их качестве?
• Оформление штангласов в помещениях хранения и в ассистентской.
• Химический контроль при заполнении штангласов в ассистентской резорцина, димедрола и серебра нитрата.
• Алгоритм внутриаптечного контроля при заполнении штангласов и бюреточных установок.
Материальное обеспечение
• кислота серная концентрированная;
• раствор гидроксида натрия;
• раствор гидроксида аммония;
• раствор нитрата серебра;
• раствор хлорида железа окисного;
• фталевый ангидрид (кристаллический).
Посуда, приборы, оборудование:
• колба емкостью 100 мл.
Общие указания
Приемочный контроль проводят с целью предупреждения поступления в аптеку некачественных лекарственных средств. Приемочный контроль заключается в проверке поступающих лекарственных средств на соответствие требованиям по показателям «Описание», «Упаковка», «Маркировка», а также наличия сертификатов качества и расчетных документов (счетов).
Конфоль но показателю «Описание» включает проверку внешнего вида и запаха. В случае сомнения в качестве лекарственных средств образцы направляются в территориальную контрольно-аналитическую лабораторию. Такие лекарственные средства с обозначением «Забраковано при приемочном контроле» хранятся в аптеке отдельно от других лекарственных средств.
При проверке по показателю «Упаковка» особое внимание обращается на ее целостность и соответствие физико-химическим свойствам лекарственных средств.
При конфоле по показателю «Маркировка» обращается внимание на соответствие оформления лекарственных средств действующим гребовани- ям. На этикетках должно быть указано:
• предприятие-изготовитель или предприятие, производившее фасовку;
• наименование лекарственного средс тва;
• масса или объем;
• конценфация или состав;
• номер анализа КАЛ;
У сердечных гликозидов указывают количество единиц действия в 1 г или 1 мл. Упаковки с ядовитыми и наркотическими веществами должны быть оформлены в соответствии с фебованиями действующих приказов и инструкций.
У лекарственных средств, предназначенных для изготовления растворов для инъекций или инфузий, должно быть указание «Годен для инъекций».
В помещениях хранения на всех штангласах с лекарственными средствами должны быть указаны:
• номер серии предприятия-изготовителя;
• номер анализа конфольно-аналитической лаборатории;
По приказу М3 РФ № 214 от 16.07.97 подвергаются качественному анализу обязательно’.
—■ все лекарственные средства, конценфаты и полуфабрикаты (в том числе гомеопатические настойки, тритурации, растворы, разведения), поступающие из помещений хранения в ассистентскую комнату, а в случае сомнения — и лекарственные средства, поступающие со склада;
• концентраты, полуфабрикаты и жидкие лекарственные средства в бюреточной установке и штангласах с пипетками при заполнении в ассистентской комнате.
В ассистентских комнатах на штангласах с лекарственными веществами должны быть указаны;
• подпись заполнившего штанглас;
• подпись проверившего подлинность лекарственного средства;
На штангласах с ядовитыми и сильнодействующими средствами должны быть указаны высшие и суточные дозы, а у стерильных лекарственных средств должна быть предупредительная надпись «Для стерильных лекарственных форм».
Штангласы с растворами, настойками и жидкими полуфабрикатами должны быть обеспечены нормальными каплемерами или пипетками. Число капель в определенном объеме должно быть установлено взвешиванием и обозначено на штангласе.
Заполнение штангласа, бюретки, штангласа с нормальным каплеме- ром должно производиться только после полного использования лекарственного средства и санитарной обработки.
Resorcinum
Резорцин
ОН
Свойства
Белый или белый со слабым желтоватым оттенком кристаллический порошок со слабым характерным запахом. Под влиянием света и воздуха постепенно окисляется и окрашивается в розовый цвет.
Растворимость
Очень легко растворим в воде и спирте^легко растворим в эфире, очень мало растворим в хлороформе, растворим в глицерине и жирном масле.
Подлинность
• Цветная реакция с хлоридом окисного железа
0,01 г препарата растворяют в 10 каплях воды, прибавляют 1 каплю раствора хлорида окисного железа. Появляется сине-фиолетовое окрашивание, переходящее от прибавления раствора аммиака в буровато-желтое.
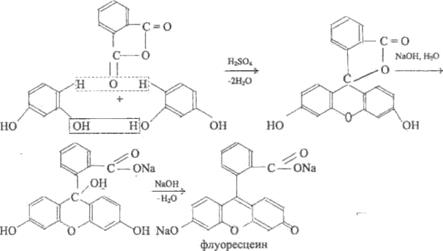
• Реакция образования флуоресцеина
При сплавлении в фарфоровой чашке нескольких кристаллов препарата с избытком фталевого ангидрида получается плав желто-красного цвета. При растворении плава в растворе едкого натра появляется интенсивная зеленая флюоресценция.
В хорошо Хранение
укупоренных банках оранжевого стекла.
ХранениеВ хорошо укупоренных банках оранжевого стекла.
Источник
Предупредительные мероприятия



Предупредительные мероприятия в аптеках заключаются в выполнении следующих требований:
1. Соблюдение санитарных норм и правил, противоэпидемического режима, а также условий асептического изготовления лекарственных средств в соответствии с действующими нормативными документами.
2. Соблюдение правил получения, сбора и хранения воды очищенной, воды для инъекций, своевременная санитарная обработка трубопровода, контроль за своевременным изъятием стерильных растворов, воды очищенной, воды для инъекций для испытания на стерильность в соответствии с действующими требованиями.
Сборники для воды очищенной, воды для инъекций должны иметь четкую надпись «Вода очищенная», «Вода для инъекций». На сборнике воды прикрепляется бирка с указанием даты ее получения, номера анализа и подписи проверившего. При одновременном использовании нескольких сборников, они должны быть пронумерованы.
3. Обеспечение исправности и точности приборов, аппаратов и весового хозяйства, регулярности их проверки.
4. Тщательный просмотр поступающих в аптеку рецептов и требования лечебных организаций с целью проверки правильности их выписывания; совместимости веществ, входящих в состав лекарственных средств, соответствие прописанных доз возрасту больного и наличия указаний о способах применения лекарственных средств.
5. Соблюдение технологии лекарственных средств (в том числе гомеопатических) в соответствии с требованиями действующей ГФ, нормативных документов, методических указаний.
6. Обеспечение в аптеке условий хранения лекарственных средств в соответствии с их физико-химическими свойствами и требованиями ГФ, действующих нормативных документов.
7. В помещениях хранения на всех штангласах с лекарственными средствами должны быть указаны: номер серии организации-изготовителя, номер анализа КАЛ (центра контроля качества лекарственных средств), срок годности, дата заполнения и подпись, заполнившего штанглас. На штангласах с лекарственными средствами, содержащими сердечные гликозиды, должно быть указано количество единиц действия в одном грамме лекарственного растительного сырья или в одном миллилитре лекарственного средства.
8. В ассистентских комнатах на всех штангласах с лекарственными веществами должны быть указаны: дата заполнения, подпись заполнившего штанглас и проверившего подлинность лекарственного вещества. На штангласах с ядовитыми и сильнодействующими лекарственными веществами должны быть указаны высшие разовые и суточные дозы, а на штангласах с лекарственными веществами, предназначенными для изготовления стерильных лекарственных форм, должна быть предупредительная надпись «Для стерильных лекарственных форм».
9. Штангласы с растворами, настойками и жидкими полуфабрикатами должны быть обеспечены нормальными каплемерами или пипетками. Число капель в определенном объеме должно быть установлено взвешиванием и обозначено на штангласе.
10. Заполнение штангласа, бюретки в бюреточной установке, штангласа с нормальным каплемером или пипеткой должно проводиться только после полного использования лекарственного средства и соответствующей обработки штангласа.
11. Номенклатура концентратов, полуфабрикатов и внутриаптечной заготовки лекарственных средств, изготовляемых в аптеках, должна утверждаться территориальной контрольно-аналитической лабораторией и доводиться до сведения всех аптек соответствующей территории. В данный перечень могут включаться только порошки, содержащие совместимые лекарственные вещества, на которые имеются методики анализа для химического контроля. В порядке исключения изготовление ароматных вод, внутриаптечные заготовки лекарственных средств для наружного применения, содержащих деготь, ихтиол, серу, нафталанскую нефть, коллодий, свинцовую воду, а также гомеопатических лекарственных средств, анализ которых не может быть осуществлен в условиях аптеки, производится под наблюдением провизора, занятого контролем качества лекарственных средств.
12. Руководителям аптеки необходимо один раз в квартал осуществлять контроль за соблюдением правил хранения

лекарственных средств в отделениях лечебных организаций, прикрепленных к аптеке.
В отделениях лечебных организаций не допускается изготовление лекарственных средств, расфасовка, перемещение из одной емкости (упаковки) в другую и замена этикеток. Лекарственные средства должны храниться в отделениях только в оригинальной (заводской, фабричной или аптечной) упаковке.
Для контроля за сроком годности на упаковке фасовки, отпускаемой аптекой в отделение лечебной организации, должна быть указана серия организации-изготовителя.
Лекарственные средства из аптек в лечебные организации должны отпускаться только уполномоченному медицинскому персоналу (приказ №214 от 16.07.97г.) «О контроле качества лекарственных средств, изготовляемых в аптечных организациях (аптеках)».
Источник