PsyAndNeuro.ru
Смертельный чай: ингибиторы ацетилхолинэстеразы
В этот понедельник немецкие врачи клиники Шарите (Берлин) лабораторно подтвердили [7], что Алексей Навальный, был отравлен ингибиторами ацетилхолинэстеразы (АХЭ). В связи с этим, мы решили написать небольшую статью о том, что это за вещества и как они работают в нервной системе.
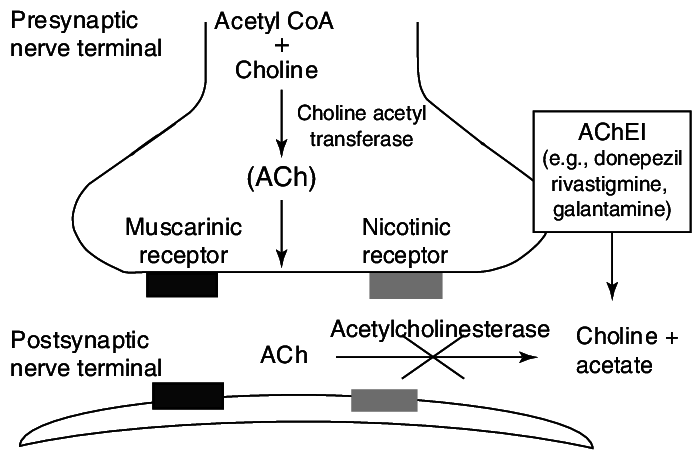
Ацетилхолин является одним из основных нейромедиаторов как в периферической, так и в центральной нервной системе. За его утилизацию в синаптической щели отвечает АХЭ (рис. 1). Соответственно, все вещества, которые прекращают или замедляют активность АХЭ, называются ингибиторами АХЭ и приводят к увеличенной концентрации ацетилхолина в синаптической щели.
Рис. 1 Схема действия АХЭ
Так как ацетилхолин является основным медиатором парасимпатической нервной системы, основные симптомы отравления ингибиторами АХЭ будут проявляться через усиление ее активности, то есть, у человека будет наблюдаться брадикардия, гипотензия, сужение просвета бронхов, также возможна диарея.
При длительном воздействии таких препаратов или при действии особо сильных ингибиторов АХЭ развивается холинергический криз, при котором мышцы не успевают отдохнуть от избыточной стимуляции ацетилхолином и, в результате, перестают на него реагировать. Клинически это проявляется вялым параличом и острой дыхательной недостаточностью. Лечение холинергического криза состоит во введении антагонистов холинергических рецепторов (атропин) и поддержании жизненно важных функций организма при помощи, например, ИВЛ (искусственной вентиляции лёгких). К сожалению, из-за узкой специфики ацетилхолина в центральной нервной системе, предсказать последствия такого отравления для когнитивных способностей является проблематичным.
Ингибиторы АХЭ применяются как в медицине, так и за ее пределами. В медицине ингибиторы АХЭ хорошо известны как лекарства для лечения болезни Альцгеймера, как например галантамин или физостигмин. Данные препараты, как правило, являются обратимыми ингибиторами АХЭ. Проще говоря, они выводят фермент из строя не навсегда.
Боевые отравляющие вещества или яды из группы ингибиторов АХЭ, как правило, необратимо связываются с активным центром фермента. В результате единственной возможной тактикой лечения такого отравления будут атропин и поддержание жизнедеятельности пациента до момента, пока организм не синтезирует в достаточном количестве АХЭ, а яд не начнёт выводиться из организма.
Самой известной группой таких ядов являются фосфорорганические соединения, сокращенно ФОС. Они широко используются, как в качестве инсектицидов в домашнем хозяйстве (дихлофос относится именно к этой группе веществ), так и в качестве боевых отравляющих веществ.
Механизм ФОС как необратимого ингибитора заключается в том, что они фосфорилируют АХЭ, навсегда выводя этот фермент из строя.
Есть две основные серии нервно-паралитических агентов ФОС: серия G и серия V. Члены одной серии имеют схожие свойства и получают общее имя (например, зарин) и идентификатор НАТО (например, GB). Агенты серии G известны как нестойкие, а агенты серии V – стойкие.
Серия G названа так потому, что их первыми синтезировали немецкие ученые (G как указание на страну – Germany). Все соединения этого класса были обнаружены и синтезированы во время Второй мировой войны или незадолго до нее под руководством Герхарда Шрадера (позже под руководством компании IG Farben ).
Эта серия является первым семейством нервно-паралитических агентов. Первым синтезированным нервно-паралитическим агентом был GA (табун) в 1936 году, за ним последовал GD (зоман) в 1944 году и, наконец, GF (циклозарин) в 1949 году.
Газ зарин, печально известный после террористической атаки секты Аум Синрикё в токийском метро также относится к ФОС G-серии и был синтезирован в 1939 году.
Рис. 2 боеголовка американской ракеты Honest John с зариновыми бомбами M134 (ок. 1960 г.)
V-серия является вторым семейством нервно-паралитических агентов и включает пять хорошо известных представителей: VE, VG, VM, VR и VX, а также еще несколько малоизвестных аналогов.
Самый изученный агент в этой семье, VX, был изобретен в 1950-х годах в Портон-Дауне в Соединенном Королевстве. Ранаджит Гош, химик из Лаборатории защиты растений компании Imperial Chemical Industries (ICI), исследовал класс органофосфатных соединений (фосфорорганические эфиры замещенных аминоэтантиолов). Как и Шредер, Гош обнаружил, что это довольно эффективные пестициды. В 1954 году ICI выпустила на рынок один из них под торговой маркой Amiton. Впоследствии его отозвали, так как он был слишком токсичным и не подходил для безопасного использования. Токсичность не осталась незамеченной, и некоторые из наиболее токсичных материалов были отправлены в исследовательский центр британских вооруженных сил в Портон-Дауне. После завершения оценки несколько членов этого класса соединений стали новой группой нервно-паралитических агентов, V-агентами (в зависимости от источника, V обозначает Победа (Victory), Ядовитый (Venomous) или Вязкий (Viscous)). [5]
Самым известным из них, вероятно, является VX. Все V-агенты являются стойкими агентами, а это означает, что они не разлагаются и не смываются, а следовательно, могут оставаться на одежде и других поверхностях в течение длительного времени. По консистенции эти средства похожи на масло.
VX был использован сектой Аум Синрикё в покушении на двух человек, один из которых скончался[1]. Также с помощью VX 13-го февраля 2017-го года был убит единокровный брат Ким Чен Ына – Ким Чон Нам [2], [3].
Помимо вышеперечисленных агентов, так же не стоит обделять вниманием серию “Новичок”. Агенты “Новичок” были разработаны в Советском Союзе и в России в период с середины 1960-х по 1990-е годы. Программа Новичок была направлена на разработку и производство смертоносного химического оружия неизвестного Западу. Новые агенты были разработаны таким образом, чтобы их нельзя было обнаружить с помощью стандартного оборудования НАТО, а также для поражения средств химической защиты.
Часть веществ серии “Новичок” превосходят по мощности газ VX в пять или восемь раз [4]. Все вещества серии “Новичок” являются бинарными агентами, это означает, что непосредственно перед применением яда, его прекурсоры смешиваются. Прекурсоры, как правило, значительно менее опасны, чем сами агенты, поэтому этот метод значительно упрощает транспортировку яда. Кроме того, прекурсоры обычно намного легче стабилизировать, чем сами агенты, поэтому этот метод также позволяет увеличить срок хранения агента.[6]
Серия “Новичок” получила широкую известность после отравления Сергея Скрипаля и его дочери Юлии 4 марта 2018 года в г. Солсбери.
Эта статья не является расследованием состояния Алексея Навального. Она лишь поверхностно описывает группы веществ, которые, по мнению врачей клиники Шарите, ответственны за нынешнее состояние его здоровья.
Авторы текста: Коровин А.С., Алмазова Т.А.
Источник
Взаимодействие ингибиторов ахэ с другими лекарственными средствами
Кафедра нервных болезней Военно-медицинской академии им. С.М. Кирова, Санкт-Петербург
Военно-медицинская академия, Санкт-Петербург
Кафедра нервных болезней Военно-медицинской академии им. С.М. Кирова, Санкт-Петербург
Военно-медицинская академия, Санкт-Петербург
Роль антихолинэстеразных средств в оптимизации лечения цереброваскулярных заболеваний (теоретические предпосылки и клиническая феноменология)
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2014;114(8-2): 57-64
Живолупов С. А., Бардаков С. Н., Самарцев И. Н., Гневышев Е. Н. Роль антихолинэстеразных средств в оптимизации лечения цереброваскулярных заболеваний (теоретические предпосылки и клиническая феноменология). Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2014;114(8-2):57-64.
Кафедра нервных болезней Военно-медицинской академии им. С.М. Кирова, Санкт-Петербург


Холинергическая нейротрансмиттерная система является наиболее распространенной в организме человека. Ацетилхолин обеспечивает взаимодействие нейронов центральной нервной системы, а также обусловливает передачу нервных импульсов от периферических нейронов к органам эффекторам. Результаты исследований последних лет продемонстрировали значимость дисфункции холинергической системы в развитии целого комплекса неврологических заболеваний. Oдной из наиболее широко используемых групп фармакологических средств для их лечения являются ингибиторы холинэстеразы. В обзоре рассмотрены особенности препаратов этой группы и их практическое применение при сосудистых заболеваниях нервной системы.
Кафедра нервных болезней Военно-медицинской академии им. С.М. Кирова, Санкт-Петербург
Военно-медицинская академия, Санкт-Петербург
Кафедра нервных болезней Военно-медицинской академии им. С.М. Кирова, Санкт-Петербург
Военно-медицинская академия, Санкт-Петербург
Реализация национальной программы по борьбе с инсультами значительно расширила современные представления о патогенезе, своевременной диагностике и рациональной терапии цереброваскулярных заболеваний (ЦВЗ). В частности, общепризнанной считается парадигма агрессивной стратегии консервативной терапии, направленной на контроль факторов риска ЦВЗ и нейропротекцию.
В связи с этим в последние годы на роль нейропротекторов претендует огромное количество лекарственных средств из различных фармакологических групп. Среди них особое место занимают антихолинэстеразные средства (от др.-греч. α&ngr;&tgr;&igr; — против, &khgr;&ogr;λ&eegr; — желчь и эстераза – ферменты класса гидролаз или ингибиторы ацетилхолинэстеразы (АХЭС)), поскольку их применение согласуется с концепцией нейроваскулярной единицы как матрицы функциональной активности центральной нервной системы (ЦНС), суть которой состоит в том, что мозговая перфузия поддерживается на адекватном уровне не только и не столько за счет сосудистого фактора, сколько вследствие поляризационной активности нейрональных сетей, модулируемой холинергической системой [1]. Это означает, что восстановление нарушенных функций при ЦВЗ можно вызвать не только вазоактивными средствами, но и препаратами, поддерживающими функциональную активность нейронов (например, АХЭС).
АХЭС — одна из наиболее перспективных групп лекарственных препаратов в неврологической практике, уменьшающих активность холинэстеразы и приводящих к повышению содержания ацетилхолина в синапсах. Это облегчает проведение возбуждения в периферической нервной системе, в межнейрональных соединениях ЦНС и, в целом, активизирует холинергическую систему организма. Под последней понимают комплекс нейрональных структур, включающий в себя центральные и периферические холинергические нейроны, рецепторный аппарат пре- и постсинаптических мембран, ферменты (ацетилхолинэстераза, бутирилхолинэстераза) и универсальный медиатор — ацетилхолин [2]. Необходимость качественного понимания клиницистами важности и значимости холинергической системы организма человека продиктована ее широким распространением, выраженной уязвимостью и главенствующей ролью в компенсаторно-восстановительных процессах при патологии нервной системы.
Ацетилхолин — основной нейромедиатор холинергической системы, относящийся к четвертичным аммонийным основаниям, осуществляющий передачу нервного возбуждения в ЦНС, вегетативных ганглиях, окончаниях парасимпатических и двигательных нервов. Ацетилхолин образуется в терминальной части холинергических нейронов из ацетилкоэнзима А и холина при участии холинацетилтрансферазы. После высвобождения в синаптическую щель ацетилхолин быстро гидролизуется ферментом ацетилхолинэстеразой на холин и ацетат [1].
Холинергические рецепторы (холинорецепторы) — комплексные белковые структуры, локализованные на постсинаптических мембранах, как в периферической, так и в ЦНС. Они могут располагаться на пресинаптических мембранах холинергических нейронов и в синапсах с другим типом нейромедиатора. Холинорецепторы выполняют функцию регулятора высвобождения нейромедиатора в синаптическую щель. По типу чувствительности к мускарину (алкалоид Amanita muscaria) и никотину (алкалоид Nicotinia tabacum) выделяют соответственно М-холинорецепторы (мускариночувствительные) и N-холинорецепторы (никотиночувствительные). Ингибиторы холинэстеразы (ИХЭ) способны усиливать холинергические эффекты как в никотиновых, так и в мускариновых рецепторах [2].
N-холинорецепторы. N-холинорецептор является гетероолигомерным комплексом, состоящим из четырех разных белковых субъединиц, названных соответственно их молекулярной массе (в кДа): α (40), β (50), γ (60), δ (65). В постсинаптические мембраны встраивается функциональный пентамер со стехиометрией α2βγδ (рис. 1). 
М-холинорецепторы. Мускариновые рецепторы являются метаботропными, сопряженными и состоят из одной полипептидной цепи длиной 440-540 остатков аминокислот с внеклеточным N-концом и внутриклеточным С-концом. Аминокислотная последовательность в этих отрезках является очень консервативной (более 90% совпадений) во всех пяти типах мускариновых рецепторов. На третьей внутриклеточной петле, а также на С-конце рецепторной молекулы расположено несколько последовательных отрезков, на которых происходит фосфорилирование при передаче нервного импульса. Ацетилхолин связывается с участком, который находится в складке, сформированной спирально закрученными трансмембранными доменами [4].
М-холинорецепторы расположены в постсинаптической мембране клеток эффекторных органов у окончаний постганглионарных холинергических (парасимпатических) волокон. Кроме того, они имеются на нейронах вегетативных ганглиев и в ЦНС (табл.1, см. рис.1) [4].
Пресинаптические М-холинорецепторы локализуются на симпатических сосудосуживающих нервах. Их активация сопровождается снижением выброса норадреналина в ответ на нервные импульсы. Введение эфиров холина приводит к расширению сосудов. Точек приложения у этих веществ несколько: холинорецепторы тормозных синапсов на пресинаптических симпатических окончаниях и холинорецепторы на сосудах, расположенные вне синапсов. Сосудорасширяющее действие ацетилхолина возможно только при неповрежденном эндотелии. Активация М-холинорецепторов эндотелия приводит к выделению из него NО (эндотелиального фактора расслабления сосудов). Диффундируя от эндотелия к гладким мышцам, NО вызывает расширение сосудов [5].
Холинергическая система головного мозга. Описано восемь групп холинергических клеток, от которых начинаются проводящие пути в структуры ЦНС [6]. Медиальное ядро перегородки и вертикальное ядро диагонального пучка — основные скопления холинергических клеток, от которых начинаются проводящие пути к гиппокампу, поясной извилине, обонятельной луковице и гипоталамусу. От горизонтального края ядра диагонального пучка нервные волокна направляются к обонятельной луковице, тогда как базальное ядро Мейнерта практически полностью обеспечивает иннервацию коры головного мозга и миндалевидных ядер (рис. 2). 
Холинергические волокна направляются во все слои коры головного мозга; самая высокая плотность холинергических волокон наблюдается в первом и втором слоях, а также в верхней части третьего слоя коры [7]. Мускариновое действие растормаживает клетки пирамидного слоя коры мозга, усиливая внутрислойную передачу информации между группами клеток. Наоборот, никотиновое действие усиливает торможение [8]. Различные зоны коры человеческого мозга различаются по концентрации холинергической иннервации: самая большая плотность аксонов этого типа отмечается в образованиях лимбической системы, к которой относятся миндалевидные ядра и гиппокамп; следующее место по плотности аксонов занимают образования паралимбической области; уни- и гетеромодальные ассоциативные пути коры имеют среднюю плотность холинергических волокон, а основная часть зрительной коры имеет самое незначительное представительство холинергических волокон [9].
Нейроны базальных ядер и комплекса базальных структур переднего мозга не имеют реципрокной связи со многими зонами их кортикальной проекции. Афферентный путь к базальным ядрам обеспечивается главным образом волокнами, исходящими из лимбической системы мозга, к которым относятся препириформная и орбитофронтальная области коры, переднеинсулярная зона, полюс и средняя часть височной коры, энторинальная кора, ядра перегородки, n. accumbens и гипоталамус. Фактически единственное начало афферентных путей из лимбической системы к базальным ядрам в сочетании с их обширной представленностью в коре, лимбической и паралимбической зонах, предопределяет функцию этой структуры — установление соответствия эмоционального ответа характеру раздражителя, модуляция воздействия эмоционально релевантной информации на корковые функции [10].
М1 является наиболее распространенным подтипом мускариновых рецепторов в коре головного мозга. Самая высокая их концентрация обнаруживается в зубчатой извилине, гиппокампе, переднем обонятельном ядре, коре мозга, обонятельном бугорке и n. accumbens; умеренная концентрация — в обонятельных луковицах и миндалевидных ядрах [10].
М2-рецепторы обнаруживаются в зонах мозга, содержащих большое количество холинергических нейронов, а именно в интерпедункулярном ядре и базальных отделах переднего мозга. М2-рецептор — это пресинаптический ауторецептор, который регулирует высвобождение ацетилхолина. М3-рецепторы в основном концентрируются в диэнцефальной области и в стволе мозга, а М4-рецепторы обнаруживаются главным образом в полосатом теле и обонятельном бугорке [7] (рис. 3, см. на цв. вклейке). 
В настоящее время установлено, что по мере старения организма происходит угасание активности холинергической системы ЦНС (снижение «холинергического профиля»), приводящее к формированию когнитивных нарушений и всей гаммы проявлений старения. Одной из главных причин данного феномена считается прогрессирующее с возрастом повышение активности холинэстераз [11].
Холинэстеразы — группа ферментов класса гидролаз карбоновых кислот, субстратами которых являются сложные эфиры холина с уксусной, пропионовой или масляной кислотами. Выделяют ацетилхолинэстеразу (АХЭ) и бутирилхолинэстеразу (БХЭ).
АХЭ (истинная холинэстераза; холинэстераза) — фермент, катализирующий гидролиз ацетилхолина до холина и остатка уксусной кислоты. АХЭ обнаруживается не только в холинергических синапсах, но и в других структурах холинергических нейронов (дендритах, теле, аксонах) [12]. Представлена в двух формах: гомомерных олигомеров (ди-, моно- и тетра-) и гетеромеров. Гомомерные формы (сывороточная холинэстераза) свободно растворены в цитоплазме и выполняют в организме защитные функции, в частности предохраняют от инактивации АХЭ, поскольку с большой скоростью гидролизуют ингибитор данного фермента — бутирилхолин. Гетеромерные комплексы — тетрамеры представлены в нейрональных и нервно-мышечных синапсах. Дезактивация (гидролиз) ацетилхолина в синаптической щели занимает меньше 1 мс и обусловливает переход клетки-мишени в состояние покоя.
Ген, кодирующий фермент АХЭ у человека, находится на длинном плече 7 хромосомы. Альтернативный сплайсинг РНК этого гена приводит к образованию четырех изоформ АХЭ — T, H, R и 4.
В синапсах АХЭ присутствует в виде тетрамера изоформы T, присоединенного к коллагеноподобному белку, который кодируется отдельным геном COLQ и обеспечивает фиксацию АХЭ на постсинаптической мембране. Мутация этого гена является одной из наиболее распространенных причин наследственной миастении. Кроме этого АХЭ обнаружена в плазматических мембранах эритроцитов (изоформа H) и является Yt-антигеном крови. В нейронах АХЭ может локализоваться внутриклеточно (изоформа T); причем накопление АХЭ внутри ядер клеток нейробластомы приводит к апоптозу [12].
БХЭ (ложная холинэстераза, псевдохолинэстераза, бутирилхолинэстераза, холинэстераза II) — семейство ферментов, широко распространенных в организме. БХЭ обнаруживается в плазме крови, печени, коже, гладких мышцах, где находится в растворенном состоянии. Фермент не имеет топографической связи с холинергическим синапсом и субстратной специфичности. Гидролизует сложные эфиры (бутирилхолин, пропионилхолин). В глиальных клетках ЦНС и мантийных глиоцитах БХЭ содержится в низкой концентрации; в центральных и периферических нейронах она почти отсутствует. БХЭ обнаруживается главным образом в печени (где она в основном и образуется) и в плазме. Выполняет рудиментарную физиологическую функцию — гидролиз эфиров холина, содержащихся в растительной пище [9].
АХЭ и БХЭ различаются по скорости гидролиза ацетилхолина и бутирилхолина, а также по реакции на избирательные ингибиторы. Почти все фармакологические эффекты ингибиторов АХЭ обусловлены подавлением активности именно этого фермента и, как следствие, накоплением эндогенного ацетилхолина в холинергических синапсах и окружающих тканях. ИХЭ являются некоторые природные и синтетические соединения: фосфорорганические соединения (ФОС), эфиры N-алкилкарбаминовых кислот (карбаматы), четвертичные аммониевые основания, гетероциклические соединения, содержащие третичный или четвертичный атом азота. ИХЭ относятся к непрямым холиномиметикам, хотя в высоких дозах многие из них способны непосредственно взаимодействовать с холинорецепторами.
В терапевтических дозах они, в отличие от холиномиметиков прямого действия, усиливают возбуждение всех типов периферических холинорецепторов, а проходящие гематоэнцефалический барьер, также холинорецепторов ЦНС (табл.2) [13].
Ингибиторы АХЭ связываются с тремя доменами фермента: ацильным карманом активного центра, холиновым участком и периферическим анионным участком. Эти же домены определяют различия между АХЭ и БХЭ (табл.3).
По механизму инактивации фермента антихолинэстеразные средства делятся на три группы:
Ингибиторы анионного центра
К ним относятся простые аммониевые четвертичные соли, взаимодействующие с анионным центром (холиновым) и по конкурентному механизму блокирующие доступ ацетилхолина [14]. Ингибирование фермента только по анионному центру быстро обратимо, поэтому время действия таких препаратов короткое: эдрофоний + , К + , Ca 2+ ) [22, 23]. В неврологической практике широко применяются ИХЭ с обратимым блокированием ацетилхолинэстеразы и конкурентным механизмом связывания. Данные особенности позволяют контролировать желаемые клинические эффекты ИХЭ и своевременно корректировать побочные эффекты. Важным аспектом клинической эффективности ИХЭ является различная степень проникновения через ГЭБ, что позволяет использовать ИХЭ при дементных расстройствах, ряде психопатологических синдромов, в период восстановления перенесенного инсульта и других поражений ЦНС. А наличие препаратов двойного действия (нейромидин), в равной мере влияющих на центральные и периферические холинергические синапсы, расширяет спектр корригируемой патологии и позволяет оптимизировать терапевтические подходы в неврологической практике.
Источник