- Выбрать лекарственные средства по лечению лейкоза
- Доктор Питер
- Трудно лечится у взрослых и лишает жизнь радостей? Мифы от правды при раке крови отделила врач НМИЦ онкологии
- «Триумф онкологии». Какие лекарства успешно побеждают рак
- Долгий путь из лаборатории к пациенту
- Как заставить работать иммунитет
- Каждый шестой умирает от рака
- Хронический лейкоз
- Вам поставили диагноз: Хронический лейкоз?
- Филиалы и отделения, где лечат хронический лейкоз
- Хронический лимфолейкоз (ХЛЛ)
- Химиотерапия хронического лейкоза:
- Филиалы и отделения Центра, в которых лечат хронический лейкоз
Выбрать лекарственные средства по лечению лейкоза
Доктор Питер
Трудно лечится у взрослых и лишает жизнь радостей? Мифы от правды при раке крови отделила врач НМИЦ онкологии
Всероссийский центр изучения общественного мнения (ВЦИОМ) накануне представил результаты исследования «Рак крови: что мы знаем о нем и в чем заблуждаемся?». Социологи опросили 1600 россиян, предложив им несколько суждений о болезни — участники должны были сказать, согласны они с ними или нет. «Доктор Питер» выбрал те, с которыми чаще всего соглашались опрошенные. Подтвердить или опровергнуть популярные мифы мы попросили специалиста НМИЦ онкологии им. Петрова.
Рак крови плохо поддается лечению у взрослых (с этим утверждением скорее согласны 61% респондентов)
— Это, скорее, миф. Если рассуждать в общем, то имеет значение возрастной рубеж в 55-60 лет. У пожилых пациентов, действительно, острые лейкозы плохо поддаются лечению. Это связано с тем, что в таком возрасте сложно проводить высокодозную химиотерапию из-за имеющегося у них букета сопутствующих заболеваний. У пациентов моложе 55 острые лейкозы лечатся, как правило, успешнее.
В лечении лейкозов важную роль играет не столько возраст, сколько генетические особенности заболевания. Прежде чем начать лечение, мы обязательно обследуем пациента — выясняем, какой у него вариант лейкоза. От этого зависит всё, включая тактику лечения и прогноз.
Рак крови неизлечим (скорее согласны 31%)
— Это миф. Еще 15-20 лет назад мы могли добиваться какой-то ремиссии и «прощаться» с пациентами. Сейчас лейкоз — болезнь, от которой реально можно вылечиться.
Но надо понимать, что разновидностей лейкозов — их обычно называют «рак крови» — великое множество и для каждого своя тактика лечения и свои риски. Только видов острого лейкоза насчитывается около 40-50, а есть еще хронический.
К примеру, у детей чаще всего развиваются лимфобластные лейкозы (более 80% случаев) — для них не требуется трансплантация костного мозга и они излечимы в 90% случаев. После 18 начинают преобладать миелобластные лейкозы — у них процент достижения первой ремиссии (индукции) в среднем составляет 50-60% (при одних видах процент стремится к 75%, при других, генетически неблагоприятных — может снижаться даже до 35%).
Если рак крови появляется во время беременности, то ребенок родится нездоровым (скорее согласны 26%)
— Это, скорее, миф. Все зависит от того, на каком сроке беременности возникает лейкоз. Если в первом триместре, то обычно такую беременность прерывают. Агрессивная терапия для мамы в этот период — неоправданно высокий риск для развития плода. В поздние сроки беременности используются разные подходы в лечении — их определяет врачебный консилиум.
Каких-то конкретных формул нет. Врачи стараются по возможности быстрее разобщить ребенка и маму — неонатологи научились выхаживать 500-граммовых детей, поэтому в последнем триместе выбирается подходящий момент для родов и только потом начинается лечение. Бывает по-другому — первый курс высокодозной терапии проводят во время беременности, потом роды и продолжение лечения женщины. В любом случае развитие лейкоза во время беременности совсем не обязательно говорит о том, что ребенок тоже заболеет лейкозом или родится нездоровым.
Лечение рака крови полностью оплачивается государством (скорее согласны 24%)
— Это правда. Что касается непосредственно лечения пациента — химиотерапии, обследований, лекарств, компонентов крови, операции по пересадке костного мозга — все это действительно полностью оплачивается из федерального бюджета. Под это выделяются так называемые квоты на высокотехнологичную медпомощь.
Сложности возникают на этапе поиска донора костного мозга, при том что пересадка требуется большинству пациентов с острым лейкозом. Если не удается найти донора в российском регистре, который пока не очень многочисленный, приходится обращаться в международные. Так называемую активизацию донора обычно оплачивают благотворительные фонды. В нее входят вызов донора в клинику, типирование, мобилизация (донору вводятся специальные лекарства, которые «выманивают» клетки костного мозга в кровь — в норме их там нет), дорога и проживание, если донор живет в другом городе или даже стране.
Кроме неродственных аллогенных трансплантаций, проводятся пересадки костного мозга от неполностью совместимых доноров. К примеру, от мамы или папы — подростку, от взрослых детей — родителю. В этих случаях затраты на активизацию донора будут минимальны. Такой вариант — самый простой и дешевый для пациента.
Те, кто переболел раком крови, не смогут вести активную жизнь (скорее согласны 20%)
— Это миф. Цель тяжелого и трудоемкого лечения лейкоза — не просто выживание пациента, а достижение хорошего качества жизни. Сейчас все клеточные технологии направлены на то, чтобы человек смог вернуться к полноценной жизни — работе, самореализации, общению. Большинство пациентов, действительно, возвращаются. Помешать может иммунная реакция при неродственной трансплантации костного мозга — так называемая реакция «трансплантат против хозяина» (РТПХ), когда донорские клетки атакуют собственные ткани человека. В таких случаях пациенту дополнительно назначается иммуносупрессивная терапия (для подавления иммунитета), у которой есть свои риски. Когда удается контролировать реакцию с помощью медикаментов, качество жизни пациента не страдает. Если врачи изначально предполагают развитие тяжелой иммунной реакции, от трансплантации отказываются. Тогда используется поддерживающая терапия — для каждого вида лейкоза свои препараты. Новые лекарства появились совсем недавно и большинство из представленных на сегодня в мире уже зарегистрированы в России. С этого года Минздрав выделяет федеральным клиникам квоты на иммунную терапию лейкозов. Наш НМИЦ онкологии тоже участвует в программе. Эта терапия позволяет хорошо контролировать ремиссию и убирать минимальные «остатки» болезни тем пациентам, у которых лейкоз лечат без трансплантации костного мозга.
Источник
«Триумф онкологии». Какие лекарства успешно побеждают рак
«Ученые обещают лечить рак одним уколом», «Открыто новое лекарство от рака», «Найдено универсальное средство от злокачественных новообразований» — подобные заголовки появляются в СМИ едва ли не каждую неделю. Однако врачи полагаются на давно опробованные методы: хирургическое удаление опухоли, химио- и лучевую терапию. Практически все онкологические заболевания неизлечимы. РИА Новости разбирается, куда пропадают сенсационные разработки и когда наука победит рак.
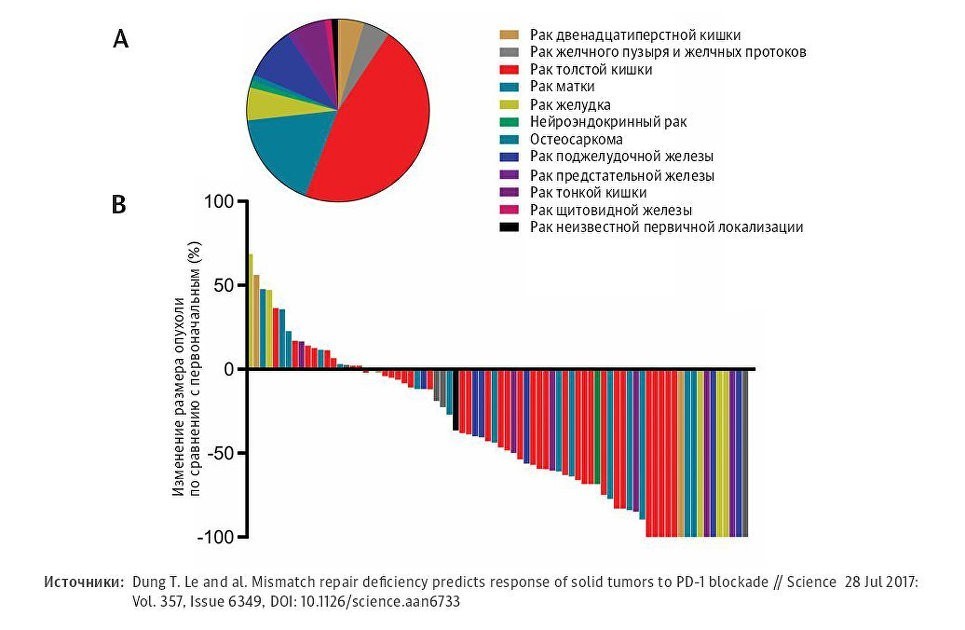
В июле прошлого года в журнале Science вышла статья, наделавшая много шума в научном мире: в результате испытаний нового противоракового препарата от онкологических заболеваний полностью вылечились два десятка человек. У всех были поражены разные органы — матка, желудок, простата, щитовидная железа.
Единственное, что объединяло пациентов, — их опухоли не отвечали на стандартное лечение из-за редких мутаций в геноме. После приема нового лекарства — моноклональных антител, помогающих иммунной системе атаковать болезнь, — 66 из 86 участников исследования почувствовали себя лучше. Их опухоли значительно уменьшились в размерах и стабилизировались, прекратив рост. Восемнадцати пациентам повезло еще больше: рак покинул их навсегда.
И хотя тестирование проходило в урезанном виде, без обязательной в таких случаях контрольной группы, принимающей плацебо, уже через год FDA, главный регулятор лекарственных средств в США, рекомендовал его для лечения сразу нескольких видов рака у детей и взрослых. По мнению специалистов, скорость, с которой была дана рекомендация, — беспрецедентная, и государство могло пойти на такие уступки только в том случае, если разработка действительно оказалась прорывной.
(А) — типы раковых опухолей, обнаруженные у участников исследования; (В) — ответ раковых опухолей на терапию пембролизумабом (результат после первых 20 недель лечения)
На самом деле этой истории почти 11 лет, ведь пембролизумаб (так назывался новый препарат) Грегори Карвен, Ханс ван Эненнаам и Джон Дулос создали в 2007 году. К испытаниям приступили только в 2013-м, а с 2018-го пациенты, страдающие агрессивными видами рака, не отвечающими на стандартную терапию, могли рассчитывать на лечение. Конечно, это состоятельные люди: один курс стоит около 150 тысяч долларов.
Долгий путь из лаборатории к пациенту
«Это долгий и сложный путь: от идеи до пациента. Все перспективные молекулы сначала тестируются на животных, потом проходят исследования с участием 10-20 пациентов, затем их число растет, счет идет на тысячи. На каждый следующий этап препарат переходит, только если продемонстрирует эффективность и безопасность на предыдущем. Это занимает годы, но защищает больных от неприятных последствий», — рассказывает Марина Секачева, руководитель Центра персонализированной онкологии, профессор кафедры онкологии Первого МГМУ им. И. М. Сеченова.
На каждом из этих этапов лекарство может быть выбраковано из-за нулевой эффективности или — еще хуже — негативного воздействия на организм пациентов. Например, в 2017 году во время клинических испытаний препарата CAR-T один из участников исследования умер. Несмотря на доказанную несколькими месяцами ранее эффективность терапии при лечении множественной миеломы и лейкемии, эксперимент был немедленно прекращен.
Похожая история произошла и с инновационным методом лечения рака ROCKET. В ходе клинических испытаний второй фазы проверяли эффективность и безопасность биопрепарата JCAR015, предназначенного для лечения рецидивирующего или устойчивого к терапии В-клеточного острого лимфобластного лейкоза. В июле 2016 года тестирование приостановили на два месяца из-за смерти трех пациентов. Спустя год от исследований лекарства и вовсе отказались, так как еще двое участников исследования скончались по одной и той же причине — отек головного мозга.
Как заставить работать иммунитет
Технология CAR предусматривает введение пациенту его собственных генно-модифицированных Т-лимфоцитов. Таким способом к лечению подключают иммунитет больного. Иммунные клетки распознают опухоль и атакуют ее. Несмотря на первые отрицательные результаты, исследования в этом направлении одобрены в некоторых странах.
«Последние пять лет в онкологии — это триумф иммуноонкологических препаратов, которые делают опухоль доступной для собственной иммунной системы пациента. И мы еще в процессе активного изучения этих лекарств: подбираем оптимальное сочетание, время назначения, последовательность; смотрим, как они влияют на хирургические результаты», — уточняет Марина Секачева.
Каждый шестой умирает от рака
Несмотря на идущую уже четыре десятилетия войну с раком, эта болезнь уносит сегодня жизнь каждого шестого обитателя планеты. По данным Всемирной организации здравоохранения, чаще всего люди погибают от рака легких (один миллион 690 тысяч смертей в год), печени (788 тысяч), толстой и прямой кишок (774 тысячи), желудка (754 тысячи) и молочной железы (571 тысяча).
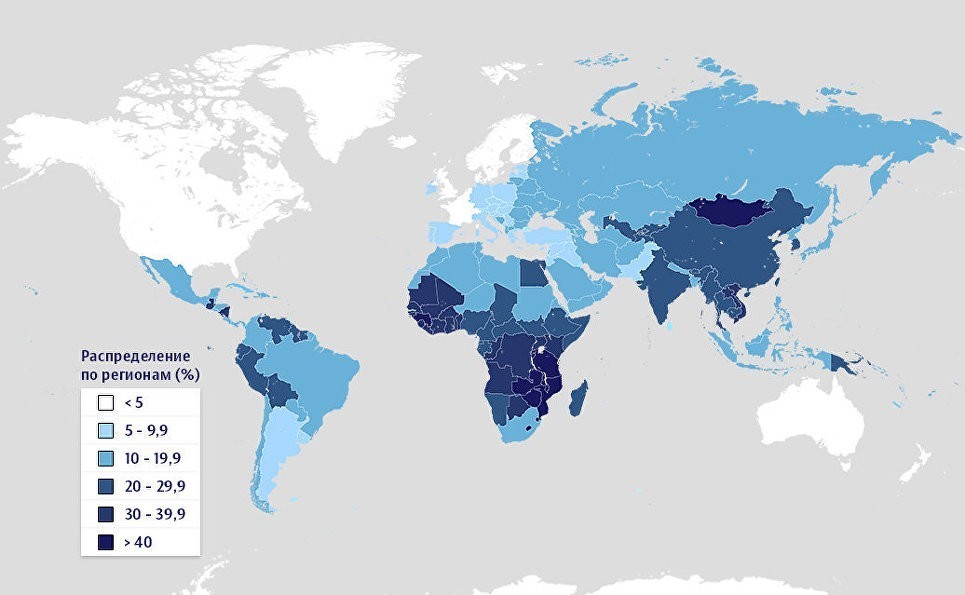
Как отмечают специалисты, помимо физических канцерогенов (например, ультрафиолетового излучения) и вредных химических веществ (табак, асбест) риск заболевания повышают генетические особенности. В последние годы открыли гены, у носителей которых больше вероятность возникновения рака. С другой стороны, злокачественная опухоль часто образуется у тех, кто когда-то перенес инфекции, вызываемые некоторыми вирусами, бактериями или паразитами. Четверть онкологических заболеваний в развивающихся странах вызваны гепатитом и вирусом папилломы человека.
Ежегодный экономический ущерб от рака, по некоторым оценкам, достигает триллиона долларов. На разработку препаратов из года в год тратятся миллиарды. Однако, несмотря на все усилия, говорить о том, что в ближайшем будущем рак будет побежден, не приходится.
© Pathogen-Associated Malignancies Integrated Research Center, Fred Hutch
Доля онкологических больных, чья опухоль связана с перенесенными ранее инфекциями. Распределение по странам мира.
«К сожалению, человечество изобрело пока не так много лекарственных препаратов, позволяющих добиться полного излечения от того или иного недуга — главным образом, это касается инфекций. В большинстве случаев нам удается лишь перевести заболевание из смертельного или мучительного в хроническое и без выраженных симптомов. Эта тенденция прослеживается и в онкологии. В редчайших случаях лекарственная противоопухолевая терапия приводит к полному излечению, но примеров, когда удается перевести рак в длительный вялотекущий процесс, все больше. Скажем, хронический лимфолейкоз, рак молочной или предстательной железы. Мы каждый день (без преувеличения) открываем молекулярные особенности злокачественных новообразований, и это позволяет нам найти новые пути их лечения», — резюмирует онколог.
Источник
Хронический лейкоз
Вам поставили диагноз: Хронический лейкоз?
Наверняка Вы задаётесь вопросом: что же теперь делать?
Подобный диагноз всегда делит жизнь на «до» и «после». Все эмоциональные ресурсы пациента и его родных брошены на переживания и страх. Но именно в этот момент необходимо изменить вектор «за что» на вектор «что можно сделать». Очень часто пациенты чувствуют себя безгранично одинокими вначале пути. Но вы должны понимать — вы не одни.
Мы поможем вам справиться с болезнью и будем идти с вами рука об руку через все этапы вашего лечения.
Предлагаем вашему вниманию краткий, но очень подробный обзор хронического лейкоза.
Его подготовили высоко квалифицированные специалисты Отдела лекарственного лечения злокачественных новообразований МРНЦ имени А.Ф. Цыба и Отдела лекарственного лечения опухолей МНИОИ имени П.А. Герцена – филиалов ФГБУ «НМИЦ радиологии» Минздрава России под редакцией заведующих отделами, д.м.н. ФАЛАЛЕЕВОЙ Н.А. и д.м.н. ФЕДЕНКО А.А.
Филиалы и отделения, где лечат хронический лейкоз
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отдел лекарственного лечения опухолей
Заведующий отделом, д.м.н. ФЕДЕНКО Александр Александрович
тел: 8 (494) 150 11 22
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отдел лекарственного лечения злокачественных новообразований
Заведующая отделом, д.м.н. ФАЛАЛЕЕВА Наталья Александровна
тел: 8 (484) 399 – 31-30
Хронический лимфолейкоз (ХЛЛ)
— Опухолевое заболевание, морфологическим субстратом которого являются малого размера зрелые В-лимфоциты, обнаруживающиеся преимущественно в крови, костном мозге, лимфатических узлах, селезёнке и печени.
Для установления диагноза ХЛЛ, согласно современным критериям, необходимо наличие трех признаков: абсолютное число лимфоцитов крови не менее 5 х10 9 /л, более 30% лимфоцитов в костном мозге, иммунологическое подтверждение наличия опухолевых лимфоцитов со строго определенными характеристиками, без которого диагноз ХЛЛ не может считаться доказанным, поскольку дифференциальный диагноз с похожими заболеваниями проводится на основании именно иммунофенотипирования .
ХЛЛ — наиболее распространенный вид лейкоза в странах Европы и Северной Америки, где на его долю приходится до 30% всех лейкозов. Ежегодная заболеваемость ХЛЛ в этих странах составляет 3-3,5 случая на 100000 населения в год, при этом среди лиц старше 65 лет – до 20 случаев и старше 70 лет – до 50 на 100000.
Средний возраст заболевших — 65 лет, почти 70% заболевают между 50 и 70 годами, только около 10% — до 40 лет. Мужчины заболевают в 2 раза чаще женщин.
В большинстве случаев на ранних этапах ХЛЛ характеризуется медленным течением с постепенно нарастающим лейкоцитозом, который без лечения может достигать 500-1000 х109/л и более, лимфоцитозом, обычно коррелирующим с уровнем лейкоцитоза и составляющим 70-85-99%. Уровни гемоглобина, числа тромбоцитов на ранних этапах болезни обычно нормальные. При высоком лейкоцитозе и лимфоцитозе — уровни гемоглобина и числа тромбоцитов часто сниженные за счет вытеснения нормального кроветворения лейкозным клоном или присоединения нередких для ХЛЛ аутоиммунных осложнений – аутоиммунной гемолитической анемии и/или тромбоцитопении.
Темпы течения болезни и продолжительность жизни при ХЛЛ колеблются в широких пределах – от 2-3 до 20-30 лет. Медленное развитие в начале болезни – причина того, что у 70% пациентов с ХЛЛ диагностируется при анализе крови, сделанном в связи с другими заболеваниями. Примерно у 15-20% больных клинические и гематологические признаки заболевания остаются стабильными и минимально выраженными без лечения на протяжении многих лет и не влияют на продолжительность жизни.
При медленном прогрессировании ХЛЛ больной остается под наблюдением (выжидательная тактика), сигналом к началу лечения служат:
• Массивная инфильтрация костного мозга лимфоцитами (более 80% лимфоцитов в миелограмме), особенно если при этом имеется снижение уровня эритроцитов и тромбоцитов.
• Быстрое нарастание лимфоцитоза – удвоении абсолютного числа лимфоцитов в крови менее чем за 12 мес.
Химиотерапия хронического лейкоза:
В настоящее время препаратом выбора при ХЛЛ являются флударабин и флударабинсодержащие режимы. Схема FCR (флударабин, циклофосфамид, ритуксимаб) является стандартом терапии 1-й линии у молодых пациентов без тяжелой сопутствующей патологии. Хлорамбуцил (лейкеран), в настоящее время остаются стандартом стартовой терапии у пациентов преклонного возраста. Увеличение показателей выживаемости без прогрессирования может быть достигнуто путем добавления к хлорамбуцилу ритуксимаба.
Препарат Бендамустин, вследствие своей низкой токсичности иногда является единственной возможностью терапии у пожилых пациентов, а также больных с сопутствующей патологией.
Таргетная (избирательная, точечная) терапия ХЛЛ: Важным шагом в разработке новых методов терапии при ХЛЛ стало добавление к флударабин-содержащим режимам моноклональных антител к антигену CD20 (ритуксимаб, обинотузумаб). В настоящее время лечение большинства пациентов проводится с использованием моноклональных анти-CD-20-антител.
Спектр таргетных препаратов при ХЛЛ расширяется с каждым годом. В настоящее время в России зарегистрирован препарат ибрутиниб (ингибитор тирозинкиназы Брутона) для лечения крайне неблагоприятной группы пациентов ХЛЛ с делецией хромосомы 17р или мутацией ТР53. Список таргетных препаратов постоянно обновляется.
Филиалы и отделения Центра, в которых лечат хронический лейкоз
ФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, химиотерапевтического и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.
Отдел лекарственного лечения злокачественных новообразований МРНЦ имени А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России
Заведующая отделом, д.м.н. ФАЛАЛЕЕВА Наталья Александровна
8 (484) 399 – 31-30, г. Обнинск, Калужской области
Отдел лекарственного лечения опухолей МНИОИ имени П.А. Герцена –филиал ФГБУ «НМИЦ радиологии» Минздрава России
Заведующий отделом, д.м.н. ФЕДЕНКО Александр Александрович
Источник