- Евросовет рекомендовал разрешить въезд привитым одобренными вакцинами туристам
- В EMA заявили об эффективности одобренных вакцин против всех вариантов коронавируса
- Привитые одобренными EMA и ВОЗ вакцинами смогут въехать в ЕС
- Российские вакцины пока не одобрены ВОЗ и EMA
- Рекомендации Совета не являются обязывающими
- Евросоюз и НАТО на постсоветском пространстве
- Интеграция в Европу
- Евросоюз и НАТО на постсоветском пространстве
- Программа ЕС «Восточное партнерство»
- Евросоюз и НАТО на постсоветском пространстве
- «Восточное партнерство» двух скоростей
- Евросоюз и НАТО на постсоветском пространстве
- Кому нужна виза в ЕС
- Евросоюз и НАТО на постсоветском пространстве
- Интеграция в НАТО
- Какие вакцины от коронавируса используют в мире
Евросовет рекомендовал разрешить въезд привитым одобренными вакцинами туристам
Совет ЕС обновил рекомендации о въезде иностранных туристов в европейские страны в условиях пандемии коронавируса. Об этом говорится на сайте ведомства.
Согласно новой версии документа, основанием для въезда без дополнительных ограничений может быть прохождение полного курса вакцинации не позднее чем за две недели до поездки. При этом прививка должна быть сделана препаратом, одобренным Европейским лекарственным агентством (EMA) или Всемирной организацией здравоохранения (ВОЗ).
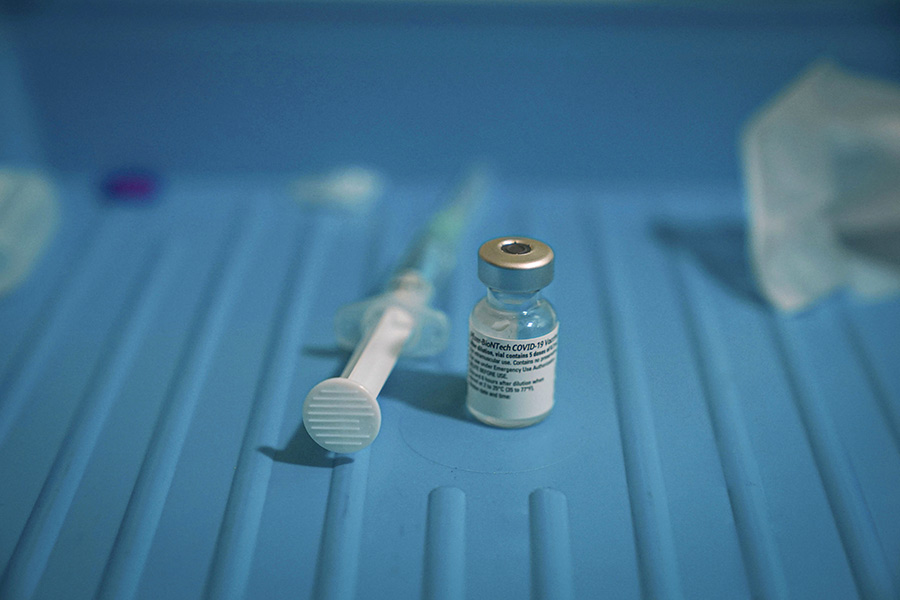
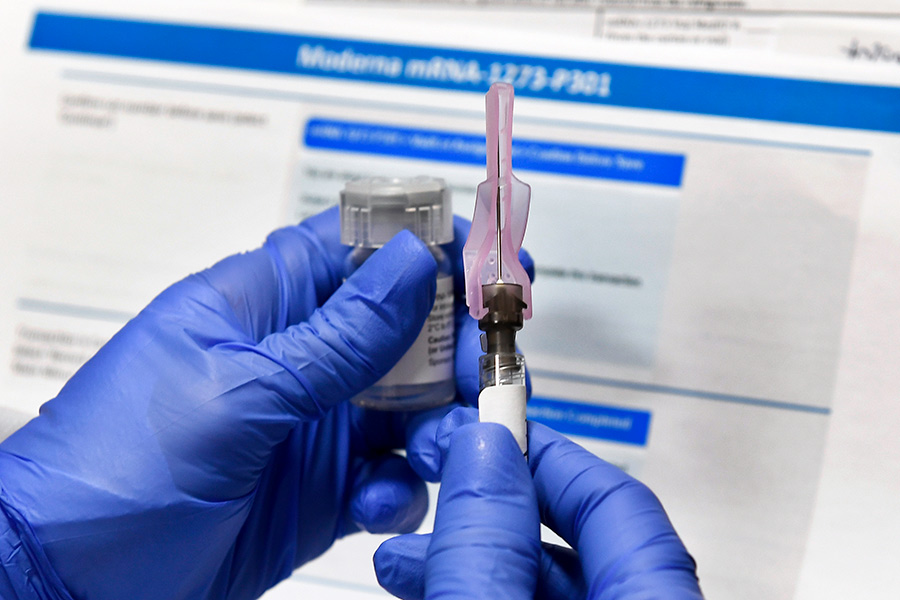
На сегодняшний день EMA одобрены вакцины компаний Pfizer/BioNTech, Moderna, AstraZeneca и Johnson & Johnson, ВОЗ — все перечисленные и китайская вакцина от Sinopharm. Разработанные в России препараты «Спутник V», «ЭпиВакКорона» и «КовиВак» в число одобренных на данный момент не входят. РФПИ сообщил, что подал заявление о регистрации препарата «Спутник V» в Евросоюзе в конце января, 4 марта Европейское агентство лекарственных средств (EMA) начало процедуру последовательной экспертизы регистрационного досье (rolling review) российской вакцины.
В соответствии с новыми рекомендациями страны ЕС также могут впускать туристов из государств, в которых число заражений коронавирусом за последние две недели не превышает 75 на 100 000 населения. При этом документ предусматривает механизм «экстренного торможения» — запрета на въезд из стран и регионов, где происходит резкий всплеск заболеваемости, в том числе из-за распространения новых штаммов COVID-19.
Рекомендация Евросовета не является юридически обязывающим документом, решения об открытии границ будут принимать правительства стран — участниц ЕС.
Накануне глава СВР России Сергей Нарышкин заявил, что EMA намеренно «тянет» с регистрацией российской вакцины от коронавируса, следуя «сигналами, которые поступают из высоких кабинетов ЕС». «Почему это происходит? В этом есть только лишь причины политического характера или еще присутствует экономический фактор? Не знаю, пусть в этом разбираются сами граждане европейских стран и правоохранительные органы, но мы понимаем, что это просто аморально», — сказал Нарышкин.
Источник
В EMA заявили об эффективности одобренных вакцин против всех вариантов коронавируса
В EMA заявили, что все одобренные в Евросоюзе вакцины могут обеспечить защиту от штамма коронавируса «Дельта», а также от других новых вариантов. В ЕС одобрены препараты Pfizer, Moderna, J&J и AstraZeneca.
Все одобренные в ЕС вакцины защищают от всех штаммов коронавируса, включая широко распространившийся вариант «Дельта». Об этом заявил руководитель отдела по вакцинации и борьбе с инфекциями Европейского агентства лекарственных средств (EMA) Марко Кавалери, сообщает Reuters со ссылкой на брифинг EMA.
Кавалери, тем не менее, призвал производителей вакцин не терять бдительности и тщательно мониторить появление новых штаммов. «За последние месяцы появилось несколько вариантов [коронавируса], и мы ожидаем еще больше», — отметил он.
В Европейском союзе разрешены четыре вакцины против COVID-19 — это препараты от Pfizer и BioNTech, Moderna, AstraZeneca и Johnson & Johnson.
Ранее главный научный сотрудник ВОЗ Сумия Сваминатан заявляла, что существующие вакцины не всегда спасают от заражения COVID-19. «Мы видели отчеты из стран, которые вакцинировали 50—60% населения, но случаи заражения все равно растут. Посмотрите на Великобританию, такие страны, как Чили, Сейшелы, Монголия», — сообщала представитель ВОЗ.
Тем не менее Сваминатан отмечает, что большинство использующихся в мире вакцин как минимум эффективны для предотвращения тяжелых случаев COVID-19, вызываемых штаммом «Дельта».
В ходе брифинга EMA также сообщило, что продолжит оценку данных с испытаний вакцины от коронавируса CureVac. Немецкая биотехнологическая компания заявила, что ее препарат эффективен только на 48% по результатам окончательного анализа.
Кроме того, агентство повторило, что оно не получало никаких заявок на авторизацию вакцины Covishield, варианта вакцины AstraZeneca, производимого Индийским институтом сыворотки. В последние дни между Индией и Европой возникли трения из-за исключения Covishield из программы вакцинных паспортов Европейского союза.
Источник
Привитые одобренными EMA и ВОЗ вакцинами смогут въехать в ЕС
Прохождение вакцинации российским препаратом пока не может служить основанием для въезда в ЕС, следует из одобренных в Брюсселе рекомендаций.
Совет ЕС обновил рекомендации о временных ограничениях на въезд в ЕС в случаях, когда речь не идет о «жизненной необходимости». Это следует из заявления совета, распространенного в четверг, 20 мая, в Брюсселе.
Изменения разрешают въезд иностранцам, привитым рядом вакцин, а также смягчают критерии, необходимые для снятия ограничений в отношении третьих стран. Основанием для въезда без дополнительных ограничений в виде сдачи ПЦР-теста или нахождения в карантине может быть вакцинация препаратами, одобренными Европейским агентством лекарственных средств (EMA) или Всемирной организацией здравоохранения (ВОЗ). При этом последняя рекомендованная доза вакцины должна быть введена не менее чем за 14 дней до въезда.
Российские вакцины пока не одобрены ВОЗ и EMA
EMA на данном этапе одобрены вакцины, разработанные компаниями BioNTech/Pfizer, Moderna, AstraZeneca и Johnson & Johnson, а ВОЗ — китайская вакцина от Sinopharm. Российские препараты в этом перечне пока не фигурируют.
Рекомендации Совета не являются обязывающими
«Государства — члены могут также отменить ограничение на несущественные поездки для тех, кто получил по крайней мере за 14 дней до прибытия последнюю рекомендованную дозу вакцины, включенной в список ВОЗ для экстренного применения», — уточняется в постановлении Совета.
В то же время рекомендация Совета не является юридически обязывающим документом. Власти государств-членов европейского сообщества остаются ответственными за принятие решений о воплощении этих рекомендаций в жизнь.
Евросоюз и НАТО на постсоветском пространстве
Интеграция в Европу
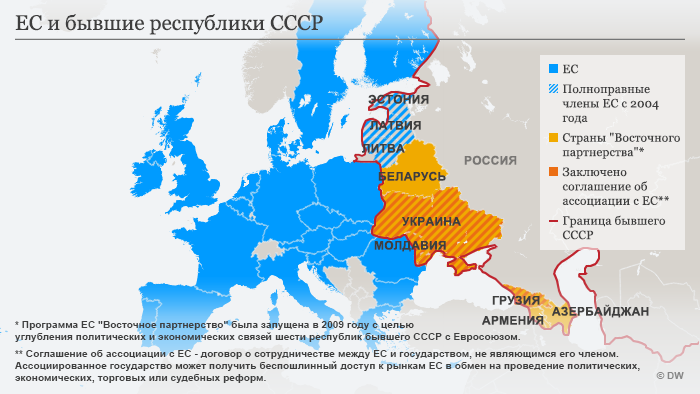
Из стран бывшего СССР полноправными членами Евросоюза на данный момент являются только страны Балтии: Латвия, Литва и Эстония присоединились к ЕС 1 мая 2004 года. Еще шесть стран участвуют в программе ЕС «Восточное партнерство»: три из них — Украина, Молдавия и Грузия — заключили соглашение об ассоциации с ЕС.
Евросоюз и НАТО на постсоветском пространстве
Программа ЕС «Восточное партнерство»
В программе «Восточное партнерство», нацеленной на углубление связей республик бывшего СССР с Евросоюзом, в данный момент участвуют шесть постсоветских стран — Беларусь, Украина, Молдавия, Грузия, Армения и Азербайджан. Примечательно, что Беларусь и Армения одновременно являются и членами Евразийского экономического союза (ЕАЭС), куда также входят Россия, Казахстан и Киргизия.
Евросоюз и НАТО на постсоветском пространстве
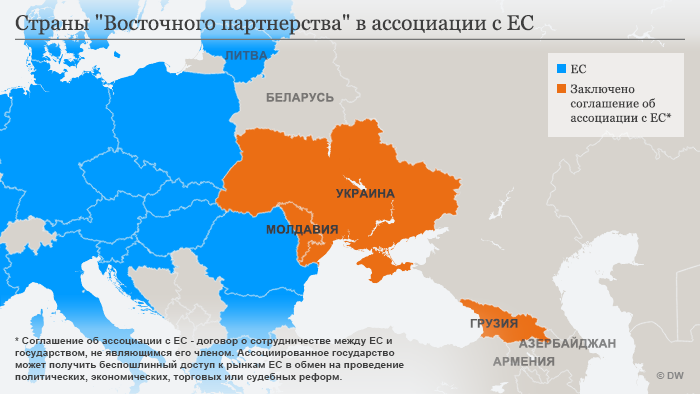
«Восточное партнерство» двух скоростей
В последнее время усилилось разделение стран «Восточного партнерства» на две группы. В первую входят Грузия, Молдавия и Украина, подписавшие договор об ассоциации с ЕС. Во вторую — Беларусь, Азербайджан и Армения, не заключившие такого соглашения. 1 мая вступит в силу договор о расширенном партнерстве между Арменией и ЕС, в рамках которого ЕС предоставит Еревану 175 млн евро на проведение реформ.
Евросоюз и НАТО на постсоветском пространстве
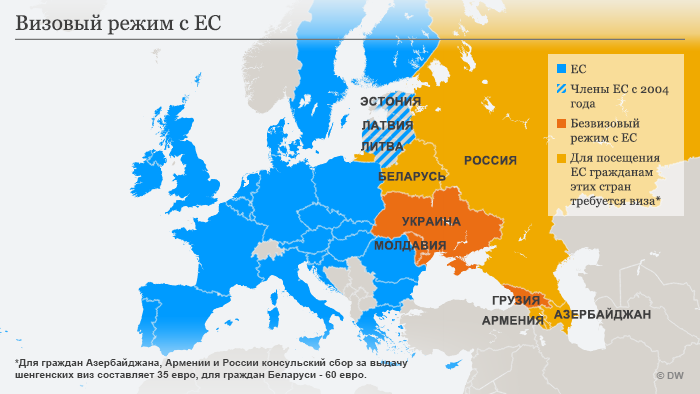
Кому нужна виза в ЕС
Граждане стран Балтии, вступивших в ЕС в 2004 году, пользуются правом свободного передвижения и могут работать в любой стране Евросоюза наравне с гражданами того или иного государства ЕС. Обладатели украинского, молдавского или грузинского паспортов могут посещать страны Шенгенской зоны без виз. Гражданам же России, Беларуси, Армении и Азербайджана для этих целей по-прежнему требуется виза.
Евросоюз и НАТО на постсоветском пространстве
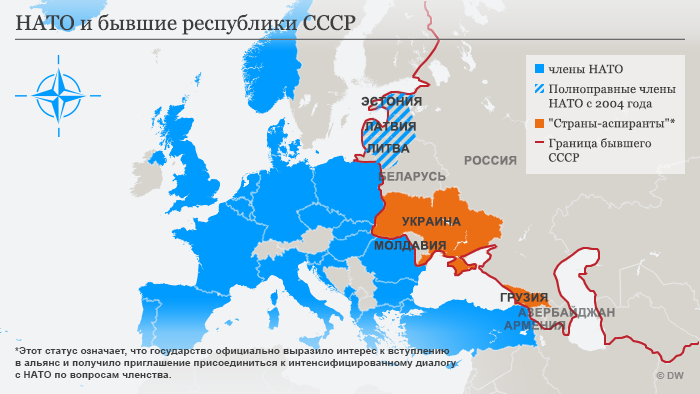
Интеграция в НАТО
Из республик бывшего СССР полноправными членами Североатлантического альянса пока также являются только три страны Балтии. Украине и Грузии предоставлен статус «страны-аспиранта»: это означает, что государство официально выразило интерес к вступлению в НАТО и получило приглашение присоединиться к интенсивному диалогу по вопросам членства.
Источник
Какие вакцины от коронавируса используют в мире
В России массовая вакцинация от COVID-19 началась 18 января. В мире на конец марта прививают население уже в 141 стране. Какие вакцины используют — в обзоре РБК
«Спутник V», разработанная Центром эпидемиологии и микробиологии имени Н.Ф. Гамалеи, получила госрегистрацию Минздрава в августе. Вакцину зарегистрировали после второй фазы испытаний, а третий финальный этап стартовал в сентябре.
Эффективность «Спутника V» разработчики оценили выше, чем в 95%. Эти данные были получены при исследовании добровольцев, получивших две инъекции препарата. «Спутник V» разработан в двух видах: замороженном (жидкая «Гам-КОВИД-Вак» хранится при температуре не выше минус 18 °С) и лиофилизированном (порошок «Гам-КОВИД-Вак-Лио» хранится при температуре от плюс 2 до 8 °С). Препарат вводится двукратно с интервалом в три недели. В ФАС заявили, что стоимость инъекции «Спутником V» не превысит 1 тыс. руб.
5 декабря Москва стала первым российским регионом, начавшим масштабную вакцинацию «Спутником V», а с 18 января началась массовая вакцинация во всей России. Первой среди зарубежных стран, зарегистрировавших российский препарат, стала Белоруссия. Такое же решение приняли власти Аргентины, Венесуэлы и некоторых других стран
Немецкая компания BioNtech разработала вакцину совместно с американской Pfizer. На третьей фазе клинических испытаний препарат показал эффективность на уровне 95%. У вакцины есть обязательное условие использования: ее нужно хранить при температуре не выше минус 70 градусов Цельсия, а после разморозки она пригодна в течение пяти дней. Разработка Pfizer-BioNTech вводится в два приема с промежутком в три недели. Великобритания стала первой страной, одобрившей применение Pfizer и BioNTech, за ней последовали Канада, США и страны Европы и Ближнего Востока. Массовая вакцинация в США и Канаде началась 14 декабря, а в европейских странах — 27 декабря
Эффективность вакцины американской фармацевтической компании Moderna составила 94,5%, а при тяжелых случаях заболевания — 100%. Вакцин вводят в два приема с интервалом в четыре недели. Препарат можно до 30 дней хранить при 2–8 градусах Цельсия. В этом году Moderna планирует выпустить 600 млн доз.
18 декабря США одобрили использование Moderna и заказали 200 млн доз с возможностью покупки еще 300 млн. Следом разрешение на использование она получила в Канаде, Израиле, Великобритании и Швейцарии. 6 января Европейский регулятор одобрил препарат американского производства
Вакцина, разработанная британской компанией AstraZeneca вместе с Оксфордским университетом, показала эффективность на уровне 70%, а при одном из способов введения (сначала вводят половину дозы, а через месяц — полную) — 90%.
У препарата есть два преимущества: его можно хранить при той же температуре, которую позволяет создать обычный холодильник, а его стоимость составляет $4–5. Вводится два раза с интервалом в 4–12 недель.
Великобритания первой в мире разрешила использовать AstraZeneca и заказала 100 млн доз. Препарат получил разрешение на использование в Индии, Аргентине, Доминиканской Республике, Сальвадоре, Мексике и Марокко.
В марте 2021 года вокруг препарата AstraZeneca разразился скандал. Более 15 стран Европы, в том числе Германия, Франция, Испания, и некоторые страны Азии и Африки частично или полностью отказались от препарата. Такое решение власти приняли на фоне сообщений об образовании тромбов у привившихся и смертельных исходах.
В самой компании указывают на отсутствие доказательств, что к смерти пациентов привела именно вакцинация. 18 марта вышло заключение Европейского агентства лекарственных средств (EMA) о том, что AstraZeneca не увеличивает риски по образованию тромбов. ВОЗ также продолжает рекомендовать использование препарата. После этих заявлений европейские страны, кроме некоторых скандинавских, возобновили иммунизацию AstraZeneca.
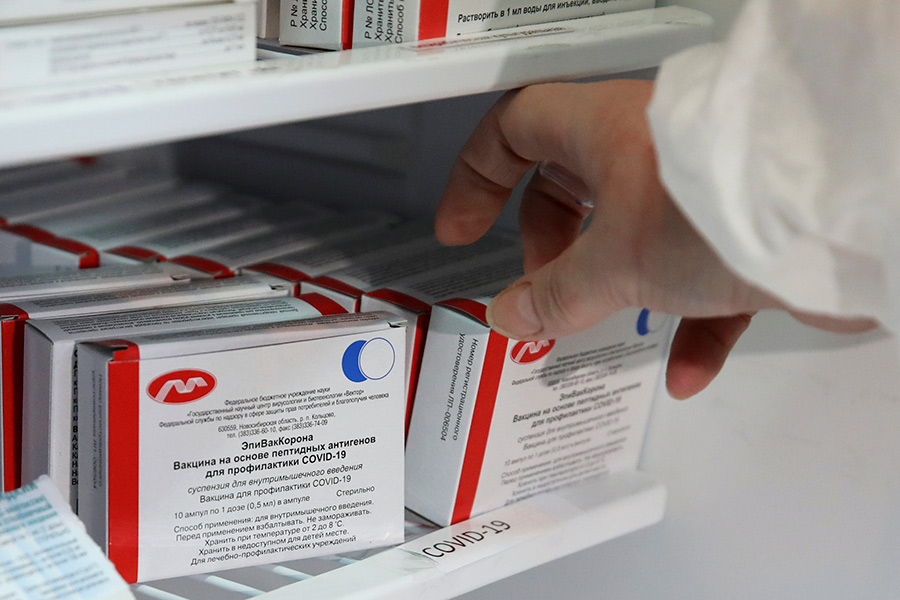
Пептидная вакцина новосибирского научного центра «Вектор» «ЭпиВакКорона» получила регистрационное удостоверение в октябре 2020 года. Она, как и «Спутник V», была зарегистрирована после двух стадий клинических испытаний.
Вакцину вводят двукратно внутримышечно с интервалом в две-три недели. Препарат можно хранить при температуре от 2 до 8 градусов выше нуля. В Роспотребнадзоре отмечают, что вакцина подходит для пожилых и людей с хроническими заболеваниями. В центре «Вектор» заявили, что стоимость препарата будет эквивалента стоимости «Спутника V», то есть около 1 тыс. руб.
Глава Роспотребнадзора Анна Попова сообщала, что «ЭпиВакКорона» поступила в гражданский оборот в пяти городах — Москве, Санкт-Петербурге, Ростове-на-Дону, Туле и Новосибирске. После завершения пострегистрационных клинических испытаний в 2021 году может начаться массовая вакцинация «ЭпиВакКороной»
Инактивированная вакцина CoronaVac, разработанная китайской Sinovac Biotech, хранится в холодильнике при плюс 2–8 градусах Цельсия. В Sinovac заявили, что обеспечат производство 300 млн доз в год. Для иммунизации требуется две дозы, а это означает, что CoronaVac смогут привиться 150 млн человек — чуть больше десятой части населения Китая.
Данные об эффективности вакцины от Sinovac разнятся. Последние испытания в Бразилии показали 50,4% эффективности, а в Индонезии и Турции — 65,3% и 91,5% соответственно.
Вакцина была одобрена для экстренного применения в группах высокого риска в Китае с июля. Использование этой вакцины 13 января разрешили власти Турции. Несколько азиатских стран — Сингапур, Малайзия и Филиппины, а также Бразилия и Украина подписали соглашения о закупках CoronaVac
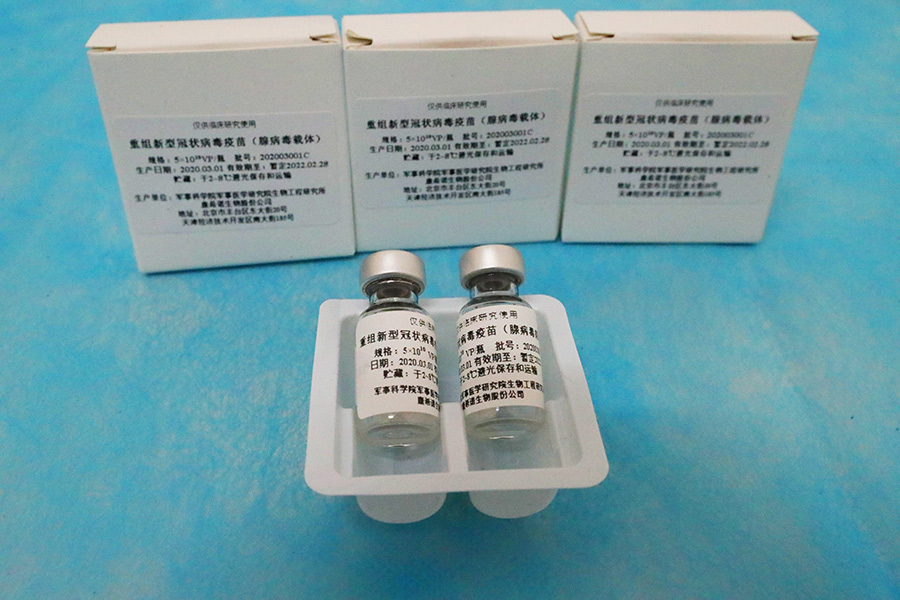
Еще одна китайская вакцина Ad5-nCoV («Конвидеция»), на основе человеческого аденовируса типа 5, разработана фармкомпанией CanSino Biologics. Преимуществом этого препарата является однократное введение, а также возможность хранения при температуре от плюс 2 до плюс 8 градусов Цельсия.
В ноябре 2020 года были поданы документы в Минздрав России для регистрации вакцины. В декабре Минздрав выдал разрешение на проведение третьего международного этапа клинического исследования Ad5-nCov. В случае, если вакцина покажет высокую эффективность и безопасность, CanSino Biologics с российским «Петроваксом» организуют ее производство в России.
Согласно промежуточным результатам третьей фазы клинических испытаний в России, Ad5-nCoV показала эффективность в 92,5%. Окончательные результаты исследования появятся в середине 2021 года
Другую китайскую инактивированную вакцину разработала China National Biotec Group (CNBG) (подразделение Sinopharm). Она не требует отрицательной температуры хранения и вводится двумя дозами с интервалом в две недели.
30 декабря Sinopharm объявила, что на третьем этапе испытаний препарат показал эффективность на 79%. Однако Объединенные Арабские Эмираты, которые одобрили вакцину Sinopharm в этом месяце, заявили, что эффективность вакцины составила 86%. Кроме Китая и ОАЭ вакцина Sinopharm проходит клинические испытания в Бахрейне, Иордании, Перу и Аргентине.
В Китае препарат Sinopharm с июля используется в рамках программы по экстренному вакцинированию, а 31 декабря Государственное управление по лекарственным средствам Китая одобрило препарат для широкого использования
Вакцину Janssen американской корпорации Johnson & Johnson 11 марта одобрил ЕС. Чуть раньше экстренное применение препарата разрешило Управление США по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). Препарат также включен в список для экстренного применения ВОЗ.
В ходе клинических испытаний с участием 44 тыс. человек из США, Южной Африки и стран Латинской Америки препарат показал эффективность в 67%.
Вакцина Janssen хранится при температуре -20 градусов по Цельсию. Но у нее есть особенность — на протяжении трех месяцев она может находиться в условиях от 2 до 8 градусов по Цельсию. Главное преимущество — однодозное введение.
Источник