Гемостатические средства
Гемостатические средства — лекарственные средства, способствующие остановке кровотечений. Все гемостатики, в зависимости от механизма действия, подразделяются на три большие группы:
- ингибиторы фибринолиза (антифибринолитики);
- средства, усиливающие свертывание крови (коагулянты);
- средства, понижающие сосудистую проницаемость.
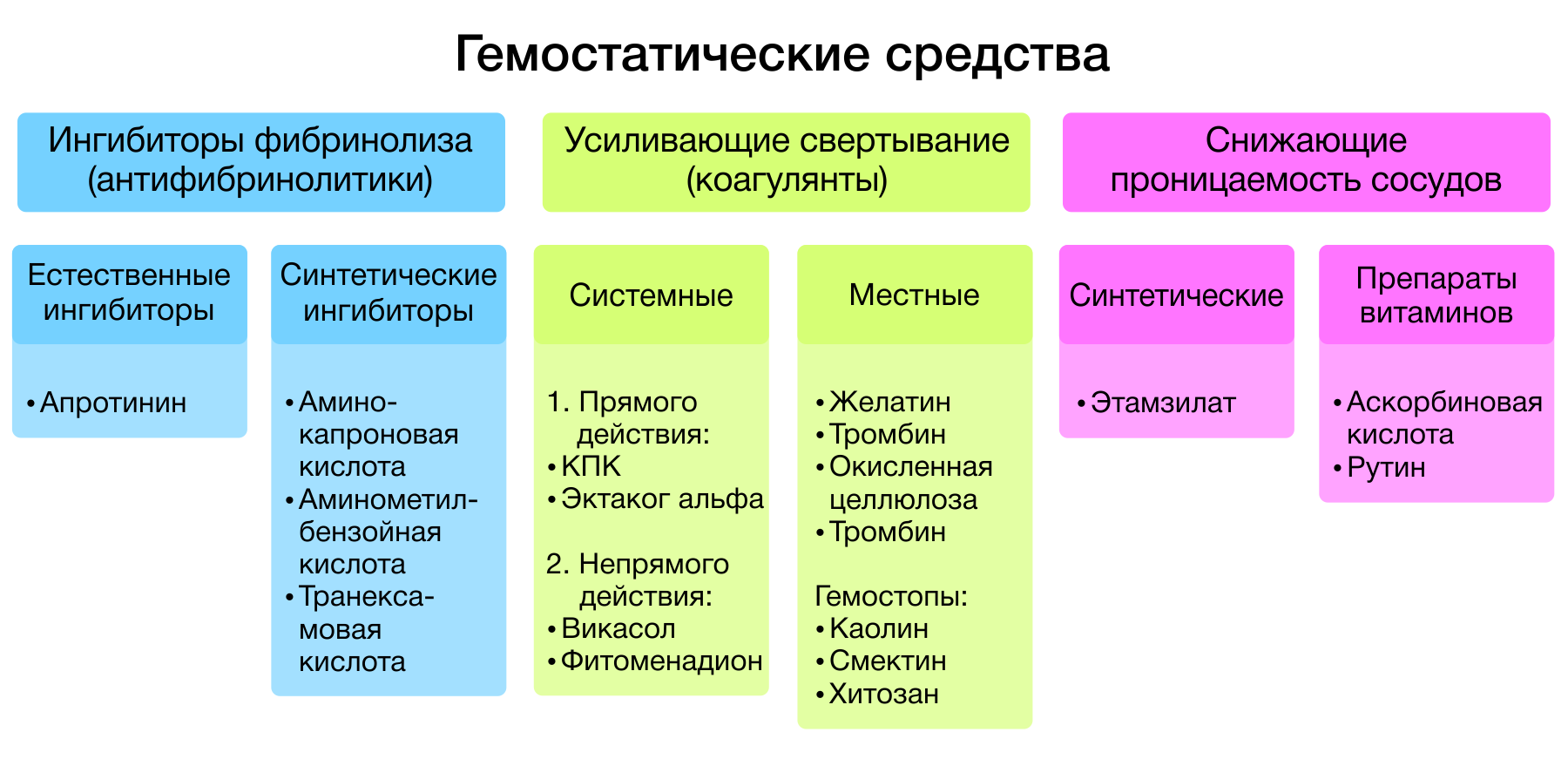
Рисунок 1 | Классификация гемостатиков.
1. Ингибиторы фибринолиза.
В клинической практике широкое распространение получили две группы препаратов ингибиторов фибринолиза: естественные ингибиторы фибринолиза (апротинин и его аналоги) и синтетические ингибиторы фибринолиза (аминокапроновая кислота, аминометилбензойная кислота, транексамовая кислота).
Апротинин — полипептид, получаемый из легких, поджелудочной и околоушной желез крупного рогатого скота, действующий аналогично α2-антиплазмину. Апротинин разрушает свободный плазмин, практически не взаимодействует со связанным плазмином, а также угнетает активацию тромбоцитов. Являясь сериновой протеазой, апротинин блокирует калликреин-кининовую систему путем разрушения калликреина, снижает активность отдельных протеолитических ферментов, таких как: трипсин, химотрипсин, кининогеназа. Изначально препарат был включен в рекомендации по лечению острого панкреатита и панкреонекроза, однако не подтвердил свою эффективность, и показания к его применению были пересмотрены.[1]
Аминокапроновая кислота – 6-аминогексановая кислота — синтетическое производное лизина. Присоединяясь к лизин-связывающему участку плазминогена, аминокапроновая кислота обратимо блокирует процесс фибринолиза, снижает активность стрептокиназы, урокиназы, тканевых киназ, калликреина, трипсина и гиалуронидазы. Аналогичным фармакологическим эффектом обладает производное аминокапроновой кислоты — аминометилбензойная кислота, отличающаяся улучшенной фармакокинетикой. Аминокапроновая кислота снижает активность тромболитических препаратов и может быть использована для нейтрализации их эффекта.
Транексамовая кислота — транс-4-(аминометил)-циклогексанкарбоновая кислота — обратимо блокирует эффект плазминогена, адгезию лейкоцитов и тромбоцитов на поверхность тромба за счет конкурентного ингибирования активатора плазминогена. Оказывает противоаллергическое и противовоспалительное действие посредством подавления образования кининов и других активных пептидов, участвующих в аллергических и воспалительных реакциях. По мощности антифибринолитического действия транексамовая кислота значительно превосходит аминокапроновую кислоту. Активность препарата в плазме сохраняется на протяжении 7-8 часов, в тканях — до 17 часов.[2]
У больных с высоким риском массивной кровопотери в плановой хирургии (сердечно-сосудистая хирургия, травматология и ортопедия, трансплантология) применение ингибиторов фибринолиза уменьшает интраоперационную кровопотерю и снижает потребность в трансфузии донорской крови. На протяжении 20 лет проводилось множество исследований, результаты которых были неоднозначны: мнения склонялись то в пользу апротинина, то в пользу синтетических производных лизина.
В 2007 году компания Bayer завершила исследование BART (Blood conservation using antifibrinolytics in a randomized trial), в котором было изучено действие апротинина у кардиохирургических больных высокого риска. Исследователи выявили большой риск летальных исходов и осложнений при использовании апротинина. В группе апротинина количество больных с массивной кровопотерей было несколько меньше, но 30-дневная летальность на 50% превышала аналогичный показатель в других группах.[3]
После публикации результатов BART компания Bayer уведомила Управление по контролю за качеством пищевых продуктов и лекарственных средств США (FDA) о намерении изъять апротинин с рынка. Показания к назначению были пересмотрены, и препарат был исключен из списка безопасных лекарственных средств.
Огромный мета-анализ позволил сделать вывод, что транексамовая кислота обеспечивает такое же снижение периоперационной трансфузии, какое наблюдается при использовании апротинина, но более безопасна. Согласно рекомендациям Европейского общества анестезиологов по ведению пациентов с массивной периоперационной кровопотерей (2013 г.), при массивном кровотечении рекомендуется применение транексамовой кислоты (20-25 мг/кг); она может быть введена повторно или применяться в виде пролонгированной инфузии (1-2 мг/кг/ч).[4]
2. Препараты, усиливающие свертывание крови
Среди средств, повышающих скорость свертывания крови, выделяют: средства системного действия и для местного применения. К препаратам системного действия относят непрямые коагулянты (фитоменадион, менадиона натрия бисульфит) и коагулянты прямого действия (факторы свертывания: концентрат протромбинового комплекса, эптаког альфа).
Менадиона натрия бисульфит — синтетический водорастворимый аналог витамина К3. Субстратно стимулирует витамин K-редуктазу, активирующую витамин К и обеспечивающую его участие в печеночном синтезе витамин K-зависимых плазменных факторов гемостаза (II, VII, IX, X). Фитоменадион является синтетическим структурным аналогом витамина К1, обладает большей активностью и более ранним началом реализации эффектов (через 6-10 часов после перорального применения, против 18-24 часов у менадиона натрия бисульфита). Данная группа препаратов показана для коррекции нарушений системы гемостаза, вызванных дефицитом витамина К1, передозировкой антикоагулянтов непрямого действия (варфарина), а также для предоперационной профилактики кровотечений.
Концентрат протромбинового комплекса (КПК) — лекарственный препарат, содержащий факторы II, VII, IX, X, а также следовые концентрации антитромбина III, гепарина, протеинов С и S. Основным показанием к применению КПК служит коррекция приобретенного дефицита витамин К1-зависимых факторов в экстренных ситуациях (кровотечение, экстренная операция). Помимо этого, КПК широко используется как средство для лечения и профилактики кровотечений у пациентов с врожденным дефицитом одного из К1 зависимых факторов свертывания (врожденная гипопротромбинемия, врожденный дефицит фактора Стюарта – Прауэра).[5]
Эптаког альфа — рекомбинантный активированный VII фактор свертывания. Механизм действия препарата заключается в прямой активации фактора Х на поверхности активированных тромбоцитов. Это вызывает «тромбиновый взрыв» независимо от имеющейся концентрации факторов VIIIa и IXa. В результате образуется стабильный фибриновый сгусток. Считается, что эптаког альфа инициирует гемостаз только в месте повреждения ткани и не вызывает системной активации механизмов свертывания. Препарат был разработан для лечения кровотечений и проведения хирургических вмешательств у пациентов с наследственной или приобретенной гемофилией и высоким титром ингибитора факторов свертывания VIIIa или IXa. Его применение у пациентов с массивным кровотечением можно сформулировать согласно рекомендациям ESA (2013): «Применение рекомбинантного фактора VII возможно только при кровотечениях, которые не могут быть устранены хирургическими методами или путем комплексной гемостаз-корригирующей терапии». Необходимо серьезное обоснование для применения данного препарата [6].
3. Местные гемостатики
Местные гемостатики используются для остановки капиллярных и паренхиматозных кровотечений преимущественно в неотложной хирургии и стоматологии. Данная группа включает в себя широкий спектр препаратов с различным механизмом действия.
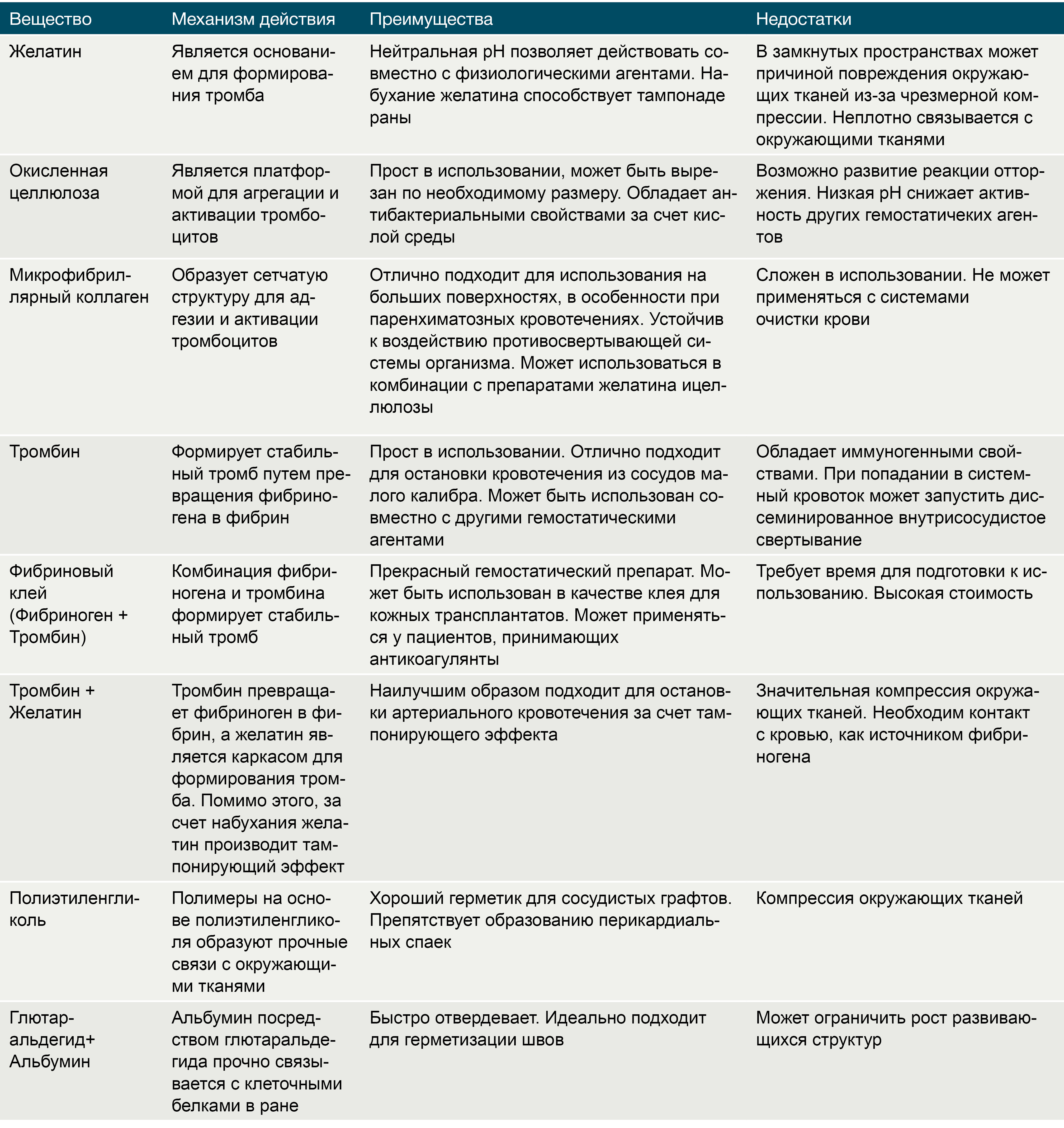
Препараты на основе желатина, получаемого из свиной кожи, существуют в трех формах: пленка, губка и порошок. Желатин чрезвычайно гигроскопичен, и за счет этого свойства он абсорбирует влагу, увеличиваясь в размерах и заполняя тканевой дефект. Существуют комбинации желатина с тромбином, которые помимо пассивного гемостатического эффекта напрямую запускают коагуляционный каскад и активируют тромбоциты в месте нанесения. Желатин разрушается протеиназами в течение 4-6 недель. Несмотря на абсолютную индифферентность, желатин может служить в качестве хронического очага инфекции. Помимо этого, одним из существенных недостатков данных препаратов является отсутствие прочных связей с окружающими тканями [7].
Тромбин является естественным компонентом свертывающей системы крови. Раствор тромбина используют только местно при капиллярных или паренхиматозных кровотечениях в ходе нейрохирургических вмешательств, операций на печени и почках, в стоматологической практике. Попадание тромбина в крупные кровеносные сосуды может вызвать распространенный тромбоз [7].
Окисленная целлюлоза выпускается в виде пленок, сеток, пучков и губок. Данный биологический агент играет роль субстрата для агрегации тромбоцитов и активации механизмов гемостаза. Целлюлоза значительно снижает рН среды, что приводит к лизису эритроцитов с образованием кислого гематина, который формирует дополнительный искусственный сгусток. Помимо этого окисленная целлюлоза обладает антибактериальным эффектом, в том числе в отношении антибиотикорезистентных микроорганизмов [7].
Микрофибриллярный коллаген, производимый из кожи крупного рогатого скота, имеет ряд преимуществ перед остальными топическими биологическими кровоостанавливающими агентами, среди которых: быстрый гемостатический эффект, минимальная реактивность тканей и высокая способность к реабсорбции. Аналогично целлюлозе, микрофибриллярный коллаген является матрицей для активации тромбоцитов, агрегации и образования тромбов [7].
Подвидом местных кровоостанавливающих средств являются гемостопы, получившие большое распространение в военной медицине. Это препараты внешнего воздействия, которые почти не влияют на свертывающую и противосвертывающую системы крови. Многообразие форм выпуска обеспечивает удобство применения в полевых условиях и полностью удовлетворяет потребностям оказания неотложной помощи при любых кровотечениях. На сегодняшний день наиболее эффективным средством считается хитозан.
Хитозан – это полисахаридный биополимер, получаемый из хитиновых панцирей ракообразных. Кровоостанавливающий эффект данного вещества достигается путем связывания хлопьев хитозана с отрицательно-заряженными эритроцитами и образования гелеобразного сгустка в месте контакта с кровью. Среди преимуществ препаратов на основе хитозана выделяют его антимикробные свойства, длительный срок хранения, стабильность при перепадах температур и безопасность при наружном использовании [8].
Наиболее известным представителем группы средств, понижающих сосудистую проницаемость, является этамзилат. Гемостатический эффект данного препарата обусловлен активацией тромбопластина в месте повреждения сосудов микроциркуляторного русла и снижением синтеза простациклина PGI-2 в эндотелии сосудов, что в конечном итоге приводит к усилению адгезии и агрегации тромбоцитов, остановке или уменьшению кровоточивости. За счет антигиалуронидазного действия этамзилат обладает ангиопротективным эффектом, улучшает микроциркуляцию и нормализует проницаемость сосудистой стенки при патологических процессах [9].
Источники
- Fergusson D. A. et al. A comparison of aprotinin and lysine analogues in high-risk cardiac surgery //New England Journal of Medicine. – 2008. – Т. 358. – №. 22. – С. 2319-2331.
- Williams-Johnson J. A. et al. Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with significant haemorrhage (CRASH-2): a randomised, placebo-controlled trial //West Indian Medical Journal. – 2010. – Т. 59. – №. 6. – С. 612-624.
- Ferraris V. A. et al. Perioperative blood transfusion and blood conservation in cardiac surgery: the Society of Thoracic Surgeons and The Society of Cardiovascular Anesthesiologists clinical practice guideline //The Annals of thoracic surgery. – 2007. – Т. 83. – №. 5. – С. S27-S86.
- Sedrakyan A., Treasure T., Elefteriades J. A. Effect of aprotinin on clinical outcomes in coronary artery bypass graft surgery: a systematic review and meta-analysis of randomized clinical trials //The Journal of thoracic and cardiovascular surgery. – 2004. – Т. 128. – №. 3. – С. 442-448.
- Song H. K. et al. Safety and efficacy of prothrombin complex concentrates for the treatment of coagulopathy after cardiac surgery //The Journal of thoracic and cardiovascular surgery. – 2014. – Т. 147. – №. 3. – С. 1036-1040.
- Shapiro A. D. et al. Prospective, randomised trial of two doses of rFVIIa (NovoSeven) in haemophilia patients with inhibitors undergoing surgery //Thrombosis and haemostasis. – 1998. – Т. 79. – №. 05. – С. 773-778.
- Achneck H. E. et al. A comprehensive review of topical hemostatic agents: efficacy and recommendations for use //Annals of surgery. – 2010. – Т. 251. – №. 2. – С. 217-228.
- McManus J. G., Wedmore I. Modern Hemostatic Agents for Hemorrhage Control â A Review and Discussion of Use in Current Combat Operations. – 2005.
- Okuma M. et al. Effects of etamsylate on platelet functions and arachidonic acid metabolism //Thrombosis and haemostasis. – 1982. – Т. 48. – №. 3. – С. 330-333.
Источник
Укажите лекарственные препараты используемые с гемостатической целью укажите два варианта ответа
Плоткин Д.В., Поварихина О.А.
СОВРЕМЕННЫЕ СРЕДСТВА ЛЕКАРСТВЕННОЙ ГЕМОСТАТИЧЕСКОЙ ТЕРАПИИ
«ФАРМиндекс-Практик» выпуск 6 дата стр. 40-46 Дата выхода: ноябрь 2004 Предложения производителей и поставщиков, описания из «Энциклопедии лекарств» по упоминаемым в статье препаратам:
Кровотечение является угрожающим и наиболее опасным спутником многих ранений, повреждений и заболеваний. Где бы мы ни сталкивались с его проявлениями: в операционной, эндоскопическом кабинете, в походных условиях и в быту, от врача требуются квалифицированные и быстрые действия для его остановки и предотвращения необратимых последствий кровопотери.
Широко известна классификация кровотечений по источнику геморрагии (артериальные, венозные, капиллярные и смешанные), по направленности (внутренние и наружные) и по времени возникновения (первичные и вторичные). Первичные кровотечения возникают в момент травмы и являются непосредственными результатами ранения. Вторичные кровотечения возникают спустя какое то время после ранения по различным причинам (расплавление тромба или аррозии стенки кровеносного сосуда гнойным раневым процессом). По механизму возникновения в настоящее время кровотечения делят на механические (ранения и повреждения, а так же при разъедании сосуда воспалительным, опухолевым или другим патологическим процессом) и нейро-трофические. К последним относятся геморрагии возникшие в связи с нарушениями обмена при заболеваниях печени (декомпенссированные циррозы) крови (гемофилия, болезнь Верльгофа и др.), сепсисе и некоторых инфекционных заболеваниях (группа геморрагических лихорадок и т.д.).
В ходе эволюции у позвоночных выработались защитно-приспособительные механизмы направленные на предотвращение кровопотери. Гемостаз (haimatos — кровь, stasis — остановка) сложный процесс, который предотвращает или останавливает истечение крови из просвета сосуда, обеспечивает возникновение свертка фибрина, необходимого для репарации, и наконец, удаляет фибрин, когда нужда в этом отпадает.
Позволим себе кратко напомнить этот физиологический механизм. В первый момент тромбоциты собираются в конгломерат, закупоривая дефект в сосудистой стенке. При этом высвобождаются активные амины (АДФ, тромбоксан А2, серотонин, фактор Willebranda), которые в свою очередь вызывают дальнейшую агглютинацию кровяных пластинок, происходит вазоконстрикция и каскадно активируются факторы свертывания крови, выпадают первые нити фибрина. Сущность коагуляции заключается в последовательной активации свертывающих факторов, приводящей к расщеплению фибриногена и превращающего его в нерастворимый фибрин. Механизм коагуляции запускается следующим образом: в месте повреждения происходит контакт свертывающих факторов с коллагеном поврежденного сосуда (внутренний механизм), что в купе с активацией тканевых факторов (внешний механизм) приводит к превращению протромбина в тромбин, катализирующего превращения фибриногена в фибрин.
Безусловно, помимо образования первичного тромба в адаптационной системе человека к кровопотере принимают участие следующие факторы: снижение артериального давления, повышение тонуса и спазм периферических сосудов с замедлением кровотока, остановка секреции, снижение мочеотделения. Если кровотечение происходит не очень быстро (небольшой калибр сосуда, сдавление сосуда отечными тканями и гематомой), а компенсаторные реакции хорошо развиты, то возможна самопроизвольная его остановка.
С целью остановки кровотечение на протяжении многих веков человечество придумало бесчисленное количество способов хирургического и лекарственного гемостаза. Так в знаменитом египетском папирусе Эберса (около 3 тысяч лет до н.э.) описывается лечение кровоточащих ран с помощью наложения повязок с ароматическими маслами, меда и склеивающими веществами. Судя по археологическим находкам, древние целители Междуречья, Индии успешно останавливали кровотечение из ран путем ушивания последних, лигирования сосудов. Во времена Клавдия Галена (II век н.э.) и далее вплоть до конца XVIII века практиковалось прижигание ран каленым железом и кипящими маслами, наложение давящих повязок с травяными бальзамами для остановки раневых кровотечений. С 1879 года стала широко применяться тампонада йодоформной марлей, а так же гигроскопическими салфетками пропитанными адреналином и желатином. В 1911 году американским нейрохирургом Харви У. Кушингом были предложены прогрессивные методы местного гемостаза с использованием локального гемостатического эффекта скелетной мышцы, применение серебряных сосудистых клипс и электрокоагуляция (совместно с У. Бовье). В последующем фармацевтическая промышленность предложила хирургам множество средств местного гемостатического действия, полученных из компонентов крови человека.
Напомним, что естественный гемостаз за счет механизмов свертывания крови происходит при повреждении небольших по калибру кровеносных сосудов. При патологии свертывающей системы, а так же при повреждении средних и крупных артериальных стволов, самопроизвольная остановка кровотечения может не наступить. В таком случае от врача требуются неотложные меры направленные на предотвращение невосполнимой кровопотери.
Системные гемостатические средства — группа препаратов ускоряющих коагуляцию или ингибирующих фибринолиз. К первым относятся: свежезамороженная плазма, препараты витамина К, факторы свертывания, десмопрессин. Вторую группу составляют аминокапроновая кислота, транексамовая кислота, апротинин.
Свежезамороженная плазма (СЗП) — получают путем центрифугирования или автоматического плазмофереза из цельной донорской крови. Гемостатический эффект СЗП основан на высоком содержании факторов свертывания крови и их ингибиторов.
Препараты витамина К (менадиона натрия бисульфит) — повышает свертываемость крови за счет усиления выработки в печени факторов II (протромбин), VII (проконвертин), IX (плазменный тромбопластин), X. Эффект проявляется через 16-18 часов после внутримышечного введения 2 мл водного раствора препарата. В нашей стране известен под торговыми названиями викасол, менадион.
Десмопрессин (адиуретин, минирин, эмосинт) — является синтетическим аналогом антидиуретического гормона задней доли гипофиза (АДГ, вазопрессина). Гемостатическое действие данного препарата основано на стимуляции образования фактора Willebranda и фактора VIII. При внутривенном введении эффект наступает в течение 20-30 минут достигая максимума через 2 часа при дозировке 0,4 мкг/кг.
Этамзилат натрий (дицинон) — действие препарата связано, по-видимому, с активирующим влиянием на формирование тромбопластина. Эффект препарата проявляется через 5-15 мин после внутривенной инъекции 250-500мг, максимальный эффект достигается через 1-2 ч после введения.
Концентрат фактора VIII (антигемофильный фактор А, Коэйт-ДВИ) — получают из донорской плазмы. Катализирует реакцию превращения протромбина в тромбин и образованию фибринового сгустка. При внутривенном введении 40-50 МЕ/кг эффект наступает в течении 15 минут и обеспечивает повышение фактора VIII на 80-100%. Показания к введению препарата ограничены, в основном применяется для профилактики кровотечений в предоперационном периоде у лиц страдающих гемофилией.
Криопреципитат — так же является продуктом обработки и концентрации донорской плазмы. Препарат содержит факторы свертывания крови (VIII, XIII, Willebranda, фибриноген и фибронектин) и применяется при дефиците указанных факторов, ДВС — синдроме.
Эпсилон-аминокапроновая кислота (аминокапрон, эпсикапрон) — Гемостатическое действие основано на ингибировании фибринолиза (угнетает действие плазмина). Применяется внутривенно для остановки кровотечений при повышенной фибринолитической активности плазмы при оперативных вмешательствах на печени, поджелудочной железе, предстательной железе, легких и массивном переливании компонентов крови. При массивных кровотечениях вводится до 100 мл 5% раствора раз в 4 часа.
Транексамовая кислота (трансамча) — ингибирует действие активатора плазмина и плазминогена, обладает гемостатическим действием при кровотечениях, связанных с повышением фибринолиза. Вводится внутривенно из расчета 10-15 мг на кг массы тела. Гемостатический эффект превосходит таковой в сравнении с аминокапроновой кислотой.
Апротинин (гордокс, трасилол, контрикал, ингитрил) — так же является ингибитором фибринолиза, инактивирует протеиназы плазмы и тканей (в том числе и каллекреин). Применяемым при вторичном гиперфибринолизе в высоких дозах (до 1 млн единиц). В нашей стране широко известен, как антиферментный препарат, использующийся при комплексном лечении панкреатитов.
Местные гемостатические средства — приемы местного гемостаза подразделяются на механические, термические и химические.
Рассмотрим подробней химические гемостатики. Из применяемых препаратов одни являются вазоконстрикторами, другие прокоагулянтами, а третьи проявляют гигроскопические свойства, что помогает «запломбировать» поврежденный сосуд. В настоящее время в медицине широко используются желатиновые пенки и пластинки, коллагеновые пленки, фибриновый клей, целлюлоза и комбинированные средства.
Желатиновые губки («Спонгостан», «Жельфоум») — имеют однородную пористую структуру, изготавливаются из высушенной очищенной желатиновой пены. Локальный гемостатический эффект основан на активации тромбоцитов, попадающих в поры губки, формировании тромбоцитарного агрегата на ее поверхности и образовании фибринового сгустка. Данные средства идеальны при капиллярных, паренхиматозных и венозных кровотечениях в стоматологии, малой проктологии, абдоминальной хирургии, отоларингологии и гинекологии. Полная биодеструкция губок наступает через 3-5 недель.
Коллагеновые пластинки («ТиссуФлайс», коллагеновая гемостатическая губка завода «Белкозин», «Колапол») — широко распространенные местные гемостатические средства кровоостанавливающий эффект которых основан на агрегации тромбоцитов на разветвленной сети коллагеновых волокон пластины. Применяются в общехирургической практике для остановки паренхиматозных и капиллярных кровотечений, остановки кровотечения из синусов твердой мозговой оболочки и костномозговых каналов, регенерации костной ткани. Нередко комбинируются с антисептическими и препаратами и антибиотиками.
Губка гемостатическая коллагеновая состоящая из коллагена, фурацилина и борной кислоты, оказывает гемостатическое действие, стимулирует восстановление тканей, полностью рассасывается в полости или ране. Губка используется при местном гемостазе при операциях на паренхиматозных органах, после лазерной операции эрозий шейки матки; при остановке постэкстракционного альвеолярного кровотечения и носовых кровотечений; может быть использована как раневое покрытие при лечении ран, трофических язв и пролежней. Применяется в общей хирургии, гинекологии.
Фибриновый клей («Тиссукол Кит», «Берипласт») — основные компоненты клея (фибриноген, фактор XIII, тромбин) выделяются из донорской плазмы. При нанесении на раневую поверхность происходит полимеризация клея с образованием эластичной фибриновой пленки. В ходе заживления раны образовавшийся фибриновый сверток полностью рассасывается. Клей применяется в хирургической практике для остановки паренхиматозных и капиллярных кровотечений, герметизации анастомозов, склеивания и фиксации тканей.
Препараты целлюлозы («Гемостаз», «Оксицелодекс», «Серджисел») — порошки состоящие из окисленной целлюлозы, полиглюкина и воды. Готовятся непосредственно перед применением и используются в качестве гемостатического пломбировочного материала в стоматологии, а так же при пункционных транскутанных биопсиях паренхиматозных органов.
Комбинированные препараты — одним из самых надежных и применяемых в практике комбинированных локальных гемостатических средств является «ТахоКомб». Препарат состоит из коллагеновой пластины, покрытой сухими фибриногеном, тромбином и апротенином (ингибитор фибринолиза). После контакта с раневой кровоточащей поверхностью факторы свертывания растворяются и создают прочные связи между коллагеном и раневой поверхностью, одновременно тромбин катализирует превращение фибриногена в фибрин, а апротенин тормозит фибринолиз. Полная биодегенерация пластины происходит в организме в течении 3-6 недель. Используется в качестве местного гемостатика в общехирургической практике при кровотечениях из паренхиматозных органов, при операциях аорто-коронарного шунтирования (гемостаз в местах проколов) и других оперативных пособиях.
Необходимо так же упомянуть о местном действии некоторых системных вазоконстрикторов, таких как адреналин (эпинефрин), но в настоящее время применение их ограничено стоматологией, отоларингологией и эндоскопической практикой при кровоточивости слизистых оболочек и гастродуоденальных язв.
В заключении хочется подчеркнуть, что все многообразие местных и системных гемостатических средств не заменяет хирургического гемостаза при кровотечениях из крупных венозных и артериальных стволов. Совершенствование методов остановки кровотечения и появление новых лекарственных гемостатиков позволяет надежно и эффективно бороться с кровопотерей, что в условиях современного дефицита компонентов крови является социальной и экономической необходимостью.
1. Диагностика и лечение ранений / Под редакцией Ю.Г.Шапошникова. М.: Медицина, 1984.- 340 с.
2. Кузнецов Н.А. Современные технологии лечения острой кровопотери // Consilium medicum.- 2003.- № 6.- С.347-357.
3. Молчанов И.В., Гольдина О.А., Горбачевский Ю.В. Растворы гидроксиэтилированного крахмала — современные и эффективные плазмозамещающие средства инфузионной терапии. Монографический обзор. М.: Издательство НЦССХ им. А.Н.Бакулева, РАМН., 1998.- 138 c.
4. Раны и раневая инфекция / Под ред. М.И.Кузина, Б.М.Костюченок. М: Медицина, 1990.- 592 c.
5. Arand A.G., Sawaya R. Intraoperative chemical hemostasis in neurosurgery // Neurosurgery.- 1986.- Vol.18, №2.- P.223-233.
6. Browder I.W., Litwin M.S. Use of absorbable collagen for hemostasis in general surgical patients // Am. Surg.- 1986.- Vol.52, №9.- P.492-494.
7. DeLustro F., Dasch J., Keefe J., Ellingsworth L. Immune responses to allogeneic and xenogeneic implants of collagen and collagen derivatives // Clin. Orthop.- 1990.- Vol.260.- P.263-279.
8. Evans B.E. Local hemostatic agents // NY State. Dent. J.- 1977.- Vol.47, №4.- 109-114.
9. Evans B.E. Local hemostatic agents (and techniques) // Scand. J. Haematol.- 1984.- Vol.33, Ssuppl.40.- P.417.
10. Haemostasis and Thrombosis / Eds. A.L.Bloom, D.P.Thomas. London: Churchill Livingstone, 1987.- P.614-615.
11. Light R.E. Hemostasis in Neurosurgery // J. Neurosurgery.- 1945.- Vol.2, №5.- P.414-434.
12. Light R.E., Prentice H.Z. Surgical investigation of a new absorbable sponge derived from gelatin for use in hemostasis // J. Neurosurgery.- 1945.- Vol.2, №5.- P.435-455.
13. Lindstrom P.A. Complications from the use of absorbable hemostatic sponges // AMA Arch. Surg.- 1956.- Vol.73.- P.133-141.
14. Principles of Surgery / Ed. by S.I.Schwartz / 7th Edition.- New York: McGraw-Hill, 1999.- P.92-93.
15. Pupka A., Chudoba P., Barc P. et al. Intraoperative hemostasis during kidney transplantation and the use collagen mesh dressing covered by fibrin glue (TachoComb) // Polim. Med.- 2003.- Vol.33, №3.- P.27-32.
16. Rosand J., Eckman M.H., Knudsen K.A. et al. The effect of warfarin and intensity of anticoagulation on outcome of intracerebral hemorrhage // Аrch. Intern. Med.- 2004.- Vol.164, №8.- P.880-884.
17. Tsurutani H., Ohkuma H., Suzuki S . Effects of thrombin inhibitor on thrombin-related signal transduction and cerebral vasospasm in the rabbit subarachnoid hemorrhage model // Stroke.- 2003.- Vol.34, №6.- P.1497-1500.
Источник