- В России расширили перечень стратегически значимых лекарств
- Расширен список стратегически значимых препаратов
- Подходы к формированию проекта Национальной лекарственной политики. Часть 2
- Национальная лекарственная политика как документ стратегического планирования
- О Национальной лекарственной политике
- Цели и задачи Национальной лекарственной политики
- Разработка Национальной лекарственной политики
- Основы стратегического планирования в Российской Федерации
- Достижения и проблемы системы лекарственного обеспечения в Российской Федерации сегодня
В России расширили перечень стратегически значимых лекарств
Правительство утвердило список стратегически значимых лекарств, которые должны производить в России. В новый перечень вошли 215 препаратов, в том числе вакцины из национального календаря профилактических прививок и календаря прививок по эпидемическим показаниям.
«В новый список войдут 215 позиций из перечня жизненно необходимых и важнейших лекарств», — сообщил глава кабмина, отметив, что среди этих препаратов значатся лекарства для лечения орфанных и социально значимых заболеваний. Все эти препараты будут производиться в России.
ПЕРЕЧЕНЬ
стратегически значимых лекарственных средств, производство которых должно быть обеспечено на территории Российской Федерации
- Абакавир
- Абакавир+Ламивудин
- Абиратерон
- Адалимумаб
- Азатиоприн
- Азитромицин
- Алирокумаб
- Алпростадил
- Алтеплаза
- Амикацин
- Амиодарон
- Амлодипин
- Амоксициллин
- Амоксициллин+Клавулановая кислота
- Ампициллин
- Антитимоцитарный глобулин
- Апиксабан
- Апротинин
- Аспарагиназа
- Атазанавир
- Атенолол
- Аторвастатин
- Афлиберцепт
- Ацетилсалициловая кислота
- Бевацизумаб
- Бедаквилин
- Бензатина бензилпенициллин
- Бисопролол
- Бозентан
- Бортезомиб
- Бупренорфин
- Вакцины в соответствии с национальным календарем профилактических прививок и календарем профилактических прививок по эпидемическим показаниям
- Вальпроевая кислота
- Варфарин
- Верапамил
- Гемцитабин
- Гепарин натрия
- Гидроксикарбамид
- Гидроксихлорохин
- Гидрохлоротиазид
- Гидрокортизон
- Глатимера ацетат
- Глюкагон
- Гозерелин
- Дабигатрана этексилат
- Дазатиниб
- Дакарбазин
- Дапаглифлозин
- Дапсон
- Даратумумаб
- Дарбэпоэтин альфа
- Дарунавир
- Даунорубицин
- Дексаметазон
- Диазепам
- Дигоксин
- Диметилфумарат
- Добутамин
- Доксазозин
- Доксициклин
- Доксирубицин
- Долутегравир
- Дорназа альфа
- Доцетаксел
- Зидовудин
- Золедроновая кислота
- Зуклопентиксол
- Ибрутиниб
- Идарубицин
- Изониазид
- Изосорбида динитрат
- Иматиниб
- Имиглюцераза
- Иммуноглобулин человека нормальный
- Индапамид
- Инсулин аспарт
- Инсулин аспарт двухфазный
- Инсулин гларгин
- Инсулин деглудек
- Инсулин лизпро
- Инсулин лизпро двухфазный
- Инсулин-изофан
- Интерферон бета-la
- Интерферон бета-lb
- Йогексол
- Иринотекан
- Кабазитаксел
- Канамицин
- Капецитабин
- Капреомицин
- Каптоприл
- Карведилол
- Кармустин
- Кетамин
- Клоназепам
- Клонидин
- Клопидогрел
- Ламивудин
- Ламивудин+Зидовудин
- Левомепромазин
- Левосимендан
- Левотироксин натрия
- Левофлоксацин
- Лейпрорелин
- Леналидомид
- Лизиноприл
- Линезолид
- Лозартан
- Ломустин
- Лопинавир+Ритонавир
- Маравирок
- Мелфалан
- Меропенем
- Метилдопа
- Метопролол
- Мидазолам
- Микофенолата мофетил
- Микофеноловая кислота
- Митоксантрон
- Митотан
- Моксифлоксацин
- Моксонидин
- Мороктоког альфа
- Морфин
- Налтрексон
- Невирапин
- Нилотиниб
- Нимодипин
- Нитроглицерин
- Нифедипин
- Нонаког альфа
- Норэпинефрин
- Оксалиплатин
- Оксибутират натрия
- Омализумаб
- Пазопаниб
- Паклитаксел
- Панитумумаб
- Пембролизумаб
- Пеметрексед
- Пентоксифиллин
- Периндоприл
- Пертузумаб
- Пиразинамид
- Преднизолон
- Прокарбазин
- Пропионилфенил-этоксиэтилпиперидин
- Пропранолол
- Протионамид
- Проурокиназа
- Пэгинтерферон альфа-2а
- Ралтегравир
- Ривароксабан
- Рилпивирин+Тенофовир+Эмрицитабин
- Рисперидон
- Ритонавир
- Ритуксимаб
- Рифабутин
- Рифампицин
- Саквинавир
- Симвастатин
- Сорафениб
- Соталол
- Спарфлоксацин
- Спиронолактон
- Сунитиниб
- Такролимус
- Темозоломид
- Тенектеплаза
- Тенофовир
- Теризидон
- Терифлуномид
- Тикагрелор
- Тиотропия бромид
- Тиоуреидоиминометилпиридиния перхлорат
- Тобрамицин
- Трамадол
- Трастузумаб
- Трастузумаб эмтанзин
- Третиноин
- Тримеперидин
- Трипторелин
- Урапидил
- Фактор некроза опухоли альфа-I
- Фактор свертывания крови VIII
- Фактор свертывания крови VIII + Фактор Виллебранда
- Факторы свертывания крови II, VII, IX, X
- Фентанил
- Финголимод
- Флударабин
- Фосампренавир
- Фосфазид
- Фулвестрант
- Фуросемид
- Цепэгинтерферон альфа-2b
- Цетуксимаб
- Цефтриаксон
- Циклосерин
- Циклофосфамид
- Ципрофлоксацин
- Цитарабин
- Эверолимус
- Экулизумаб
- Элсульфавирин
- Эмпаглифлозин
- Эналаприл
- Эноксапарин натрия
- Эпинефрин
- Эптаког альфа (активированный)
- Эрибулин
- Этамбутол
- Этанерцепт
- Этионамид
- Этравирин
- Эфавиренз
Источник
Расширен список стратегически значимых препаратов
«При формировании перечня мы совместно с Минздравом России опирались на действующие стандарты лечения и клинические рекомендации, учитывали мнение главных внештатных специалистов Минздрава России, основные тренды и направления развития отечественной фармотрасли», – сообщил на заседании правительства первый заместитель министра промышленности и торговли РФ Сергей Цыб.
В список вошли препараты, предназначенные для оказания скорой медицинской помощи, лечения инсулинозависимого сахарного диабета, онкологических и орфанных заболеваний, ВИЧ-инфекции, гепатитов.
Среди них противоопухолевый препарат леналидомид (Ревлимид от Celgene), который по программе «14 ВЗН» поставляет «Фармстандарт». Препарат является лидером по сумме затрат по госпрограмме – в 2019 году Миндздрав закупил леналидомид на 8,24 млрд рублей. «Фармстандарт» в июне 2020 выиграл ряд конкурсов на поставку препарата на 2020 год на 5,8 млрд рублей. Еще одним из включенных в расширенный перечень стал онкогематологический препарат ибрутиниб (Имбрувика от J&J), который в 2019 году закупили на 3,65 млрд рублей.
Вошли в список пембролизумаб (Китруда от MSD) – в 2019 году закупался на 7,795 млрд рублей, пертузумаб (Перьета от Roche, упаковывает «Р-фарм») – закупался на 6,6 млрд рублей, сунитиниб (Сунитиниб-натива от «Натива») – 4,05 млрд рублей.
Минпромторг реализует политику импортозамещения в фармпромышленности с 2009 года с помощью различных стратегий и программ – «Стратегии развития фармпромышленности до 2020 года», федеральной целевой программы и госпрограммы «Фарма-2020». Стратегически значимые лекарственные препараты (СЗЛП) являются определенным индикатором реализации задекларированных в этих документах планов. Госпрограмма, например, предполагала, что в 2018 году доля отечественных лекарств в номенклатуре перечня СЗЛП составит 90%, но по факту она достигла, по данным Vademecum, лишь 68%.
В 2019 году правительство решило продлить действие госпрограммы до 2024 года. Доля отечественных лекарств в номенклатуре ЖНВЛП должна к 2024 году вырасти до 93%, а в общем объеме потребления (в деньгах) – до 53%. Объем финансирования (108,2 млрд рублей) вырос еще на 47,5 млрд рублей.
Готовится к принятию новый отраслевой документ. Минпромторг разработал обновленную стратегию развития отечественного фармпроизводства, рассчитанную уже до 2030 года («Фарма‑2030»). Она находится на утверждении в правительстве.
Источник
Подходы к формированию проекта Национальной лекарственной политики. Часть 2
Национальная лекарственная политика как документ стратегического планирования
О Национальной лекарственной политике
В 1975 г. 28-я Всемирная ассамблея здравоохранения приняла резолюцию, рекомендующую всем странам – членам Всемирной организации здравоохранения (ВОЗ) разработать Национальную лекарственную политику (НЛП).
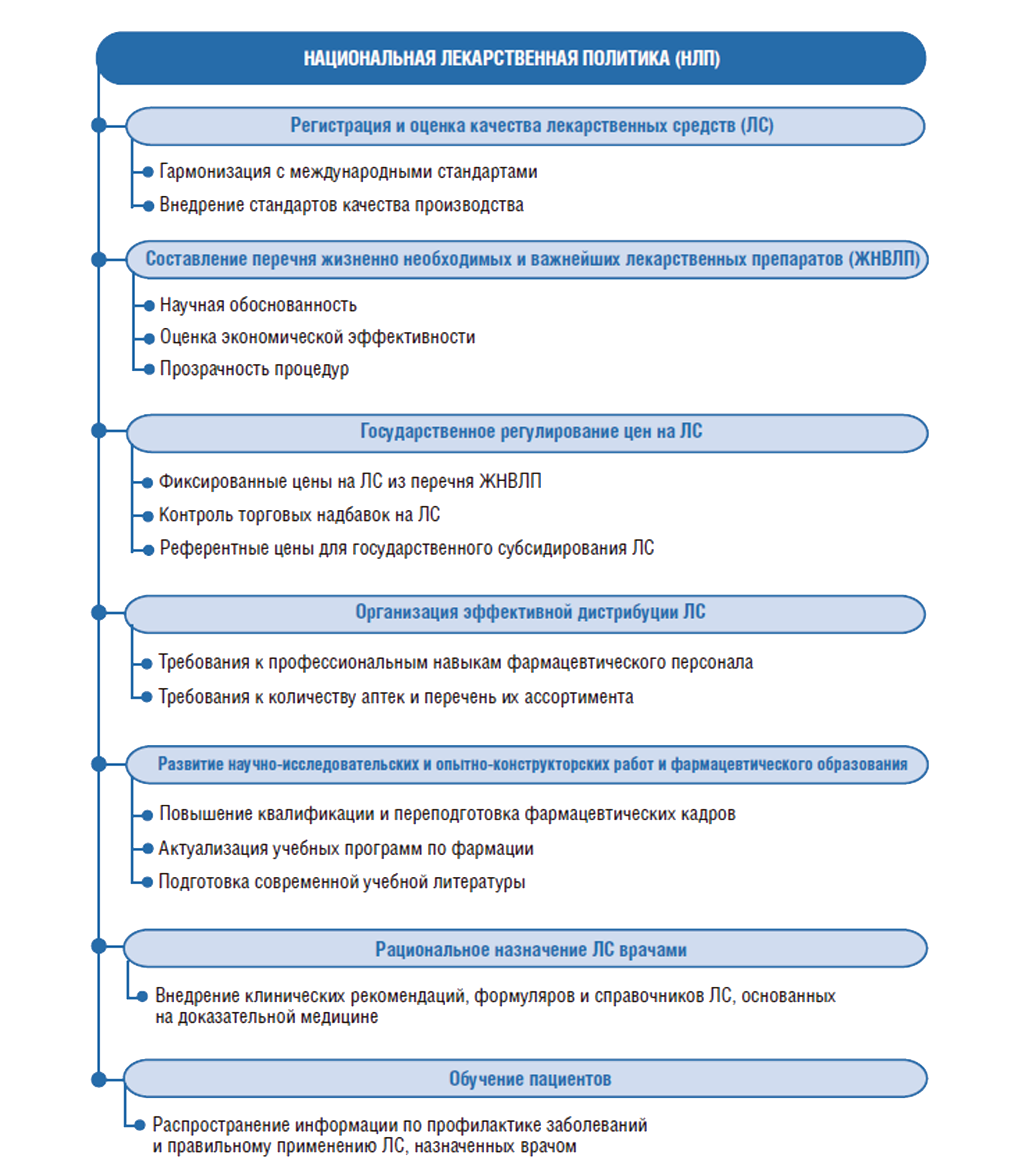
НЛП сегодня принята в 133 странах мира (из 165 исследованных стран [1] ) и есть практически во всех странах Европейского союза (ЕС). НЛП – это стратегический документ, который разрабатывается на долгосрочную перспективу, как правило, 10 лет. Он объединяет и балансирует роли многочисленных участников фармацевтического рынка – от разработки новых лекарств до их рационального потребления. Основные разделы НЛП представлены на рис.1.
Рисунок 1. Составляющие Национальной лекарственной политики 
Цели и задачи Национальной лекарственной политики
Все правила и задачи, которые устанавливает данная политика, должны быть подчинены единым целям государства в этой сфере. Для России цели Национальной лекарственной политики вытекают из указов Президента РФ В.В. Путина – № 204 от 07.05.2018 «О национальных целях и стратегических задачах развития Российской Федерации на период до 2024 года» и № 642 от 01.12.2016 «О Стратегии научно-технологического развития Российской Федерации». Это:
1) увеличение ожидаемой продолжительности жизни (ОПЖ) до 78 лет к 2024 г. и до 80 лет к 2030 г.;
2) обеспечение безопасности (независимости) РФ в сфере лекарственного обращения;
3) восстановление передового научно-технологического потенциала в разработке и производстве новых лекарственных препаратов (ЛП).
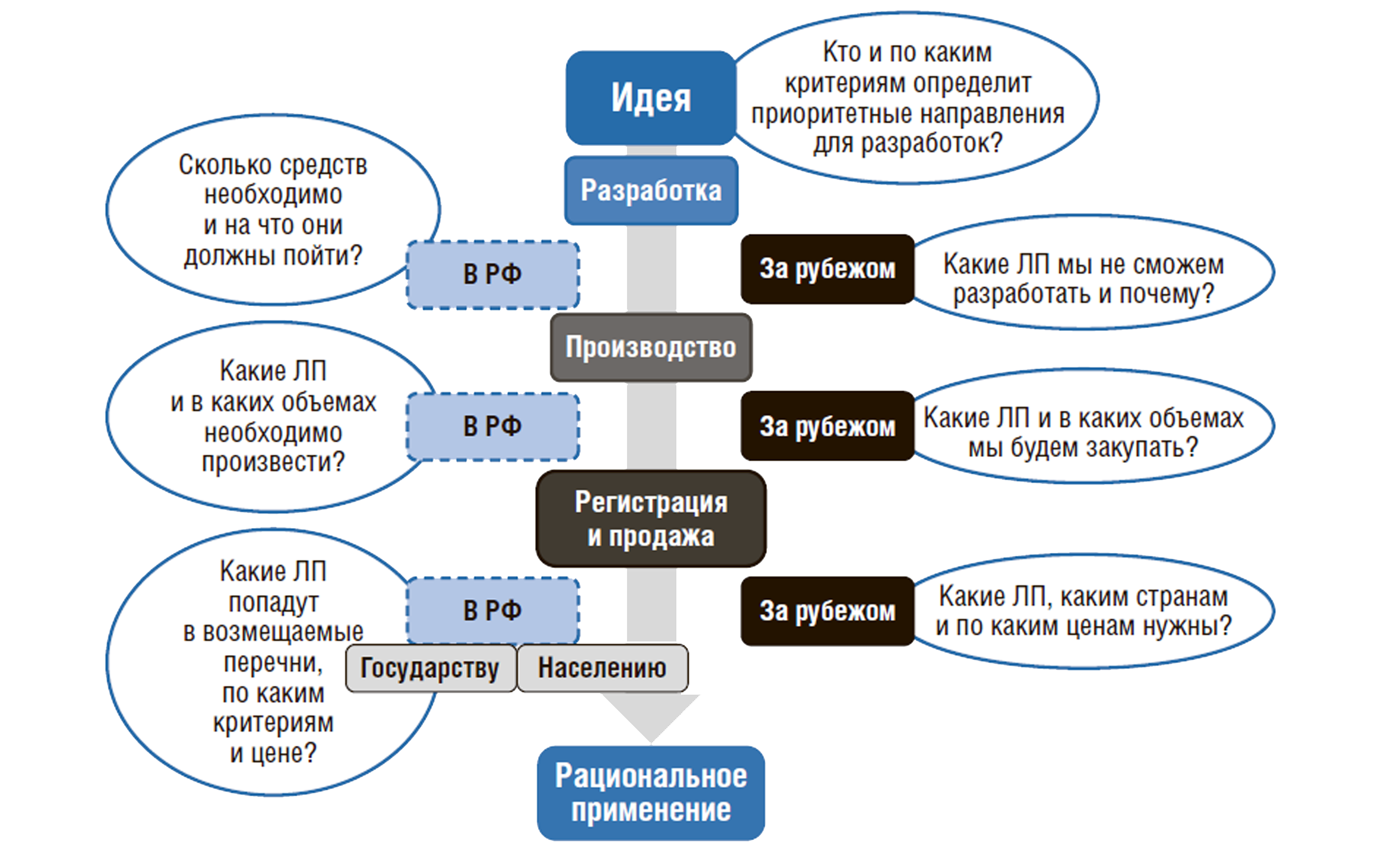
Исходя из данных целей НЛП должна ответить на ряд существенных вопросов, которые схематично представлены на рис. 2.
Рисунок 2. Вопросы, на которые должна ответить Национальная лекарственная политика
Отметим, что фармацевтический рынок не является саморегулируемым, он требует от государственных органов власти постоянного вмешательства во все процессы лекарственного обращения. Сегодня в России в регулировании этого рынка задействованы Министерство здравоохранения (Минздрав России), которое обеспечивает доступность лекарств для населения и их закупку, Министерство промышленности и торговли (Минпромторг России), отвечающее за развитие отечественного производства лекарств, Министерство науки и высшего образования (Минобрнауки России), которое занимается разработкой новых лекарств, Федеральная служба по надзору в сфере здравоохранения (Росздравнадзор), обеспечивающая качество и безопасность обращающихся на рынке лекарственных препаратов, и Федеральная антимонопольная служба (ФАС), контролирующая вопросы ценообразования на ЛП.
Соответственно принципиально важно, чтобы разработка НЛП носила межведомственный характер, а ведомственные стратегии развития были согласованы с ней и между собой. Система планирования и регулирования должна быть выстроена таким образом, чтобы разработанные и произведенные в России лекарства были действительно востребованы для снижения смертности, заболеваемости и инвалидности наших граждан, а фармацевтические производители знали объем внутреннего рынка на предстоящие годы, чтобы спланировать свои мощности.
При формировании этой политики «регуляторы-ведомства» сталкиваются с двумя непростыми задачами. Первая – необходимость соблюдения оптимального баланса между интересами множества субъектов лекарственного обращения: разными группами пациентов и их объединениями, фармацевтическими компаниями (в том числе отечественными и зарубежными производителями), оптовыми и розничными дистрибьюторами (государственными и частными), врачами и их общественными объединениями. Вторая – финансовые ограничения: общественные средства, направляемые на оказание бесплатной медицинской помощи, ограничены в любой стране.
В этой связи решение такой сложной многофакторной и межведомственной задачи, как разработка НЛП, требует серьезных научных обоснований, правильной расстановки приоритетов и неоднократных обсуждений.
Разработка Национальной лекарственной политики
Научное обоснование НЛП инициировала Российская академия наук (РАН), а головное ведомство в этой сфере – Минздрав России поддержал эту идею. Сегодня в РАН создан межведомственный Совет по научному обоснованию и сопровождению НЛП под руководством академика РАН В.П. Чехонина.В рамках 4 рабочих групп организована подготовка материалов по основным вопросам регулирования:
1. Координация фундаментальных и прикладных исследований в области разработки, создания и производства лекарственных средств (координатор – член-корр. РАН А.Д. Дурнев).
2. Оптимальные механизмы реализации системы всеобщего лекарственного возмещения (обеспечения) (координатор – акад. РАН Р.У. Хабриев).
3. Совершенствование системы формирования перечней ЛП и ценообразования на них (координатор – член-корр. РАН А.Л. Хохлов).
4. Обеспечение рационального и безопасного применения ЛП (координатор – член-корр. РАН Д.А. Сычев).
За общую координацию работ по научному обоснованию отвечает ученый секретарь Совета доктор медицинских наук Г.Э. Улумбекова. Следует отметить, что формировать стратегические документы и программы намного легче, когда поставлены конкретные цели. Мерилом предлагаемых решений в этих программах и стратегиях является время достижения целей и эффективность, т.е. возможность достижения результата за минимальные средства. Это главные принципы стратегического планирования.
Основы стратегического планирования в Российской Федерации
В РФ имеется серьезная база по стратегическому планированию:
- Федеральный закон от 28.06.2014 № 172-ФЗ (ред. от 31.12.2017) «О стратегическом планировании в Российской Федерации»;
- Постановление Правительства РФ от 02.08.2010 № 588 (ред. от 15.11.2017) «Об утверждении Порядка разработки, реализации и оценки эффективности государственных программ Российской Федерации»;
- Постановление Правительства РФ от 26.06.1995 № 594 (ред. от 28.12.2017) «О реализации Федерального закона “О поставках продукции для федеральных государственных нужд” (вместе с “Порядком разработки и реализации федеральных целевых программ и межгосударственных целевых программ, в осуществлении которых участвует Российская Федерация”, “Порядком закупки и поставки продукции для федеральных государственных нужд”, “Порядком подготовки и заключения государственных контрактов на закупку и поставку продукции для федеральных государственных нужд”)».
- Постановление Правительства РФ от 15.10.2016 № 1050 «Об организации проектной деятельности в Правительстве Российской Федерации (вместе с “Положением об организации проектной деятельности в Правительстве Российской Федерации”)».
- Методические рекомендации по подготовке паспорта приоритетного проекта правительства РФ от 20.10.2016 № 7951п-п6;
- Методические указания по разработке национальных проектов (программ), утверждены Правительством РФ 05.05.2018.
Соподчинение названных документов стратегического планирования представлено на рис. 3.
Рисунок 3. Соподчинение главных стратегических документов в части достижения ожидаемой продолжительности жизни 78 лет
НЛП, согласно этим нормативным документам, должна сбалансировать стратегии различных ведомств и роли различных сторон в интересах достижения поставленных целей (рис. 4).
Рис. 4.  Национальная лекарственная политика на стыке отраслевых стратегий и программ
Национальная лекарственная политика на стыке отраслевых стратегий и программ
1. Анализ – оценка состояния соответствующей сферы.
2. Прогнозы развития на долгосрочный период.
3. Приоритеты, задачи и показатели для их измерения.
4. Способы их эффективного достижения.
5. Сроки и этапы проведения мероприятий.
6. Ожидаемые результаты проведения мероприятий.
7. План мероприятий на среднесрочный период.
В соответствии с этими рекомендациями и будут формироваться основные разделы НЛП.
Достижения и проблемы системы лекарственного обеспечения в Российской Федерации сегодня
В РФ за последние годы благодаря государственной политике достигнуты серьезные позитивные сдвиги в сфере лекарственного обращения, а именно: принят основной Федеральный закон от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств», развивается отечественная фармацевтическая промышленность, осуществляется жесткий контроль за ценами на ЛП из списка жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП), существенно повышена прозрачность процессов включения лекарств в этот перечень, внедряется система идентификации ЛП от производителя до конечного потребителя.
Вместе с тем сохраняются проблемы. Главные из них подробно разобраны в части 1 «Анализ рынка лекарственных препаратовв РФ» (см.: ОРГЗДРАВ: новости, мнения, обучение. Вестник ВШОУЗ. 2018. Т. 4, № 4. С. 53–75).
1. Недостаточное лекарственное обеспечение населения ЛП в амбулаторных условиях – сегодня за счет государства на ЛП в РФ тратится в 2,4 раза меньше в доле ВВП, чем в «новых» странах ЕС, имеющих близкий уровень экономического развития (в 2,8 раза меньше по доллару ППС). В РФ эти средства идут только на лекарственное обеспечение тех категорий населения, которые имеют специальные льготы. Всего в РФ получают бесплатные лекарства в амбулаторных условиях за счет государства только 9 млн человек, а в развитых странах – все, кто нуждается. Кстати, в названных странах сегодня продолжительность жизни составляет 78 лет, показатель которого должна достичь РФ к 2024 г.
2. Различия в лекарственном обеспечении в разных субъектах РФ, связанные с отсутствием единых подходов в формировании перечней ЖНВЛП и ценовой политики, в ряде случаев имеет место нерациональное применение лекарств. Все это вызывает недовольство населения. Так, среди опрошенных ВЦИОМ доля граждан, которые не смогли купить необходимое лекарство из-за высокой цены, с 2013 по 2017 г. увеличилась на 20% (с 39 до 47%), также растет число обращений граждан на «горячую линию» Росздравнадзора по поводу доступности ЛП.
При формировании стратегических документов предварительно необходимо определить значения макроиндикаторов и оценить объемы необходимых ресурсов для достижения поставленных целей. В части 3, проведена оценка потребностей в необходимых объемах финансирования лекарственного обеспечения в амбулаторных условиях на ближайшие 2–5 лет и показателей по разработке новых лекарств в РФ на перспективу 10 лет.
1 Улумбекова Г.Э., Калашникова А.В. Подходы к формированию концепции национальной лекарственной политики. Часть 1. Анализ рынка лекарственных препаратов в РФ // ОРГЗДРАВ: новости, мнения, обучение. Вестник ВШОУЗ. 2018. Т. 4, № 4. С. 53–75.
Источник
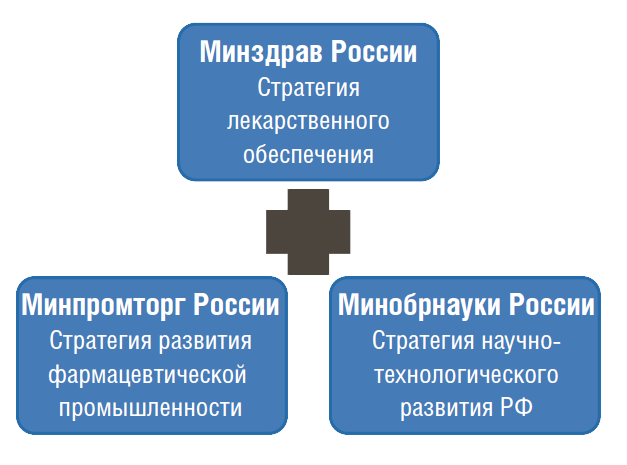 Национальная лекарственная политика на стыке отраслевых стратегий и программ
Национальная лекарственная политика на стыке отраслевых стратегий и программ

