- Особенности применения пародонтальных повязок в клинической практике
- ХАРАКТЕРИСТИКА ГРУПП ПОВЯЗОК
- Мягкие пародонтальные повязки
- Полутвердые пародонтальные повязки
- Твердые пародонтальные повязки
- Клеевые композиции
- Коллагеновые пленки
- Повязки, изготавливаемые ex tempore
- Стоматологические лекарственные пленки это
Особенности применения пародонтальных повязок в клинической практике
Д. Р. Мушарапова
студентка 4-го курса стоматологического факультета ГОУ ВПО «Казанский ГМУ» Росздрава
Л. Р. Мухамеджанова
д. м. н., доцент, заведующая кафедрой терапевтической стоматологии ГОУ ВПО «Казанский ГМУ» Росздрава
Современный отечественный и зарубежный фармацевтический рынок предлагает растущий с каждым днем ассортимент лекарственных препаратов, применяющихся для лечения заболеваний пародонта и слизистой оболочки полости рта. Препараты для местной фармакотерапии этих заболеваний представлены разнообразными гелями, мазями, коллагеновыми и клеевыми композициями. Многие из них разработаны специально для апплицирования на ткани пародонта, отличающиеся сложными топографо-анатомическими особенностями, богатым кровоснабжением и иннервацией. В процессе местного лечения лекарственные вещества, введенные в пародонтальные карманы, быстро вымываются из них, что снижает лечебный эффект препаратов. Кроме того, после оперативных вмешательств, например кюретажа пародонтальных карманов, раневая поверхность практически не защищена от травм при приеме пищи и инфицирования содержимым полости рта. Избежать этих недостатков можно путем использования пародонтальных повязок.
Пародонтальные повязки-аппликаты, фиксируемые различными способами на ткани пародонта Лечебные пародонтальные повязки служат для пролонгирования действия лекарственных препаратов в пародонтальных карманах при медикаментозном лечении и после хирургических вмешательств, ускоряя регенерацию эпителиальных и соединительнотканных структур. Целью нашего исследования является разработка требований, предъявляемых к пародонтальным повязкам, уточнение классификации пародонтальных повязок, разработка критериев эффективности пародонтальных повязок. МЕТОДЫ ИССЛЕДОВАНИЯ: обзор литературы по данной проблеме, изучение предложений отечественного и зарубежного фармацевтического рынка. В ходе исследования нами была проведена сравнительная оценка эффективности использования различных групп пародонтальных повязок, предложена собственная классификация.
Требования к пародонтальным повязкам:
должны быть устойчивы к влажной среде полости рта;
текстильный материал пародонтальной повязки должен быть совместим с лекарственным препаратом;
обладать приемлемыми органолептическими свойствами (вид, цвет, запах).
ХАРАКТЕРИСТИКА ГРУПП ПОВЯЗОК
Анализ предложений фармацевтического рынка позволил сделать вывод о том, что классификация пародонтальных повязок несколько отстает от времени, и мы предлагаем свою классификацию (1, 2, 3, 6-я группы повязок описываются во многих учебных руководствах по пародонтологии и широко применяются, а 4-я и 5-я группы включены нами и относятся к более современным).
Классификация пародонтальных повязок (Л. Р. Мухамеджанова, Д. Р. Мушарапова, 2010)
1. Мягкие пародонтальные повязки. 2. Полутвердые пародонтальные повязки. 3. Твердые пародонтальные повязки. 4. Клеевые композиции. 5. Коллагеновые пленки. 6. Повязки, изготавливаемые ex tempore.
Мягкие пародонтальные повязки
Наиболее часто используемая группа пародонтальных повязок. Отличается относительной простотой изготовления, дешевизной, однако фиксировать на тканях пародонта такие пародонтальные повязки достаточно сложно. Накладывается такая повязка не более чем на 5–7 минут. Для изготовления мягких пародонтальных повязок используются мягкие лекарственные формы: мази на водорастворимой и жирорастворимой основе, гели, пасты. Наиболее часто используемые мягкие лекарственные формы — мазь тетрациклиновая 1- и 3%-ная, мазь бетадиновая, мазь метилурациловая 10%-ная, мази гепариновая, бутадионовая, индометациновая.
Гели: солкосерил, куриозин, актовегин. В качестве носителя могут быть использованы вата, бинт (марля) или другой текстильный материал.
Существует 2 способа наложения повязки:
На текстильный носитель нужного размера наносят мягкую лекарственную форму и шпателем равномерно распределяют по всей поверхности. Затем фиксируют на альвеолярном отростке таким образом, чтобы центральная часть пародонтальной повязки была перекинута через режущий край зубов, а маргинальная и альвеолярная десны были покрыты. Размер текстильного носителя нужно рассчитать таким образом, чтобы пародонтальная повязка перекрывала границу с вестибулярной и оральной стороны.
Подготавливают 2 полости из текстильного носителя размером 3 х 0,5 см, наносят на них мягкую лекарственную форму и прикрепляют на вестибулярную и оральную поверхности альвеолярного отростка. При этом способе повязка удерживается за счет адгезивных механизмов.
Полутвердые пародонтальные повязки
Эта группа пародонтальных повязок используется значительно реже, поскольку требует определенных временных затрат. Эти повязки хорошо фиксируются на альвеолярном отростке за счет эффекта затвердевания, однако спектр лекарственных форм, применяемых для этих целей, весьма ограничен: только мази, изготовленные на жирной (ланолин, вазелин) основе. Способ изготовления: на плато смешивают в равных количествах дентин-пасту и мазь до консистенции густой сметаны. Затем эту массу быстро переносят на заранее приготовленный текстильный носитель нужного размера и фиксируют на альвеолярном отростке. Пациента просят сомкнуть челюсти и посидеть 3–7 минут. За это время повязка затвердевает.
В полости рта такая повязка удерживается в течение 3–7 часов, затем начинает крошиться. Появление крошек — сигнал к снятию повязки.
Твердые пародонтальные повязки
Твердые пародонтальные повязки подразделяются на 2 группы: 1. Готовые пародонтальные повязки(septopack). 2. Твердые 2-слойные повязки, изготавливаемые с использованием оттискных стоматологических материалов (репин, дентол).
Способ изготовления повязки septopack: при работе с данными препаратами пользоваться только сухим и стерильным шпателем; взятому этим инструментом небольшому количеству пасты в зависимости от последующего применения следует придать конусовидную или шарообразную форму. При этом на препарат не должна попадать влага. В полости рта остается пластичной лишь в течение 2–3 минут после нанесения на обрабатываемый участок, затвердевает за полчаса. Время экспозиции — до суток.
Клеевые композиции
Одна из перспективных групп пародонтальных повязок. К клеевым композициям относится клеевая повязка КЛ-3, которая представляет собой клеевую композицию на основе полиуретана, является нетоксичным биологически совместимым препаратом, аутостерильна. При нанесении на слизистую оболочку десны она полимеризуется с образованием пористой высокопластичной пленки.
Коллагеновые пленки
Коллагеновые пленки — саморассасывающиеся адгезивные пленки, пропитанные различными лекарственными веществами, например «Диплен-Дента М» с метронидазолом, «Диплен-Дента Л» с линкомицином, «Диплен-Дента ХД» с хлоргексидином и дексаметазоном, «Диплен-Дента ЛХ» с лидокаином и хлоргексидином. Пленка прозрачна, хорошо фиксируется к влажной поверхности слизистой оболочки полости рта и не вызывает дискомфорта у пациентов. Может использоваться в качестве пародонтальной повязки после проведения вмешательств на тканях пародонта, а также в качестве самостоятельного средства патогенетической терапии. Продолжительность курса лечения варьируется от 7 до 20 дней в зависимости от степени тяжести заболевания при ежедневном проведении аппликаций 1 или 2 раза в сутки. «Диплен-Дента ЛХ» применяется для поверхностной анестезии перед удалением над- и поддесневых зубных отложений и кюретажем пародонтальных карманов, а также при лечении поражений тканей полости рта с выраженной болевой симптоматикой (раны, афты, язвы, пролежни от зубных протезов и др.).
Способ изготовления повязки: извлеченную из упаковки пленку нарезают полосками длиной 5 см и шириной около 1 см и накладывают клеящей (нижней) стороной на десну в области всех зубов. Остатки пленки растворяются в полости рта, их удаление необязательно.
Повязки, изготавливаемые ex tempore
«Творческая группа» пародонтальных повязок, позволяет учитывать индивидуальную особенность заболевания. Существуют различные прописи пародонтальных повязок — вот один из примеров:
Источник
Стоматологические лекарственные пленки это
Одно из ведущих мест в современной стоматологии занимают воспалительные заболевания пародонта [2]. В терапии этих заболеваний чаще всего используются традиционные лекарственные формы (ЛФ) такие как полоскания, мази, пасты, аэрозоли. Увлажнение ротовой полости слюной обусловливает их быстрое вымывание в низлежащие отделы пищеварительного тракта, что требует многократного введения. Поэтому особое внимание уделяется разработке ЛФ для наружного применения, которые обеспечивали бы пролонгирующее терапевтическое действие. С этой точки зрения использование плёнок лекарственных (ПЛ) открыло новые возможности для лечения заболеваний в челюстно-лицевой области [3].
Целью настоящих исследований явилось создание на основе комплекса технологических, биофармацевтических, физико-химических и химических исследований эффективных и стабильных ПЛ с анилокаином, обладающих полифакторным воздействием на воспалительные процессы при стоматологических заболеваниях.
Материалы и методы исследований
В процессе исследований и разработки оптимальных составов ПЛ использовали лекарственные средства (ЛС) и вспомогательные вещества, разрешенные к медицинскому применению и отвечающие требованиям действующей нормативной документации: анилокаин (ВФС 42-2846-97), диоксидин (ФС 42-2308-97), хлоргексидина биглюконат 20 % (ФС 42-2761-98), фурацилин (ФСП 42-0037-0783-01), натрия альгинат (ФС 42-1680-97), метилцеллюлозу (ТУ 2231-107-05742755-96м), натрий карбоксиметилцеллюлозу (ТУ 2231-034-07507908-01), Бланозе Целлюлозе Гам (Blanose Gum) типов 7MF и 7M8SF (МФ 3-е изд., Т. 4, С. 190), Натросол 250 Фарм (Natrosol 250 Pharm) типов 250 НХ, 250 М, 250 G (МФ 3-е изд., Т. 4, С. 228), глицерин (ФС 42-2202-99), воду очищенную (ФС 42-2619-97).
ПЛ оценивали по следующим критериям: описание (цвет, запах, размеры и форма); определение средней массы; растворимость; рН водного раствора; микробиологическая чистота; потеря массы при высушивании; подлинность; количественное определение; упаковка, маркировка, транспортирование; срок годности. Кроме того, критериями оценки качества ПЛ служили такие технологические параметры, как паропроницаемость, механическая прочность на разрыв, толщина пленок, потеря массы при высушивании, время растворения.
Кинетическое исследование процесса высвобождения анилокаина проводили кондуктометрическим методом.
Результаты исследований и их обсуждение
Выбор оптимального состава ПЛ, обеспечивающего необходимые технологические и потребительские свойства, осуществляли в три этапа.
На первом этапе проводили отсеивающийся эксперимент, цель которого отбор вспомогательных ингредиентов – плёнкообразователей и пластификаторов, способных сформировать плёнку-матрицу для последующего введения в нее ЛС. В ходе эксперимента изучены плёнкообразующие свойства растворов полимеров природного и синтетического происхождения как отечественного, так и зарубежного производства в различных концентрациях (всего изучено 54 композиции). Критерием отбора плёночных композиций на первоначальном этапе являлся удовлетворительный внешний вид (прозрачность, эластичность, однородность, отсутствие микротрещин и разрывов в плёнке). На основании предварительных исследований выбрано 10 композиций, состав которых представлен в табл. 1.
Составы выбранных композиций
Na альгинат – 2,0
Na альгинат – 4,0
Бланозе 7МF – 3,0
Na альгинат – 2,5
Натросол 250G – 3,0
Na альгинат – 3,0
Бланозе 7МF – 1,0
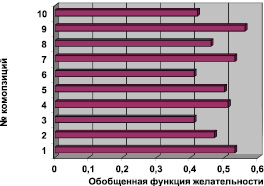
Второй этап исследований заключался в выборе оптимальной композиции матрицы – основы ПЛ методом математического планирования. Критериями отбора служили следующие показатели качества плёнок: значение рН водного раствора, толщина, влажность. Для статистической обработки результатов эксперимента использовали метод обобщенной функции желательности, предложенный Харрингтоном. По результатам обобщенной функции желательности выбраны 3 композиции основ №№ 1, 7 и 9 (рис. 1).
Рис. 1. Обобщенные функции желательности различных пленочных композиций
Дальнейший выбор плёночных матриц проводили на основании изучения следующих функциональных свойств: внешний вид, толщина, время растворения, значение рН водного раствора, потеря в массе при высушивании, паропроницаемость, механическая прочность на разрыв. Результаты изучения показателей качества, представленных в табл. 2, свидетельствуют об удовлетворительном качестве матриц.
Технологические параметры плёнок (n = 5)
Средняя масса, г
Время растворения, мин.
Механич. прочность на разрыв, s×10-5, Н/м2
Na альгинат – 4,0,
Натросол 250 G – 3,0, глицерин– 0,5
Относительную биологическую доступность анилокаина из выбранных составов определяли методом равновесного диализа in vitro через полупроницаемую мембрану и кондуктометрическим методом. Результаты изучения высвобождения анилокаина с использованием кондуктометрического метода коррелируют с результатами, полученными при применении титриметрического метода. Проведенные исследования показали, что наиболее высокая скорость высвобождения анилокаина наблюдается из полимерной матрицы на основе Натросол 250G-Pharm. (через 3 часа – 100 %), а композиции на основах Na КМЦ и Na альгинат можно отнести к пролонгированным системам, из которых полное высвобождение ЛС происходит через 7 часов.
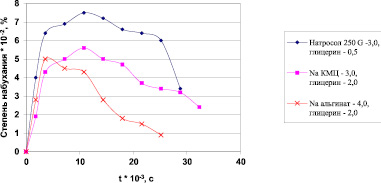
Определенный вклад в кинетику высвобождения ЛС вносит процесс набухания высокомолекулярные вещества (ВМВ). Кривые, характеризующие кинетику набухания, представлены на рис. 2. Высокую способность к набуханию имеют ПЛ на основе Натросол, меньшее набухание наблюдается у плёнок на основах Na КМЦ и Na альгинат.
Рис. 2. Степень набухания ПЛ на исследуемых основах
Таким образом, на основании изученных кинетических параметров, ПЛ следует отнести к неограниченно набухающим системам матричного типа, обеспечивающим диффузионный пролонгированный релиз ЛС.
Окончательный выбор плёнкообразователя сделали на основании пожеланий специалистов, по мнению которых, для эффективности лечения стоматологических больных необходимо пролонгирующее действие. Ввиду того, что свойства Na КМЦ и Na альгината как плёнкообразователей практически идентичны, с учетом экономической и сырьевой доступности, предпочтение на данном этапе отдано натрия альгинату. Кроме того, проведенные ранее исследования установили способность альгиновой кислоты и ее солей останавливать кровотечение, что немаловажно при оказании стоматологической помощи.
Как известно, в развитии воспалительных процессов в пародонте ведущую роль играет микрофлора. Поэтому следующий этап работы связан с введением в состав ПЛ антимикробного ЛС, в качестве которых изучены ЛС широкого спектра действия, наиболее часто применяемые в стоматологии: хлоргексидина биглюконат (ХГБ), фурацилин, диоксидин. Исследования проведены под руководством зав. кафедрой микробиологии, д.ф.н., проф. Одеговой Т.Ф. Первоначально антимикробную активность плёнок с антисептиками определяли диффузионным методом по отношению к тест-микроорганизмам – St.aureus и E. сoli. Наиболее активными в отношении грамположительных (St. аureus) и грамотрицательных (E. сoli) бактерий являются композиции №№ 1, 4, 5, 7 и 8 (табл. 3). Ввиду того, что при повышении концентрации диоксидина от 1 % до 1,5 % и хлоргексидина биглюконата от 0,1 % до 0,2 % увеличение антимикробной активности практически не происходит, для дальнейших исследований по отношению к пяти видам тест микроорганизмов St.aureus, E. сoli, St.epidermidis, Ps.aeruginosa, Cand.albicans.были выбраны составы №№ 1, 4 и 7.
Антимикробная активность ПЛ с анилокаином и различными антисептиками
Диаметр зоны задержки роста, мм
Na альгинат 4; Глицерин 2;
Анилокаин 5; Фурацилин 0,1
Na альгинат 4; Глицерин 2;
Анилокаин 5; ХГБ 0,05
Na альгинат 4; Глицерин 2№
Анилокаин 5; ХГБ 0,075
Na альгинат 4; Глицерин 2;
Анилокаин 5; ХГБ 0,1
Na альгинат 4; Глицерин 2;
Анилокаин 5; ХГБ 0,2
Na альгинат 4; Глицерин 2;
Анилокаин 5; Диоксидин 0,5
Na альгинат 4; Глицерин 2;
Анилокаин 5; Диоксидин 1
Na альгинат 4; Глицерин 2;
Анилокаин 5; Диоксидин 1,5
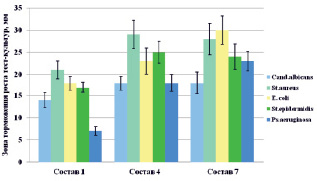
Рис. 3. Антимикробная активность ПЛ с анилокаином и различными антисептиками
Антимикробная активность выбранных концентраций антисептиков в отношении грамположительных (St.aureus, St.epidermidis), грамотрицательных (E. сoli, Ps.aeruginosa) бактерий и грибов (Cand.albicans) была подтверждена в последующих опытах (рис. 3).
Таким образом, проведенные технологические, физико-химические, биофармацевтические и микробиологические исследования позволили получить 3 состава плёнок лекарственных, представленных в табл. 4. ПЛ имеют специфический запах и горький вкус, поэтому в качестве корригирующего средства в состав пленок ввели масло мятное в количестве 0,06 г.
Композиции плёнок лекарственных
В связи с тем, что в настоящее время фурацилин характеризуется как слабый антисептик, то для дальнейших исследований и внедрения предложено 2 состава ПЛ – «Анилдиокс» и «Анилгек».
Для создания ПЛ выбран метод полива на гидрофобную подложку с последующей сушкой в сушильном шкафу при экспериментально установленной температуре 40-50 °С в течение 17–19 часов. Концентрация анилокаина составляла 5 % в пересчете на сухую массу плёнки.
При разработке методов стандартизации ПЛ за основу взяты требования и показатели качества, опубликованные Государственным НИИ по стандартизации и контролю качества лекарственных средств. В целях формирования единого подхода к стандартизации как механизма обеспечения требуемого уровня качества и безопасности продукции аптеки предложены следующие разделы контроля качества ПЛ: описание (цвет, запах, размеры и форма плёнок); подлинность лекарственных средств, входящих в состав плёнки; определение средней массы; растворимость; рН водного раствора; микробиологическая чистота; потеря массы при высушивании; количественное определение; упаковка, маркировка, транспортирование; срок годности. Кроме того, критериями оценки качества ПЛ служили такие технологические параметры, как паропроницаемость, механическая прочность на разрыв, толщина пленок, потеря массы при высушивании, время растворения.
По внешнему виду ПЛ представляют собой эластичные пластины коричневого цвета прямоугольной формы с запахом мяты.
На следующем этапе исследования разработанные для субстанций анилокаина, ХГБ, диоксидина методики идентификации модифицировали и апробировали при оценке качества ПЛ. Для количественного определения действующих веществ в ПЛ за основу взяты титриметрические, физико-химические методы, модифицированные с учетом специфики плёночных форм. Количественное определение анилокаина в плёнках проводили экстракционно-титриметрическим методом, для чего устанавливали оптимальные условия проведения анализа применительно к плёнкам. Содержание анилокаина в средних терапевтических дозах составляет: в ПЛ «Анилгек» 2,55 ± 0,03 мг и для ПЛ «Анилдиокс» – 2,51 ± 0,02 мг. Определение содержания ХГБ в ПЛ «Анилгек» и диоксидина в ПЛ «Анилдиокс» проводили спектрофотометрическим методом. Содержание ХГБ в средней терапевтической дозе (1×2 см) плёнки должно быть от 0,040 до 0,060 мг, а диоксидина в средней терапевтической дозе (1×2 см) плёнки составляет 0,506 ± 0,003 мг. Изучение стабильности ПЛ в процессе хранения определяли путем оценки технологических, микробиологических показателей, количественного определения действующих веществ в условиях естественного хранения. Установлено, что количественное содержание действующих веществ, технологические параметры и микробная чистота остались в пределах нормы в течение 2 лет и 3 мес.
На основании комплекса технологических, биофармацевтических, физико-химических и химических исследований экспериментально обоснованы состав и технология пленок лекарственных с анилокаином.
Рецензенты:
Солонинина А.В., д.фарм.н., профессор, заведующая кафедрой управления и экономики фармации, ГБОУ ВПО «Пермская государственная фармацевтическая академия» Министерства здравоохранения Российской Федерации, г. Пермь;
Олешко О.А., д.фарм.н., профессор кафедры фармацевтической технологии, ГБОУ ВПО «Пермская государственная фармацевтическая академия» Министерства здравоохранения Российской Федерации, г. Пермь.
Источник