- Риски, связанные с применением баллонов и стентов, покрытых паклитакселом
- Актуальность
- Методы
- Результаты
- Коронарные стенты из нержавеющей стали с паклитакселом
- Стоимость стальных стентов с паклитакселом
- Как купить коронарные стальные стенты с паклитакселом в нашей компании
- Стенты с лекарственным покрытием паклитаксель
Риски, связанные с применением баллонов и стентов, покрытых паклитакселом
Актуальность
Баллоны с лекарственным покрытием и стенты с лекарственным покрытием с паклитакселом одобрены для периферических вмешательств на нижних конечностях (в дополнение к коронарному стентированию).
Баллоны и стенты, как показывают исследования, эффективны в снижении частоты рестенозов. Однако согласно небольшим работам, они могут повышать риск смерти в долгосрочной перспективе.
Методы
Исследователи выполнили систематический обзор и мета-анализ с включением рандомизированных клинических исследований (РКИ), оценивающих эффективность и безопасность стентов и баллонов, покрытых паклитакселом и использующихся для вмешательств на бедренной и\или подколенной артериях.
Первичной конечной точкой безопасности являлась смертность от всех причин.
Результаты
В финальный анализ вошли 28 РКИ с общим числом участников 4683 (89% пациентов имели перемежающуюся хромоту).
- Согласно полученным данным, частота летальных исходов через 1 год после вмешательства (28 РКИ, 4432 пациентов) не различалась между группой пациентов со стентами или баллонами, покрытыми паклитакселом, и контрольной группой (2,3% vs. 2,3%, относительный риск, 1,08; 95% ДИ, 0,72–1,61).
- Смертность от всех причин через 2 года наблюдения была изучена в 12 РКИ (2316 пациентов). Показатель был достоверно выше в случае использования устройств, покрытых паклитакселом, в сравнении с контрольной группой (7,2% vs. 3,8, относительный риск, 1,68; 95% ДИ, 1,15–2,47; число пациентов, у которых применение устройств ассоциировано с вредом составляло 29 [95% ДИ, 19–59]) (number needed to harm).
- Смертность от всех причин более, чем через 5 лет (3 РКИ, 863 пациента) была также выше в группе устройств, покрытых паклитакселом, (14,7% vs. 8,1%, относительный риск, 1,93; 95% ДИ, 1,27–2,93; —number‐needed‐to‐harm, 14 [95% ДИ, 9–32]).
- Согласно данным анализа логистической регрессии, найдена достоверная ассоциация между применением паклитаксела и абсолютным риском смерти (0,4±0,1% дополнительный риск на каждый 1 мг/год паклитаксела, P
Источник
Коронарные стенты из нержавеющей стали с паклитакселом
Компания «Стентоник» производит и реализует современное высокотехнологичное оборудование для использования в кардиохирургии. Одним из наших лучших продуктов являются стенты из нержавеющей стали с паклитакселом. Это инновационное изобретение позволяет проводить операции по расширению паталогически суженных сосудов с особой эффективностью.
Коронарные стенты с паклитакселом в своём составе обеспечивают существенное снижение риска развития стеноза после проведения операции и избавляет таким образом пациента от необходимости повторного хирургического вмешательства, а также снижает срок и объем медикаментозной поддержки в восстановительном периоде. Действие паклитаксела основано на подавлении митоза и препятствовании формированию неоинтимы. Данное активное вещество наносится на поверхность стента, что становится возможным благодаря использованию особого типа сплава, на котором образуется окисная пленка.
Стенты с паклитакселом, представленные в данном разделе сайта, изготавливаются из высококачественной нержавеющей стали 316 LVM, в состав которой входят хром и молибден. Они обладают высокой устойчивостью к возникновению коррозионных процессов, остаются стабильными в любых биологических средах.
Низкая степень металлизации сосуда после проведения вмешательства обеспечивается и за счёт особенностей конструкции стента с паклитакселом. Толщина его матричной ячейки – всего 65 микрон (при толщине стенки 85 микрон). Дизайн был разработан для реализации целей возможности эффективной доставки к месту и установки, для обеспечения достаточной гибкости и жёсткости конструкции. Оборудование представляет собой металлический сетчатый полый цилиндр на системе доставки, состоящей из баллона и катетера.
Стоимость стальных стентов с паклитакселом
В компании «Стентоник» вы можете приобрести стенты из нержавеющей стали с паклитакселом на оптимальных условиях. Являясь разработчиком и производителем оборудования, мы имеем возможность предложить вам наиболее низкие цены на инновационные продукты. Наше оборудование ни в чём не уступает, а зачастую и превосходит по своим характеристикам иностранные аналоги.
Как купить коронарные стальные стенты с паклитакселом в нашей компании
Чтобы составить заказ на стенты с паклитакселом, основываясь на характеристиках предоставленной продукции, выберите на сайте необходимые вашей клинике товары в требуемом количестве. Мы также всегда готовы принять заказ по телефону. Вы можете получить исчерпывающую информацию по всем интересующим вас вопросам, позвонив по номеру: + 7 (495) 204-29-74.
Система доставки – быстросменный катетер, совместимый с проводниковым катетером 4F, 5F, 6F, в зависимости от диаметра стента, и проводником 0,014”.
Стенты коронарные баллонорасширяемые хирургические стерильные на системе доставки.
Стенты предназначены для восстановления просвета любых кровеносных сосудов путём катетерного баллонного расширения и установки эндопротеза в образовавшийся просвет.
Принцип действия основан на введении под контролем рентгеновского аппарата стента, закрепленного на баллонном катетере, к месту сужения сосуда с последующим баллонным раздуванием и установкой стента в расширенное пространство с целью увеличения просвета артерии.
Конструкция стентов: матричная (открытая ячейка с тремя или четырьмя перемычками в сегменте);
Дизайн – шести- или девятизубцовая корона;
Тип системы доставки: монорельсовая, изготовленная по технологии быстрой замены;
Обратный ход для стента баллонного расширения: не более 10% его номинального диаметра;
Укорочение стента после раскрытия: менее 5% длины;
Минимальный радиус перегиба стента: не более пяти номинальных диаметров стента;
Диаметр проксимальной части катетера: 0,63 мм (1,9 F);
Диаметр дистальной части, в зависимости от диаметра баллона: от 0,83 до 0,97 мм (от 2,5 до 2,9 F);
Максимальный диаметр проводника: 0,36 мм (0,014″);
Совместимость с интродьюсером для стентов: 1,32 мм (4 F); 1,67 мм (5 F); 2,00 мм (6 F) в зависимости от диаметра.
Стент и система доставки оснащены рентгеноконтрастными метками.
Материал: нержавеющая сталь 316 LVM с покрытием, содержащим паклитаксел;
Геометрические размеры: диаметр, мм: 2,25; 2,50; 2,75; 3,00; 3,25; 3,50; 4,00; и длиной, мм: 8; 10; 13; 16; 18; 23; 28; 33; 38.
По предварительному согласованию с потребителем длина стента (для любого варианта исполнения) может иметь значение в интервале от 8 до 40 мм включительно, с шагом в 1 мм.
Источник
Стенты с лекарственным покрытием паклитаксель
Хирургические методы лечения ИБС имеют своей целью прямое увеличение коронарного кровотока – реваскуляризацию миокарда.
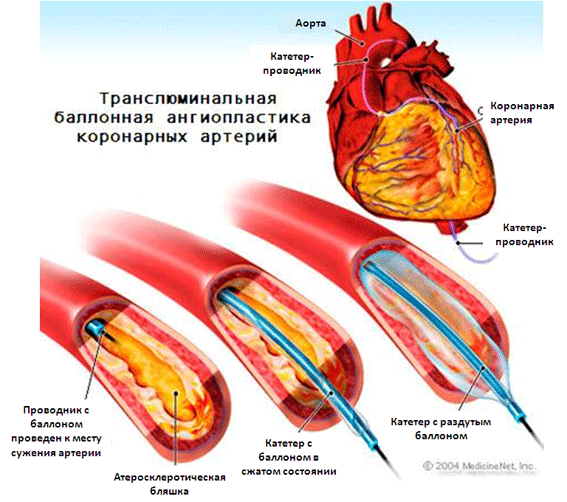
Транслюминальная баллонная ангиопластика (ТЛБАП) – операция, позволяющая восстановить кровоток в артериях сердца (коронарных артериях) путём проведения катетера с баллоном и последующем его раздуванием. Операция ТЛБАП сопровождалась высоким риском осложнений в виде повторного сужения сосуда – рестеноза, острых окклюзий. В современной эндоваскулярной хирургии ТЛБАП выполняется вместе с эндопротезированием венечных (коронарных) артерий, т.е. имплантацией стентов в коронарное русло.
Положительные результаты рандомизированных исследований сделало стентирования коронарных артерий ведущим стандартом в лечении больных ИБС. С 1999 году под термином чрескожное коронарное вмешательство «по умолчанию» подразумевать именно стентирование коронарных артерий.
Стентирование коронарных артерий или чрескожное коронарное вмешательство – операция, позволяющая восстановить кровоток в артериях сердца (коронарных артериях) путём имплантации стентов в месте сужения коронарной артерии.
Сегодня коронарное стентирование занимает ведущее место в эндоваскулярном лечении больных ИБС. Внедрение этого метода позволило значительно улучшить результаты традиционной ТЛБАП – как непосредственные, так и отдаленные. Основным недостатком стентирования (как и баллонной ангиопластики) является относительно высокая частота рестенозирования. Если применение эндопротезов кардинально решило проблему таких острых осложнений ТЛБАП, как диссекции и острые окклюзии, сведя к минимуму летальность и прочие ишемические осложнения (соответственно, и необходимость выполнения экстренной АКШ), а применение нового режима вспомогательной фармакотерапии (аспирин, клопидогрель, ингибиторы IIb/IIIa-рецепторов), с одной стороны, практически свело к нулю частоту развития подострого тромбоза стентов (и связанных с этим ишемических осложнений), а с другой – позволило имплантировать эндопротезы при остром коронарном синдроме, то в плане отдаленных результатов не произошло революционного сдвига.
Несмотря на то, что отдаленные результаты после стентирования и превосходят результаты ТЛБАП (частота рестенозирования в различных клинических ситуациях в среднем в 1,5–2,5 раза ниже, чем после баллонной дилатации), все же самым серьезным недостатком эндопротезирования (как и всех эндоваскулярных методик) остается относительно высокая частота возврата стенокардии в отдаленном периоде и, соответственно, частая необходимость повторной реваскуляризации миокарда.
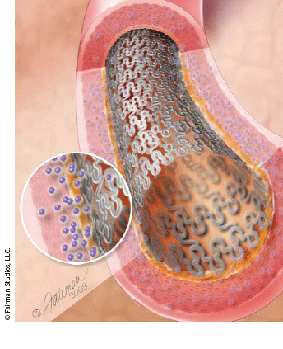
Стент – внутрисосудистый протез для поддержания стенки пораженного сосуда и сохранения диаметра его просвета. Конструкция стента представляет собой тонкий сетчатый каркас из инертного металлического сплава высочайшего качества, раскрываемый баллоном внутри сосуда до нужного диаметра.
Виды стентов:
Металлический стент (Bare Metal Stent) – внутрисосудистый протез из нержавеющей стали или кобальт-хромового сплава. Использование металлических стентов связано с риском тромбоза в первые 30 дней и требует двойной антитромбоцитарной терапии в течении 1 месяца, а также 20-30% риском рестеноза (повторного сужения сосуда) в течение 6-9 месяцев после имплантации.
Стент с лекарственным покрытием — внутрисосудистый протез с покрытием (полимером), высвобождающим лекарственное вещество
Первое поколение стентов с лекарственным покрытием: сиролимус- и паклитаксел-покрытые стенты. Множественные рандомизированные исследования показали, что сиролимус- и паклитаксел-покрытые стенты ассоциируются со снижением частоты повторной реваскуляризации и смерти от инфаркта миокарда по сравнению с металлическими стентами. В состав покрытия стентов первого поколения входили полимеры, которые облегчали высвобождение лекарственных компонентов, но оставались на стенте после растворения медикаментозного слоя. Эти постоянные полимеры могут вызывать воспаление и задержку эндотелизации, что требует длительной двойной антиагрегантной терапии с целью предупреждения высокого уровня поздних и очень поздних тромбозов стентов.
За последнее время использование стентов с лекарственным покрытием показало явное их преимущество в борьбе с рестенозом. В клинической практике при использовании стентов без покрытия частота рестеноза в отдаленном периоде оставалась на относительно высоком уровне, начали рассматривать полимерные покрытия как транспортное средство для местной доставки препарата. Целью этого является дозированное выделение необходимого лекарственного средства из устойчивого покрытия в локальную зону поражения сосудистой стенки. Выделение препарата происходит в равномерно дозированной концентрации в определенном временном интервале. Система доставки препарата не теряет своих свойств при стерилизации, так же изменяет свою геометрическую и объемную форму вслед за стентом при его имплантации и устойчива к механическим повреждениям вследствие раздувания баллона. Все вышеизложенные свойства системы локальной доставки препарата осуществляются с помощью разнообразных полимерных структур, обеспечивающих целостность данной структуры при клиническом применении.
Лекарственный препарат должен обладать способностью ингибировать наибольшее количество различных компонентов комплексного процесса рестенозирования. Безудержный рост неоинтимы по некоторым основным характеристикам схож с ростом опухоли, что навело на мысль использования цитостатических препаратов Rapamycin (Sirolimus) и Paclitaxel (Taxol). Результаты превзошли все ожидания.
Второе поколение стентов с лекарственным покрытием: зотаролимус- и эверолимус- покрытые стенты. Стенты изготовлены из более тонкого кобальт-хромового сплава (балки стента – 0,091 мм, по сравнению со стентами первого поколения, где этот показатель составлял – 0,132 мм), демонстрируют превосходную прочность и радиоконтрастность, гибкость что способствует снижению частоты рестеноза. Лекарственный компонент покрытия из более биосовместимых полимеров наносится на всю поверхность стента, примерно 95% от общего количества зотаролимуса высвобождается в течение первых 15 дней после установки стента, эверолимуса – 80% в течение 30дней, последующие 20% за 4 месяца, что позволяет уменьшить воспаление сосудистой стенки. Клинические результаты в сравнении со стентами первого поколения показали эффективность и безопасность.
Стенты третьего поколения – бесполимерные биостенты на основе поли-L лактида или магния созданы с использованием частично и даже полностью биорастворимых полимеров. Биорассасывающиеся магниево-полимерные стенты полностью исчезают после того, как необходимая доза лекарственного компонента высвободилась и лечение сосуда завершено. Высвобождение лекарственных веществ и поддержание стенки сосуда осуществляется только до тех пор, пока сосуду необходимо лечение. Стенты с покрытием, подвергающимся полному биорассасыванию снижают частоту тромбоза стентов по сравнению со стентами без и с лекарственным покрытием.
Возможные перспективы рентгеноэндоваскулярной хирургии ИБС – широкое внедрение в клиническую практику новых генераций стентов с новыми биоабсорбируемыми полимерными покрытиями. Тем не менее их начальному применению должны предшествовать длительные и всеобъемлющие исследования по изучению непосредственных, особенно отдаленных, результатов после их использования.
Таким образом, на сегодняшний день нет альтернативы применению стентов с лекарственным антипролиферативным покрытием в лечении пациентов с ИБС. Широко дискутируемые данные о возможных поздних осложнениях (поздний тромбоз) ни в коей мере не могут являться основанием к прекращению их использования, а лишь дополнительно подчеркивают важность правильного определения показаний к стентированию, тщательного соблюдения всех технических аспектов процедуры имплантации, досконального соблюдения режима двухкомпонентной дезагрегантной терапии в отдаленном периоде.
Непрерывное улучшение конструкции стентов, приводящее к внедрению новых технических методик имплантации, таких как использование высокого давления, методика прямого стентирования (возможного благодаря уменьшению профиля стентов и закреплению его на баллонный катетер доставляющей системы); внедрение таких дополнительных методов визуализации, как интракоронарное ультразвуковое исследование (позволяющих оптимизировать окончательный результат эндопротезирования с высокой степенью точности); тщательный отбор пациентов для проведения процедуры (в зависимости от прогнозируемых непосредственных и отдаленных результатов), основанный на накопленном к настоящему времени колоссальном опыте, – все это позволяет надеяться на улучшение результатов как непосредственно данного метода, так и в целом результатов лечения больных ИБС.
Таким образом, высока вероятность того, что уже в ближайшем будущем изменятся как результаты эндоваскулярного лечения больных ИБС, так и концепция выбора метода реваскуляризации миокарда, подходы к лечению этого заболевания в целом. Применение стентов с лекарственным антипролиферативным покрытием является высокоэффективным методом лечения пациентов с различными клиническими формами ИБС и разными морфологически неблагоприятными вариантами поражения коронарного русла. Применение стентов с антипролиферативным покрытием, несмотря на увеличение объема и комплексности выполняемых вмешательств, позволяет добиться значительного снижения частоты рестенозирования в отдаленном периоде наблюдения – основного фактора, ограничивающего эффективность рентгеноэндоваскулярного лечения.
Источник