- Приложение N 1. Требования к маркировке изготовленных лекарственных препаратов для медицинского применения
- Маркировка лекарств 2021
- Что собой представляет маркировка
- Сроки введения обязательной маркировки
- Категории товаров, подлежащих маркировке
- Ответственность за отсутствие маркировки
- Что нужно для маркировки
- Как производится маркировка продукции
- Что такое маркировка лекарственных препаратов — разбираемся в вопросе
Приложение N 1. Требования к маркировке изготовленных лекарственных препаратов для медицинского применения
Приложение N 1
к Правилам изготовления и отпуска лекарственных
препаратов для медицинского применения аптечными
организациями, индивидуальными предпринимателями,
имеющими лицензию на фармацевтическую деятельность,
утв. приказом Министерства здравоохранения РФ
от 26 октября 2015 г. N 751н
Требования
к маркировке изготовленных лекарственных препаратов для медицинского применения
1. Все лекарственные препараты, изготовленные и расфасованные в аптечной организации или индивидуальным предпринимателем, имеющим лицензию на фармацевтическую деятельность, оформляются соответствующими этикетками.
2. Этикетки для оформления лекарственных препаратов в зависимости от способа их применения, подразделяют на:
а) этикетки для лекарственных препаратов внутреннего применения с надписью «Внутреннее»;
б) этикетки для лекарственных препаратов наружного применения с надписью «Наружное»;
в) этикетки на лекарственные препараты для парентерального введения с надписью «Для инъекций», «Для инфузий»;
г) этикетки на глазные лекарственные препараты с надписью «Глазные капли», «Глазная мазь», «Растворы для орошения»;
д) для гомеопатических лекарственных препаратов с надписью «Гомеопатический» или «Гомеопатическое лекарственное средство».
3. Этикетки имеют на белом фоне следующие сигнальные цвета в виде поля:
а) для внутреннего применения — зеленый цвет;
б) для наружного применения — оранжевый цвет;
в) для глазных капель, глазных мазей, растворов для орошения — розовый цвет;
г) для инъекций и инфузий — синий цвет.
4. На всех этикетках для оформления изготовленных лекарственных препаратов должны быть отпечатаны предупредительные надписи, соответствующие каждой лекарственной форме:
а) для микстур — «Хранить в прохладном и защищенном от света месте», «Перед употреблением взбалтывать»;
б) для мазей, глазных мазей и глазных капель — «Хранить в прохладном и защищенном от света месте», для гомеопатических мазей «Хранить в защищенном от света месте при температуре от 5 до 15°С»;
в) для капель внутреннего применения — «Хранить в защищенном от света месте»; для гомеопатических капель — «Хранить в защищенном от света месте, при температуре не выше 25°С»; для гранул гомеопатических — «Хранить в сухом, защищенном от света месте, при температуре не выше 25°С»;
г) для инъекций и инфузий — «Стерильно».
5. Все этикетки обязательно должны содержать предупредительную надпись «Хранить в недоступном для детей месте».
6. Предупредительные надписи, наклеиваемые на изготовленные лекарственные препараты, должны иметь следующий текст и сигнальные цвета:
а) «Перед употреблением взбалтывать» — на белом фоне зеленый шрифт;
б) «Хранить в защищенном от света месте» — на синем фоне белый шрифт;
в) «Хранить в прохладном месте» — на голубом фоне белый шрифт;
г) «Детское» — на зеленом фоне белый шрифт;
д) «Для новорожденных» — на зеленом фоне белый шрифт;
е) «Обращаться с осторожностью» — на белом фоне красный шрифт;
ж) «Сердечное» — на оранжевом фоне белый шрифт;
з) «Беречь от огня» — на красном фоне белый шрифт.
7. Для лекарственных препаратов, требующих особых условий хранения, обращения и применения, на этикетках могут печататься или наклеиваться дополнительные предупредительные надписи.
8. Размеры этикеток определяются в соответствии с размерами посуды или другой упаковки, в которой отпускаются изготовленные лекарственные препараты.
9. Лекарственные препараты в зависимости от лекарственной формы и назначения следует оформлять соответствующими видами этикеток: «Микстура», «Капли», «Капли для приема внутрь гомеопатические», «Порошки», «Гранулы гомеопатические» «Глазные капли», «Глазная мазь», «Мазь», «Мазь гомеопатическая», «Оподельдок гомеопатический», «Суппозитории ректальные гомеопатические», «Масло гомеопатическое», «Наружное», «Для инъекций», «Капли в нос» и др.
10. На этикетках для оформления лекарственных препаратов, изготовленных для населения, должно быть указано:
а) наименование аптечной организации, Ф.И.О. индивидуального предпринимателя, имеющего лицензию на фармацевтическую деятельность;
б) местонахождение аптечной организации или место фармацевтической деятельности индивидуального предпринимателя;
в) номер рецепта (присваивается в аптеке);
д) наименование или состав лекарственного препарата;
е) способ применения лекарственного препарата (внутреннее, наружное, для инъекций), вид лекарственной формы (глазные капли, мазь и т.д.);
ж) подробное описание способа применения (для микстур: «по ___ ложке ___ раз в день ___ еды»; для капель для внутреннего употребления: «по ___ капель ___ раз в день ___ еды»; для порошков: «по ___ порошку ___ раз в день ___ еды»; для глазных капель: «по ___ капель ___ раз в день в ___ глаз»; для остальных лекарственных форм, применяемых наружно, должно быть оставлено место для указания способа применения, которое заполняется от руки или проставлением штампа. На этикетках лекарственных препаратов для инъекций и инфузий должно быть обязательно предусмотрено место для написания состава лекарственного препарата и указания способа его применения или введения);
з) дата изготовления лекарственного препарата;
и) срок годности лекарственного препарата («Годен до _______»);
к) цена лекарственного препарата;
л) предостережение «Хранить в недоступном для детей месте».
11. На всех этикетках для оформления лекарственных препаратов, изготовленных для медицинских организаций, должно быть указано:
а) наименование медицинской организации и её структурное подразделение (при необходимости);
б) наименование аптечной организации /Ф.И.О. индивидуального предпринимателя, имеющего лицензию на фармацевтическую деятельность;
в) местонахождение аптечной организации / фармацевтической деятельности индивидуального предпринимателя, имеющего лицензию на фармацевтическую деятельность;
г) Ф.И.О. пациента, для которого индивидуально изготовлен лекарственный препарат (при необходимости);
д) способ применения лекарственного препарата (внутреннее, наружное, для инъекций), вид лекарственной формы (глазные капли, мазь и т.д.);
е) дата изготовления лекарственного препарата;
ж) срок годности лекарственного препарата («Годен до _______»);
з) подписи изготовившего, проверившего и отпустившего лекарственный препарат («Изготовил ______, проверил _______, отпустил _______»);
и) номер анализа проверки лекарственного препарата;
к) состав лекарственного препарата (предусматривается пустое место для указания состава). На этикетках лекарственных препаратов для инъекций и инфузий должен быть указан способ применения лекарственного препарата: «Внутривенно», «Внутривенно (капельно)», «Внутримышечно».
12. Текст этикеток должен быть напечатан типографским способом на русском языке. Состав лекарственного препарата пишется от руки или наносится штампом. Наименования лекарственных препаратов, часто встречающихся в рецептуре, или изготовляемых в виде внутриаптечной заготовки, могут быть напечатаны типографским способом.
13. На этикетках для оформления гомеопатических лекарственных препаратов, изготовленных как внутриаптечная заготовка по часто встречающимся прописям, должно быть указано:
а) наименование аптечной организации, Ф.И.О. индивидуального предпринимателя, имеющего лицензию на фармацевтическую деятельность;
б) адрес местонахождения аптечной организации или места осуществления фармацевтической деятельности индивидуальным предпринимателем;
в) наименование монокомпонентного гомеопатического лекарственного препарата на русском языке (транслитерация);
наименование комплексного гомеопатического лекарственного препарата на русском языке;
г) состав для монокомпонентных и комплексных гомеопатических лекарственных препаратов (активные компоненты — на латинском языке, вспомогательные компоненты — на русском языке);
е) способ применения;
ж) вид лекарственной формы (гранулы гомеопатические, капли гомеопатические, мазь гомеопатическая, тритурация гомеопатическая и т.д.);
з) дата изготовления гомеопатического лекарственного препарата;
и) срок годности лекарственного препарата («Годен до _______»);
л) цена лекарственного препарата;
м) штрих-код (при наличии);
н) предостережение «Хранить в недоступном для детей месте», условия хранения.
Источник
Маркировка лекарств 2021
Фармацевтика всегда была под пристальным вниманием производителей поддельных препаратов, ведь продажа лекарств – самый прибыльный бизнес. Специальная система маркировки разработана для борьбы с контрафактными медикаментами. Любое нововведение вызывает много вопросов, поэтому очень важно разобраться во всех тонкостях, связанных с маркировкой лекарств.
Что собой представляет маркировка

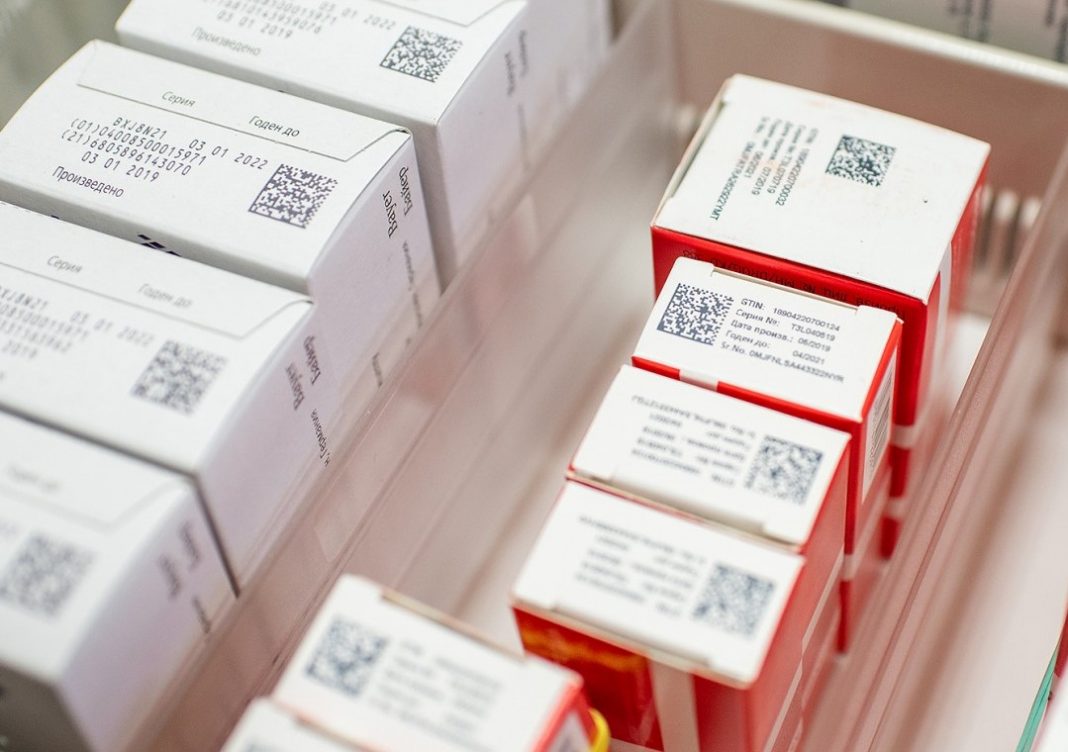
Маркировка является предупредительной мерой в борьбе с подделками. На каждую упаковку препарата наносится специальный код формата Data Matrix, который содержит в себе информацию о препарате и производителе. Его вносят в реестр системы. Электронная система учета медикаментов, контролирующая их движение по территории России — основа маркировки лекарственных средств.
Сроки введения обязательной маркировки
Внедрение маркировки будет проходило в четыре этапа, для каждого из которых предусматривались свои сроки:
Участники оборота медикаментов, применяемых для терапии нозологий, требующих высоких затрат, регистрировались в системе мониторинга «Честный знак».
Начало обязательной маркировки семи препаратов для ВЗН. Стоит отметить, что согласно ч.7.1, ст.67 Закона № 61-ФЗ, лекарства, выпущенные до 31.12.2019 г. разрешалось реализовывать, хранить на складах и перевозить до окончания срока годности без кодов.
С 01.01 по 29.02.2020 г.
Все участники оборота лекарственных средств регистрировались в ГИС мониторинга «Честный знак». Те, кто начал свою деятельность с 1 марта, обязаны были в течение 7 календарных дней пройти регистрацию.
Обязательная маркировка распространяется на все медикаменты. Производители и импортеры наносят при фасовке на упаковку индивидуальный код. Все участники рынка должны передавать информацию о движении лекарств в систему мониторинга
Аптекам и складам, хранящим и реализующим немаркированную продукцию, с 1 июля 2020 года грозит административная ответственность.
Обратите внимание! В связи с распространением коронавирусной инфекции, 2 ноября 2020 года вынесено Постановление Правительства РФ №1779, согласно которому маркировка лекарств работает в уведомительном режиме. Это значит, что отпускать лекарства в аптеке можно лишь уведомив систему маркировки, но не дожидаясь от нее ответа. Сделано это для того, чтобы технические сбои не отражались на лекарственном обеспечении.
Категории товаров, подлежащих маркировке
Закон распространяется на все лекарственные препараты независимо от их применения и стоимости. Помимо медикаментов, под маркировку попадают:
- Гомеопатические препараты и БАДы. Они не являются лекарственным средством, однако, реализуются через аптеки.
- Сушеные травы.
- Медикаменты, применяемые в ветеринарии.
- Расходники для медицинского оборудования.
- Перевязочный материал.
Процедура обязательна также для поликлиник, стационаров и оптовых баз. Для ветеринарных клиник и аптек — маркировка ветеринарных медикаментов.
Ответственность за отсутствие маркировки
За реализацию, производство и хранение немаркированных лекарств предусмотрена административная ответственность. В случае, когда вследствие реализации или изготовления медикаментов без маркировки нанесен ущерб здоровью и жизни людей, на виновников могут завести уголовное дело. Статья 15.12 КоАП РФ предусматривает следующие наказания:
От 2000 до 4000 руб.
От 5000 до 10 000 руб.
От 50 000 до 100 000 руб.
За систематические нарушения закона предприятие лишается лицензии. Получить ее повторно либо восстановить невозможно. Поэтому предприятия, реализующие фальсификат, до 2023 года прекратят свою деятельность.
Что нужно для маркировки
Для считывания кодов пользователю необходимо скачать на смартфон специальное приложение. Предприятиям, чтобы подключиться к системе, потребуется:
- убедиться, что аптека работает по общей или упрощенной системе налогообложения;
- оформить электронную подпись;
- пройти регистрацию в системе маркировки «Честный Знак»;
- установить 2D-сканер;
- для передачи данных в систему мониторинга подключить ОФД;
- обновить прошивку кассы;
- приобрести лицензии СБИС «Касса и склад» и «Маркировка», либо усовершенствовать учетную систему.
Аптекам необходимо ККТ с прошивкой, поддерживающей тег для маркированной продукции, касса с установленной программой, позволяющей передавать фискальные данные чеков с кодом Data Matrix оператору. У того, в свою очередь, должен присутствовать модуль маркировки. 2D-сканер позволит считывать штрих-коды.
Как производится маркировка продукции
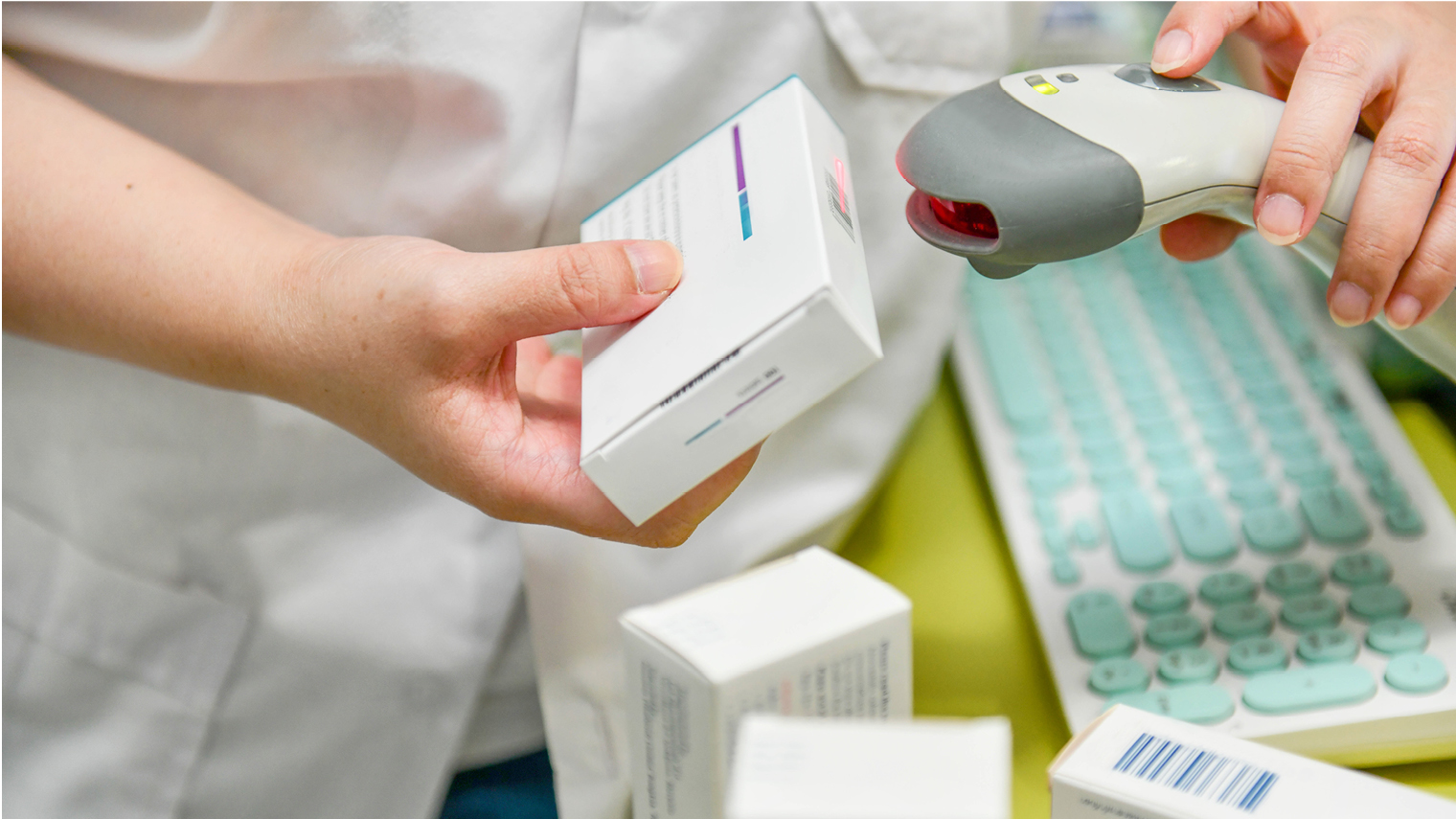
Производитель наносит уникальный код Data Matrix на вторичную или первичную упаковку. Сведения о введении продукции в оборот автоматически вносятся в базу Честного ЗНАКа (ИС МДЛП). Производитель обязан приобрести оборудование для маркировки медикаментов, а также регистратор эмиссии, который генерирует, защищает и хранит коды проверки.
Маркировка — крайне важная процедура, обеспечивающая стабильность всей фармацевтической индустрии. Именно поэтому она отличается повышенной технологичностью и технической сложностью. Стоит отметить высокую степень адаптированности разработанной государством инфраструктуры маркировки к потребностям рядовых пользователей.
Источник
Что такое маркировка лекарственных препаратов — разбираемся в вопросе
2019 год — последний год, когда система маркировка лекарственных препаратов находится в «пилотном» режиме и в нее можно вступить добровольно. С 1 января 2020 года юридические лица и индивидуальные предприниматели, осуществляющие производство, хранение, ввоз в Российскую Федерацию, отпуск, реализацию, передачу, применение и уничтожение лекарственных препаратов для медицинского применения, обеспечивают внесение информации о лекарственных препаратах для медицинского применения с учетом вида осуществляемой ими деятельности в данную систему ( ч.7* ст. 67 Федерального закона № 61-ФЗ от 12.04.2010 г. “Об обращении лекарственных средств”) .
На сайте Федеральной службы по надзору в сфере здравоохранения (Росздравнадзора) в разделе «Система маркировки лекарственных препаратов» идет временной отсчет — сколько осталось до введения обязательной маркировки лекарственных препаратов семи высокозатратных нозологий ( с 1 октября 2019 года) и обязательной маркировки всех лекарственных препаратов ( с 1 января 2020 года ).
Но, как оказалось, еще не все фармспециалисты знают о том что представляет собой система маркировки лекарственных препаратов и для чего она необходима. Давайте разберемся, что это такое — маркировка лекарственных препаратов.
Что такое система маркировки лекарственных препаратов?
Информационная система «Маркировка» — государственная информационная система, создаваемая в целях информационного обеспечения маркировки товаров контрольными (идентификационными) знаками. Внедрение данной системы позволит обеспечить мониторинг движения лекарственных препаратов от производителя до конечного потребителя.
Цели внедрения системы маркировки лекарственных препаратов
— профилактика поступления в оборот и одномоментное изъятие из оборота в автоматизированном режиме на всей территории Российской Федерации недоброкачественных, а также фальсифицированных и контрафактных лекарственных препаратов на любом из этапов их обращения от производителя до конечного потребителя;
— профилактика неэффективных расходов и экономия бюджетных средств за счет невозможности реализации схем «повторного вброса» лекарственных препаратов, невозможности легальной реализации лекарственных препаратов, подлежащих предметно-количественному учету, а также не предназначенных для розничной продажи;
— контроль адресности движения препаратов, закупаемых за счет бюджета, расходов на их приобретение;
— мониторинг ценообразования и предельных розничных цен на лекарственные препараты из списка ЖНВЛП;
— оперативное планирование и управление запасами и резервами препаратов на всех уровнях, включая стратегический.
— снижение издержек за счет более эффективного управления логистикой;
— уменьшение упущенной выгоды, обусловленной контрафактной и фальсифицированной продукцией;
— соответствие требованиям для поставок продукции на международные рынки.
- возможность с помощью персонального мобильного устройства лично проверить легальность приобретаемого (получаемого) лекарственного препарата.
Кто является участниками системы маркировки лекарственных препаратов?
- Федеральные органы исполнительной власти;
- Производители лекарственных средств;
- Российские и иностранные держатели регистрационных удостоверений и их представительства;
- Организации оптовой торговли лекарственными средствами;
- Аптечные и медицинские организации;
- Организации, осуществляющие уничтожение лекарственных препаратов.
Как будет выглядеть маркировка лекарственных препаратов?
Маркировка упаковок лекарственных препаратов — нанесение эмитентом контрольных (идентификационных) знаков на вторичную (потребительскую) упаковку лекарственного препарата (а при ее отсутствии — на первичную упаковку), а также на третичную (заводскую, транспортную) упаковку.
На вторичную (потребительскую) упаковку наносится контрольный (идентификационный) знак в виде двумерного штрихового кода, включающий:
- идентификационный номер лекарственного препарата (GTIN);
- индивидуальный серийный номер вторичной (потребительской) упаковки лекарственного препарата;
- код ТН ВЭД;
- номер производственной серии лекарственного препарата;
- дата истечения срока годности лекарственного препарата.
На третичную (заводскую, транспортную) упаковку наносится контрольный (идентификационный) знак в виде линейного штрихового кода, содержащий различные данные в зависимости от типа.
Оборудование, необходимое аптечным организациям для участия в системе маркировки
Для участия в системе маркировки аптечной организации необходимо:
- приобрести или доработать существующее и используемое программное обеспечение;
- приобрести УКЭП (усиленную квалифицированную электронную подпись) с аппаратными ключами;
- приобрести 2D сканер.
Какие санкции предусмотрены за производство и продажу лекарственных препаратов без средств идентификации?
За производство или продажу лекарственных препаратов для медицинского применения без нанесения средств идентификации, с нарушением установленного порядка их нанесения, а также за несвоевременное внесение данных в систему маркировки лекарственных препаратов для медицинского применения или внесение в нее недостоверных данных юридические лица и индивидуальные предприниматели несут ответственность в соответствии с законодательством Российской Федерации (ч.11* ст. 67 Федерального закона № 61-ФЗ от 12.04.2010 г. “Об обращении лекарственных средств”).
В соответствии со ст. 1 Федерального закона № 58-ФЗ* от 15.04.2019 г. «О внесении изменений в Кодекс Российской Федерации об административных правонарушениях» несвоевременное внесение данных в систему маркировки лекарственных препаратов для медицинского применения либо внесение в нее недостоверных данных влечет:
— наложение административного штрафа на должностных лиц в размере от пяти тысяч до десяти тысяч рублей;
— на юридических лиц — от пятидесяти тысяч до ста тысяч рублей.
Надеемся, что наша статья поможет разобраться в системе маркировки лекарственных препаратов не только владельцам и заведующим аптечных организаций, но и фармацевтам и провизорам!
Источник



