Теоретический материал. Стабилизация инъекционных растворов
учебно-методический материал
Учебный материал для студентов 3 — го курса специальности Фармация, дистанционное обучение
Скачать:
| Вложение | Размер |
|---|---|
| stabilizatsiya_inekrastv.docx | 22.99 КБ |
Предварительный просмотр:
Тема: Стабилизация инъекционных растворов
Задание: 1.Составить конспект материала
2. Прислать фото конспекта (можно часть)
3. При возникновении вопросов обратиться к преподавателю
Содержание нового материала:
Наряду с другими качествами (стерильность, чистота и др.), инъекционные растворы должны обладать стабильностью.
Стабильность – неизменность свойств содержащихся в растворах лекарственных веществ.
Если растворы не стабилизировать – могут появиться муть, осадок, изменение цвета. При этом, продукты разложения часто бывают более токсичны, чем исходные вещества.
Это обусловлено тем, что в процессе изготовления инъекционных растворов, особенно термической стерилизации ( при повышении температуры на 10 о С скорость химических реакций возрастает в 2-4 раза), и последующем хранении возможно разложение некоторых лекарственных веществ. Последние подвергаются изменениям, в основе которых лежат различные химические процессы: гидролиз, окисление – восстановление, омыление и др. Наиболее часто встречаются процессы гидролиза и окисления. Гидролизу подвергаются соединения различных классов: соли, эфиры, белки, углеводы и др. На степень гидролиза влияет химическая природа лекарственного вещества, температура и рН раствора. Это вызывает необходимость стабилизации инъекционных растворов. Стабильность достигается строгим соблюдением условий асептики, подбором оптимальной температуры и времени стерилизации, использованием стабилизаторов, соответствующих природе лекарственных веществ, использованием консервантов.
Существенным стабилизирующим фактором в парентеральных растворах является оптимальная концентрация водородных ионов.
Выбор стабилизатора в первую очередь зависит от природы веществ. Несмотря на многообразие и чрезвычайную сложность процессов разложения лекарственных веществ в инъекционных растворах, при рассмотрении вопросов стабилизации их ориентировочно можно разделить на 3 группы:
1) растворы солей слабых оснований и сильных кислот
2) растворы солей сильных оснований и слабых кислот
3) растворы легкоокисляющихся веществ
В основу деления растворов на группы положен химический процесс, который приводит к изменениям лекарственных веществ, хотя этот принцип выдержан не до конца. В первой группе растворов имеют место различные химические процессы, но общим для них является введение для стабилизации раствора кислоты хлористоводородной. Изменение лекартвенных веществ второй группы происходит за счет гидролитических процессов, третьей – за счет окисления.
Растворы солей слабых оснований и сильных кислот: К этой группе относятся растворы солей алкалоидов (морфина г/хлорид, апоморфина г/хлорид, атропина сульфат, омнопон) и синтетических азотистых оснований (новокаин, дикаин, дибазол). В зависимости от силы основания растворы этих веществ имеют нейтральную или слабокислую реакцию. В результате гидролиза солей при нагревании растворов происходит накопление в растворе труднорастворимого азотистого основания, т.к. при этом увеличивается степень диссоциации воды и повышается рН раствора. В растворах солей очень слабых оснований, малорастворимых в воде, даже незначительное повышение рН приводит к образованию осадка (в растворах дибазола, папаверина г/хл и др). При значительном увеличении рН раствора (щелочное стекло) иногда наблюдается выделение даже сравнительно сильных свободных оснований, например, новокаина, констатируемого по замасливанию стенок сосуда. Иногда свободное основание не выпадает в осадок вследствие способности реагировать со щелочью с образованием растворимых продуктов, но изменяет окраску раствора (раствор морфина желтеет, апоморфина зеленеет). Если алкалоид или синтетическое азотистое основание имеет сложноэфирные группы (атропин, новокаин, дикаин и др.), то при нагревании происходит омыление сложного эфира, сопровождающееся изменением фармакологического действия.
Вышеуказанные изменения вызывают необходимость стабилизации растворов многих солей алкалоидов и азотсодержащих оснований.
Большинство из них по ГФ ХI стабилизируют добавлением 0,1 н. раствора кислоты хлористоводородной (НСl). Она нейтрализует щелочь, выделяемую стеклом, смещает рН раствора в кислую сторону, что препятствует гидролизу, омылению сложных эфиров, окислению фенольных и альдегидных групп.
Количество кислоты зависит от свойств лекарственного вещества. Наиболее часто добавляют 10 мл 0,1 н. раствора НСl на 1 литр стабилизируемого раствора, что соответствует образованию 0,001н. раствора НСI (рН 3 — 4). Указанное количество НСl рекомендовано для растворов атропина сульфата, дибазола, дикаина, апоморфина гидрохлорида и некоторых других веществ.
Для получения устойчивого раствора новокаина для инъекций 0,5 – 1 – 2 % добавляют кислоту до рН 3,8 – 4,5:
— для 0,25 % раствора новокаина берут 3 мл кислоты;
— 1 и 2 % — по 9 мл;
— 5 и 10 % — по 12 мл 0,1н. кислоты на 1 л раствора.
Для приготовления стабильного раствора новокаина (1 – 2 %) на изотоническом растворе натрия хлорида следует добавлять 5 мл 0,1н. раствора кислоты на 1 л раствора. Растворы морфина гидрохлорида 1 – 5 % стабилизируют добавлением 10 — 20 мл 0,1н.раствора НСI на 1 л раствора.
Растворы солей сильных оснований и слабых кислот: кофеин-бензоат натрия, натрия тиосульфат, натрия нитрит. В водных растворах эти вещества легко гидролизуются, образуя слабощелочную реакцию среды. Это приводит к образованию труднорастворимых соединений, дающих в растворах муть или осадок, что недопустимо для инъекционных растворов. Гидролитические процессы усиливаются в кислой среде за счет того, что вода для инъекций, поглощая при хранении из воздуха углекислоту, к концу суток уменьшает значение рН (образуется угольная кислота). Достаточно ее следов в воде, чтобы при растворении в ней указанных веществ вызвать необратимые реакции разложения. Для подавления реакции гидролиза необходимо добавление 0,1 н. раствора натрия гидроксида или натрия гидрокарбоната.
Раствор натрия нитрита — добавляют 2 мл 0,1 н. раствора натрия гидроксида на 1 л раствора.
Раствор натрия тиосульфата — добавляют 20,0 натрия гидрокарбоната.
Раствор кофеин-бензоата натрия — добавляют 4 мл 0,1 н. раствора натрия гидроксида.
Растворы легкоокисляющихся веществ: кислота аскорбиновая, глюкоза, натрия сульфацил, тиамина бромид, натрия салицилат, стрептоцид растворимый и другие лекарственные вещества, содержащие карбонильные, фенольные, этанольные, аминные группы с подвижными атомами водорода. В процессе изготовления инъекционных растворов этих веществ в присутствии кислорода, содержащегося в воде и в воздухе над раствором, происходит окисление перечисленных групп, особенно во время термической стерилизации. В результате в растворах образуются продукты окисления, часто более токсичные или физиологически неактивные, изменяется цвет раствора. Окисление в значительной степени усиливается под влиянием света, тепла, значения рН, кислорода и др. Для устранения факторов, способствующих окислению лекарственных форм, применяют следующие технологические приемы:
— вводят стабилизаторы – антиоксиданты
— применяют комплексные стабилизаторы
— используют свежепрокипяченную в течение 30 мин воду для инъекций и быстро охлажденную
— заполняют флаконы доверху
— пропускают растворы через мембранные или бумажные беззольные фильтры
— изготавливают растворы быстро
Остановимся подробнее на стабилизаторах – антиоксидантах, которые являются сильными восстановителями.
Прямые (натрия сульфит, Косвенные (карбоновые кислоты,
аскорбиновая кислота, оксикислоты, трилон Б)
унитиол, натрия метаби-
Окисляются быстрее, чем лекарст- Связывают в недиссоциируемые
венные вещества вещества катионы тяжелых металлов
Механизм стабилизирующего действия различных антиоксидантов весьма сложен и не во всех случаях одинаков, что обусловлено не только природой антиоксидантов и лекарственных веществ, но и наличием в растворах микропримесей тяжелых металлов, действием света и тепла и др.
Прямые антиоксиданты содержат серу низкой валентности, и действие их основано на быстром окислении серы. Они не останавливают цепной процесс окисления, но замедляют его.
Большое влияние на процесс окисления лекарственных веществ оказывает присутствие следов тяжелых металлов (железа, марганца, меди и др.), которые являются катализаторами процессов окисления. Ионы тяжелых металлов переходят в раствор из стекла, аппаратуры или могут присутствовать в лекарственном веществе в качестве производственной примеси. Общим свойством комплексонов является способность образовывать прочные внутрикомплексные водорастворимые соединения с большим числом катионов, в т.ч. и тяжелых металлов.
Скорость реакции окисления во многом зависит от значения рН раствора, поэтому для замедления процессов окисления во многие растворы легкоокисляющихся веществ добавляют кислоту хлористоводородную или буферные смеси. Также для стабилизации предложено использовать высокомолекулярные вещества (полиглюкин, пропиленгликоль и др.).
Общая технология изготовления стабилизируемых растворов: в части воды для инъекций (примерно половинном объеме) растворяют лекарственное вещество, добавляют стабилизатор и доводят водой для инъекций до нужного объема.
Наиболее часто в аптеках готовят раствор глюкозы. При стерилизации растворов глюкозы происходит ее окисление и карамелизация, при этом наблюдается пожелтение, а иногда и побурение раствора. По ГФ ХI растворы глюкозы стабилизируют добавлением 0,2 натрия хлорида и 0,1 н. раствором кислоты НСI до рН 3,0 – 4,0. В условиях аптеки для удобства работы стабилизатор готовят по прописи:
Натрия хлорид 5,2
Кислоты НСI разбавл. 4,4 мл
Воды для инъекций до 1 литра
Независимо от концентрации раствора глюкозы этот стабилизатор берут в количестве 5 % от общего объема раствора. Срок годности стабилизатора 1 сутки. Также нужно учитывать содержание в глюкозе воды. С учетом влажности глюкозы берут на 10 % больше от ее общей массы или умножают количество глюкозы на коэффициент влажности, определенный аналитиком.
Rp: Sol. Glucosi 10 % — 500 ml
Общий объем 5000 мл (500 мл х 10)
Количество глюкозы по рецепту: 500,0
Количество глюкозы с учетом влажности: 550,0 (500,0 – 100 %
Количество стабилизатора: 250 мл (5000 мл – 100 %
Х – 5 %; х = 250 мл)
Вода для инъекций: до 5000 мл
Для изготовления 250 мл стабилизатора Вейбеля необходимо взять:
Натрия хлорид: 1,3 (5,2 – 1000 мл
Кислота НСI разбавл.: 1,1 мл (4.4 мл – 1000 мл
Вода для инъекций: до 250 мл
Технология изготовления раствора глюкозы: Отдельно готовят стабилизатор Вейбеля — в стерильной подставке в небольшом количестве воды для инъекций (100 мл) растворяют 1,3 натрия хлорида, добавляют 1,1 мл кислоты хлористоводородной разбавленной, перемешивают и доводят водой до 250 мл. Небольшое количество отдают на анализ.
В другой стерильной подставке (стеклянном баллоне соответствующего объема) в части воды для инъекций, примерно половинном объеме, растворяют 550,0 глюкозы, добавляют стабилизатор Вейбеля 250 мл, перемешивают и доводят водой для инъекций до 5000 мл. Часть раствора отдают на анализ. Раствор фильтруют в стерильные флаконы по 500 мл.
Раствор кислоты аскорбиновой – стабилизируют добавлением натрия метабисульфита в количестве 2,0 на 1 л 5 % раствора. С целью снижения болезненности инъекций к раствору добавляют натрия гидрокарбонат в эквивалентных количествах.
По теме: методические разработки, презентации и конспекты
Теоретический материал для изучения основ работы с контрольно-кассовой техникой по профессиональному модулю ПМ.05 «Выполнение работ по профессии кассир» разработан на основе Федерального государ.
Презентации теоретического материала «Сестринский уход при инфекционных заболеваниях»Тема №1. Основные сведения об инфекционных болезняхТема №3. Понятие об эпидемическом процессе. Противоэпидемические.
Представлен доклад по изучению педагогического опыта активного обучения.
Специальность 34.02.01 «Сестринское дело» уровень подготовки — базовый, квалификация – медицинская сестра/медицинский брат.
Материалы для подготовки к занятиям.
Учебный материал для студентов 3 -го курса специальности 33.02.01 Фармация.
Учебный материал «Изотонирование инъекционных растворов» для дистанционного изучения для студентов 3 курса специальности Фармация.
Источник
Стабилизирующие вещества (стабилизаторы)
Стабильность — свойство лекарственных средств сохранять физико-химические и микробиологические свойства в течение определенного времени с момента выпуска. Стабилизацию лекарственных препаратов в настоящее время следует рассматривать как весьма актуальную комплексную проблему в целом: устойчивость лекарственных форм, представляющих собой дисперсные системы (растворы, суспензии, эмульсии),
 |
устойчивость лекарственных веществ (химических соединений различной природы) и устойчивость лекарственных препаратов к микробной контаминации (схема 5.3).
СХЕМА 5.3. Стабилизирующие вспомогательные вещества

| Физико-химических (дисперсных) систем: желатоза, производные МЦ, микробные полисахариды, поливинилпирролидон, бентониты, твин-80 и др. |



вещества, тормозящие окислительно-восстановительные процессы (натрия метабисуль-фит, тиомочевина, трилон, Б и др.)


Металлорганические соединения; Органические соединения (спирты, фенолы, кислоты, сложные эфиры, соли четвертичных аммониевых соединений, эфирные масла)

системв основном имеют большое значение для гетерогенных (неоднородных) систем (суспензий и эмульсий), довольно часто используемых в медицинской практике благодаря ценным фармакокинетиче-ским, терапевтическим свойствам: возможность изготовления и использования лекарственных препаратов из труднорастворимых или практически нерастворимых лекарственных средств; продленность действия лекарственных веществ; осуществимость различных способов введения, в том числе и инъекционного; снижение раздражающих свойств и неприятного вкуса; точность дозирования этих лекарственных форм. Так, стабильные суспензии бария сульфата, широко используемые при исследованиях, позволяют своевременно диагностировать изменения слизистой оболочки желудочно-кишечного тракта; эмульсии масла вазелинового, необходимые для больных с атонией кишечника, для стимуляции его функции. Получены эмульсии и для внутривенного введения с некоторыми жирораствори-
мыми цитостатиками и многие другие эффективные лекарственные препараты.
К стабилизаторам лекарственных форм — гетерогенных дисперсных систем — можно отнести производные МЦ, пектины, альгинаты, бентонитовые глины, аэросил, твины и спены и ряд других веществ. Нередко с целью снижения количества этих веществ и повышения их активности используют различное сочетание стабилизаторов.
Стабилизаторы химических веществ используются в процессе изготовления и длительного хранения лекарственных препаратов. Этот вид стабилизации имеет большое значение для лекарственных форм, подвергающихся различным видам стерилизации, особенно термической. В данном случае используется химический метод стабилизации, который особенно необходим для жидких лекарственных форм. Применение стабилизаторов основано на угнетении процессов гидролитического или окислительно-восстановительного разложения лекарственных веществ. Для предотвращения гидролитических процессов используют кислоты (хлороводородную и др.) или щелочные компоненты (натрия гидроксид, натрия гидрокарбонат) в зависимости от свойств раствора лекарственного вещества. Иногда наиболее эффективно в этом случае использовать буферные системы: боратно-аце-татные, боратные, фосфатные и др. Одним из основных способов повышения устойчивости лекарственных веществ является применение ПАВ и ВМС. При этом стабилизирующее действие осуществляется путем мицеллообразования и связывания молекул лекарственных веществ с мицеллами. Например, анионо-генные ПАВ уменьшают скорость гидролиза дикаина в 10 раз, новокаина — в 4 раза.
В технологии лекарственных форм используют добавление стабилизаторов, тормозящих окислительно-восстановительные процессы в растворах лекарственных веществ и ряда вспомогательных компонентов (мазевых и суппозиторных основ и др.), так как окисление физиологически активных веществ происходит довольно часто. Особенно чувствительны к окислению ненасыщенные жиры и масла, соединения с альдегидными и фенольными группами, а также полимерные упаковочные материалы. Реакции окисления могут быть ингибированы путем добавления не-
 |
больших количеств вспомогательных веществ, называемых антиоксидантами (противоокислителями). Известно множество антиоксидантов (АО) как природного, так и синтетического происхождения. Механизмы процессов окисления и торможения с помощью АО в настоящее время хорошо изучены. АО, как правило, в химическом отношении являются очень реакционно-способными веществами и вступают во взаимодействие с активными ингредиентами, влияя на стойкость и эффективность лекарственных препаратов. В качестве АО предложены производные фенола, ароматические амины, производные серы (натрия сульфит и метабисульфит, ронголит, тиомочевина и др.), а также трилон Б, кислота аскорбиновая, токоферолы и многие другие соединения.
По механизму действия АО делят на 3 группы. К первой группе относятся собственно АО, которые ингибируют процесс окисления, реагируя со свободными радикалами первичных продуктов окисления, чем прекращают развитие цепной реакции (бутилокси-анизол, бутилокситолуол, нордигидрогваяретовая кислота, токоферолы). Вторая группа представлена восстанавливающими АО, имеющими более низкий окислительно-восстановительный потенциал, чем находящиеся в системе окисляющиеся соединения. Окислению последних предшествует окисление восстановителя находящимся в системе кислородом (производные кислоты сернистой, органические соединения серы, кислота аскорбиновая и др.). Третья группа— синергисты АО, собственное антиокислительное действие которых незначительно, однако они способствуют усилению действия других АО, например, образуя комплексы с ионами металлов, катализирующих окисление, или регенерируя АО (кислоты лимонная и винная, ЭДТА и др.).
В технологии лекарственных форм в последние годы довольно часто используют комплекс стабилизаторов, обладающих синергическим эффектом.
Противомикробные стабилизаторы (консерванты) используют для предохранения лекарственных препаратов от микробного воздействия. Консервирование не исключает соблюдения санитарных правил производственного процесса, которые должны способствовать максимальному снижению микробной контаминации лекарственных препаратов. Консерванты явля-
ются ингибиторами роста тех микроорганизмов, которые попадают в лекарственные препараты в процессе их многократного использования. Они позволяют сохранить стерильность лекарственных препаратов или предельно допустимое число непатогенных микроорганизмов в нестерильных лекарственных препаратах. К консервантам предъявляются те же требования, что и к другим вспомогательным веществам, но обращается внимание на наличие широкого спектра их антимикробного действия.
В ГФ XI в качестве антисептических веществ для инъекционных растворов, других лекарственных форм, сывороток и вакцин включены: хлорбутанол-гидрат (0,05—0,5%); фенол (0,25—0,3%); хлороформ (0,5%); мертиолат (0,01 %); нипагин (0,1 %); нипазол; кислота сорбииовая (0,1—0,2 %) и другие вещества, разрешенные к медицинскому применению. В ГФ XI в отличие от предыдущих фармакопеи приведены консерванты, предназначенные для всех неинъекционных лекарственных форм.
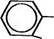
COONa S — Hg — C2H5
Мертиолат представляет собой порошок кремового цвета, устойчив на воздухе, разлагается на свету, растворяется в 1 части воды и 8 частях этанола. Мертиолат применяется для консервирования глазных капель (0,005 %), глазных мазей (0,02 %), инъекционных растворов (0,01 %), мазей (0,1 %).
Мертиолат является эффективным консервантом, однако нередко вызывает аллергические реакции при продолжительном применении.
Органические соединения многочисленны. К этой
группе противомикробных стабилизаторов (консерван
тов) относятся спирты, фенолы, органические кислоты,
сложные эфиры парагидроксибензойной кислоты, соли
четвертичных аммониевых соединений, эфирные масла.
4—941 97

Спирт этиловый — этанол (Spiritus aethyli-cus), являясь экстрагентом при получении настоек, экстрактов и концентратов из лекарственного растительного сырья, в то же время выполняет роль консерванта. Для консервирования некоторых эмульсий применяют этанол в количестве 10—12 % от водной фазы, в галеновых и новогаленовых препаратах — до 20 %. Однако наилучшими антисептическими свойствами обладает 70 % этанол, поэтому, присутствуя в галеновых препаратах в количестве до 20 %, он оказывает слабый консервирующий эффект.
Большей активностью по сравнению с этанолом обладает спирт бензиловый (Spiritus ben-zylicus):
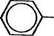 |
Спирт бензиловый представляет собой жидкость с приятным ароматическим запахом и жгучим вкусом. Растворяется в 25 частях воды, 1 части 50 % этанола. Спирт бензиловый в 0,9 % концентрации применяют для консервирования глазных капель (содержащих кортизона ацетат), гидрофобных, гидрофильных и эмульсионных мазевых основ; в количестве 2 % — для консервирования 15 % раствора нембутала для инъекций, а также препаратов радиоактивных изотопов и противоопухолевых веществ.
Эффективным консервантом является хлорбутанолгидрат (Chlorbutanolum hydratum):
1 ‘ 1
CI —С—С —ОН-V2H2O I I CI СНз

его используют для консервирования глазных капель, эмульсий, капель для носа. Хлорбутанолгидрат совместим со многими лекарственными веществами.
Другую группу консервантов — органических соединений представляют фенолы (фенол, хлоркрезол). Наиболее старым из них является фенол (Phe-nolum):
U,25—0,5 % растворы фенола эффективны для препаратов инсулина, вакцин и сывороток. Однако при местном применении фенол обладает раздражающим действием. Он нередко способствует аллергическим проявлениям. Поэтому фенол не применяется для консервирования мазей, глазных капель, суппозиториев.
Наиболее часто из производных фенола используется в качестве консерванта хлоркрезол (Clor-cresolum):
| он |
| CI |
-О-
Хлоркрезол представляет собой бесцветные кристаллы с характерным запахом. Растворим в 250 частях воды (лучше в горячей), этаноле, маслах жирных. Хлоркрезол в 10—13 раз активнее фенола в отношении бактерий и грибов, в то же время он менее токсичен. Растворы хлоркрезола применяются для консервирования глазных капель (0,05 %), инъекционных растворов (0,1 %), мазей (0,1—0,2 %).
Широкое распространение в фармацевтической технологии как консерванты получили органические кислоты: бензойная и сорбиновая. Кислота бензойная (Acidum benzoicum):
представляет собой кристаллическое вещество белого цвета со слабым характерным запахом. 1,0 г кислоты
растворим в 350 мл воды или 3 мл этанола, или 8 мл хлороформа. Кислота бензойная широко используется как консервант. Обычно применяется в виде натриевой соли, хорошо растворимой в воде (1,0 г в 1 мл воды). Кислота бензойная и ее соли оказывают сильное действие на дрожжевые грибы, особенно в кислой среде. Кислоту бензойную и ее натриевую соль используют для консервирования сиропов сахарного и лекарственного, эмульсии масла вазелинового, суспензий с антибиотиками и других препаратов, предназначенных для внутреннего применения.
Наиболее эффективным и биологически безвредным консервантом является кислота сорби новая (Acidum sorbicum):
Кислота сорбиновая представляет собой белый мелкокристаллический порошок со слабым раздражающим запахом и слабокислым вкусом. Она в концентрации до 0,15 % растворима в воде, до 0,2 % — в маслах жирных и минеральных, хорошо растворима в этаноле. Помимо кислоты сорбиновой, в качестве консервантов применяют ее калиевую соль.
В настоящее время кислоту сорбиновую синтезируют чаще всего путем взаимодействия кротонового альдегида с малоновой кислотой в присутствии пиридина.
Кислота сорбиновая разрешена во многих странах мира для консервирования пищевых продуктов, так как менее токсична, чем обычно применяемые кислоты-консерванты, и безвредна для человека даже в больших количествах. Она способствует повышению иммунобиологической активности организма. Подобно другим кислотам-консервантам, кислота сорбиновая наиболее эффективна при значениях рН 3,0—4,0. Она проявляет очень сильную фунгицидную активность, тормозит рост кишечной палочки, золотистого стафилококка, вульгарного протея и др.
Большой интерес представляет использование кислоты сорбиновой для консервирования галеновых препаратов (сахарный и лечебные сиропы, экстракты и др.). Ее рекомендуют для консервирования концентрированных растворов натрия бромида, кальция
хлорида, микстуры Павлова. Растворы кислоты сорбиновой (0,2 %) являются эффективными консервантами мазей, особенно эмульсионного типа, и линиментов промышленного производства.
Сложные эфиры парагидроксибензоинои кислоты — парабены (нипагин, нипазол) нашли широкое применение в пищевой, парфюмерной и фармацевтической промышленности многих стран. Они включены во многие фармакопеи и, в частности, в ГФ XI. Наиболее широко используют метиловый и пропиловый эфиры.
Нипагин (Nipaginum) представляет собой метиловый эфир парагидроксибензоинои кислоты:
| СОО — СНз |
О
Пропиловый эфир парагидроксибензоинои кислоты известен под названием нипазол (Nipasolum):
Эфиры парагидроксибензоинои кислоты представляют собой белые кристаллические, без запаха и вкуса порошки, плохо растворимые в воде, растворимые в маслах и очень хорошо — в органических растворителях. Лучшей растворимостью обладает нипагин, поэтому он чаще применяется в водных растворах, нипазол одинаково растворим в воде и маслах. По антисептическим свойствам парабены в значительной степени превосходят фенол, например пропиловый эфир — 17 раз. Более сильное консервирующее действие достигается при сочетании 0,025 г пропилового и 0,075 г метилового эфиров (1 : 3). Особенно эффективна смесь ингредиентов в этом соотношении для консервирования мазей и эмульсий, если ее взять 0,2 % от массы мази или эмульсии.
Парабены рекомендуют для консервирования глазных капель. Малая токсичность парабенов позволяет использовать их для лекарственных препаратов, предназначенных для внутреннего применения, галеновых препаратов (сиропа сахарного), настоев и отваров, концентрированных растворов, суспензий рент-
геноконтрастных, гормональных и противотуберкулезных средств, антибиотиков, пероральных эмульсий; их также вводят в состав желатиновых капсул. Широко используются парабены для консервирования мазей и их основ.
Представителями солей четвертичных аммониевых соединений являются бензалкония хлорид, диметил-додецилбензиламмония хлорид. Как антибактериальные вещества значительное распространение получили соли четвертичных аммониевых соединений, относящиеся к группе синтетических катионоактивных ПАВ, основным из которых является бензалкония хлорид (Benzalconii chloridum).
 |
| СшНз7 |
| НгС- |
Для консервирования лекарственных препаратов наиболее широкое применение нашел бензалкония хлорид — смесь хлоридов алкилметилбензиламмония. Установлено, что антибактериальная активность бензалкония хлорида проявляется при содержании в радикале от 8 до 16 атомов углерода.
Бензалкония хлорид представляет собой кристаллическое вещество белого цвета, очень хорошо растворимое в воде. Водные растворы его бесцветны, устойчивы к изменениям температуры, рН среды. Он сохраняет активность в присутствии большой группы лекарственных веществ. При разведении 1 : 50 000 бензалкония хлорид эффективен в отношении многих грамотрицательных, грамположительных бактерий и грибов и не обладает токсичностью. При использовании в мазях не оказывает раздражающего и аллер-гизующего действия. Бензалкония хлорид в концентрации 1:10 000 применяют в настоящее время почти во всех зарубежных странах преимущественно для консервирования глазных лекарственных форм, капель для носа, где требуются отсутствие раздражающего действия и быстрый бактерицидный эффект.
Другим соединением этой группы, представляющим значительный интерес, является отечественное вещество, синтезированное на кафедре органической
химии I ММИ им. И. М. Сеченова — д и м е т и л-Годецилбензиламмония хлорид (Dime-thyldodecylbenzilammonium chloridum) ДМДБАХ.
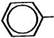 |
| СГ |
СНз I СНг—С— N —С12Н25
Это — желтовато-белый порошок с ароматическим запахом, очень хорошо растворимый в воде, этаноле. ДМДБАХ в отличие от зарубежного бензалкония хлорида представляет собой индивидуальное вещество.
Изучение отечественного консерванта, проведенное на кафедре аптечной технологии лекарственных форм фармацевтического факультета I ММИ им. И. М Сеченова совместно с сотрудниками Московского научно-исследовательского института глазных болезней им. Гельмгольца Минздрава РСФСР, Всесоюзного кож-но-венерологического института им. Короленко и Центральной научно-исследовательской лаборатории им. С. И. Чечулина I ММИ им. И. М. Сеченова, позволило установить преимущество этого вещества по сравнению с зарубежным бензалкония хлоридом (БАХ). ДМДБАХ оказывает быстрое антимикробное действие в 0,01 % концентрации. Гибель микроорганизмов наступает через 15—60 мин, что имеет большое значение для консервирования лекарственных препаратов, применяемых многократно в течение суток. По сравнению с зарубежным БАХом ДМДБАХ обладает сильными спороцидными свойствами, он активнее в отношении синегнойной палочки, которая обычно является представителем сопутствующей флоры при глазных заболеваниях, нередко осложняя течение последних. Антимикробная активность ДМДБАХ не снижается в присутствии многих лекарственных веществ, он совместим с пролонгирующими компонентами (МЦ, поливинолом и др.) и мазевыми основами (вазелином, консистентной эмульсией, гидрофильными и глазными основами).
Эфирные масла (Olea aetherea) используют в качестве консервантов для лекарственных препаратов наружного применения (мази, эмульсии, линименты и др.). Особый интерес представляют эфирные
масла, содержащие фенольные соединения, например лавровое, укропное, лавандовое, розовое, анисовое, лимонное. Они обладают не только консервирующими свойствами, но и бактерицидной активностью в отношении патогенной микрофлоры кожи, в том числе дрожжей, вызывающих кандидозы.
В настоящее время все большее применение находят не индивидуальные консерванты, а сочетания антимикробных веществ, обладающих синергическим эффектом и имеющих широкий спектр антимикробного действия.
Примеры повышения качества лекарственных препаратов (стабильности) при добавлении консервантов приведены в табл. 5.1.
Таблица 5.1. Сроки использования глазных капель и примочек
| Препарат | Капли, сут | Примочки, сут |
| Без консерванта С консервантом | 3 30 | Свежеприготовленные 10 |
Консервирование удобно для аптек (возможность внутриаптечной заготовки) и больного (сокращение числа обращений в аптеку), важно экономически (использование всего выписанного количества лекарственного препарата.
Решение проблемы стабильности лекарственных препаратов является весьма актуальным. Нестабильность жидких лекарственных препаратов, изготовляемых в аптеках, находит отражение в регламентации сроков их хранения (от 1 до 10 сут). Сроки же хранения лекарственных препаратов после вскрытия упаковки при применении лекарственных препаратов в домашних условиях и лечебных учреждениях еще не установлены. Нестойкость сдерживает процесс сокращения количества лекарственных препаратов индивидуального изготовления и увеличения доли серийного внутриаптечного производства, мешает централизованному изготовлению в крупных аптеках и снабжению ими сельских аптек.
5.3.3. Солюбилизирующие вещества (солюбилизаторы)
С целью увеличения растворимости труднорастворимых или практически нерастворимых лекарственных веществ применяют ПАВ, имеющие высокое значение ГЛБ, например твин-80, желчные кислоты. Эти вещества часто называют солюбилизаторами. Солю-билизация — процесс самопроизвольного перехода нерастворимого в воде вещества в разведенный водный раствор ПАВ с образованием термодинамически устойчивой системы. С повышением ГЛБ улучшаются гидрофильные свойства ПАВ, что сопровождается возрастанием их растворимости в воде. Физико-химнческие свойства ПАВ: поверхностная активность, величина ККМ и ГЛБ, являются определяющими для их солюбилизирующих свойств.
В фармацевтической практике давно используют солюбилизированные растворы. Ихтиол представляет собой ихтиоловое масло, солюбилизированное аммониевой солью сульфаихтиоловой кислоты; мыльно-крезоловые препараты и др. Солюбилизаторы используют для изготовления лекарственных форм (чаще растворов) для наружного, внутреннего и инъекционного введения. Применение солюбилизатора позволяет готовить лекарственные формы с новыми практически нерастворимыми высокоэффективными лекарственными веществами. Это группы новых антибиотиков, цитостатиков, гормональных препаратов и других соединений. Так, например, при использовании твина-80 получены инъекционные лекарственные формы нового высокоэффективного цитостатика фене-стерина, гормонов (синестрола, октэстрола) для инъекций (ранее таблетки), эфирных масел (мятного для изготовления воды мятной), водные растворы камфоры (взамен масляных) и др.
Положительным моментом при использовании растворов солюбилизированных веществ, с точки зрения эффективности лечения, является быстрая и полная резорбция лекарственного вещества, что обеспечивается высокой дисперсностью его и влиянием ПАВ на мембранную проницаемость клеток. Это может привести и к снижению дозировки лекарственных веществ. Многие солюбилизированные лекарственные вещества (гидрокортизон, преднизолон, синестрол,
S
 |
барбитураты, антибиотики и др.) не теряют, а нередко благодаря улучшению резорбции повышают свою активность, особенно в водных растворах.
Кроме того, при использовании солюбилизаторов появляется возможность замены растворителя для инъекционных растворов. В частности, это очень важно при изготовлении инъекционных растворов камфоры. Часто назначаемые больным при сердечнососудистых заболеваниях масляные растворы камфоры плохо рассасываются и нередко образуют олеомы — опухоли, что не отмечается при введении водных растворов камфоры.
Использование солюбилизаторов позволяет также заменить один путь введения лекарственного вещества другим, менее опасным и более удобным для больного. Например, таблетки гризеофульвина (противогрибковый антибиотик, нерастворимый в воде), назначаемые больному в течение продолжительного времени при кожных заболеваниях, можно заменить солюбилизированным раствором его, применяемым наружно. В данном случае снижается опасность кандидомикоза, возникающего при длительном перо-ральном использовании антибиотиков.
Таким образом, применение солюбилизаторов открывает широкие технологические возможности получения высокоэффективных лекарственных препаратов с более удобным для больного способом введения.
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.
Источник