- ДНК как лекарство: клеточная и генная терапия меняют фармацевтику
- Стволовые клетки и генная инженерия
- Генный рынок
- Рыночные перспективы стволовых клеток
- Что дальше?
- Медицина будущего: технологии генетической инженерии для создания высокоспецифичных лекарств и инструментов молекулярной диагностики
- Версия для печати:
- Генно-инженерное конструирование лекарств
- Перепрограммирование клеток человека
- Технологии терапевтического применения РНК-интерференции
ДНК как лекарство: клеточная и генная терапия меняют фармацевтику
Лекарства, полученные с помощью генной инженерии и клеточных технологий, вряд ли в ближайшие годы станут столь массовыми, что обгонят по продажам антибиотики и жаропонижающие. Но эти современные препараты незаменимы в лечении некоторых видов рака, редких наследственных заболеваний, терапии ВИЧ и других вирусных инфекций. А это большой рынок с потенциальным оборотом в десятки миллиардов долларов.
Стволовые клетки и генная инженерия
Генная терапия — общее название для технологий (а также соответствующих лекарств), которые используют изменение генов для достижения нужных медицинских эффектов. Например, в организм пациента могут доставить ген, кодирующий определенный белок. Когда нужная ДНК попадет в клетки, те смогут начать производство данного протеина, что будет иметь лечебное воздействие.
Другой вариант — отредактировать «дефектные» варианты генов, чтобы они начали работать правильно. Если у человека есть только одна мутантная версия гена, который вызывает заболевание, можно просто отрезать ее — и ДНК починит себя сама, скопировав генетическую информацию со своей второй «половинки». В случае, когда повреждены обе цепи ДНК, можно доставить в клетки донорскую последовательность.
Наконец, есть возможность с помощью специальных препаратов управлять экспрессией генов. Если активность определенного гена приводит к болезни, ее подавляют. И наоборот: в ситуации, когда заболевание возникает по причине «недоработки» какого-то гена, лекарство помогает его включить.
Что касается клеточной терапии, она в большинстве случаев представляет собой лечение стволовыми клетками. Они могут развиться в клетки любого типа, любого органа, если правильно управлять их ростом. И эту науку ученые освоили, но важно было еще и получить достаточный запас стволовых клеток. Проблему решил японский ученый Синья Яманака, который в 2006 году впервые смог получить индуцированные плюрипотентные стволовые клетки, то есть вернуть клетки взрослого человека в то состояние, когда из них может вырасти что угодно. Перед наукой открылись захватывающие перспективы: можно выращивать новые органы, восстанавливать поврежденные участки нервной системы, лечить заболевания крови — все это становится возможным с применением стволовых клеток.
На стыке клеточной и генной терапии находится технология модификации клеток. Сегодня ученые экспериментируют в основном с клетками иммунитета — Т-лимфоцитами. С помощью генетического редактирования их «учат» лучше распознавать вредителей (например, раковые клетки) и эффективно их уничтожать.
Генный рынок
В 2016 году рынок препаратов для генной терапии оценивался в $584 млн. А к 2023 году, по прогнозам аналитиков, глобальная выручка от продажи таких препаратов превысит $4,4 млрд — это более 30% роста ежегодно.
Среди лидеров рынка как традиционные фармацевтические гиганты (такие, как Novartis и GlaxoSmithKline), так и более специализированные компании (Spark Therapeutics, Bluebird bio, Amgen, Celgene).
Как следует из отчета Allied Market Research, подавляющее большинство препаратов генной терапии производится для больных с онкологическими патологиями. И в ближайшее время — как минимум до 2023 года — эта ниша сохранит свое первенство на рынке. Следом за лекарствами от рака идут средства генной терапии от редких заболеваний, сердечнососудистых болезней, неврологических расстройств, инфекций.
Лидеры рынка следуют за трендами и разрабатывают препараты для онкобольных. Например, в компании Amgen, которая возглавила топ-25 биотехнологических компаний в 2017 году с капитализацией в $129,1 млрд, из 37 препаратов в стадии клинических испытаний 20 относятся к лечению опухолей и заболеваний крови.
А компания Novartis стала первой, кому американское управление по санитарному надзору за качеством пищевых продуктов и медикаментов (Food and Drug Administration, FDA) разрешило запустить массовое производство клеточной терапии рака, основанной на генетической модификации. Это тот самый случай, когда фармкомпания производит лекарство из Т-лимфоцитов, превращая их в средство борьбы с онкологией, а именно с острым лимфобластным лейкозом.
Novartis уже начала получать первые деньги от продажи своего препарата под названием Kymriah. И немалые — каждый курс генной терапии рака стоит порядка $475 000. Вслед за этим FDA одобрило еще одно лекарство для лечения онкологии с подобным механизмом действия — Yescarta от компании Gilead Sciences (капитализация в 2017 году — $103 млрд); оно будет продаваться по цене в $373 000 за курс и помогать больным с неходжкинской лимфомой.
На продажах Kymriah фармгигант Novartis сможет зарабатывать порядка $300 млн в год. А Gilead Science аналитики пророчат выручку от препарата Yescarta в $250 млн за 2018 год.
Novartis хочет расширить спектр применения своего лекарства, чтобы его также можно было назначать пациентам с неходжкинской лимфомой — это позволит компании побороться за рынок, который оценивают примерно в $1 млрд. Но фармгиганту придется конкурировать не только с Gilead Sciences, которые уже предложили свое — и более дешевое — решение, но и с Bluebird Bio и Juno Therapeutics, разрабатывающими аналогичные продукты.
Прибыльность клеточной генной терапии аналитики пока затрудняются оценить. Но по их данным, стоимость производства подобных лекарств от рака должна составлять не менее $200 000 за курс.
По-настоящему революционные открытия, которые происходят на рынке генной терапии и грозят перевернуть фармацевтический рынок (как минимум в области лечения онкологии), привлекают в отрасль инвестиции: за последние пять лет компании-производители получили порядка $600 млн венчурного капитала на свои разработки.
Рыночные перспективы стволовых клеток
По прогнозу аналитиков из Grand View Research, рынок препаратов, основанных на стволовых клетках, к 2025 году достигнет $15,6 млрд. Сегодня самые перспективные сферы применения стволовых клеток — это лечение болезни Паркинсона и болезни Альцгеймера, а также повреждений спинного мозга, сахарного диабета первого типа, заболеваний крови и онкологии.
Но пока что даже топовые компании, занимающиеся стволовыми клетками, не могут похвастаться такими же масштабами, как их коллеги по генной терапии. Например, крупнейшая компания, которая торгуется на бирже NASDAQ — Sangamo Therapeutics, — имеет капитализацию всего в $2,1 млрд.
В данный момент Sangamo Therapeutics разрабатывает два вида терапии на основе собственных — аутологичных — стволовых клеток для лечения заболеваний крови. Если производитель добьется успеха, то с помощью этих препаратов можно будет лечить такие генетические болезни крови, как бета-талассемия и серповидноклеточная анемия.
Развитие рынка стволовых клеток тормозится тем, что лекарства на основе аутологичных клеток делать невыгодно, так как такое производство нельзя масштабировать: лекарство, созданное для одного пациента, нельзя применить для другого. В то же время может быть прибыльно производить препараты на основе чужих — аллогенных — стволовых клеток. Но на разработку таких средств требуется много времени: необходимо сделать их «незаметными» для иммунитета пациентов, чтобы снизить риск отторжения.
Что дальше?
По всем оценкам, рынок клеточной и генной терапии в ближайшие годы будет активно развиваться, и средний годовой рост продаж составит не менее 30%. Новые открытия в сфере генной терапии обещают 2200 клинических испытаний, которые проводятся по всему миру: ученые ищут средства от различных видов рака, редких генетических нарушений, болезни Паркинсона, ВИЧ и других болезней.
Впереди планеты всей, как всегда, США — около 55% исследований происходят именно там. Также разработками в сфере генной терапии занимаются в Европе, Канаде и Китае. Один препарат, созданный при участии генной инженерии, запустили и в России — это Неоваскулген, лекарство, призванное помочь при ишемии нижних конечностей.
Что же касается стволовых клеток, рост рынка ожидается в результате появления новых препаратов регенеративной медицины — сейчас многие из них находятся в стадии разработки. Большинство исследований проходят в США, но новые решения в области стволовых клеток также появляются в Сингапуре и Японии.
Источник
Медицина будущего: технологии генетической инженерии для создания высокоспецифичных лекарств и инструментов молекулярной диагностики
Повышение качества и продолжительности жизни человека — ключевые приоритеты развитых экономик мира. Для более эффективной профилактики, диагностики и лечения социально значимых заболеваний, а также реабилитации пациентов необходимы технологические прорывы в области биомедицины. Они прежде всего связаны с созданием принципиально новых лекарств, продуктов для клеточной и генной терапии, инструментов высокоспецифичной молекулярной диагностики.
Технологии генетической инженерии — конструирование функционально активных генетических структур, введение их в организм человека, интеграция в геном — позволяют выработать новые, в некоторых случаях уникальные генетические, биохимические и физиологические свойства. Создание новых биофармпрепаратов, культур клеток-продуцентов биологически активных молекул в перспективе обеспечит отечественный рынок доступными инновационными лекарствами и средствами диагностики.
В настоящем выпуске информационного бюллетеня представлены три технологических тренда, с развитием которых уже через 5-7 лет появятся новые разработки в области генно-инженерного конструирования лекарств, перепрограммирования клеток человека и терапевтического применения РНК-интерференции, имеющие перспективы выхода на массовые рынки.
Версия для печати:
Генно-инженерное конструирование лекарств
Для эффективного лечения многих болезней, в первую очередь иммунной природы, требуются точечные воздействия, иногда на уровне отдельных клеток. Создание мишень-ориентированных препаратов, в том числе конъюгированных и ДНК-вакцин, повысит эффективность лечения онкологических, ревматических, инфекционных заболеваний, а также болезней нервной системы.
Первое направление развития тренда связано с применением рекомбинантной ДНК для получения биологических продуктов с заданными терапевтическими свойствами и высокими показателями биодоступности и специфичности действия. В результате появятся новые лекарства, эффективные при заболеваниях, вызванных нарушениями иммунной системы.
Создание диагностических биосенсоров — другое направление использования терапевтических клеточных продуктов и специфических молекулярных фрагментов, получаемых на основе технологий генетической инженерии. Эти решения могут повысить диагностическую ценность портативных тестов, выводимых на рынок медицинских изделий для «домашней медицины».
Эффекты
Снижение заболеваемости и смертности от онкологических, ревматических, аутоиммунных заболеваний.
Развитие персонализированной медицины, основанной на использовании генно-инженерных лекарственных средств и диагностических процедур с высокой степенью индивидуализации к пациенту.
Оценки рынка
может достичь к 2020 году объем мирового рынка биопрепаратов при сохранении среднегодового темпа роста на уровне 13,5%. Он будет развиваться в направлении разработки моноклональных антител, рекомбинантного человеческого инсулина, факторов роста и др. Объем рынка продуктов молекулярной диагностики (онкология, наследственные болезни, инфекционные заболевания и др.) может достичь 8 млрд долларов при среднегодовом темпе роста не менее 9,9%.
Драйверы и барьеры
Возрастающая потребность в эффективных и высокоспецифичных методах профилактики, диагностики и терапии социально значимых заболеваний, развитие биофармтехнологий, постепенно сменяющих традиционные фармацевтические практики с применением химических субстанций, выступают основными драйверами тренда.
Сдерживают его развитие конкуренция с рынком традиционных лекарственных препаратов и вакцин, а также относительно высокая стоимость генно-инженерных лекарственных препаратов.
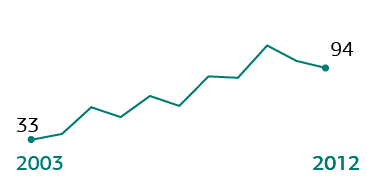
Международные
публикации
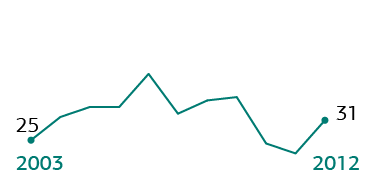
Международные
патентные заявки
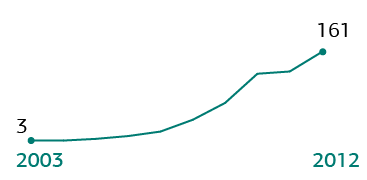
Уровень развития
технологии в России
«Заделы» — наличие базовых знаний, компетенций, инфраструктуры, которые могут быть использованы для форсированного развития соответствующих направлений исследований.
Перепрограммирование клеток человека
Технологии направленного перепрограммирования стволовых и модификации дифференцированных клеток дают возможность исследовать их свойства, получать клетки с новыми функциональными характеристиками. На этой основе разрабатываются технологии регенеративной медицины, нацеленные на восстановление травмированных или пораженных болезнью тканей и утраченных физиологических функций.
В русле этого тренда активнее всего развиваются следующие технологии: манипуляции геномом клеток разного уровня дифференцировки и использование негеномных средств их перепрограммирования, включая рентгеновское облучение, моделирование процессов регенерации, стресс-индуцированную трансформацию и др.
Эти технологии составляют основу для разработки биомедицинских клеточных продуктов (минимально манипулированные клетки, препараты на базе нуклеиновых кислот и стромально-клеточной фракции), а также продуктов культивирования модифицированных клеток.
Эффекты
Развитие персонализированной медицины.
Более эффективное лечение сердечно-сосудистых заболеваний и болезней нервной системы, ожогов и др.; сокращение периода реабилитации пациентов.
Снижение экономических потерь вследствие высокой заболеваемости и инвалидности.
Оценки рынка
составляет объем мирового рынка клеточной терапии. К 2019 году он может вырасти до 119,5 млрд долларов при сохранении среднегодового темпа роста на уровне 24,2%.
На российском рынке представлены, в основном, услуги по сбору и хранению стволовых клеток. В будущем ожидается высокий спрос на аутологичные клеточные продукты.
Драйверы и барьеры
Драйвером тренда является потребность в эффективных средствах для регенеративной и клеточной медицины.
Барьер — возможные риски злокачественного перерождения перепрограммированных соматических клеток.
Международные
публикации
Международные
патентные заявки
Уровень развития
технологии в России
«Заделы» — наличие базовых знаний, компетенций, инфраструктуры, которые могут быть использованы для форсированного развития соответствующих направлений исследований.
Технологии терапевтического применения РНК-интерференции
Многие неизлечимые заболевания возникают в силу патологических изменений генома клеток. Традиционные лекарства недостаточно эффективны при их лечении — из-за низкой специфичности и, в ряде случаев, значительного токсического воздействия на организм. Но главное — они не действуют на саму причину подобного рода заболеваний — соматические мутации генома. Ожидается, что точечно воздействовать на экспрессию генов, прерывая последовательность патологических изменений в клетке, управлять ключевыми механизмами развития, например, онкологических заболеваний станет возможным с помощью технологий терапевтического применения РНК-интерференции.
РНК-интерференция — один из основных методов исследования функций генов в культурах клеток и живых организмах — имеет большой терапевтический потенциал. Посредством посттранскрипционного подавления экспрессии генов (когда двухцепочечная РНК индуцирует деградацию гомологичной мРНК) можно воздействовать на уровне синтеза кодируемых ими белков, модулируя таким образом активность генома клеток на любом этапе развития заболеваний, связанных с нарушениями нуклеотидной последовательности. Характерное преимущество технологии — возможность точной локализации терапевтического действия, например, в очаге опухоли.
Эффекты
Возможность лечения генетически обусловленных болезней, в частности онкологических.
Переход на новые модели медицины, связанные с персонализированным подходом к лечению социально значимых заболеваний.
Оценки рынка
может составить к 2017 году объем глобального рынка созданных на основе технологий РНК-интерференции средств биомедицинского назначения и лекарственных препаратов для лечения онкологических, иммунодефицитных и других заболеваний (при сохранении среднегодового темпа роста на уровне 13,6%).
Отдельный сегмент рынка будут занимать реагенты для процедур РНК-интерференции, предназначенных для валидации лекарственных кандидатов и биологических мишеней.
Драйверы и барьеры
Необходимость использования для терапии ранее неизлечимых заболеваний новых лекарственных средств, обладающих высоким уровнем специфичности, эффективности и безопасности, стимулирует развитие тренда.
Основные барьеры — нерешенные задачи направленной доставки лекарства до органа-мишени; экономические риски в связи с более высокой стоимостью препаратов на основе технологии РНК-интерференции.
Международные
публикации
Международные
патентные заявки
Уровень развития
технологии в России
«Заделы» — наличие базовых знаний, компетенций, инфраструктуры, которые могут быть использованы для форсированного развития соответствующих направлений исследований.
Мониторинг глобальных технологических трендов проводится Институтом статистических исследований и экономики знаний Высшей школы экономики (issek.hse.ru) в рамках Программы фундаментальных исследований НИУ ВШЭ.
При подготовке трендлеттера использовались следующие источники: Прогноз научно-технологического развития РФ до 2030 года (prognoz2030.hse.ru), материалы научного журнала «Форсайт» (foresight-journal.hse.ru), данные Web of Science, Orbit, strategyr.com, researchandmarkets.com, grandviewresearch.com, transparencymarketresearch.com и др.
Более детальную информацию о результатах исследования можно получить в Институте статистических исследований и экономики знаний НИУ ВШЭ: issek@hse.ru, +7 (495) 621-82-74.
© Национальный исследовательский университет «Высшая школа экономики», 2015
Источник