- Разъяснения по «Маркировке»
- Вступление: три категории пользователей
- Ответы на вопросы
- Росздравнадзор: действия с маркированными и немаркированными товарами
- Оптовик и дальнейший оборот «доиюльских» препаратов отечественного производства.
- Включение в гражданский оборот произведенного за границей лекарства.
- Ввоз лекарств без нанесения средств идентификации.
- Последовательное представление сведений в систему МДЛП.
- Приемка лекарств медицинской организацией
Разъяснения по «Маркировке»
Специалисты оператора ЦРПТ комментируют вопросы аптек: ФАПы, отпуск лекарственных средств по безналу, работа в личном кабинете ИС «Маркировка», перемещение ЛП внутри аптечной сети и другие практические аспекты
Мы продолжаем серию материалов, в которых представители «Центра развития перспективных технологий» отвечают на вопросы читателей «Катрен-Стиль», посвященные работе с маркированными лекарственными препаратами. Вопросы возникают в ходе специальных бесплатных вебинаров, а также приходят на почту редакции. На этот раз руководитель проекта «Фарма» компании «ЦРПТ» Алексей Косарев и его коллеги решили ответить на самые распространенные вопросы, которые повторяются из раза в раз. Для большей ясности в начале статьи авторы объясняют, где брать информацию самостоятельно — кому из пользователей МДЛП пригодится тот или иной официальный документ.
Вступление: три категории пользователей
Всех пользователей МДЛП можно условно разделить 3 категории. Первая — это участники оборота с объемами более 10 упаковок в день. Они работают с МДЛП через ИТ-интеграторов и ККТ, которые передают данные в МДЛП автоматически. ЦРПТ сотрудничает со всеми крупными ИТ-интеграторами и поставщиками ККТ. Если ваш поставщик ПО есть на сайте «Честный знак» в разделе «Партнеры и Протестированные решения», то интеграция у вас уже есть. Если вы работаете с другим поставщиком, то уточните у него наличие в системе модуля для работы с маркированным товаром. Если у вас «самописная» система, ее надо доработать в соответствии с документами, которые предназначены для ИТ-специалистов (см. ниже). Рекомендуем получить все разъяснения у провайдеров услуг и пройти обучение по работе с новым функционалом в том интерфейсе, в котором вы осуществляете свою ежедневную деятельность.
Вторая категория — это участники оборота с объемами менее 10 упаковок в день. Они могут (но не должны) работать с ИС «Маркировка», внося данные о лекарственных средствах «вручную» через личный кабинет.
Третья категория пользователей — это ИТ-специалисты, которые взаимодействуют с МДЛП на уровне программы.
Для этих трех категорий пользователей подготовлены схемы и инструкции разного уровня погружения в технические детали. Просим обращать внимание на это при изучении ответов на вопросы. Для 1‑й категории основной документ — «Паспорта процессов». Для 3‑й категории (и 2‑й по желанию) основной документ — это «Логическая модель файлов обмена функциональной подсистемы информационной системы маркировки товаров контрольными (идентификационными) знаками лекарственных препаратов для медицинского применения».
Ответы на вопросы
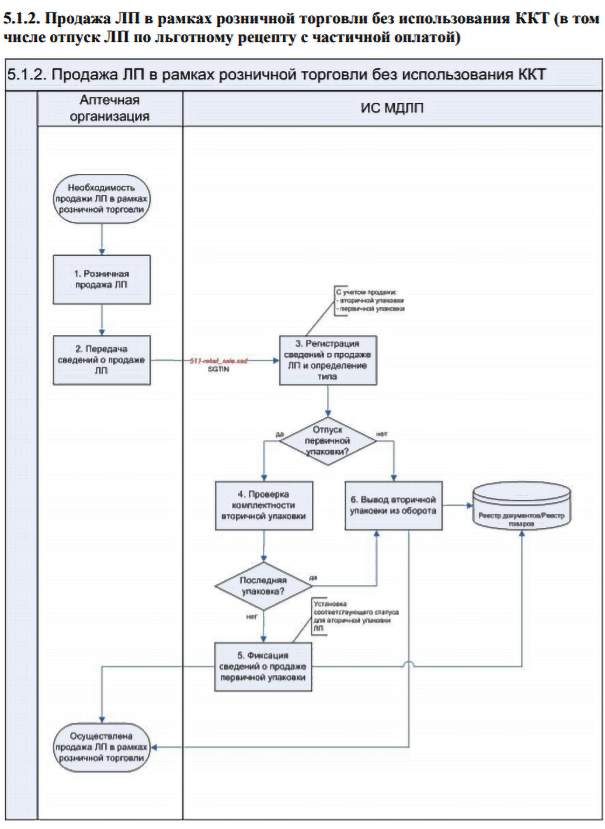
Как будет проходить процесс маркировки товаров в аптечных учреждениях отдаленных населенных пунктов, где работают онлайн-кассы без передачи данных?
Сведения о розничной продаже маркированных лекарств должны передаваться вручную через личный кабинет или через головную организацию при наличии таковой (в таком случае процесс не меняется).
При наличии у учреждения вышестоящей (головной) организации, сведения о выбытии передает указанная организация. Действия происходят по схеме:
Детальное описание последовательности действий описано в документе «Паспорта процессов» в разделе 5.1.2.
Подскажите, мы планируем осуществлять деятельность в рамках договора комиссии с ФАП, расположенными в сельской местности. Каким образом нам организовать деятельность по маркировке ЛП?
При отпуске лекарственных препаратов через ФАП, сведения о выбытии передаются вышестоящей организацией.
Отпуск препаратов на медпункты, детские сады и детские лагеря при оплате по безналичному расчёту (без ККМ). Как работать с маркированными ЛС?
Если участник оборота, которому осуществляется отпуск ЛП, имеет лицензию на медицинскую деятельность, то он должен быть зарегистрирован в МДЛП. Если не зарегистрирован, тогда выполняется операция отгрузки ЛП под названием «Регистрация в ИС «Маркировка» сведений об отгрузке лекарственных препаратов на незарегистрированное место деятельности».
Как отражать в МДЛП безналичный расчет между организациями, как аптека регистрирует выбытие ЛП, купленных по безналичному расчету другой организацией?
В данном случае осуществляются операции об отгрузке лекарственных препаратов со склада отправителя/приема лекарственных препаратов на склад. Детальное описание последовательности действий описано в документе «Паспорта процессов» в разделах 4.1 и 4.2 соответственно.
Подскажите, какие действия нужно совершать поставщику. Мы небольшая компания, зарегистрированы в «Честном знаке». Дальше непонятно — что нам нужно делать, когда мы получаем товар от производителя и когда мы производим отгрузку в ЛПУ. Где можно найти подробную инструкцию по работе дистрибьютора?
Каждая операция (приемка, перемещение, выбытие лекарственных препаратов) должна фиксироваться в МДЛП. Для каждой из этих операций определен состав передаваемых данных и последовательность действий. Имеется два руководящих документа. Последовательность действий описана в документе «Паспорта процессов».
Первично осуществляется приемка товара от производителя. Для этого необходимо использовать операцию «Регистрация в ИС «Маркировка» подтверждения (акцептования) сведений».
Далее при реализации товара другому участнику оборота (ЛПУ), выполняются следующие операции:
- В случае прямого акцептования — «Регистрация в «ИС «Маркировка» сведений об отгрузке лекарственных препаратов со склада отправителя»
- В случае обратного акцептования — «Регистрация в ИС «Маркировка» подтверждения (акцептования) сведений».
Допустимо ли будет с 01.01.2020 для аптечной сети отражать в ИС МДЛП перемещение отозванной из обращения (забракованной) серии лекарственного препарата между местами осуществления деятельности (из аптеки на аптечный склад) при осуществлении централизованного возврата поставщику с аптечного склада?
Допустимо, если в дальнейшем с отозванной из обращения серией будут выполнены следующие операции:
- Регистрация в ИС «Маркировка» сведений о передаче лекарственных препаратов на уничтожение.
- Регистрация в ИС «Маркировка» сведений о факте уничтожения лекарственных препаратов.
Как будет производиться отпуск лекарственных препаратов в структурные подразделения юридического лица? Как будет осуществляться отпуск в структурных подразделениях, если в них нет программы товарного учета, а только ККТ? Как осуществлять отпуск по договорам, школам и т. д.?
Для выполнения операции перемещения лекарственных средств между местами деятельности в рамках одного ИНН необходимо выполнить операцию — «Регистрация в ИС «Маркировка» сведений о перемещении лекарственных препаратов между различными адресами осуществления деятельности».
При использовании ККТ в аптеке данные о выбытии ЛП будут передаваться в МДЛП в момент осуществления покупки. Данные передаются оператором фискальных данных автоматически, в рамках стандартного пакета.
Учреждения, обладающие лицензией на медицинскую или фармацевтическую деятельность, должны быть зарегистрированы в ИС МДЛП. Реализация ЛП происходит по операциям:
- В случае прямого акцептования — «Регистрация в «ИС «Маркировка» сведений об отгрузке лекарственных препаратов со склада отправителя».
- В случае обратного акцептования — «Регистрация в ИС «Маркировка» подтверждения (акцептования) сведений».
Если препарат в стационаре забракован после списания в отделение регистратором выбытия — как его вернуть поставщику?
Необходимо выполнить операцию повторного ввода ЛП в оборот, а затем осуществить возврат поставщику. Далее выполнить операции:
«Регистрация в ИС «Маркировка» сведений о передаче лекарственных препаратов на уничтожение» и «Регистрация в ИС «Маркировка» сведений о факте уничтожения лекарственных препаратов».
Что будет с остатками в МДЛП, если аптека не смогла принять КиЗы от поставщика при обратном акцептовании (КиЗы, например, на производителе), а продавать уже начала?
В МДЛП рассматривается возможность реализации реестра ожиданий, позволяющего выводить ЛП до момента акцептования. После того как ЛП будет оприходован, он будет выведен из оборота.
Как можно будет осуществлять перемещение товара из одной аптеки в другую в одной сети аптек?
Движение ЛП между местами деятельности в рамках одного ИНН регистрируется операцией — «Регистрация в ИС «Маркировка» сведений о перемещении лекарственных препаратов между различными адресами осуществления деятельности». Данные передаются автоматически через товарно-учетную систему, интегрированную с МДЛП, или вручную посредством функционала личного кабинета МДЛП (последнее целесообразно, если оборот — не более 10 уп./сутки).
Как осуществлять возврат ЛС от структурных подразделений?
Возврат регистрируется операцией — «Регистрация в ИС «Маркировка» сведений о перемещении лекарственных препаратов между различными адресами осуществления деятельности». Данные передаются автоматически.
Если у вас еще остались вопросы по работе с маркированными ЛС, приглашаем вас 11 декабря посетить очередной бесплатный вебинар на тему «АРМ в аптеке: знакомимся с техническими средствами маркировки». Там вы сможете не только услышать официальные рекомендации, но и задать свои вопросы в режиме онлайн. Спешите регистрироваться, количество мест ограниченно.
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.
Источник
Росздравнадзор: действия с маркированными и немаркированными товарами
Автор: Шелег Е. Е., эксперт журнала
Росздравнадзор разработал рекомендации по действиям субъектов обращения лекарственных средств с маркированными и немаркированными препаратами в наиболее типичных ситуациях[1]. Подобный свод ответов на часто задаваемые вопросы был анонсирован в ходе совместного с ЦРПТ совещания в начале сентября. Посмотрим, что интересует участников рынка[2].
Оптовик и дальнейший оборот «доиюльских» препаратов отечественного производства.
Ситуация: организация оптовой торговли закупила партию отечественных лекарственных средств, произведенных до 01.07.2020 и введенных в гражданский оборот после 01.07.2020.
Вопрос: может ли оптовик осуществлять дальнейший оборот указанного лекарства как немаркированного товара?
Юридические лица и индивидуальные предприниматели, осуществляющие производство, хранение, ввоз в Российскую Федерацию, отпуск, реализацию, передачу, применение и уничтожение лекарственных препаратов для медицинского применения (далее – ЛП), с 01.07.2020 обеспечивают в порядке и в составе, которые установлены Правительством РФ с учетом вида осуществляемой ими деятельности, внесение информации о препаратах в систему мониторинга движения лекарственных препаратов для медицинского применения (далее – система МДЛП). Об этом сказано в ч. 7 ст. 67 Закона № 61-ФЗ[3].
Вместе с тем некоторые ЛП подлежат хранению, перевозке, отпуску, реализации, передаче, применению без нанесения средств идентификации до истечения срока их годности. Это предусмотрено ч. 7.1 ст. 67 Закона № 61-ФЗ – речь идет оЛП, предназначенных для обеспечения лиц, больных гемофилией, муковисцидозом, гипофизарным нанизмом, болезнью Гоше, злокачественными новообразованиями лимфоидной, кроветворной и родственных им тканей, рассеянным склерозом, лиц после трансплантации органов и (или) тканей, произведенные до 31.12.2019, а также иные ЛП, произведенные до 01.07.2020.
Постановлением Правительства РФ от 31.12.2019 № 1954 производителям лекарственных средств предоставлено право начиная с 01.01.2020 наносить средства идентификации ЛП на первичную упаковку препарата (если вторичная упаковка не предусмотрена) и на вторичную (потребительскую) упаковку ЛП (далее – упаковка ЛП). При этом нанесение средства идентификации лекарства на упаковку ЛП должно сопровождаться предоставлением производителями лекарственных средств в систему МДЛП сведений о нанесении средств идентификации.
Таким образом, перемещение маркированных ЛП по товаропроводящей цепи в указанный период могло не отражаться на балансе участников в системе мониторинга.
С учетом правовых норм и требований (в совокупности) представляется возможным следующий план действий:
если на упаковке ЛП, произведенного до 01.07.2020 (за исключением ЛП, предназначенных для обеспечения лиц по программе высокозатратных нозологий), отсутствуют средства идентификации, дистрибьютор может продолжать оборот указанного ЛП после 01.07.2020 как немаркированного товара;
если на упаковке ЛП, произведенного до 01.07.2020, средства идентификации имеются (поступили маркированные препараты), дистрибьютор обязан передавать сведения об обороте ЛП в систему МДЛП в соответствии с ч. 7 ст. 67 Закона № 61-ФЗ при условии, что в системе мониторинга содержатся сведения о нахождении данного ЛП на балансе грузоотправителя. Для этого дистрибьютору необходимо сформировать и отправить в систему МДЛП запрос по методу API 8.3.2 либо проверить наличие уведомления об отправке грузоотправителем в систему мониторинга в соответствии с установленными законодательством сроками сведений о поставке маркированных лекарств с использованием схемы 415;
в случае отсутствия сведений о том, что поставленный ЛП находится по данным системы мониторинга на балансе грузоотправителя, дистрибьютор может продолжать оборот указанного ЛП после 01.07.2020 как немаркированного товара.
Включение в гражданский оборот произведенного за границей лекарства.
Ситуация: российский производитель выполнил завершающие стадии производства (упаковка и маркировка) ЛП, произведенного до 01.07.2020 за пределами территории РФ и ввезенного в форме in bulk в Россию.
Вопрос: может ли указанный товар поступать в обращение без нанесения на упаковку средства идентификации?
В соответствии с ч. 4 ст. 67 Закона № 61-ФЗ с 01.07.2020 производители лекарственных средств наносят (в установленном Правительством РФ порядке) на первичную упаковку (в отношении ЛП, для которых не предусмотрена вторичная упаковка) и вторичную (потребительскую) упаковку ЛП средства идентификации, за исключением ЛП, производимых для проведения клинических исследований, экспорта, ЛП, указанных в ч. 5 и 8 ст. 13 закона, радиофармацевтических ЛП, пиявок медицинских и газов медицинских.
Ввоз лекарств без нанесения средств идентификации.
Ситуация: лекарства, произведенные до 01.10.2020, ввозятся (после 01.07.2020) на территорию РФ.
Вопрос: может ли быть осуществлен ввоз таких ЛП без нанесения на упаковку средства идентификации?
Особенности ввода в гражданский оборот без маркировки отечественных ЛП, произведенных в период с 01.07.2020 до 01.10.2020, а также ввоза в Россию без нанесения средств идентификации в целях ввода в гражданский оборот ЛП (за исключением ЛП, предназначенных для обеспечения лиц, больных гемофилией, муковисцидозом, гипофизарным нанизмом, болезнью Гоше, злокачественными новообразованиями лимфоидной, кроветворной и родственных им тканей, рассеянным склерозом, лиц после трансплантации органов и (или) тканей), произведенных за пределами РФ до 01.10.2020, определены Положением[4], утвержденным Постановлением Правительства РФ от 30.06.2020 № 955.
В соответствии с Положением выпуск таможенными органами указанных ЛП, ввозимых (ввезенных) в Россию в соответствии с таможенными процедурами выпуска для внутреннего потребления или реимпорта, а также ввод в гражданский оборот ЛП без нанесения средства идентификации осуществляются на основании согласования с Росздравнадзором ввода в гражданский оборот ЛП (далее – согласование на обращение ЛП), оформленного на основании решения созданной при этой службе межведомственной комиссии по выдаче согласований на обращение ЛП (Приказ Росздравнадзора от 03.07.2020 № 5645). Росздравнадзор ведет реестр согласований, содержащиеся в нем сведения являются открытыми и общедоступными. Реестр размещен на сайте службы в разделе «Система маркировки лекарственных препаратов».
С учетом изложенного после 01.07.2020 для ввоза ЛП без нанесения средств идентификации необходимо наличие согласования на обращение ЛП, выданного Росздравнадзором на основании решения межведомственной комиссии.
Последовательное представление сведений в систему МДЛП.
Ситуация: производитель осуществил в адрес дистрибьютора поставку маркированных ЛП, произведенных до 01.07.2020, предоставив сведения об отгрузке в систему МДЛП (прямой акцепт).
Дистрибьютор отгрузил в аптечную сеть ЛП как немаркированный товар.
Аптека реализовала данные ЛП.
Вопрос: какие действия должны были предпринять участники цепочки?
Сведения в систему МДЛП субъектом обращения лекарственных средств при осуществлении операций с ЛП представляются последовательно. При этом сведения об очередной операции с препаратом передаются после получения субъектами подтверждения об успешной обработке системой мониторинга сведений о предыдущей операции с ЛП, что позволяет обеспечить прослеживаемость движения ЛП от производителя до конечного потребителя.
В соответствии с законодательством РФ представление субъектами обращения лекарственных средств в систему МДЛП сведений о действиях с маркированными ЛП до 01.07.2020 не носило обязательного характера.
Таким образом, перемещение маркированных ЛП по товаропроводящей цепи в указанный период могло не отражаться на балансе участников в системе мониторинга.
Реализация оптовиками, аптеками после 01.07.2020 поступившего от дистрибьютора маркированного товара, произведенного до 01.07.2020, в отношении которого на момент поставки в системе мониторинга отсутствовали сведения о нахождении на балансе грузоотправителя, без передачи соответствующих сведений в систему МДЛП не является нарушением.
Представление сведений в систему МДЛП при передаче ЛП между субъектами обращения лекарственных средств в рамках гражданско-правовых отношений допускается двумя способами:
в прямом порядке – сведения передает субъект, передающий ЛП;
в обратном порядке – сведения передает субъект, осуществляющий приемку ЛП.
Решение о выборе прямого либо обратного порядка передачи сведений при обороте ЛП принимается субъектами обращения лекарственных средств, представляющими такие сведения, самостоятельно.
Сведения в систему мониторинга передаются в течение рабочего дня:
от фактической даты отгрузки ЛП – при прямом порядке;
от даты приемки ЛП – при обратном порядке.
В случае выбора обратного порядка подачи сведений при обороте ЛП перед приемкой маркированных ЛП и представлением в систему МДЛП необходимых сведений аптечной или медицинской организации рекомендуется убедиться, что поставленный товар находится по данным системы мониторинга на балансе грузоотправителя. Для этого необходимо сформировать и отправить в систему мониторинга запрос по методу API 8.3.2 или воспользоваться мобильным приложением «Честный знак», который при сканировании кода маркировки покажет информацию о текущем владельце лекарственного препарата. Код маркировки ЛП по данным системы мониторинга должен находиться в статусе «В обороте», при этом сведения о текущем владельце ЛП в системе мониторинга должны совпадать с данными фактического грузоотправителя.
В случае отсутствия в системе мониторинга сведений о том, что поставляемые ЛП, произведенные после 01.07.2020, находятся на балансе дистрибьютора, следует отказаться от приемки данного товара.
Кроме того, необходимо неукоснительно соблюдать сроки представления сведений в систему мониторинга. В противном случае (при несвоевременном внесении данных в систему МДЛП либо внесении в нее недостоверных данных) на хозяйствующий субъект будет наложен административный штраф в соответствии со ст. 6.34 КоАП РФ. В частности:
на должностных лиц – в размере от 5 000 до 10 000 руб.;
на юридических лиц – в размере от 50 000 до 100 000 руб.
За административные правонарушения, предусмотренные ст. 6.34 КоАП РФ, лица, осуществляющие предпринимательскую деятельность без образования юридического лица, несут административную ответственность как юридические лица.
Приемка лекарства при отсутствии в реестре согласований на обращение препарата соответствующей информации
Ситуация: идет приемка произведенных после 01.07.2020 отечественных немаркированных лекарств, информация по которым вреестре согласований на обращение ЛП отсутствует.
Вопрос: может ли дистрибьютор отказать в приемке такого лекарства?
При отсутствии согласования данный немаркированный ЛП, произведенный после 01.07.2020, находится в обращении с нарушением законодательства, и его обращение должно быть приостановлено. Информация о выявлении такого препарата должна направляться в Росздравнадзор.
Приемка лекарств медицинской организацией
Ситуация: медицинская организация получает оторганизаций оптовой торговли маркированные (независимо от даты производства ЛП) препараты.
Вопрос: может ли медицинская организация при получении такого ЛП требовать от поставщика передачу сведений о поставляемом ЛП в систему мониторинга?
Субъекты обращения лекарственных средств начиная с 01.07.2020 обеспечивают в порядке и в составе, которые установлены Правительством РФ с учетом вида осуществляемой ими деятельности, внесение в систему МДЛП информации о препаратах (ч. 7 ст. 67 Закона № 61-ФЗ).
Вместе с тем в отношении маркированных ЛП, произведенных до вступления в действие поименованной нормы (до 01.07.2020), обязательность предоставления в систему мониторинга сведений отсутствовала.
Таким образом, перемещение маркированных ЛП по товаропроводящей цепи в указанный период могло не отражаться на балансе участников в системе мониторинга. Требования медицинских организаций о предоставлении сведений о поставляемом товаре в систему МДЛП выполнимы при наличии сведений о нахождении ЛП на балансе грузоотправителя.
[1] См. по ссылке https://roszdravnadzor.gov.ru/i/upload/images/2020/9/10/1599729293.08582-1-158809.pdf.
[2] Дополнительно рекомендуем ознакомиться со статьей Н. Н. Луговой «Ввод лекарств в оборот без нанесения средств идентификации», № 8, 2020.
[3] Федеральный закон от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств».
[4] Положение об особенностях ввода в гражданский оборот лекарственных препаратов для медицинского применения.
Источник