- Главный «антистрессовый» гормон организма
- Лечение синдрома поликистозных яичников
- +7 (812) 323-07-49 или +7 (921) 932-14-79
- СПКЯ — что это такое?
- Фенотипы СПКЯ
- Клинические признаки СПКЯ
- Причины развития СПКЯ
- Осложнения
- Диагностика СПКЯ
- Дифференциальная диагностика
- Гиперандрогения — симптомы и лечение
- Определение болезни. Причины заболевания
- Распространённость
- Причины
- Симптомы гиперандрогении
- Патогенез гиперандрогении
- Роль андрогенов
- Избыток андрогенов
- Классификация и стадии развития гиперандрогении
- Истинная гиперандрогения
- Другие формы гиперадрогении
- Осложнения гиперандрогении
- Диагностика гиперандрогении
- Лечение гиперандрогении
- Способы удаления волос при гирсутизме
- Прогноз. Профилактика
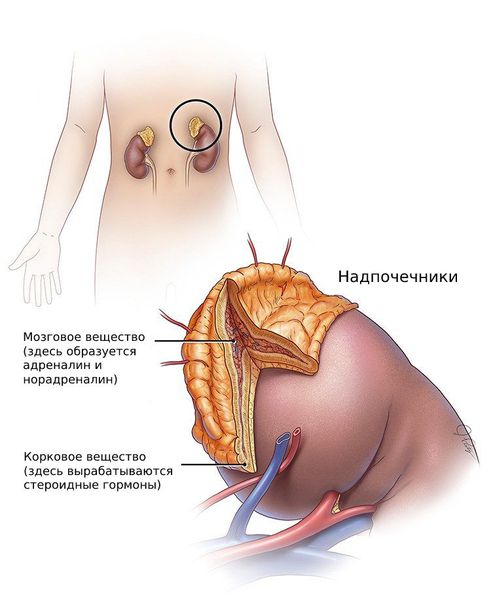
Главный «антистрессовый» гормон организма
Дегидроэпиандростерон или ДГЭА — является гормоном с андрогенной активностью. ДГЭА отвечает за развитие вторичных половых признаков, поддержание половой функции, а также обладает анаболическим действием. 90% гормона образуется в коре надпочечников, остальные 10% синтезируется у мужчин в семенниках, у женщин в яичниках.
Предшественником ДГЭА является холестерин. В свою очередь, ДГЭА преобразуется в другие стероидные гормоны. В организме мужчин ДГЭА конвертируется в более сильные андрогены: тестостерон и андростендион; у женщин — эстроген и прогестерон. Производство гормона происходит под контролем АКТГ.
Уровни ДГЭА достигают пика в юношеском возрасте, а затем постепенно снижаются. В 70–80 лет значения ДГЭА составляют лишь 10–20% от пикового значения в пубертатном периоде.
В классическом варианте анализ на ДГЭА назначают, чтобы:
- оценить функцию надпочечников;
- выявить причину избытка мужских гормонов у женщин (избыточное оволосение, снижение либидо, отсутствие менструации, бесплодие и т.д);
- понять причину преждевременного полового созревания у мальчиков.
Повышенные значения гормона указывают на избыточный синтез андрогенов. Такие уровни связывают с опухолями коры надпочечников; эктопическими опухолями, продуцирующими АКТГ; болезнью Иценко-Кушинга; синдромом поликистозных яичников, фетоплацентарной недостаточностью и ВДКН. Низкие значения ДГЭА чаще ассоциированы с недостаточной функцией надпочечников. Хронический стресс и болезни могут приводить к снижению ДГЭА, указывая на синдром стресса надпочечников.
ДГЭА во многом работает как синергетический близнец другого гормона стресса — кортизола. Это помогает организму более эффективно адаптироваться к стрессовому воздействию. Стресс может быть любым: физическим, психическим и эмоциональным, но его воздействие всегда происходит длительно. Например, учеба, которая дается человеку с трудом или изнуряющие условия на работе — могут стать источником серьезных проблем для здоровья.
Исследования показали, что снижение уровня ДГЭА связано с аллергией, воспалением, усталостью, аутоиммунными проблемами, сексуальной дисфункцией, инфекциями, бессонницей, снижением когнитивных функций, сердечно-сосудистыми заболеваниями, потерей массы костной ткани, депрессией и раком.
ДГЭА и кардиоваскулярная патология
ДГЭА оказывает защитное действие по отношению к заболеваниям сердечно-сосудистой системы. Результаты исследования, опубликованные в 2014 г в журнале Американского колледжа кардиологов, показали, что низкий уровень ДГЭА в крови связан с риском развития коронарной болезни сердца у пожилых мужчин. Ученые из Гарвардской школы общественного здравоохранения обнаружили связь между низкими уровнями ДГЭА и высоким риском развития инсульта у пожилых женщин.
ДГЭА и остеопороз
ДГЭА улучшает минеральную плотность костной ткани и тормозит остеопороз. Особенно это важно для женщин, которые находится в постменопаузе и страдают от дефицита женских половых гормонов.
ДГЭА и сексуальное поведение
Здоровые уровни ДГЭА поддерживают здоровую сексуальную жизнь. ДГЭА улучшает либидо у мужчин и женщин в равной степени.
ДГЭА и когнитивные функции
Исследования показали, что ДГЭА поддерживает здоровые когнитивные функции и настроение. Гормон поддерживает производство и функционирование нейротрансмиттеров в мозге — химических веществ, которые влияют на память и настроение.
Было обнаружено, что ДГЭА обладает регенеративной активностью по отношению к тканям мозга. Люди, страдающие от болезни Альцгеймера, имеют низкий уровень факторов роста, жизненно необходимых для нервной ткани. ДГЭА может защитить тонкие ткани мозга, сохранив их.
Люди с низким уровнем ДГЭА более восприимчивы к тревоге и депрессии.
ДГЭА и метаболический ответ на инсулин
ДГЭА предотвращает развитие сахарного диабета. Гормон позволяет клеткам более эффективно усваивать глюкозу, тем самым снижая резистентность тканей к инсулину. Как известно, это ведущая причина развития сахарного диабета 2-го типа.
ДГЭА и здоровье иммунной системы
ДГЭА имеет решающее значение для укрепления иммунной системы. При хроническом стрессе уровень кортизола падает, и иммунная система оказывается подавленной. Но здоровые уровни ДГЭА могут уравновесить это состояние.
Некоторыми исследователями было продемонстрировано, что ДГЭА играет определенную роль в борьбе с аутоиммунными состояниями, особенно с красной волчанкой.
Недостаток ДГЭА способствует ряду заболеваний и состояний, поэтому для поддержания оптимального сердечно-сосудистого здоровья и жизнеспособности на протяжении всей жизни важно следить за уровнем ДГЭА. Возможно определение гормона в образцах крови, а также в образцах слюны.
Поскольку для хорошего здоровья имеет значение правильный баланс гормонов, поэтому уровень ДГЭА сопоставляют с уровнем кортизола.
Тестирование уровня ДГЭА и сохранение гормонального баланса между стресс-гормонами является ключом успеха на пути к долголетию. Хороший уровень ДГЭА поможет почувствовать себя моложе, сильнее и увереннее.
Источник
Лечение синдрома поликистозных яичников
+7 (812) 323-07-49 или +7 (921) 932-14-79
Почти каждая молодая женщина, видя в зеркале лишний вес, жирный блеск и высыпания на коже, в ужасе устремляется в салон красоты и фитнес-клуб. Только в погоне за красотой это, увы, может оказаться не по адресу. Если вы не переедаете и на косметике не экономите, необходимо срочно записаться на прием к гинекологу . Вышеперечисленные проблемы могут служить сигналами заболеваний яичников.
Здоровые интимной сферы у женщин – это не только беспроблемное наступление беременности, ее легкое течение и здоровые дети. Женские половые гормоны отвечают за упругое тело с плоским животом, за гладкую матовую кожу, за крепкие блестящие волосы и ногти. Гормоны формируют наше настроение и в конечном итоге – отношение к жизни: известно, что позитивный человек и выглядит лучше, и болеет реже, и живет дольше.
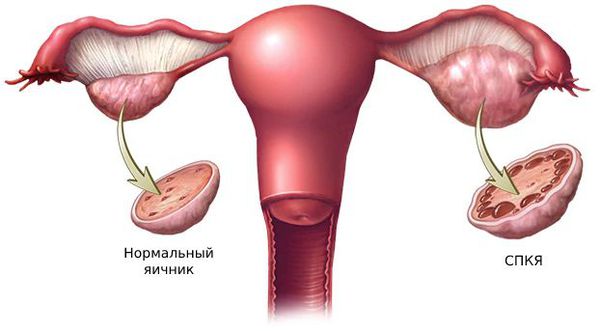
СПКЯ — что это такое?
Синдром поликистозных яичников (СПКЯ) – диагноз, с которым сталкивается каждая пятая женщина репродуктивного возраста. Это означает, что каждая пятая женщина подпадает как минимум под 2 из 3 диагностических критерией:
- овуляторная дисфункция – отсутствие овуляции в большинстве циклов (олигоановуляция), либо ее полное отсутствие (ановуляция);
- биохимическая или клиническая гиперандрогенемия / гирсутизм – избыточная секреция и/или активность мужских половых гормонов (андрогенов) / избыточный рост волос на теле;
- поликистозная морфология яичников – наличие множества мелких кист (фолликулов) в каждом яичнике, отсутствие доминантного фолликула, увеличение объема яичников.
Фенотипы СПКЯ
Выделяют 4 фенотипа в зависимости от комбинаций симптомов:
- классический, или фенотип A (овуляторная дисфункция + гиперандрогенемия/гирсутизм + поликистоз)
- ановуляторный, или фенотип B (овуляторная дисфункция + гиперандрогенемия/гирсутизм)
- овуляторный, или фенотип C (гиперандрогенемия/гирсутизм + поликистоз)
- неандрогенный, или фенотип D (овуляторная дисфункция + поликистоз)
Почти в половине случаев у пациенток с СПКЯ наблюдаются «классический фенотип», сочетающий в себе все клинические, лабораторные и ультрасонографические признаки СПКЯ. Если смотреть в целом, поликистозная морфология яичников наблюдается у 82% среди всех пациенток с СПКЯ, овуляторная дисфункция – у 77%, андрогенемия – 87%, гирсутизм – у 75%. СПКЯ является ведущей причиной бесплодия в развитых странах.
Основные показатели репродуктивного потенциала у женщин с СПКЯ могут значительно различаться в зависимости от фенотипа, однако шанс забеременеть без вспомогательных технологий есть среди всех фенотипов. Грамотно подобранное лечение поможет увеличить шанс наступления беременности и избежать развития сопутствующих заболеваний.

Клинические признаки СПКЯ
Из-за присущего пациенткам с СПКЯ гормонального сбоя самыми очевидными клиническими признаками служат:
- продолжительность цикла менее 21 дня или более 35 дней;
- менструальные кровотечения продолжительностью менее 2 дней или более 7;
- боль в нижней части живота;
- сальность кожи и волос;
- жесткие темные волосы на теле вместо пушковых, на голове — наоборот;
- отложение жира преимущественно в области живота и талии;
- перепады настроения, проблемы со сном и ночные апноэ, расстройства пищевого поведения;
- повышенное артериальное давление;
- ненаступление беременности более полугода.
Причины развития СПКЯ
СПКЯ тесно коррелирует с нарушением углеводного и липидного обмена. При высоком уровне инсулина в крови и/или сниженном преобразовании холестерина в прогестерон стимулируется избыточный синтез андрогенов в яичниках. Степень выраженности клинических проявлений СПКЯ зависит от генов, отвечающих за контроль метаболических процессов обмена глюкозы, синтез стероидных гормонов и восприимчивость тканей к андрогенам. Современные исследования как зарубежных, так и российских ученых, рассматривают инсулинорезистентность и дислипидемию в качестве главных факторов развития СПКЯ.
Осложнения
С возрастом, если не лечить СПКЯ и вызвавшие его причины, у пациенток могут развиться тяжелые сопутствующие заболевания – сахарный диабет, сердечно-сосудистые заболевания, неалкогольный жировой гепатоз, остеопороз, не говоря уже о дальнейших последствиях самого СПКЯ — эндометриальной гиперплазии и раке тела матки.

Диагностика СПКЯ
Внимание! Поскольку некоторые гормональные показатели у женщин зависят от фазы цикла, результаты анализов будут максимально информативны, если день обследования назначит врач.
Биохимический анализ крови включает в себя липидограмму (общий холестерин, триглицериды, липопротеины низкой, очень низкой и высокой плотности), анализ на глюкозу натощак и пероральный глюкозотолерантный тест (ПГТТ). Вместо ПГТТ можно сдать анализ на гликозилированный гемоглобин. Также часто у пациенток с СПКЯ наблюдается дефицит витамина D, поэтому крайне желательно сдать данный анализ.
При диагностике овуляторной дисфункции берут анализы крови на фолликулостимулирующий гормон (ФСГ), лютеинизирующий гормон (ЛГ), эстрадиол (Е2), прогестерон. Анализ на прогестерон необходимо сдавать до 3 циклов подряд в зависимости от первых результатов и сохранности менструального цикла.
Андрогенный статус определяется результатами анализов на общий тестостерон, свободный тестостерон, а также глобулин, связывающий половые гормоны (ГСПГ). Количество тестостерона, доступного для использования тканями организма, зависит от колебания уровня ГСПГ. Вспомогательными маркерами гиперандрогении могут служить анализы на мужские гормоны дегидроэпиандростерон-сульфат (ДГЭА-С) и андростендион.
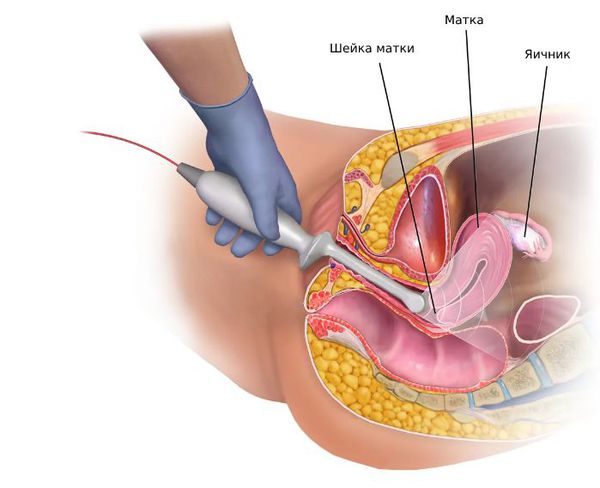
Для оценки морфологии яичников проводят УЗИ органов малого таза .
Дифференциальная диагностика
Дифференциальная диагностика прежде всего предполагает исключение схожих по клиническим признакам заболеваний щитовидной железы и гипофизарно-надпочечниковой системы. По большей части именно с этой целью все пациентки с подозрением на СПКЯ обязательно сдают анализы на тиреотропный гормон (ТТГ), пролактин, 17-гидроксипрогестерон, дегидроэпиандростерон-сульфат (ДГЭА-С), кортизол. Уровни данных гормонов часто отклоняются от нормы при СПКЯ, но клиническая значимость результатов наиболее высока при дифференциальной диагностике.
Источник
Гиперандрогения — симптомы и лечение
Что такое гиперандрогения? Причины возникновения, диагностику и методы лечения разберем в статье доктора Скатова Бориса Васильевича, андролога со стажем в 27 лет.
Определение болезни. Причины заболевания
Гиперандрогения — это состояние, при котором у женщины в крови значительно повышен уровень мужских половых гормонов (андрогенов): тестостерона, дигидротестостерона, андростендиона и других.
Распространённость
Гиперандрогения встречается у 17–18 % женщин детородного возраста. Заболеванием страдают 16–22 % пациенток с бесплодием и 55–62 % — с эндокринным нарушением репродуктивных функций [1] .
Причины
- снижение уровня глобулина, связывающего половые гормоны (ГСПГ), и увеличение концентрации свободного тестостерона;
- синдром поликистозных яичников (СПКЯ);
- опухоли яичников и коры надпочечников, выделяющие андрогены;
- гиперплазия коры надпочечников, в том числе врождённые формы, вызванные мутациями генов CYP21, CYP11B1, HSD3B;
- аденома гипофиза (синдром Иценко — Кушинга);
- синдром HAIR-AN — наследственное заболевание, при котором высокий уровень андрогенов сочетается с инсулинорезистентностью и чёрным акантозом (гиперпигментацией кожи);
- профессиональные занятия единоборствами, хоккеем, футболом и тяжёлой атлетикой [14][15] ;
- приём андрогенов и анаболических стероидов;
- хронический стресс;
- табакокурение и злоупотребление алкоголем[2] .
Симптомы гиперандрогении
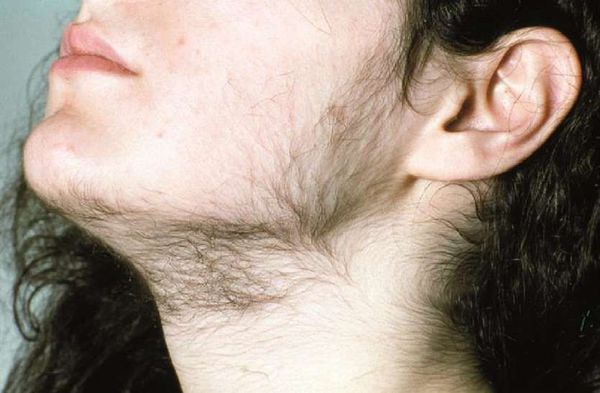
- гирсутизм (избыточное оволосение по мужскому типу) — значительный рост жёстких чёрных волос в зонах, наиболее чувствительных к мужским гормонам: вокруг сосков, на лице, груди, животе, спине и бёдрах;
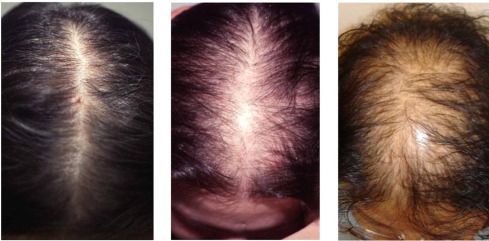
- андрогенная алопеция;
- бесплодие;
- маскулинизация — проявление и усиление у женщин мужских черт, при котором расширяется плечевой пояс, сужаются бёдра и снижается тембр;
- ожирение по мужскому типу, при котором жир откладывается в брюшной полости;
- нарушения менструального цикла: олигоменорея (редкие и скудные менструации) или аменорея (длительное отсутствие менструаций);
- угревая сыпь, жирная кожа и себорея;
- повышенное половое влечение;
- увеличение клитора и уменьшение молочных желёз;
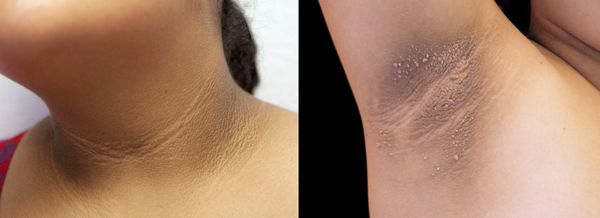
- чёрный акантоз — кожа утолщается и меняет цвет из-за избыточного ороговения клеток эпителия и эпидермиса, а также увеличения уровня пигмента меланина [3] ;
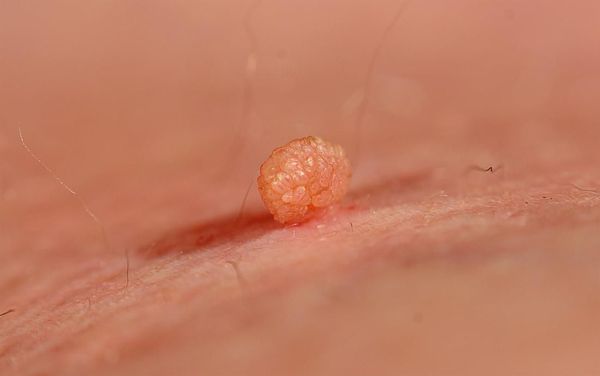
- мягкие фибромы на коже в области шеи, подмышек и паховых складок — доброкачественные новообразования округлой формы и мягкой консистенции.
Патогенез гиперандрогении
Андрогены — стероидные половые гормоны, которые вырабатываются из холестерина в коре надпочечников, а также в клетках фолликулов и соединительной ткани яичников.
К андрогенам относятся:
- тестостерон;
- андростендион;
- дегидроэпиандростерон и др.
В печени, жировой ткани и волосяных фолликулах андрогены способны превращаться в более активную форму — дегидротестостерон. Кроме того, в жировой ткани андрогены преобразуются в женский половой гормон эстрадиол [3] .
Роль андрогенов
В женском организме андрогены поддерживают гормональный баланс и после начала полового созревания инициируют рост волос на лобке и в подмышечных впадинах. Также они необходимы для выработки эстрогена и возникновения полового влечения.
Андрогены замедляют потерю кальция в костях и регулируют работу внутренних органов и систем: репродуктивной, почечной, мышечной и сердечной.
Гормональная регуляция происходит почти мгновенно с малым количеством активного вещества — гормона. Другая её особенность заключается в дистанцировании: гормон может вырабатываться в одной железе, а попадать в орган-мишень, находящийся в другой части организма.
Кроме этого механизма, андрогены могут действовать опосредованно, например через эстрогены — женские половые гормоны [4] .
В плазме крови андрогены взаимодействуют с глобулином, связывающим половые гормоны (ГСПГ). Он выполняет транспортную роль: вместе с ним андрогены доставляются с кровью в клетки органов-мишеней.
Выработка андрогенов зависит от возраста и объёма жировой массы. При старении, ещё до менопаузы, их уровень постепенно уменьшается, особенно снижается концентрация дегидроэпиандростерона и андростендиона. На уровень тестостерона возраст влияет меньше: яичники вырабатывают его почти в прежнем объёме и в постменопаузе [13] .
Избыток андрогенов
К избытку андрогенов могут приводить различные патологические механизмы:
- Развитие опухолей и множественных кист яичников. Изменённые клетки яичников влияют на ферменты, участвующие в обмене стероидных гормонов. К таким ферментам относится 17-альфа-гидроксилаза, играющий ключевую роль в синтезе андрогенов в яичниках.
- Образование опухолей в надпочечниках и гиперплазия коры надпочечников также приводят к избыточной выработке андрогенов.
- На дисбаланс андрогенов влияют другие гормоны: пролактин, эстрадиол и тиреотропные гормоны. Они взаимодействуют друг с другом, например при снижении уровня эстрадиола может расти уровень тестостерона. Это происходит из-за нарушения ферментных систем яичников, которые позволяют андрогенам яичникового происхождения превращаться в эстрогены.
- Гипотиреоз (снижение функции щитовидной железы и, соответственно, гормонов Т3, Т4) сопряжён с ростом уровня пролактина, который воздействует на кору надпочечников и стимулирует выработку андрогенов.
- При недостатке трийодитрина (Т3, самый активный гормон щитовидной железы) снижается концентрация глобулина, связывающего половые гормоны, и растёт уровень свободного тестостерона.
Повышать уровень андрогенов могут и другие внешние факторы, например приём стероидов и гормональных препаратов. Интересно, что при всех гиперандрогенных состояниях, андрогены происходят более чем из одного источника. Так, при поликистозе яичников увеличен синтез тестостерона, но большая часть этого гормона образуется вне яичников — в надпочечниках.
Большую роль в развитии первичной гиперандрогении играют генетические факторы. Одной из причин синдрома поликистозных яичников (СПКЯ) является генетически предопределённый избыток лютеинизирующего гормона (ЛГ). ЛГ стимулирует образование мужских половых гормонов: тестостерона и андростендиона. Их чрезмерная выработка нарушает процесс развития фолликулов: они преждевременно перерождаются в жёлтое тело и в этой области образуются фолликулярные кисты.
Другая причина развития СПКЯ — генетически обусловленное нарушение выработки инсулина и развитие инсулинорезистентности, то есть недостаточный ответ тканей на его действие.
К гиперандрогении, как было сказано выше, может приводить врождённая гиперплазия коры надпочечников. Причина её развития — мутации генов, которые отвечают за синтез ферментов или транспортных белков, участвующих в выработке кортизола.
Классификация и стадии развития гиперандрогении
Согласно Международной классификации болезней (МКБ-10), гиперандрогения кодируется как Е.28.1 Избыток андрогенов. Выделяют истинную гиперандрогению и другие её формы.
Истинная гиперандрогения
Истинная гиперандрогения бывает яичниковой и надпочечниковой
Яичниковая гиперандрогения:
1. Синдром поликистозных яичников. Первичный СПКЯ (синдром Штейна — Левенталя) возникает при нарушении в системе гипоталамус-гипофиз-яичники. Вторичный СПКЯ развивается при эндокринной патологии, например на фоне сахарного диабета, заболеваний щитовидной железы или под воздействием внешних факторов: интоксикации, стресса, травмы и инфекции.
2. Стромальный текоматоз яичников (синдром Френкеля) — тяжёлая форма овариальной неопухолевой гиперандрогении. При заболевании разрастается соединительная ткань и возникает синдром HAIR-AN (высокий уровень андрогенов, инсулинорезистентности, ожирение и чёрный акантоз). Это редкая патология выявляется преимущественно в постменопаузе.
3. Андроген-продуцирующая опухоль яичников:
- гранулезоклеточная опухоль;
- текома;
- андробластома;
- липидоклеточные опухоли.
Надпочечниковая гиперандрогения:
- врождённая гиперплазия коры надпочечников;
- андрогенома — опухоль коры надпочечников, продуцирующая андрогены (тестостерон и дегидроэпиандростерон-сульфат).
Другие формы гиперадрогении
- Транспортная (снижение уровня глобулина, связывающего половые гормоны).
- Периферическая:
- рецепторная;
- метаболическая (повышение уровня фермента 5-альфа-редуктазы).
- Ятрогенная — при приёме андрогенов, анаболических стероидов и глюкокортикоидов. Анаболические гормоны принимаются при выраженном истощении, восстановлении массы тела после тяжёлых заболеваний и травм. Глюкокортикоиды назначают для лечения аутоиммунных заболеваний, например ревматоидных болезней, системной красной волчанки и др.
- Вторичная — андрогензависимые дерматопатии: вульгарные угри, гирсутизм, алопеция и себорея[1] .
Осложнения гиперандрогении
- Ожирение верхней части тела и инсулинорезистентность. Избыток андрогенов влияет на рецепторы инсулина, которыми насыщена жировая ткань верхней части тела. Инсулин переводит углеводы в жировые запасы, и развивается ожирение.
- Сахарный диабет второго типа и гестационный диабет.
- Дислипидемия (повышение уровня холестерина и липопротеидов низкой плотности) и развитие атеросклероза.
- Сердечно-сосудистые заболевания.
- Невынашивание беременности, синдром потери плода, фетоплацентарная недостаточность, гестоз.
- Бесплодие.
- Онкологические процессы матки, молочных желёз и яичников.
- Обильные маточные кровотечения, геморрагический шок и анемия[1][5] .
Наиболее частые осложнения гиперандрогении: бесплодие, инсулинорезистентность и ожирение. Нарушение обмена липидов, сахарный диабет, сердечно-сосудистая патология возникают как следствие этих процессов.
Механизмы развития гиперандрогении и гиперинсулинемии до конца не изучены. Теоретически возможны три варианта взаимодействия: гиперандрогения вызывает гиперинсулинемию, гиперинсулинемия приводит к гиперандрогении и есть третий фактор, ответственный за оба феномена.
Предположение о том, что гиперандрогения вызывает гиперинсулинемию, основано на следующих фактах:
- у женщин, которые принимают оральные контрацептивы, содержащие прогестины с андрогенными свойствами, нарушается толерантность к глюкозе;
- длительный приём тестостерона приводит к развитию инсулинорезистентности.
О том, что гиперинсулинемия вызывает гиперандрогению, свидетельствует следующее: инсулинорезистентность сохраняется у пациенток с удалёнными яичниками и при длительном приёме препаратов, подавляющих выработку андрогенов.
Диагностика гиперандрогении
Диагностика проводится эндокринологом или гинекологом-эндокринологом.
Этапы:
1. Опрос (сбор анамнеза). Врач беседует с пациенткой и выясняет следующие факты:
- приём лекарств, особенно содержащих мужские половые гормоны, например препараты тестостерона — «Андриол», «Омнадрен», «Андрогель» и др.;
- регулярность менструального цикла;
- сведения о беременности и родах;
- время появления и скорость развития избыточного оволосения;
- изменение формы лица и прибавка в весе;
- наличие залысин и характер выпадения волос;
- присутствие угрей и степень жирности кожи;
- наличие диабета у близких родственников;
- образ жизни: употребление алкоголя, курение, уровень физической активности и особенности диеты.
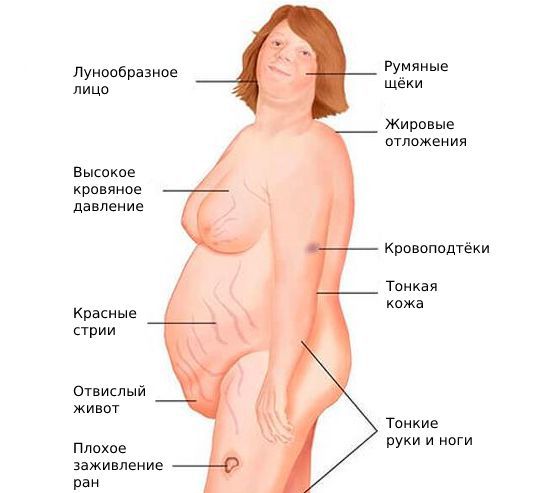
2. Осмотр. Доктор обращает внимание на следующие симптомы:
- признаки синдрома Иценко — Кушинга: лунообразное лицо, жировые отложения на шее, ожирение при тонких конечностях и длинных пальцах, сухая кожа, стрии (растяжки) и язвы на теле;
- чёрный акантоз, мягкие фибромы и угревая сыпь;
- признаки мужественности и ожирения по мужскому типу;
- увеличенный клитор;
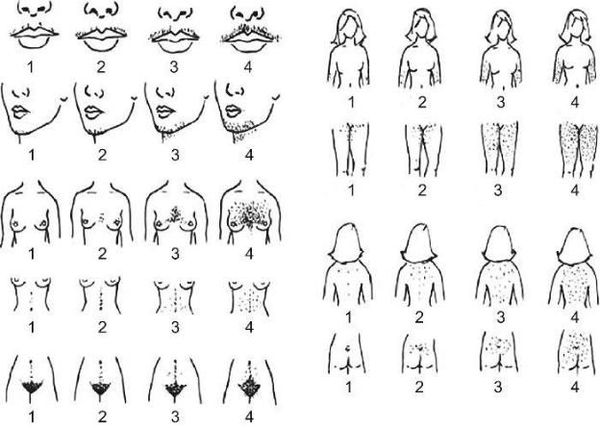
- распределение волос на теле, которое оценивается по визуальной шкале гирсутизма Ферримана — Голлвея.
3. Лабораторные исследования:
- Оценка работы половой системы — анализ крови на общий тестостерон, ГСПГ (глобулин, связывающий половые гормоны), ФСГ (фолликулостимулирующий гормон), ЛГ (лютеинизирующий гормон), пролактин, эстрадиол, альбумин, дигидротестостерон, прогестерон, андростендион, дегидроэпиандростерон-сульфат.
- Оценка гормонов надпочечников — анализ крови на кортизол и на 17-гидроксипрогестерон.
- Оценка работы щитовидной железы и углеводного обмена — анализ крови на ТТГ (тиреотропный гормон), Т3 свободный, Т4 свободный, Т3 реверсивный, АТ к ТПО (антитела к тиреопероксидазе), АТ к ТГ (тиреоглобулину), АТ к рецепторам ТТГ (тиреотропному гормону), анализ на содержание йода в моче, уровень глюкозы и инсулина натощак (индекс Хома), гликированный гемоглобин.
Направление на анализы выписывает врач, так как часть из них нужно проводить в определённые дни менструального цикла.
4. Инструментальная диагностика:
- Трансвагинальное УЗИ яичников позволяет обнаружить признаки синдрома поликистозных яичников, кист и других новообразований.
- УЗИ щитовидной железы выявляет новообразования, кисты, признаки воспаления щитовидной железы и позволяет оценить её размер и структуру.
- УЗИ, МСКТ (мультиспиральная компьютерная томография) и МРT (магнитно-резонансная томография) надпочечников. Исследования выявляют дисплазию и новообразования надпочечников.
- Сцинтиграфия надпочечников после внутривенного введения радиоактивного меченого холестерина. Позволяет выявить скрытую дисплазию и небольшие опухоли надпочечников. Несмотря на применение радиоактивных элементов, процедура безопасна для организма. Вводимые вещества обладают высокой скоростью полураспада: обычно процесс длится не более шести часов. Этого времени достаточно, чтобы провести процедуру, но не навредить организму [1][2][3][6][7] .
Лечение гиперандрогении
Заболевание лечит врач-эндокринолог или гинеколог-эндокринолог.
Лечение поможет устранить симптомы и достичь основных целей:
- нормализовать менструальный цикл;
- устранить бесплодие, вызванное нарушением созревания яйцеклетки и выхода её из яичника;
- устранить кожные проявления;
- вылечить обменные нарушения.
Нормализация менструального цикла уменьшает риск гиперплазии эндометрия и рака тела матки, маточных кровотечений и постгеморрагической анемии.
- комбинированные оральные контрацептивы (КОК);
- циклический или постоянный приём прогестогенов и средств, повышающих чувствительность периферических тканей к инсулину (метформин).
В редких случаях выполняют операции на яичниках.
Комбинированные оральные контрацептивы (КОК) снижают уровень гонадотропинов, а значит и концентрацию андрогенов, которые производятся в яичниках. Содержащиеся в КОК эстрогены увеличивают синтез глобулина, связывающего половые гормоны и, следовательно, снижают уровень свободного тестостерона. Кроме того, прогестагены в составе КОК уменьшают синтез андрогенов в надпочечниках, подавляют фермент 5-альфа-редуктазу и блокируют связывание андрогенов с рецепторами.
Оптимальными будут КОК, содержащие прогестаген с антиандрогенным действием: ципротерон, хлормадинон, диеногест и дроспиренон. Также предпочтительны оральные контрацептивы с этинилэстрадиолом.
Наиболее известные КОК, применяемые для лечения гиперандрогении:
- «Джес», «Димиа», «Ярина» — результат достигается быстро, уже через две недели, но у препаратов много побочных эффектов. Среди них: головная боль, боли в животе, тошнота, рвота; болезненность и нагрубание молочных желёз; увеличение веса, нарушение толерантности к глюкозе, задержка жидкости в организме; изменение либидо и снижение настроения; отёки век, кожная сыпь, узловая эритема, конъюнктивит, неприятные ощущения при ношении контактных линз; тромбофлебит, периферическая и центральная тромбоэмболия (может проявляться ухудшением зрения и слуха); генерализованный зуд, холестатическая желтуха, холелитиаз, повышение артериального давления; межменструальное кровотечение, изменение влагалищной секреции, кандидоз влагалища. Побочные эффекты могут возникать в первые несколько месяцев приёма препарата и обычно уменьшаются со временем.
- «Жанин», «Хлое» — могут назначаться молодым нерожавшим женщинам при избыточном оволосении, совместимы со многими препаратами.
- «Логест» — предпочтителен при выпадении волос.
- «Белара» — при СПКЯ и ожирении.
- «Линдинет-30», «Регулон», «Ярина», «Диане-35» и другие препараты [7][8] .
Прогестагены нормализуют менструальный цикл при циклическом или постоянном приёме. Однако есть гипотезы, что прогестерон сам обладает андрогеноподобным действием. Его, как правило, не назначают для лечения гиперандрогении, но применяют для нормализации второй фазы менструального цикла.
Блокаторы андрогенных рецепторов из–за выраженной тератогенности (влияния на внутриутробную закладку органов будущего ребёнка) беременным принимать запрещено.
Основные препараты из группы блокаторов андрогенных рецепторов:
- «Спиронолактон» — широко применяется в США как диуретик и нестероидный антиандроген. Эффективен при избыточном оволосении по мужскому типу.
- «Ципротерон» — снижает уровни тестостерона и андростендиона, подавляя секрецию лютеинизирующего гормона, блокирует действие андрогенов в периферических тканях. Среди побочных эффектов выделяют надпочечниковую недостаточность и снижение полового влечения [8][9] .
- «Финастерид» — уменьшает гирсутизм, но оказывает сильное тератогенное действие на эмбрионы мужского пола, поэтому при его приёме необходима надёжная контрацепция [11] .
Дозировку и режим приёма препаратов врач назначает индивидуально.
Фитотерапия играет вспомогательную роль. Применяют экстракт зелёного чая, сереноа (экстракт южно-американской пальмы), семя льна, пион, сою, стевию и дягель [10] [16] .
Способы удаления волос при гирсутизме
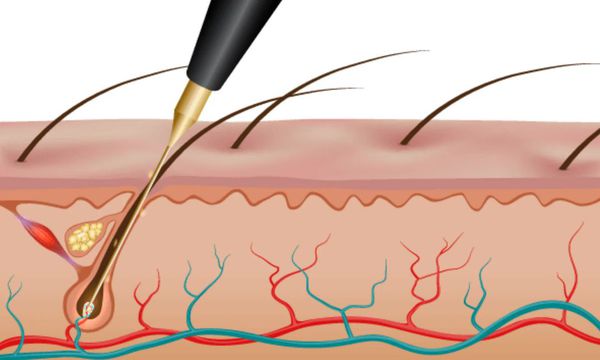
Электроэпиляция позволяет избавиться от волос на долгий срок, но потребуется несколько процедур, количество которых подбирают индивидуально [3] .
Существуют три вида электроэпиляции:
- электролиз — в волосяной фолликул вводят один или несколько стерильных электродов, по ним поступает постоянный ток и специальное химическое вещество;
- термолиз — через стерильный электрод в волосяной фолликул подают высокочастотный переменный ток, создающий тепло и разрушающий фолликул;
- смешанный тип — применяют два вида тока.
Побочные эффекты электроэпиляции: ожоги, раздражение кожи, редко — образование рубцов.
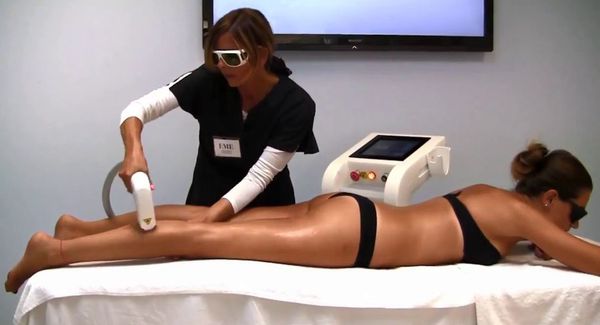
Лазерная эпиляция позволяет повредить волосяной фолликул, не разрушив окружающие его ткани. Процедуры нужно проводить многократно, но полностью избавиться от волос удаётся редко. В зависимости от источника светового излечения лазеры для удаления волос делятся на три группы:
- красные — рубиновый лазер с длиной волны 694 нм;
- инфракрасные — александритовый лазер (с длиной волны 755 нм), диодный (800 нм) и неодимовый (1064 нм);
- импульсные источники лазерного излучения высокой интенсивности (590–1200 нм) [12] .
Прогноз. Профилактика
Если своевременно обратиться к врачу и правильно подобрать лечение, то можно уменьшить неприятные симптомы и избежать серьёзных осложнений.
Результаты терапии следует оценивать через 3–6 месяцев, потому что антиандрогенные препараты действуют медленно: они постепенно накапливаются в организме и встраиваются в обмен веществ. Их приём требует адекватного дозирования, а также регулярной оценки результатов и возможных побочных действий.
Лечение позволяет избавиться от симптомов, поэтому для грамотной коррекции терапии пациентке необходимо регулярно посещать врача-эндокринолога
Профилактика:
- обратиться к доктору при появлении первых признаков гиперандрогении;
- вести здоровый образ жизни;
- избегать хронических стрессов;
- сбалансировать питание;
- не злоупотреблять алкоголем;
- с осторожностью заниматься борьбой, бодибилдингом и тяжёлой атлетикой;
- исключить приём препаратов с мужскими половыми гормонами, анаболических стероидов и глюкокортикоидов [7] .
Источник