Скорость растворения лекарственных средств зависит от
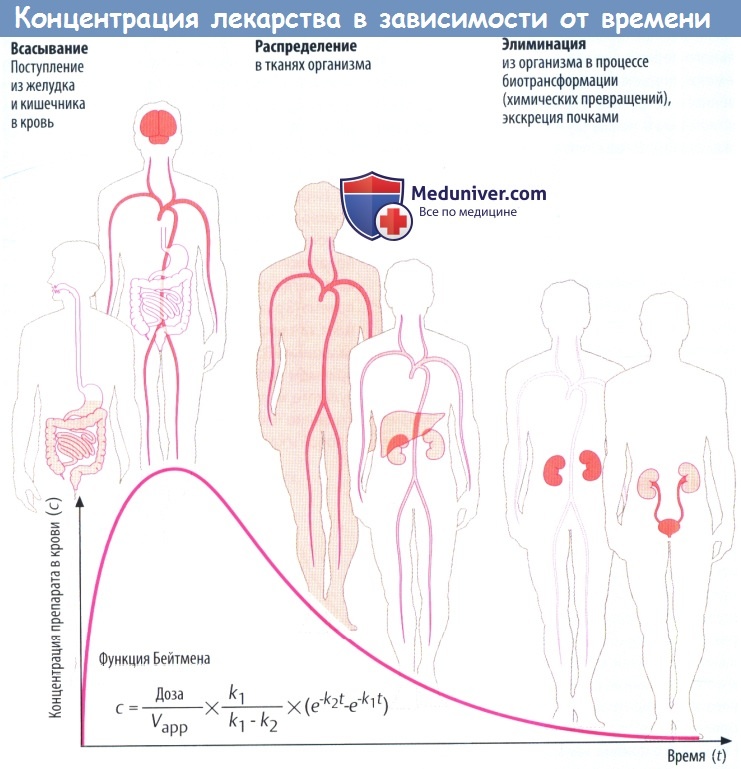
(А) Лекарственные средства попадают в организм и выводятся из него разными путями. Таким образом, организм представляет собой открытую систему, в которой фактическая концентрация препарата отражает взаимодействие между его поступлением (приемом) и эвакуацией (элиминацией).
Скорость всасывания препарата в желудке и кишечнике зависит от множества факторов: скорости растворения вещества (в случае приема твердой лекарственной формы) и транзита по ЖКТ, проницаемости слизистой для препарата, его градиента концентрации на границе слизистой и крови,кровоснабжения слизистой оболочки.
Всасывание из кишечника приводит к повышению концентрации лекарственного вещества в крови. Препарат разносится с кровью к различным органам (распределение), которые поглощают его в количестве, соответствующем его химическим свойствам и скорости кровотока через орган.
Например, органы с хорошим кровоснабжением, такие как головной мозг, получают большее количество препарата, чем органы с низким кровоснабжением. В результате поглощения тканями происходит снижение концентрации лекарственного вещества в крови. По мере снижения градиента на границе слизистой оболочки и крови всасывание в кишечнике замедляется. Пик концентрации в крови достигается тогда, когда количество вещества, покидающего кровь за единицу времени, равно количеству всосавшегося.
Поступление вещества в ткани печени и почек представляет собой перемещение в органы выведения. Концентрация препарата в крови в различные периоды времени представляет собой совокупность процессов абсорбции, распределения и элиминации, которые пересекаются во времени.
Если распределение происходит значительно быстрее, чем элиминация, снижение концентрации в крови вначале происходит быстро, а затем замедляется. Фаза быстрого снижения обозначается как α-фаза (фаза распределения), медленного — как β-фаза (фаза элиминации). Если препарат распределяется быстрее, чем абсорбируется, концентрацию препарата в крови можно описать математически упрощенной функцией Бейтмена (k1 и k2 — константы скорости для абсорбции и элиминации соответственно).
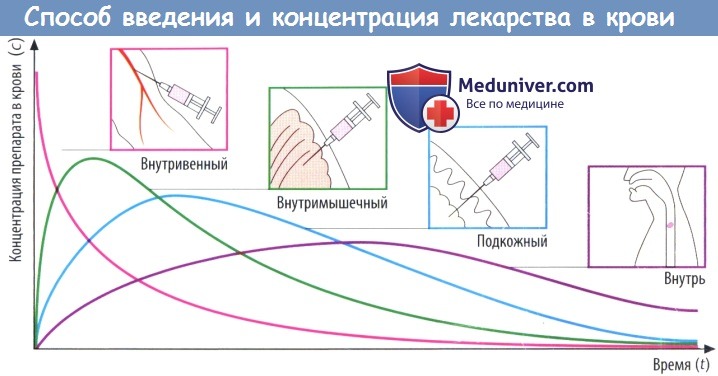
(В) Скорость абсорбции зависит от способа введения препарата. Чем выше скорость абсорбции, тем короче будет время (tmax), которое требуется для достижения пика концентрации в плазме (cmax), тем выше будет cmax и тем раньше уровень препарата в крови снова начнет снижаться.
Площадь под кривой, описывающей зависимость концентрации препарата в крови от времени (AUC), не зависит от пути введения препарата при условии, что доза и биодоступность остаются теми же (закон соответственных состояний). Таким образом, AUC можно использовать для вычисления биодоступности (F) препарата.
Значение AUC, измеренное после приема внутрь и в/в введения определенной дозы конкретного лекарственного вещества, соответствует проценту вещества, попавшего в системный кровоток после приема внутрь: F = AUCприем внутрь/AUCв/в введение.
Определение концентрации препарата в крови позволяет сравнить различные патентованные лекарственные средства, содержащие одно и то же действующее вещество в одинаковой дозе. Идентичные кривые зависимости концентрации в крови от времени для препаратов различных производителей (при условии стандартных лекарственных форм) означают биоэквивалентность стандартного вещества и нового исследуемого препарата.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Скорость растворения лекарственных средств зависит от
Управление солюбилизационными характеристиками лекарственных веществ является одним из основных направлений в разработках современных систем доставки лекарств (Drug Delivery Systems) [22]. В этом направлении наиболее востребованы методы повышения растворимости и скорости растворения активных фармацевтических субстанций – лекарственных веществ (ЛВ). Растворимость играет существенную роль в действии лекарств, прежде всего предназначенных для перорального приема, так как максимальная скорость пассивного транспорта препарата через биологические мембраны – основной путь для поглощения ЛВ – зависит от проницаемости мембраны и концентрации раствора/растворимости. Учитывая, что
40 % выпускающихся лекарственных субстанций классифицируются как практически нерастворимые, а
85 % самых продаваемых препаратов в США и Европе принимаются перорально, актуальность исследований в данном направлении становится очевидной.
В настоящее время FDA принята система биофармацевтической классификации лекарств [24, 26] для прогнозирования биодоступности при пероральном приеме. Эта система основана на использовании соотношений параметров растворимости и проницаемости стенок желудочно-кишечного тракта (ЖКТ). Растворимость классифицирована на основании стандартов Фармакопеи США (USP) [23]. Так, лекарственное вещество считается хорошо растворимым, когда максимальная разрешенная его доза растворяется в 90 процентов его дозы проникает в кровоток при пероральном введении. Ниже приводятся основные классы ЛВ по критериям «проницаемость стенок ЖКТ – растворимость».
Класс I – высокая проницаемость, высокая растворимость. Эти соединения хорошо всасываются и скорость абсорбции, как правило, выше, чем выведение.
Класс II – высокая проницаемость, низкая растворимость. Пример: большинство нестероидных противовоспалительных средств. Биодоступность таких продуктов ограничена скоростью их растворения (кинетический барьер) и растворимостью (термодинамический барьер). К этому классу относится
> 30 % выпускающихся и разрабатываемых лекарств.
Класс III – низкая проницаемость, высокая растворимость. Пример: большинство антибиотиков бета-лактамного типа. Низкая скорость абсорбции ограничивает проникновение в кровоток, но препараты растворяются очень быстро.
Класс IV – низкая проницаемость, низкая растворимость. Пример: антигельминтики – альбендазол, карбендацим, фенбендазол; растительные флавоноиды – рутин, кверцетин, дигидрокверцетин. Эти соединения имеют низкую биодоступность. Обычно они плохо поглощаются слизистой оболочкой кишечника. К этому классу относится
10 % выпускающихся и разрабатываемых лекарств.
Таким образом, ЛВ, относящиеся к II и IV классам, нуждаются в технологиях повышения их водорастворимости. К этим классам относятся до 50 % разрабатываемых и выпускающихся фармацевтической промышленностью ЛВ.
Для повышения растворимости лекарств используют различные физико-химические подходы: уменьшение размеров частиц, модификация кристаллической структуры, получение твердых дисперсий ЛВ с наполнителями и т.д. [20, 18]. Так, при измельчении субстанций антигельминтных препаратов «карбендацим» (бензимидазолил-2-метил карбамат) и «альбендазол» (5-тиопропилбензимидазолил-2-метилкарбамат) в планетарно-центробежном активаторе АГО–2 в «жестких» условиях активации (40 – 60g) было показано не только уменьшение размера частиц, но также стабильность химической структуры, а именно, при сравнении ИК-спектров исходных и измельченных субстанций не было обнаружено изменений в расположении полос поглощения основных функциональных групп (NH, C = N, C = O, OCH3). В спектрах измельченных субстанций наблюдалось увеличение интенсивности этих сигналов, что позволило предполагать лишь о разрушении межмолекулярных водородных связей [11]. Изучение растворения исходного и измельченного образцов карбендацима в среде «желудочного сока» показало, что скорость растворения измельченной субстанции выше, нежели неизмельченной субстанции.
Однако, по нашему мнению, наиболее значимые результаты достигаются за счет перевода ЛВ в их водорастворимые соли (если ЛВ имеет выраженные кислотно-основные свойства), а также за счет включения молекул ЛВ в супрамолекулярные водорастворимые образования (межмолекулярные комплексы, мицеллы) со специально подобранными «вспомогательными» веществами.
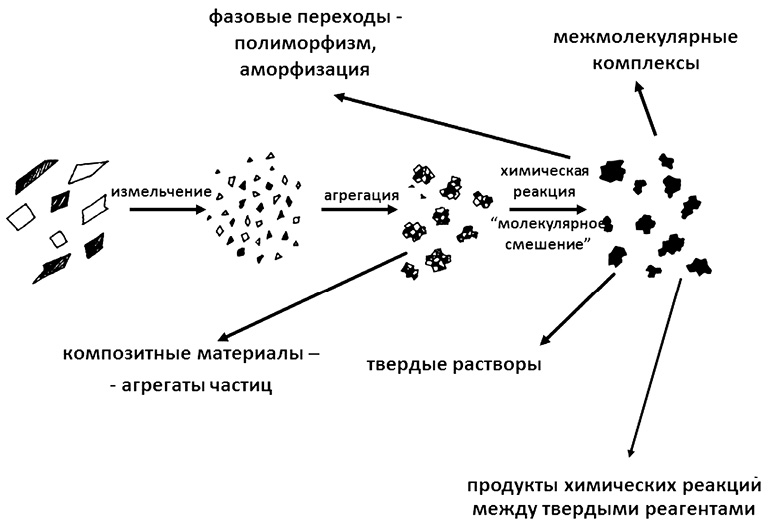
Механохимия является разделом химии твердого тела, в котором изучаются физико-химические превращения твердых веществ и их смесей в условиях интенсивных ударно-истирающих воздействий, обычно реализующихся в специальных мельницах. На рис. 1 показаны возможные пути трансформаций в смесях твердых веществ при их механохимической обработке [3].
Суть нашей технологии заключается в получении твердых дисперсий лекарственных веществ со вспомогательными веществами различной химической природы. Увеличение растворимости ЛВ и повышение эффективности фармакологического действия в зависимости от их физико-химических свойств достигается:
– образованием твердых дисперсий, в которых ЛВ диспергировано в молекулярной форме или находится в аморфном состоянии;
– образованием водорастворимых солей;
– образованием водорастворимых комплексов включения с полисахаридами по типу «гость-хозяин», а также мицелл.
Далее мы рассмотрим вышеуказанные случаи.
Рис. 1. Схема механохимических превращений в смесях твердых веществ (ЛВ + вспомогательные вещества) при их механической обработке ударно-истирающими воздействиями
Получение и свойства твердых дисперсий, в которых ЛВ находится в аморфизованном состоянии или диспергирована в молекулярной форме
Высвобождение в раствор фармакологически активного вещества из твердых лекарственных форм (порошков, таблеток и т.д.) во многом определяется скоростью растворения его кристаллической фазы. Однако многие фармакологические активные вещества крайне медленно растворяются в воде во многом за счет плохой смачиваемости и «прочности» кристаллической решетки. Очевидно, что получение твердых растворов – молекулярных дисперсий – таких веществ в хорошо растворимом наполнителе либо разупорядочение их кристаллических фаз будет способствовать ускорению процесса растворения. Именно этот принцип был применен нами к модификации антигельминтика карбендацима и ряда транквилизаторов бензодиазепинов – диазепама, оксазепама и медазепама, лекарственные субстанции которых практически нерастворимы в воде.
Для модификации солюбилизационных характеристик бензодиазепинов нами механохимическим способом были получены их твердые дисперсии с лактозой и микрокристаллической целлюлозой в весовых соотношениях 1:5, 1:10 и 1:15. В дифрактограммах механически активированных образцов наблюдалось резкое падение интенсивности рефлексов (без их заметного уширения) кристаллических фаз ЛВ вплоть до их полного исчезновения. Рефлексы веществ – наполнителей (лактозы и отчасти целлюлозы) претерпевали уширение, что свидетельствовало о накоплении дефектов и уменьшении кристалличности. К сожалению, методы термического анализа оказались неэффективны из-за относительно низких температур разложения веществ-наполнителей.
Проведенные исследования растворимости образцов продемонстрировали во всех случаях увеличение скорости растворения ЛВ в механохимически полученных образцах по сравнению со смесями, не подвергавшимися механохимической обработке и тем более измельченными исходными субстанциями [5]. Проведенные испытания биологической доступности образцов модифицированных препаратов оксазепама на лабораторных животных – кроликах – показали увеличение действующей концентрации оксазепама в крови и сокращение времени достижения ее максимального значения. Биодоступность оксазепама по сравнению с неактивированной смесью увеличивается в 1,56 ± 0,25 раза. Таким образом повышается эффективность действия лекарственного средства.
Получение и свойства твердых дисперсий, образующих водорастворимые соли ЛВ
Многие малорастворимые ЛВ обладают кислотными или основными свойствами и способны к ионизации в водных растворах и образованию соответствующих солей. Как правило, ионизированная форма является более гидрофильной и имеет более высокую водорастворимость. Многие ЛВ с целью повышения их растворимости выпускаются в виде их солей [9, 12]. Так, лекарственные вещества, имеющие основной характер, – в виде гидрохлоридов, а органические кислоты – в виде солей металлов или органических оснований. Соли получают реакцией жидкофазной нейтрализации с последующим выделением (сушкой). При этом требуются большие объемы растворителей, громоздкое оборудование, значительные производственные площади. Кроме того, в процессе сушки возможно разложение целевого продукта.
Рассмотрим возможности этого подхода на примере ацетилсалициловой кислоты (аспирина). Малая растворимость в воде ( Примечания:
Cmax – максимальная концентрация в крови;
Tmax – время достижения максимальной концентрации в крови;
AUC – площадь под фармакокинетической кривой, в относительных единицах;
* – навески препаратов взяты в эквивалентных по действующему веществу концентрациях.
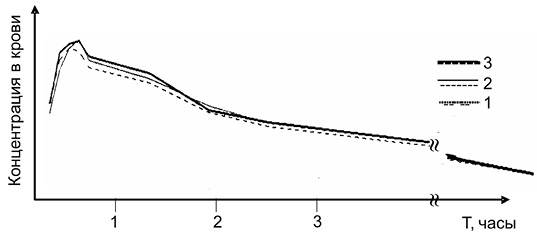
Рис. 3. Фармакокинетика препаратов «АСК – Na2CO3» и «Аспирин + С» при разных способах приема препаратов. Прием раствора таблеток «Аспирин + С» (1), раствора таблеток нашего препарата (2) и таблеток нашего препарата без предварительного растворения (3) в эквивалентных по АСК дозах
В соответствии с действующими правилами нами были разработаны фармакопейные статьи на таблетки и субстанцию, проведены фармакологические испытания [1, 2] и препарат зарегистрирован для применения в РФ.
Композиция состава АСК/CaCO3 = 78/22 вес. % также представляет значительный интерес. Она обладает высокой химической стабильностью при хранении и меньшей гигроскопичностью, но замедленной скоростью растворения. Методом прямого прессования из нее были получены таблетки с двумя дозировками АСК – 0,1 г (вес таблетки 0,128 г) и 0,5 г (вес таблетки 0,64 г). По своим характеристикам – химическая чистота, время растворения, кислотонейтрализующая емкость (для таблеток по 0,5 г) – эти таблетки соответствуют требованиям USP к так называемым «буферированным» таблеткам ацетилсалициловой кислоты. Разработанный нами препарат, получивший название «Антиагрегин», показал при сравнительных опытах с применяемыми в медицинской практике импортными препаратами практически равнозначную эффективность и безопасность для лечения и профилактики сердечно-сосудистых заболеваний (табл. 2).
Сравнительные характеристики разработанных в ИХТТМ СО РАН растворимых таблеток и их импортных аналогов
Источник
Всасывание, распределение и выведение лекарственных средств

Полнота и скорость всасывания лекарственного вещества определяют его биодоступность. Она характеризуется долей попадающего в кровь лекарства от общего его количества, введенного в организм. Биодоступность зависит от ряда факторов, включающих путь введения препарата, его физические и химические свойства, а также физиологические особенности принимающего его человека.
Единицей лекарственного средства является та или иная его форма, содержащая определенную дозу активного вещества — таблетка, капсула, свеча, пластырь или ампула. Активное вещество обычно объединено с другими компонентами. Например, таблетки — это смесь действующего средства и добавок, которые выполняют роль растворителей, стабилизаторов, размельчителей и формообразующих компонентов. Смесь гранулируют и прессуют в форму таблетки. Время, необходимое для ее растворения, зависит от вида и количества добавок, а также степени их спрессованности. Изготовители лекарственных препаратов подбирают эти параметры так, чтобы скорость и объем всасывания были оптимальными.
Если таблетка растворяется и активное вещество высвобождается слишком быстро, его концентрация в крови может вызывать чрезмерную реакцию. С другой стороны, если растворение таблетки и высвобождение лекарственного средства происходит недостаточно быстро, большая его часть будет проходить по кишечнику и выводиться с каловыми массами, не попадая в кровь в нужном количестве. Понос или слабительные средства, ускоряющие прохождение пищевой массы через желудочно-кишечный тракт, уменьшают всасывание препарата. Таким образом, на биодоступность лекарственного средства влияют пища, другие лекарства и болезни желудочно-кишечного тракта.
Желательно, чтобы лекарства с одинаковым международным названием имели схожую биодоступность. Химически эквивалентные препараты содержат одно и то же активное действующее средство, но могут иметь различные неактивные компоненты, влияющие на скорость и объем всасывания. Действие препаратов, изготовленных разными фармацевтическими фирмами, нередко отличается даже при одинаковой дозе активного вещества. Лекарства биоэквивалентны, если они не только содержат один и тот же активный компонент, но и создают одинаковую его концентрацию в крови через определенное время. Биоэквивалентность гарантирует сходный лечебный эффект, поэтому биоэквивалентные препараты взаимозаменяемы.
Некоторые лекарства изготовлены таким образом, чтобы их активные компоненты высвобождались в течение 12 часов или более. Существуют специальные лекарственные формы препаратов, которые обеспечивают медленное поступление действующего вещества в кровоток (препараты пролонгированного действия). Например, частицы лекарственного средства в капсуле покрыты слоями полимеров (химических веществ) разной толщины, подобранными с таким расчетом, чтобы полимеры растворялись в желудочно-кишечном тракте в разное время.
Некоторые таблетки и капсулы имеют защитное покрытие, предотвращающее повреждение слизистой оболочки желудка раздражающими веществами типа аспирина или разрушение активных компонентов в кислой среде желудка. Эти лекарственные формы покрыты материалом, который начинает растворяться только при контакте с менее кислой средой или с пищеварительными ферментами тонкой кишки. Однако такое покрытие не всегда растворяется полностью, и у многих людей, особенно пожилых, эти таблетки в неизмененном виде попадают в каловые массы.
На всасывание препарата после приема внутрь влияют и другие свойства твердых лекарственных форм (таблеток и капсул). Например, капсулы состоят из действующих веществ и добавок, окруженных желатиновой оболочкой. Намокая, желатин набухает и позволяет содержимому проникнуть наружу, а сама оболочка, как правило, быстро разрушается. Кроме того, на скорость всасывания влияет размер частиц активного вещества и неактивных компонентов. Лекарства всасываются быстрее из капсул с жидким, а не твердым содержимым.
Распределение
После того как лекарство попало в кровоток, оно быстро разносится по всему организму, поскольку кровь совершает полный круг по кровеносной системе в среднем за 1 минуту. Однако переход лекарственного средства из крови в ткани тела может происходить медленно. Лекарство поступает в различные ткани с неодинаковой скоростью в зависимости от его способности проникать через мембраны клеток. Например, средство для наркоза тиопентал быстро попадает в мозг, а антибиотик пенициллин — медленно. Как правило, жирорастворимые препараты проходят через мембраны клеток легче, чем водорастворимые.
Большинство лекарственных средств после всасывания распределяются в организме неравномерно. Одни из них задерживаются в крови или мышцах, а другие скапливаются в определенных органах — щитовидной железе, печени или почках. Существуют лекарства, которые прочно связываются с белками крови и покидают кровоток очень медленно, в то время как многие средства быстро переходят из крови в другие ткани. Иногда в каком-то месте создается такая высокая концентрация препарата, что оно превращается в его «депо» в организме, таким образом увеличивая продолжительность терапевтического эффекта. Некоторые лекарства циркулируют в крови в течение нескольких дней после прекращения их приема, поскольку они продолжают постепенно высвобождаться из ткани, где произошло их накопление.
Кроме того, распределение лекарственных средств зависит от индивидуальных особенностей больного. Например, людям крупного телосложения, имеющим больший объем тканей и циркулирующей крови, требуется большее количество препарата. В организме человека, страдающего ожирением, может задерживаться значительное количество лекарств, которые откладываются в жировой ткани, в то время как у худощавых людей таких «возможностей» относительно немного. Накопление лекарственных средств в жировой ткани также замечено у пожилых людей, потому что доля жировой ткани в организме с возрастом увеличивается.
Выведение
Лекарства либо подвергаются метаболизму (видоизменяются) в организме, либо выводятся в неизмененном виде. Метаболизм — это процесс, в ходе которого происходит химическое изменение лекарственных средств. В основном он протекает в печени. Продукты метаболизма (метаболиты) могут быть неактивны, а могут иметь похожую или отличающуюся от исходного препарата активность и токсичность. Некоторые лекарства (пролекарства) применяют в неактивной форме, а активными они становятся и вызывают желаемые эффекты после соответствующего превращения. Эти активные метаболиты выводятся в неизмененной форме (главным образом с мочой или калом) или подвергаются дальнейшим преобразованиям и в конечном счете также выводятся из организма.
Печень содержит ферменты, благодаря которым происходят химические реакции окисления, расщепления и гидролиза лекарств, а также ферменты, присоединяющие к лекарству другие вещества в ходе реакции конъюгации. Конъюгаты (молекулы лекарственного средства с присоединенными веществами) выводятся с мочой.
У новорожденных метаболические ферментные системы развиты только частично, поэтому метаболизм многих лекарств у младенцев затруднен и, следовательно, им требуется меньшее количество лекарственного средства на единицу веса тела, чем взрослым. В то же время дети от 2 до 12 лет нуждаются в большем количестве лекарств. Подобно новорожденным, у пожилых людей тоже уменьшена ферментативная активность, и они не способны видоизменять (метаболизировать) лекарства, как молодые люди. В итоге новорожденные и пожилые люди, как правило, нуждаются в меньших, а подростки в больших дозах лекарственных средств на единицу веса тела.
Термин выделение (экскреция) обозначает процессы, с помощью которых организм освобождается от лекарства. Главными органами выделения являются почки. Они особенно важны для удаления водорастворимых препаратов и их метаболитов.
Почки фильтруют лекарство из крови и выводят с мочой. На их выделительную способность оказывают влияние многие факторы, например состояние почек и скорость кровотока через них, существование нарушений, препятствующих оттоку мочи. Кроме того, лекарственные средства или их метаболиты должны быть растворимы в воде и не слишком сильно связаны с белками плазмы крови. Скорость, с которой выделяются некоторые лекарства, имеющие кислотные или основные (щелочные) свойства, зависит от кислотности мочи.
По мере старения человека функциональные возможности почек уменьшаются. При выделении лекарств почка 85-летнего человека работает приблизительно в половину мощности по сравнению с почкой 35-летнего. Множество болезней, особенно высокое артериальное давление, сахарный диабет и хронические почечные инфекции, а также воздействие больших количеств токсических веществ, могут ухудшать способность почек выводить лекарства.
Если работа почек нарушена, врач скорректирует дозу лекарства, выведение которого осуществляется прежде всего через эти органы, учитывая естественный процесс снижения функции почек с возрастом. Однако более точный способ рассчитать нужную дозу состоит в том, чтобы оценить функции почек с помощью специального анализа крови (измерение количества креатинина в ее сыворотке), иногда в сочетании с анализом мочи (измерение количества креатинина в моче, собранной за 12–24 часа).
Некоторые лекарства удаляются из организма с желчью благодаря работе печени. Они поступают в желудочно-кишечный тракт и либо выводятся с калом, либо повторно всасываются из кишечника и поступают в кровоток, либо разрушаются. Существуют препараты, которые в небольшом количестве выводятся со слюной, потом, грудным молоком и даже выдыхаемым воздухом. Для человека, страдающего болезнью печени, необходимо скорректировать дозу лекарственного средства, выделяемого в основном через этот орган. Но простых способов оценить функцию печени, связанную с метаболизмом лекарств, подобно тем, что используют для оценки функции почек, не существует.
Источник