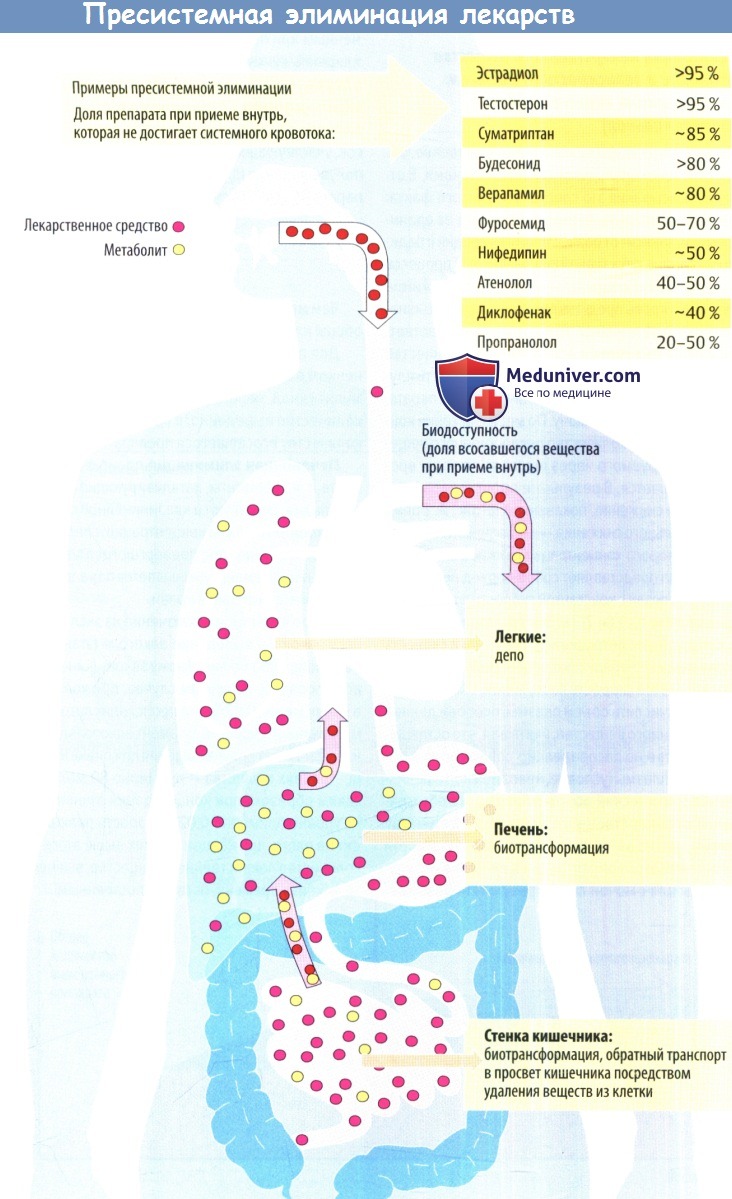
Системная элиминация лекарственных средств это
Морфологические барьеры организма проиллюстрированы в предыдущей статье на сайте. Физико-химические свойства лекарственного средства определяют, достигнет ли он цели, расположенной на поверхности или внутри клеток организма либо бактериальных клеток, и в какой степени.
В тех случаях, когда препарат принимается внутрь или вводится парентерально, фармакокинетические процессы идут совершенно иначе, чем при местном применении.
Это становится очевидным, если проследить путь принятого внутрь препарата, начинаяс места всасывания до попадания в кровоток. Возможен один из следующих вариантов развития событий.
1. Препарат проникает через эпителий кишечника в энтероциты, однако Р-гликопротеид транспортирует его обратно в просвет кишечника. Поэтому итоговое всосавшееся количество препарата может быть значительно меньше.
Этот «противотранспорт» различен у разных людей в отношении одного и того же вещества и, кроме того, подвержен влиянию других лекарственных средств.
2. На пути из просвета кишечника в общее циркуляторное русло принятый внутрь препарат расщепляется под воздействием ферментов, например цитохромоксидазы Р450.
(а) Разрушение может начаться уже в слизистой кишечника. Другие лекарственные средства или химические вещества могут подавлять или стимулировать активность изоферментов цитохрома в кишечнике.
Отдельный пример — сок грейпфрута, который подавляет активность оксидаз CYP3A4 в стенке кишечника и вызывает повышение в крови концентрации некоторых лекарственных средств до токсического уровня.
(б) Самую важную роль играет метаболизм в печени, которому подвергается любое лекарственное средство, попадающее в организм. В печени работает множество ферментов, химически преобразующих эндогенные и экзогенные вещества, чтобы обеспечить их выведение из организма. Только часть всосавшегося количества может попасть в кровь печеночной вены, это зависит от количества препарата, поглощенного и переработанного гепатоцитами.
Следует учитывать, что другие препараты могут вызывать повышение активности ферментов (увеличение гЭР).
Процессы, о которых говорится выше, объединены термином «пресистемная элиминация».
3. Парентеральное введение лекарственного вещества позволяет обойти пресистемную элиминацию. При в/в, п/к и в/м введении препарат проходит через полую вену, попадает в правый желудочек и, через легкие, в левый желудочек, далее — в системный кровоток.
Богатые жиром и имеющие большую поверхность легкие всасывают некоторое количество липофильных и амфифильных веществ, а затем медленно выделяют их после снижения концентрации в крови.
Во время быстрого поступления лекарственного средства в организм легкие играют роль буфера и защищают сердце от избыточной концентрации веществ после в/в введения.
В некоторых ситуациях желательна быстрая пресистемная элиминация. Яркий пример — назначение глюкокортикоидов при бронхиальной астме.
Поскольку большая часть ингалированного препарата обычно проглатывается, глюкокортикоиды с полной пресистемной элиминацией оказывают минимальную системную нагрузку на организм.
Использование клопидогрела для ингибирования агрегации тромбоцитов — пример желательной пресистемной активации.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Лекция 3 элиминация лекарственных средств
Элиминация (лат. elimimo, elimmatum — выносить за порог, удалять) представляет собой удаление лекарственных средств из организма в результате биотрансформации и экскреции.
Лекарственные средства элиминируются только из центральной камеры. Лекарства, находящиеся в периферической камере, предварительно транспортируются в центральную камеру, а затем подвергаются элиминации.
Элиминация лекарственных средств из плазмы крови происходит согласно экспоненциальной кинетике первого порядка — выводится постоянная часть от концентрации за единицу времени. При работе систем элиминации в условиях насыщения возникает кинетика нулевого порядка — выводится постоянное количество препарата за единицу времени.
Элиминацию лекарственных средств характеризует ряд фармакокинетических параметров:
• Константа скорости элиминации — часть от концентрации в крови, удаляемая за единицу времени (вычисляется в %);
• Период полуэлиминации — время, за которое концентрация в крови снижается наполовину (Т1/2);
• Клиренс (англ. clearance — очищение) — объем жидких сред организма, освобождающихся от лекарств в результате их биотрансформации, выведения с желчью и мочой (вычисляется в мл/мин’кг).
Различают печеночный (метаболический, желчный) и почечный клиренсы. Например, у циметидина — противогистаминного средства, применяемого для терапии язвенной болезни, почечный клиренс равен 600 мл/мин, метаболический — 200 мл/мин, желчный — 10 мл/мин. Клиренс зависит от состояния ферментных систем печени и итенсивности печеночного кровотока. Для элиминации препарата с быстрым метаболизмом в печени — местного анестетика лидокаина основное значение имеет печеночный кровоток, для элиминации антипсихоти-ческих средств группы фенотиазина — активность ферментных систем детокси-кации.
При повторном применении лекарственных средств в биофазе циторецепторов создается равновесное состояние, когда количество поступающего препарата равно количеству элиминируемого. При равновесном состоянии концентрация колеблется в небольших пределах, а фармакологические эффекты проявляются в полной мере. Чем короче период полуэлиминации, тем скорее достигается равновесная концентрация, и тем больше разница между максимальной и минимальной концентрациями. Обычно равновесное состояние наступает через 3-5 периодов полуэлиминации.
Биотрансформация лекарственных средств
Биотрансформация представляет собой метаболические превращения лекарственных средств. В большинстве реакций образуются метаболиты, более полярные, чем исходные лекарственные средства. Полярные метаболиты хуже растворяются в липидах, но обладают высокой растворимостью в воде, меньше подвергаются энтерогепатической циркуляции (выведение с желчью в кишечник и повторное всасывание в кровь) и реабсорбции в почечных канальцах. Без биотрансформации одна терапевтическая доза снотворного средства этаминала могла бы находиться в организме 100 лет.
Эндобиотики подвергаются превращениям под влиянием специфических ферментов, осуществляющих метаболизм их эндогенных аналогов. Ксенобиотики используют для метаболизма ферменты с малой субстратной специфичностью, например, окисляются при участии ци-тохрома Р-450, созданного в эволюции 3,5 миллиарда лет тому назад для инактивации стероидов.
Биотрансформация ксенобиотиков происходит в печени (90-95%), слизистой оболочке тонкого кишечника, почках, легких, коже, крови. Наиболее изучены процессы биотрансформации на мембранах гладкого эндоплазматического ретикулума (ЭПР) печени. При гомогенизации и ультрацентрифугировании клеток канальцы ЭПР разрываются и превращаются в функционально активные фрагменты — микросомы. Реакции биотрансформации протекают также в ядре, цитозоле, митохондриях, плазматической мембране.
Процессы биотрансформации разделяют на 2 фазы. В реакциях первой фазы — метаболической трансформации молекулы лекарственных средств подвергаются окислению, восстановлению или гидролизу. Большинство лекарств преобразуется в неактивные метаболиты, но также могут появляться активные и токсические производные (табл. 3.1). Во второй фазе — реакциях конъюгации лекарственные средства присоединяют ковалентной связью полярные фрагменты с образованием неактивных продуктов. Для реакций конъюгации необходима затрата энергии.
Активные метаболиты лекарственных средств
Источник
Элиминация лекарств
Элиминацией лекарств (лат.elimino– выносить за порог) – называют совокупность процессов метаболизма и выведения, которые способствуют удалению активной формы лекарства из организма и снижению его концентрации в плазме крови. Элиминация включает в себя 2 процесса: биотрансформацию (метаболизм) и экскрецию лекарств. Основными органами элиминации являются печень и почки. В печени элиминация протекает путем биотрансформации, а в почках – путем экскреции.
Биотрансформация лекарств. Несинтетические и синтетические реакции метаболизма.
Биотрансформацией (метаболизмом) называют изменение структуры лекарств в результате их химической модификации. Основная направленность процессов метаболизма – перевод лекарств в гидрофильную форму, которая лишена фармакологической активности и способна легко выводиться из организма.
Метаболизм лекарств включает 2 фазы:
I фаза – несинтетические реакции метаболизма.К этой фазе относят окисление, восстановление или гидролиз молекул лекарства. Основная направленность реакций этого типа – лишить ксенобиотик активности.
Восстановление.Реакции восстановления характерны для:
К
Нитроредукции ароматических соединений, содержащих нитрогруппу. Данный вид реакций протекает в печени и кишечнике. Таким образом происходит метаболизм метронидазола. R-NO2¦R-NH2
Гидролиз.Наиболее характерен для сложных эфиров и замещенных амидов. Протекает в стенке кишечника, печени и крови. Функцию гидролиза эфиров в крови чаще всего осуществляет фермент псевдохолинэстераза (бутирилхолинэстераза), который имеет низкую субстратную специфичность и может гидролизовать любую эфирную связь.
Путем гидролиза протекает метаболизм эналаприла, тестостерона пропионата (эфирный гидролиз), лидокаина (амидный гидролиз).
Окисление.Окисление биологических субстратов – универсальный механизм инактивации ксенобиотиков, который обеспечивают микросомальные ферменты печени. Это группа липофильных белков, сосредоточенная в мембранах эндоплазматического ретикулума гепатоцитов. Основой микросомальной системы ферментов являются 2 энзима: флавопротеин-НАДФ·Н-зависимая цитохром Р450редуктаза и гемопротеин цитохром Р450.
Схема 6. Цикл микросомального окисления. Пояснения в тексте. Л – лекарственное вещество.
Первоначально, окисленный Р450присоединяет лекарственное вещество. Затем, комплекс цитохром-лекарство восстанавливается НАДФ·Н-зависимой редуктазой и присоединяет кислород. Для активации молекулы кислорода НАДФ·Н-зависимая редуктаза повторяет цикл восстановления. На финальном этапе, один из атомов кислорода включается в молекулу воды, а второй – в лекарственное вещество, после чего цитохром регенерирует в исходное состояние.
Цитохром Р450является не 1 ферментом, а суперсемейством из более чем 300 изоформ, способных катализировать около 60 типов окислительных реакций, с сотнями потенциальных субстратов. Фактически, цитохромы способны обеспечить окисление не только всех существующих в настоящее время молекул лекарств, но и все лекарства, которые когда-либо еще будут синтезированы.
Молекулы цитохрома Р450, которые функционируют в клетках человека могут быть объединены в 17 семейств:CYP1-CYP17. Наибольшую роль в метаболизме лекарств играют первые 3 семействаCYP1-CYP3 (из них изоформыCYP3A4/3A5 иCYP2D6 метаболизируют 75% всех лекарств).
II фаза – синтетические реакции метаболизма.Как правило, эти реакции протекают только после того, как завершиться фазаI. Синтетические реакции метаболизма призваны повысить гидрофильность ксенобиотика. Все реакции этой группы могут быть разделены на 2 вида:
Реакции, в которых активируется конъюгирующее вещество:
Источник
Пресистемная элиминация
При приеме препарата внутрь, кроме биологических мембран, стоящих на пути из просвета кишечника в кровь, имеется еще один фактор, ограничивающий поступление лекарства в системный кровоток – печеночный метаболизм. Лекарственное вещество, поступая из ЖКТ по воротной вене в печень, может подвергнуться ферментативному разрушению, в связи с чем в системный кровоток попадает лишь часть (иногда незначительная часть) принятой дозы. Данный феномен носит название«эффект первого прохождения через печень». Так, некоторые лекарственные средства, обладая высокой абсорбцией, попадают в системный кровоток в очень небольшом количестве, не оказывающем терапевтического эффекта. Этот эффект характерен для быстро метаболизирующихся (см. фазу биотрансформации) средств и при значительной выраженности исключает возможность приема соответствующего препарата внутрь (например, антиаритмик лидокаин). В других случаях его можно корригировать увеличением дозы, которая оказывается значительно выше, чем при внутривенном введении (верапамил, морфин, пропранолол). Весьма демонстративным в этом плане является пример нитроглицерина. Эффект первого прохождения через печень у этого препарата достигает 85-97% дозы, что объясняет необходимость его назначения «в обход» печени (сублингвально или внутривенно) и делает бессмысленным нередко встречающееся назначение внутрь «капель Вотчала» (раствор нитроглицерина в ментоле).
Часть введенной дозы, достигшая системного кровотока, является важнейшей характеристикой препарата. Последняя обозначается как «биодоступность» и по определению ВОЗ понимается как степень и скорость, с которой вещество или его активная часть доставляется из лекарственной формы в системный кровоток. При внутривенном введении биодоступность принимается за 100%. При приеме внутрь она зависит от ряда факторов: устойчивости лекарства к действию соляной кислоты желудочного сока, активности разрушения препарата ферментами в просвете и стенке кишечника, выраженности эффекта первого прохождения через печень, то есть от потерь вследствие, так называемой,пресистемной элиминации.
Пресистемная элиминация зависит не только от препарата, но и от ряда факторов организма пациента и условий применения лекарства. На пресистемную элиминацию влияют взаимодействия с пищей и другими лекарственными средствами (см. гл. 9), скорость эвакуации из желудка, моторная функция кишечника, состояние функции печени и портального кровообращения. При нарушении функции печени (при циррозе), а также при развитии системы анастомозов между воротной веной и полыми венами (при портальной гипертензии) лекарственное средство попадает в системный кровоток, минуя печень. При этом снижается эффект первого прохождения через печень, что может вести к передозировке лекарства несмотря на назначение терапевтической дозы.
Кроме перечисленных факторов на биодоступность влияют еще и особенности технологии приготовления лекарственной формы. Поэтому биодоступность одного и того же активного вещества, выпускаемого в разных лекарственных формах или в лекарствах различных производителей, может колебаться в широких пределах. Однако такие колебания существенно затрудняют эффективное и безопасное дозирование лекарственных средств. В связи с этим перед регистрацией лекарства необходимо провести исследование биодоступности нового препарата в сравнении с эталонным лекарственным средством. В результате получается информация о сравнительной биодоступности или о биоэквивалентности.
Тут вы можете оставить комментарий к выбранному абзацу или сообщить об ошибке.
Источник



