- ИММУНОГЛОБУЛИН ЧЕЛОВЕКА ПРОТИВ КЛЕЩЕВОГО ЭНЦЕФАЛИТА
- Производители
- Инструкция по применению
- Состав
- Описание
- Фармакотерапевтическая группа
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Беременность и лактация
- Способы применения и дозы
- Побочные эффекты
- Передозировка
- Взаимодействие
- Особые указания
- Влияние на способность управлять трансп. ср. и мех.
- Условия хранения и срок годности
- Что такое иммуноглобулин? Анализ крови на антитела.
- 1. Что такое анализ крови на антитела?
- 2. Зачем это делается?
- 3. Как подготовиться и как проводится анализ?
- Как подготовиться к анализу на иммуноглобулин?
- Как проводится анализ крови на антитела?
- 4. Каковы риски и что может помешать анализу?
- Каковы риски анализа крови на антитела?
- Что может помешать анализу на иммуноглобулин?
- О чём стоит знать?
- Иммунная система человека
ИММУНОГЛОБУЛИН ЧЕЛОВЕКА ПРОТИВ КЛЕЩЕВОГО ЭНЦЕФАЛИТА
Лекарственная форма: Р-Р ДЛЯ В/М ВВЕД
Производители
Инструкция по применению
Состав
Активный компонент: иммуноглобулин человека в концентрации по белку от 100 до 160 мг /мл;
вспомогательные вещества: аминоуксусная кислота (глицин) от 15 до 30 мг /мл, вода для инъекций до 1 мл.
Описание
Прозрачная или слегка опалесцирующая жидкость, бесцветная или слабо желтой окраски. Допускается появление незначительного осадка, исчезающего при встряхивании.
Фармакотерапевтическая группа
Фармакодинамика
Иммунологически активное средство, получаемое путем фракционирования человеческой плазмы, содержащей антитела к вирусу клещевого энцефалита, проверенной индивидуально от каждого донора на отсутствие антител к ВИЧ-1, ВИЧ-2, к вирусу гепатита С и поверхностного антигена вируса гепатита В. Препарат повышает также неспецифическую резистентность организма.
Фармакокинетика
Максимальная концентрация антител в крови достигается через 24-48 часов после введения; период полувыведения антител из организма составляет 4-5 недель.
Показания
Препарат предназначен для экстренной профилактики и лечения клещевого энцефалита у взрослых и детей.
Противопоказания
Противопоказанием для применения иммуноглобулина являются тяжелые аллергические реакции в анамнезе на введение препаратов крови человека.
Лицам, страдающим аллергическими заболеваниями или имевшим в анамнезе клинически выраженные реакции на какие-либо аллергены (пищевые, лекарственные и др.), в день введения иммуноглобулина и в течение последующих 8 дней рекомендуется назначение антигистаминных средств.
Если у Вас одно из перечисленных заболеваний, перед применением препарата обязательно проконсультируйтесь с врачом.
Беременность и лактация
Исследования по влиянию иммуноглобулина на репродуктивную функцию не проводились, опыт применения у беременных женщин ограничен. Иммуноглобулин следует применять только при убедительных показаниях. Следует с осторожностью применять в период лактации (грудного вскармливания). Иммуноглобулины переходят в материнское молоко и могут способствовать передаче защитных антител новорожденным.
Способы применения и дозы
Вводят внутримышечно, в верхний наружный квадрант ягодичной мышцы или в наружную поверхность бедра. Запрещается вводить препарат внутривенно!
Перед инъекцией ампулу с препаратом выдерживают в течение 2 часов при комнатной температуре (20±2)°С. Вскрытие ампул и процедуру введения осуществляют при строгом соблюдении правил асептики и антисептики. Во избежание образования пены препарат набирают в шприц иглой с широким просветом.
Препарат во вскрытой ампуле хранению не подлежит.
Доза иммуноглобулина и кратность его введения зависят от показаний к применению.
Профилактика до укуса клеща
Препарат возможно применять перед вероятным контактом с вирусом клещевого энцефалита — укусом клеща в эндемическом районе (доэкспозиционная профилактика). Защитное действие проявляется через 24-48 часов и продолжается около 4 недель. Для сохранения иммунологической защиты в случае опасности заражения рекомендуется повторить введение иммуноглобулина через 4 недели.
С целью профилактики препарат вводят внутримышечно однократно из расчета 0,1 мл на 1 кг массы тела.
Таблица профилактических дозировок препарата иммуноглобулина против клещевого энцефалита
Объем инъекций, мл
Профилактика после укуса клеща
С целью экстренной профилактики препарат вводят в первую очередь непривитым против клещевого энцефалита или получившим неполный курс вакцинации, отмечавшим присасывание клещей в эндемических районах, а также при подозрении на лабораторное заражение вирусом клещевого энцефалита.
В случаях повышенного риска заражения (выявлено инфицирование присосавшегося клеща, многократные укусы или одновременное присасывание нескольких клещей) препарат вводят и привитым лицам. Детям до 12 лет — 1 мл; 12-16 лет — 2 мл; от 16 лет и старше — 3 мл.
В случае нового контакта с клещами возможно повторное применение препарата через один месяц после первого введения.
Во всех случаях препарат следует вводить в возможно более ранние сроки с момента предполагаемого заражения, не позднее 4 дней после укуса клеща.
С лечебной целью иммуноглобулин вводят в возможно более ранние сроки после начала заболевания в различных дозировках в зависимости от массы тела, клинической формы инфекции, тяжести течения и периода болезни.
— Больным со стертой и абортивной формами клещевого энцефалита (лихорадочные формы инфекции) иммуноглобулин вводят ежедневно в разовой дозе 0,1 мл/кг массы тела, на протяжении 3-5 дней до регресса общеинфекционных симптомов (улучшение общего состояния, исчезновение лихорадки). Курсовая средняя доза для взрослого составляет при этих формах не менее 21,0 мл препарата.
— При менингеальной форме клещевого энцефалита препарат применяется ежедневно в разовой дозе 0,1 мл/кг массы тела с интервалом 10-12 часов в течение не менее 5 дней до улучшения общего состояния пациента по объективным показателям (исчезновение лихорадки, регресс общеинфекционных симптомов, стабилизация и уменьшение менингеальных симптомов). Курсовая средняя доза иммуноглобулина для взрослого составляет при менингеальной форме инфекции не менее 70,0 мл.
— Больным с очаговыми формами клещевого энцефалита в зависимости от тяжести течения заболевания препарат вводят ежедневно в разовой дозе 0,1 мл/кг массы тела с интервалом 8-12 часов на протяжении не менее 5-6 дней до снижения температуры и стабилизации неврологических симптомов. Курсовая средняя доза для взрослого пациента составляет в среднем не менее 80,0-130,0 мл иммуноглобулина.
При крайне тяжелом течении заболевания разовая доза препарата может быть увеличена до 0,15 мл/кг массы тела.
Если больным менингеальной и очаговой формами клещевого энцефалита по каким-либо причинам в лихорадочной стадии заболевания специфическая терапия не проводилась, возможно введение иммуноглобулина и на стадии апирексии острого периода болезни с лечебной целью на протяжении 5-6 дней в разовой дозе 0,1 мл/кг массы тела через 10-12 часов.
В случае двухволнового течения клещевого энцефалита препарат применяют повторно по схеме лечения менингеальной или очаговой форм в зависимости от характера клинических проявлений.
Побочные эффекты
Если при использовании препарата соблюдены все рекомендации по введению, дозировке и меры предосторожности, реакции на введение иммуноглобулина, как правило, отсутствуют.
В редких случаях может появиться гиперемия в месте введения и повышение температуры до 37 °С в течение первых суток после введения.
У отдельных лиц с измененной реактивностью могут развиться аллергические реакции различного типа, в исключительных случаях — анафилактический шок, в связи с чем лица, получившие препарат, должны находиться под медицинским наблюдением в течение 30 минут. В помещении, где вводят препарат, должны иметься средства противошоковой терапии.
Передозировка
В настоящее время о случаях передозировки препарата не сообщалось.
Взаимодействие
Препарат можно использовать в комплексе с любыми другими лекарственными средствами при условии введения его в виде отдельной инъекции, не смешивая с другими препаратами.
Особые указания
Лечение препаратами иммуноглобулина снижает эффективность вакцинации, поэтому прививки проводят не ранее, чем через 2-3 месяца после введения иммуноглобулина.
Лицам, страдающим аллергическими заболеваниями или склонным к аллергическим реакциям, в день введения иммуноглобулина и в течение последующих 8 дней рекомендуется назначение антигистаминных препаратов. В период обострения аллергического процесса введение препарата осуществляется по заключению аллерголога.
При развитии анафилактоидных реакций применяют антигистаминные препараты, глюкокортикостероиды и адреномиметики.
Лицам, страдающим аутоиммунными заболеваниями (болезни крови, соединительной ткани, нефрит и другие) препарат следует вводить на фоне соответствующей терапии.
Иммуноглобулины для внутримышечного введения категорически запрещено вводить внутривенно.
Не пригоден к применению препарат в ампулах с нарушенной целостностью и маркировкой, при изменении физических свойств (мутность, интенсивное окрашивание, наличие не разбивающихся при встряхивании хлопьев).
Влияние на способность управлять трансп. ср. и мех.
Не выявлено влияние иммуноглобулина на способность к выполнению работы, требующей повышенного внимания и быстроты психомоторных реакций.
Условия хранения и срок годности
В сухом защищенном от света месте при температуре от 2 до 10 °С. Не замораживать.
Хранить в недоступном для детей месте.
Транспортировать любым видом крытого транспорта при температуре от 2 до 10 °С.
Не использовать по истечении срока годности, указанного на упаковке.
Источник
Что такое иммуноглобулин? Анализ крови на антитела.
- УЗИ
- Функциональная диагностика
- Рентген методы
- Эндоскопические методы
1. Что такое анализ крови на антитела?
Анализ крови на иммуноглобулин измеряет содержание иммуноглобулина в крови. Иммуноглобулин – это особые антитела в крови. Иммуноглобулин появляется в ответ на бактерии, вирусы, грибок и раковые клетки. Антитела прикрепляются к инородным субстанциям, чтобы иммунная система могла их уничтожить.
Антитела различны для каждой субстанции. Например, иммуноглобулин против туберкулёза может прикрепиться только к бактерии туберкулёза. Антитела также образуются в результате аллергической реакции. В редких случаях антитела начинают вырабатываться против тканей самого организма. Это явление называется аутоиммунным заболеванием.
Если в вашей крови низкий уровень антител, то у болезней больше шанса на рецидив. У некоторых слабая иммунная система с рождения, у некоторых она становится такой в результате заболеваний, например, рака.
Существуют пять основных типов антител в крови:
IgA. IgA антитела находятся в таких областях организма, как дыхательная система, пищеварительный тракт, уши, глаза и влагалище. IgA антитела также находятся в слюне, слёзах и крови. IgA антитела защищают поверхности организма, которые подвергаются внешнему воздействию. От 10% до 15% всех антител в организме принадлежат к этому типу.
IgG. IgG антитела находятся во всех жидкостях организма. Это самые маленькие, но самые распространённые антитела (75%-80%). IgG антитела очень важны для борьбы с бактериальными и вирусными инфекциями. IgG антитела – это единственные антитела, которые могут проникнуть сквозь плаценту и защитить плод.
IgM. IgM антитела – это самые большие антитела. Они находятся в крови и лимфе. IgM антитела – первые антитела, которые появляются в ответ на инфекцию. IgM антитела составляют 5%-10% от всех антител.
IgE. IgE антитела находятся в лёгких, коже и слизистых оболочках. IgE антитела заставляют организм реагировать на инородные вещества: пыльца, споры, перхоть животных. IgE антитела являются причиной аллергических реакций на молоко, некоторые лекарства и ядовитые вещества. IgE антитела имеют большую концентрацию в крови людей, подверженных аллергии.
IgD. IgD антитела содержаться в тканях живота и груди. Как они работают неизвестно.
Процентное содержание каждого антитела может дать информацию доктору о проблемах со здоровьем.
2. Зачем это делается?
Анализ крови на иммуноглобулин делается для того, чтобы:
- Найти определённую аллергию или аутоиммунное заболевание;
- Найти определённые типы рака (множественная миелома или макроглобулинемия);
- Определить, является ли рецидив болезней результатом низкого уровня иммуноглобулина;
- Проверить ход лечения рака костного мозга;
- Проверить ход лечения от бактерии helicobacter pylori;
- Проверить процесс иммунизации;
- Проверить, есть ли у вас инфекция и была ли она ранее.
Анализ на иммуноглобулин проводится тогда, когда результаты анализа на электрофорез или общий белок крови аномальные.
3. Как подготовиться и как проводится анализ?
Как подготовиться к анализу на иммуноглобулин?
Подготовка к анализу на иммуноглобулин не требуется.
Как проводится анализ крови на антитела?
Анализ на антитела проводится после взятия крови из вены. Забор крови проводится по стандартной процедуре.
4. Каковы риски и что может помешать анализу?
Каковы риски анализа крови на антитела?
Если вы сдаёте анализ крови на антитела, то возможные риски могут быть связаны только с забором крови. В частности, появление синяков на месте забора крови и воспаление вены или артерии (флебит). Тёплые компрессы по нескольку раз в день избавят вас от флебита. Если вы принимаете разжижающие кровь препараты, то возможно кровотечение в месте пункции.
Что может помешать анализу на иммуноглобулин?
Анализ крови на иммуноглобулин может быть бесполезным по следующим причинам:
- Приём определённых лекарств. Сообщите доктору обо всех препаратах, которые вы принимаете;
- Лечения рака химиотерапией или лучевой терапией;
- Переливание крови полгода назад или менее;
- Вакцинация, особенно повторная;
- Алкогольная или иная интоксикация;
- Осмотр с использованием радиации за три дня до теста.
О чём стоит знать?
Анализ на иммуноглобулин используется для диагностики заболеваний, определения их степени, перед переливанием крови и по многим другим причинам. Поэтому одновременно может проводиться тест на определение разных типов иммуноглобулина.
Источник
Иммунная система человека
к.м.н. Гольдинберг Б. М., Васюк Я.В.
Городской центр трансфузиологии учреждения здравоохранения «6-я городская клиническая больница», г. Минск,
учреждение здравоохранения «7-я городская детская поликлиника», г. Минск
ИММУНННАЯ СИСТЕМА ЧЕЛОВЕКА
Введение
Группа органов, имеющих общее происхождение, единый план строения и выполняющая общую функцию называется системой органов. Пять из всех десяти систем органов являются регулирующими (управляющими): нервная, кровеносная, эндокринная, лимфатическая и иммунная. Уточним, что лимфатические органы и лимфатических узлы, которых насчитывается около 600, функционально является частью иммунной системы, а к собственно лимфатической системе относится обширная сеть сосудов, которая проходит почти через все наши ткани, обеспечивая движение жидкости, называемой лимфой.
Слово «иммунитет» происходит от латинского «immunis» (на английском – immunity), что означает «чистый от чего-либо», невосприимчивый к чему-либо. Иммунная система появилась вместе с многоклеточными организмами и развивалась, как помощница их выживанию. Она объединяет органы и ткани, которые гарантируют защиту организма от генетически чужеродных клеток и веществ, поступающих из окружающей среды.
Иммунная система представлена тремя уровнями: органным, клеточным и молекулярным.
Органы иммунной системы человека
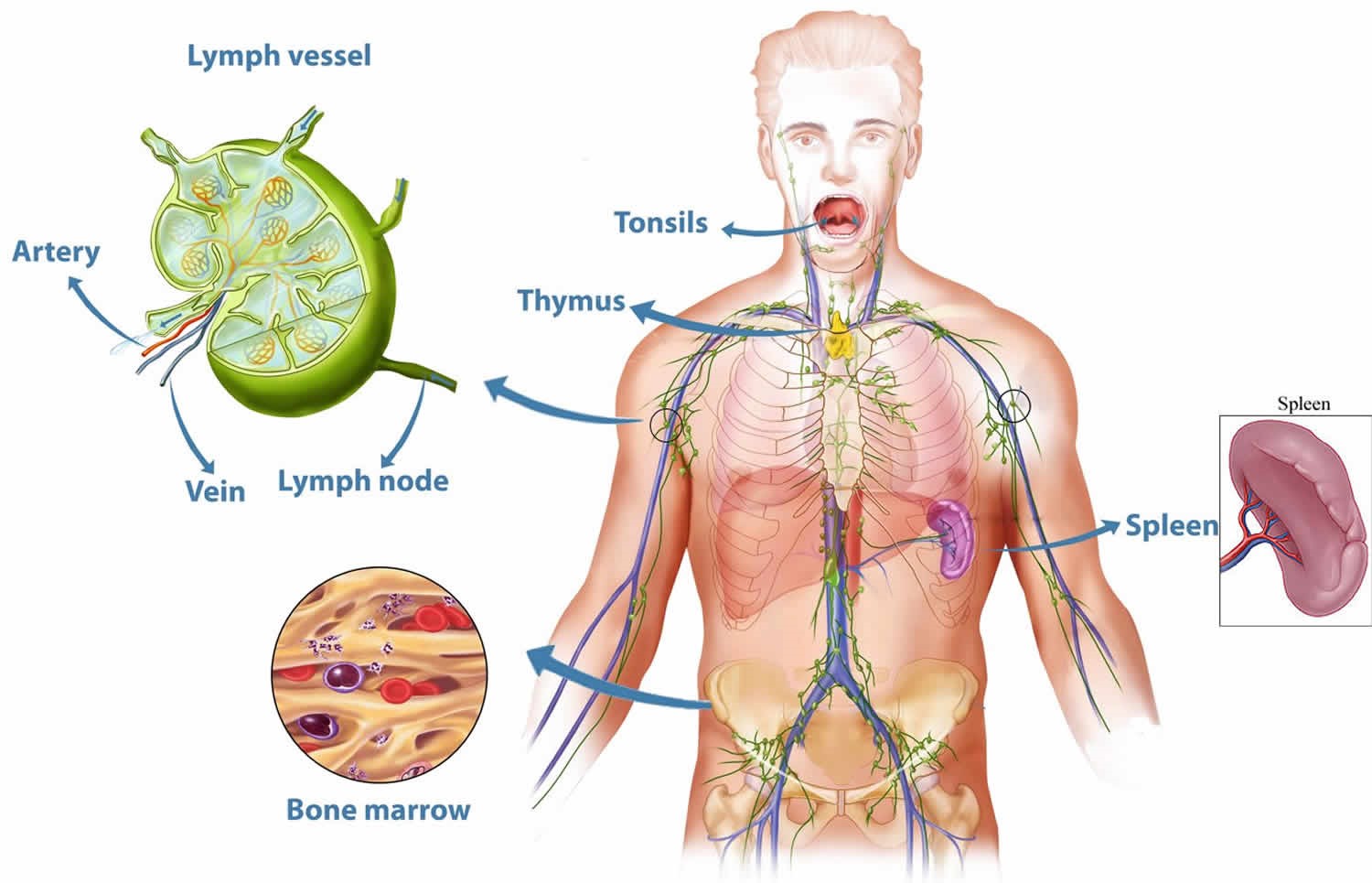
Иммунная система включает центральные и периферические органы.
Центральные органы иммунной системы представляют собой красный костный мозг и тимус.
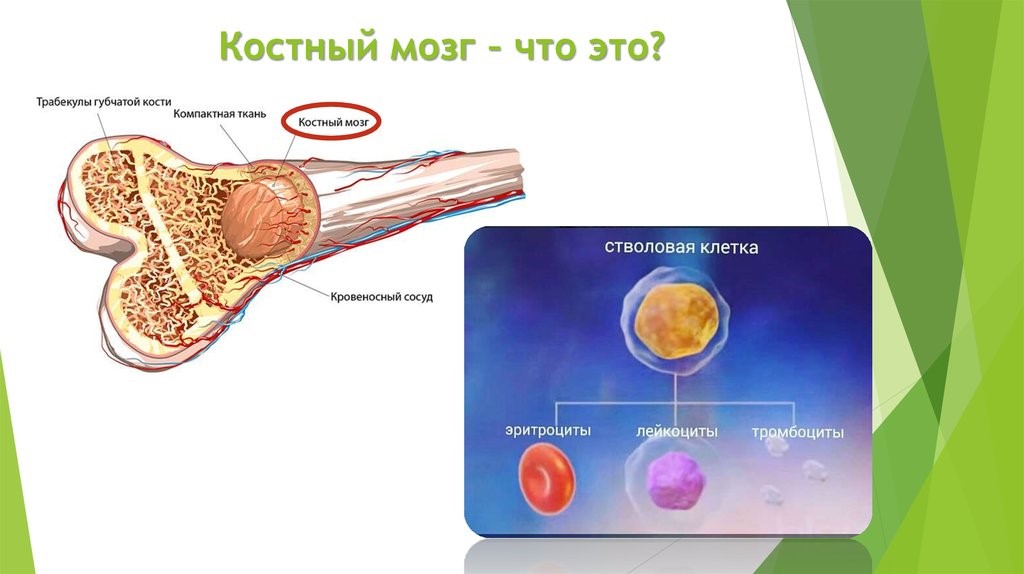
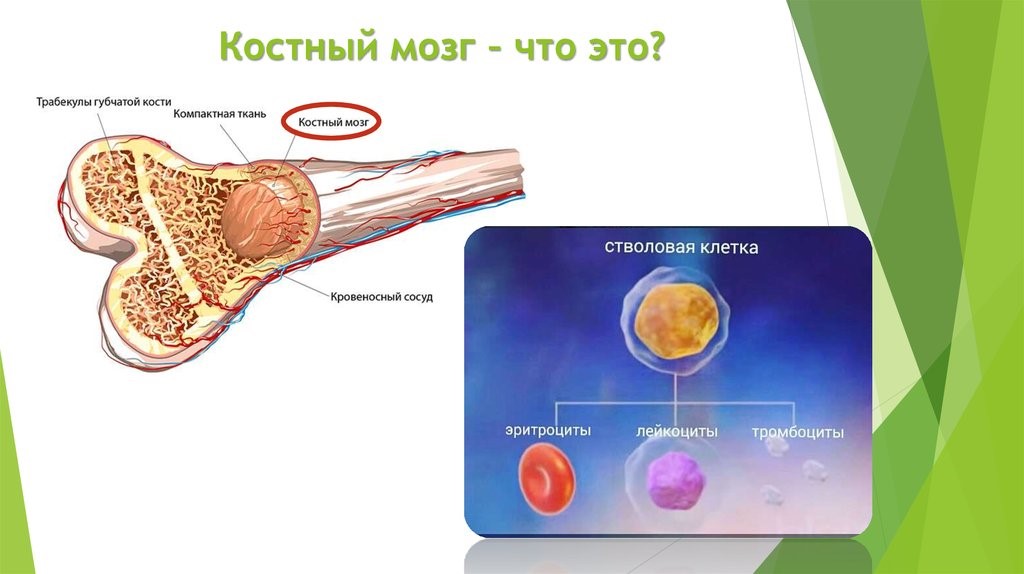
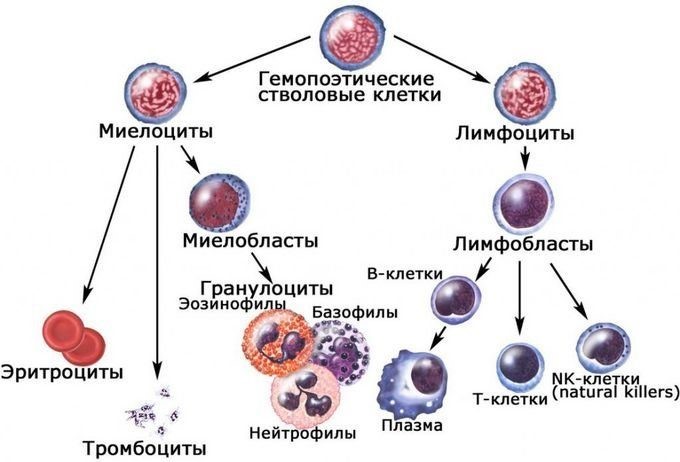
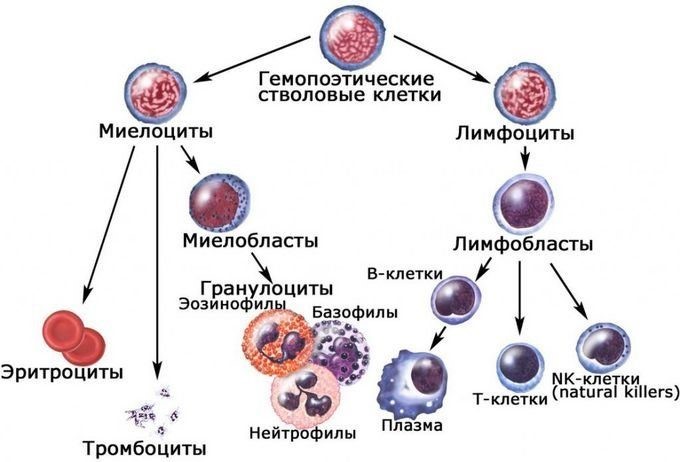
Костный мозг является хранилищем стволовых клеток, из которых образуются клетки крови (рис.1). В зависимости от ситуации, стволовые клетки трансформируются в иммунные В-лимфоциты. При необходимости, определенная часть B-лимфоцитов превращается в плазматические клетки, которые способны вырабатывать антитела.
Рис.1. Костный мозг содержит стволовые клетки
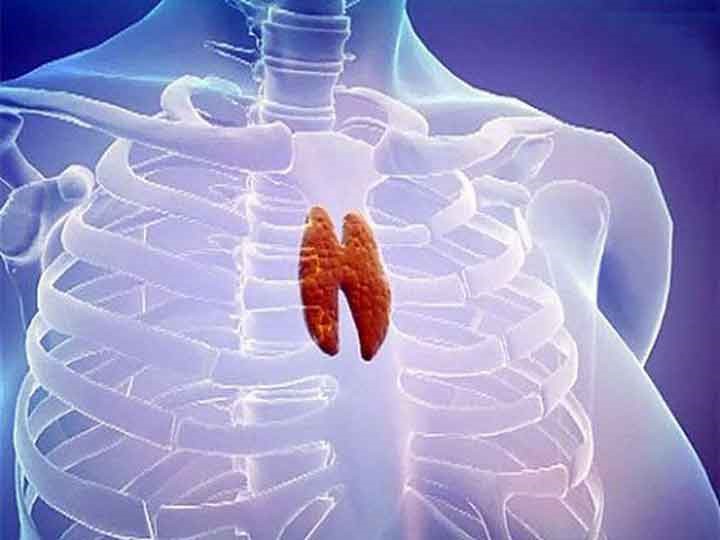
Тимус (или вилочковая железа) – один из главных органов иммунной системы, расположенный у человека за грудиной ниже ключиц, который отвечает за образование Т-клеток иммунной системы в лимфоидных тканях организма (рис.2).
К периферическим органам относятся селезенка, миндалины и лимфоузлы, в которых находятся зоны созревания иммунных клеток.
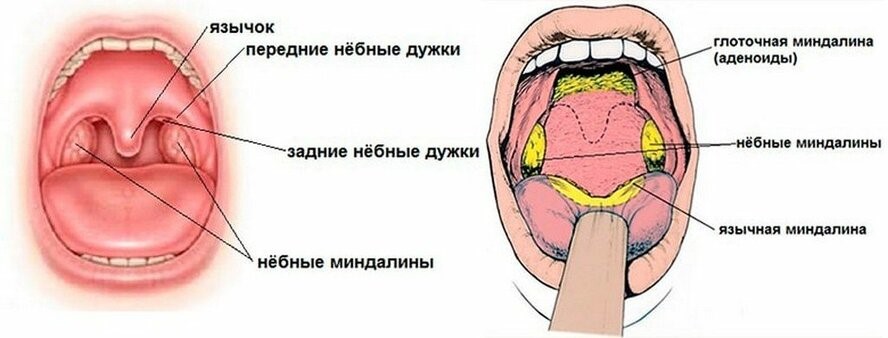
Миндалины, получившие свое название из-за внешней схожести с миндалем, представляют собой скопление лимфоидной ткани в верхней части носоглотки. У человека шесть миндалин: две небные, две грудные и по одной носоглоточной и язычной.
Самыми крупными из них являются небные миндалины, или гланды, которых легко осмотреть самостоятельно в зеркале, если достаточно широко раскрыть рот (рис.3).
Рис. 3. Небные миндалины
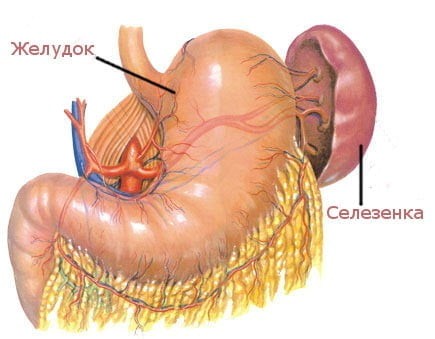
Селезенка является самым крупным лимфоидным органом (рис. 4). Кроме того, она может накапливать некоторое количество крови. В экстренных ситуациях селезенка способна послать свои запасы в общий кровоток. Это позволяет улучшить качество и скорость иммунных реакций организма. Селезенка очищает кровь от бактерий и перерабатывает всевозможные вредные вещества. В ней полностью разрушаются эндотоксины, а также остатки умерших клеток при ожогах, травмах или других повреждениях тканей. У людей, оставшихся по какой-либо причине без селезенки, ухудшается иммунитет.
Рис. 4. Селезенка
Лимфатические узлы представляют собой небольшие образования округлой формы (рис. 5), расположенные в грудной полости (бронхолегочные, бронхотрахеальные) и брюшной полости (пейеровы бляшки, аппендикс и другие), окологрудные на поверхности грудной клетки, на шее и на конечностях. Лимфоузел – это один из барьеров на пути инфекций и раковых клеток, играющий роль своеобразной таможни (рис. 5). В нем образуются лимфоциты – специальные клетки, которые принимают активное участие в уничтожении вредных веществ.
Рис. 5. Лимфоузел
Центральные органы иммунной системы отвечают за образование и созревание клеток, а периферические органы обеспечивают защиту, то есть иммунный ответ. Периферические и центральные органы иммунной системы выполняют свои работу только вместе и если выходит из строя какой-либо один из этих органов, то организм лишится защитного барьера.
Компоненты иммунной системы
Современная иммунология различает два взаимодействующих компонента иммунной системы – врожденный и приобретенный виды иммунитета, обеспечивающие развитие иммунного ответа на генетически чужеродные субстанции (сущности).
Врожденный (видовой) иммунитет – наследственно закрепленная система защиты организма человека от патогенных и непатогенных микроорганизмов, а также продуктов тканевого распада. Клетки врожденного иммунитета распознают патоген по специфичным для него молекулярным маркёрам – так называемым «образам патогенности». Эти маркёры не позволяют точно определить принадлежность патогена к тому или иному виду, а лишь сигнализируют о том, что иммунитет столкнулся с возмутителями спокойствия: чужаком или своим, но ставшим для организма предателем (рис.6).
Рис.6. Врожденный иммунитет: главное – спокойствие!
Врожденный иммунитет на клеточном уровне представляют:
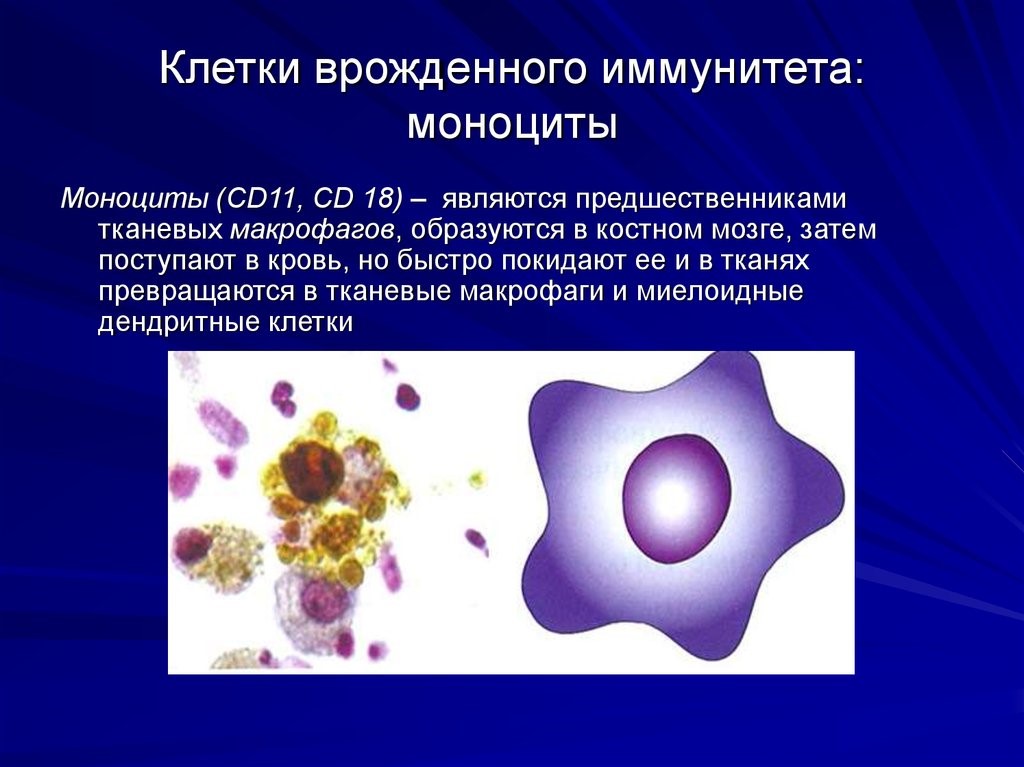
- моноциты – предшественники макрофагов (клетки, пожирающие чужеродные частицы). Образуются в костном мозге, затем поступают в кровь, но быстро ее покидают, превращаясь в тканевые макрофаги и дендритные клетки (рис. 7);
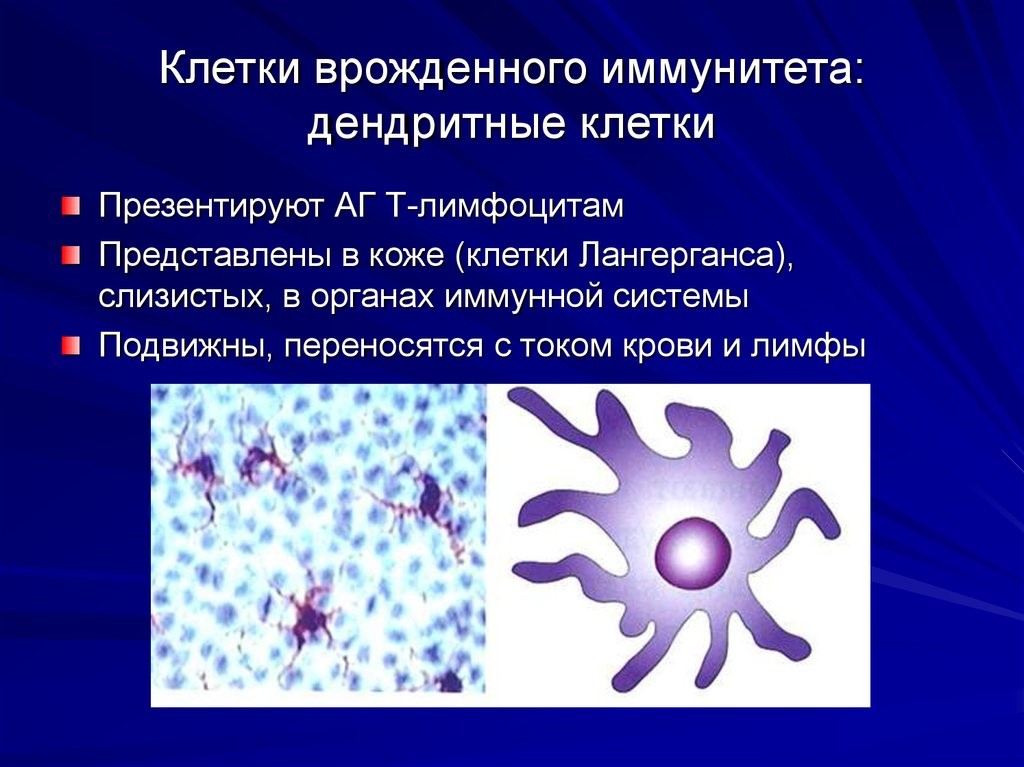
- макрофаги и дендритные клетки расположены в коже, слизистых. Обладают подвижностью, переносятся с током крови и лимфы. Они поглощают (фагоцитируют) патоген, и уже внутри себя при помощи содержимого вакуолей растворяют его. Дендритные клетки ветвятся подобно дереву. Благодаря ветвям-антеннам они работают связистами между врожденным и приобретенным видами иммунитета(рис.8);
Рис.8. Дендритная клетка и
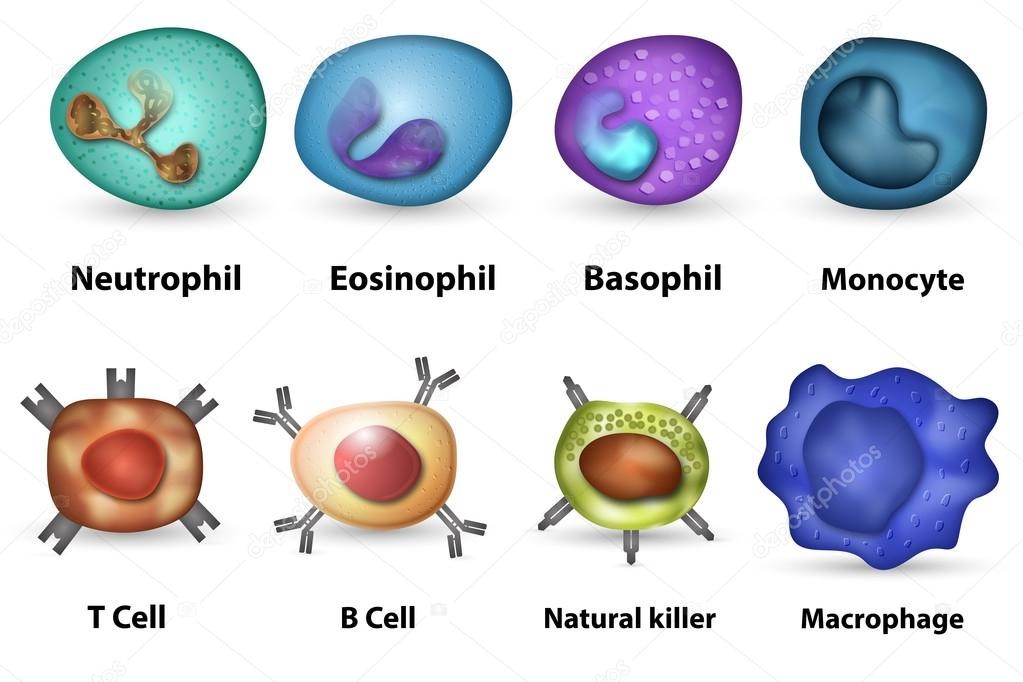
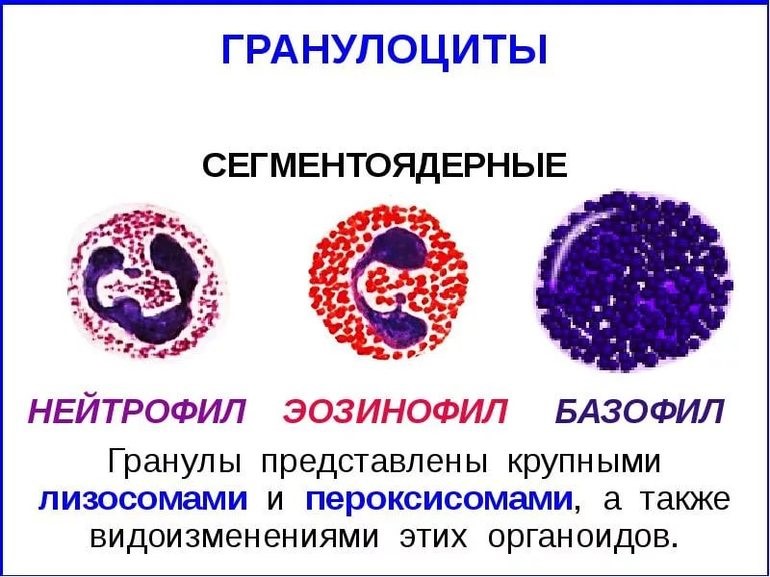
- клетки крови, содержащие в цитоплазме гранулы (гранулоциты): нейтрофилы, эозинофилы и базофилы (рис.9);
Нейтрофилы – самые многочисленные иммунные клетки в крови человека. Они циркулируют в крови всего 8-10 часов и бόльшую часть своей жизни путешествуют по тканям организма. При встрече с патогеном они его захватывают и переваривают, после чего обычно сами погибают. Из разрушенных нейтрофилов высвобождаются гранулы, содержащие антибиотические вещества.
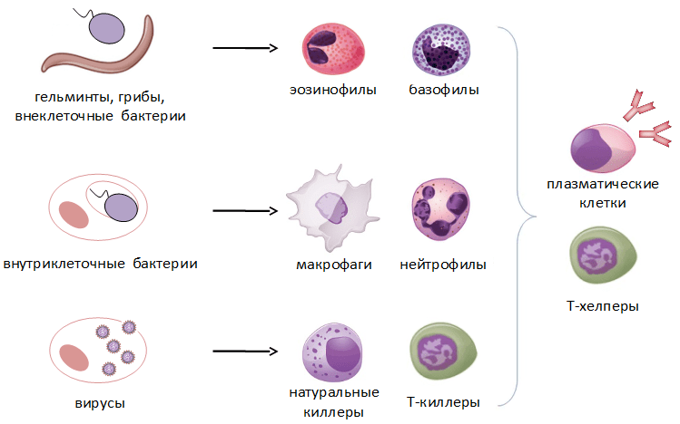
Гранулы эозинофилов и базофилов осуществляют химическую защиту организма от крупных патогенов, например, паразитических червей, грибов, внеклеточных бактерий. Однако при чрезмерной активности могут участвовать и в развитии аллергической реакции;
- натуральные (естественные) киллеры или NK-клетки (англ. Natural killer cells, NK cells) – тип цитотоксическихлимфоцитов, участвующий в функционировании врождённого иммунитета. Они на высокой скорости уничтожают клетки, инфицированные бактериями и вирусами, а также опухолевые клетки.
Рис.10. Натуральный киллер
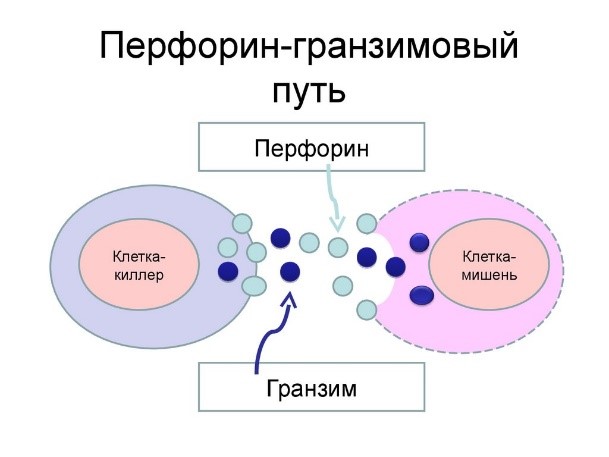
Действуют натуральные киллеры с помощью агрессивных веществ перфорина и гранзима, которые наподобие буравчиков «кусают» и разрушают пораженную клетку, ставшую для них мишенью (рис.11)
Рис.11. Проникновение перфорина и гранзима в раковую клетку и ее уничтожение
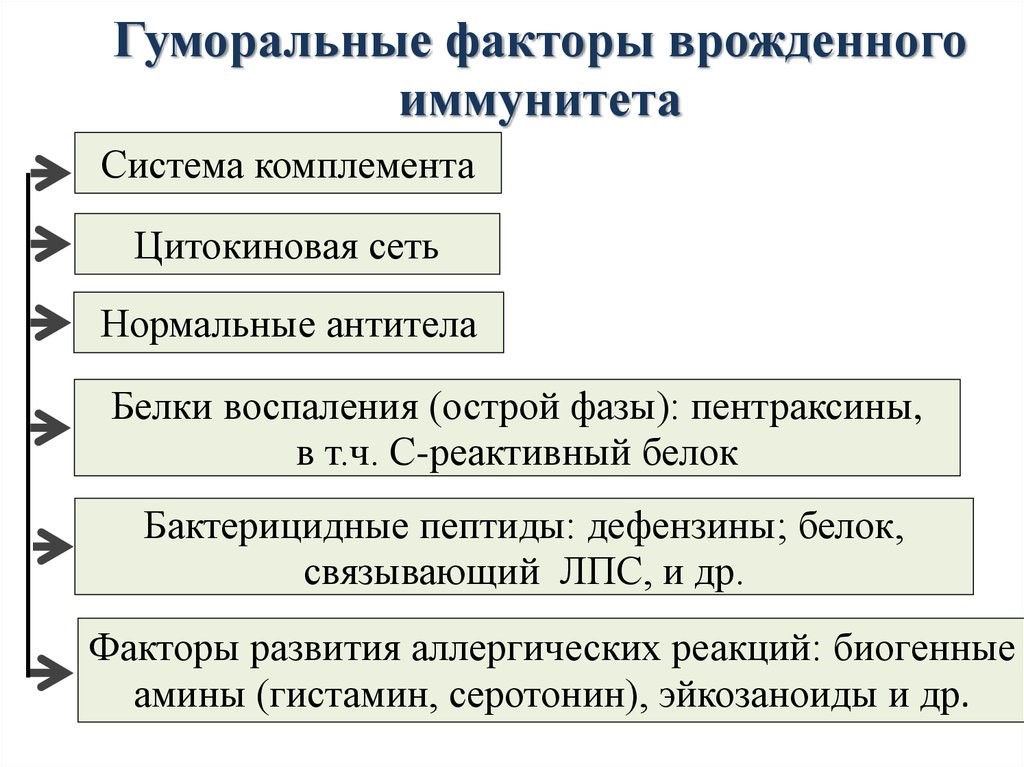
Молекулярными(гуморальные) факторами врожденного иммунитета являются (рис.12):
- белки, связывающие ионы металлов (железа, цинка), необходимых для жизнедеятельности и размножения патогенов – лактоферрин, кальпротектин, мембранный белок и другие;
- ферменты, генерирующие окислители – кислород и оксид азота:
- ферменты, способные расщеплять клеточную мембрану патогенов – лизоцим, хитиназа, фосфолипаза А2;
- белки и пептиды, нарушающие целостность клеточной оболочки микроорганизма – комплемент, эозинофильный протеин, дефензины и другие.
Рис.12.Гуморальные факторы врожденного иммунитета
Система комплемента – это многокомпонентная самособирающаяся система более 20 сывороточных белков, которые в норме находятся в неактивном состоянии.
После активации проявляются биологические эффекты комплемента: образование мембраноатакающего комплекса для лизиса патогенов, выброса медиаторов воспаления для привлечения фагоцитов и усиления их поглотительной способности.
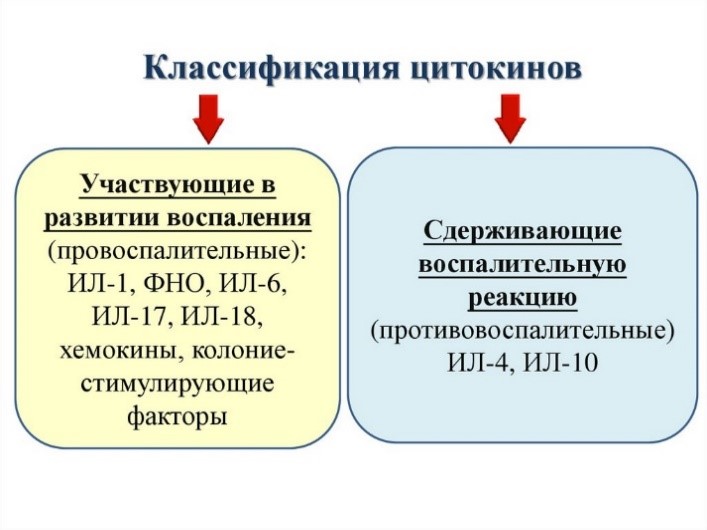
Цитокины – это система низкомолекулярных белков организма, синтезируемых преимущественно активными клетками иммунной и кроветворной систем, регулирующих межклеточные взаимодействия «универсальный» язык для всех клеток), представленные на рис.13 и 14.
Рис. 13. Цитокины: ИЛ – интерлейкины, которых в настоящее время насчитывается 34 разновидности;
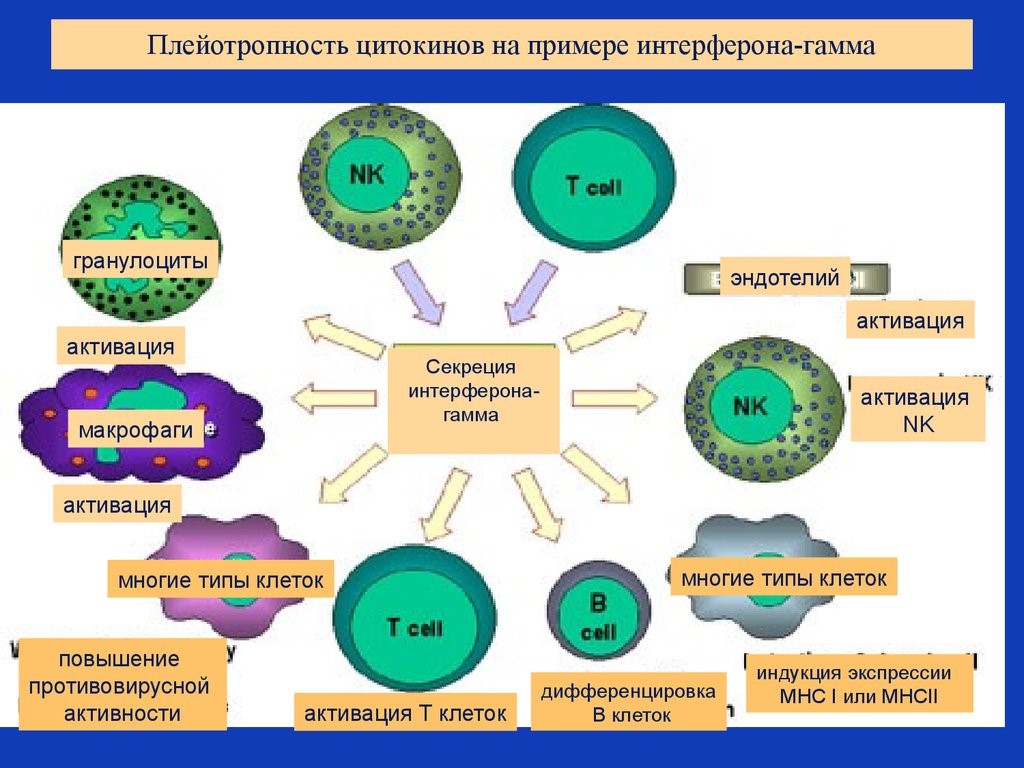
Рис. 14. Разнонаправленность действия цитокинов на примере гамма-интерферона
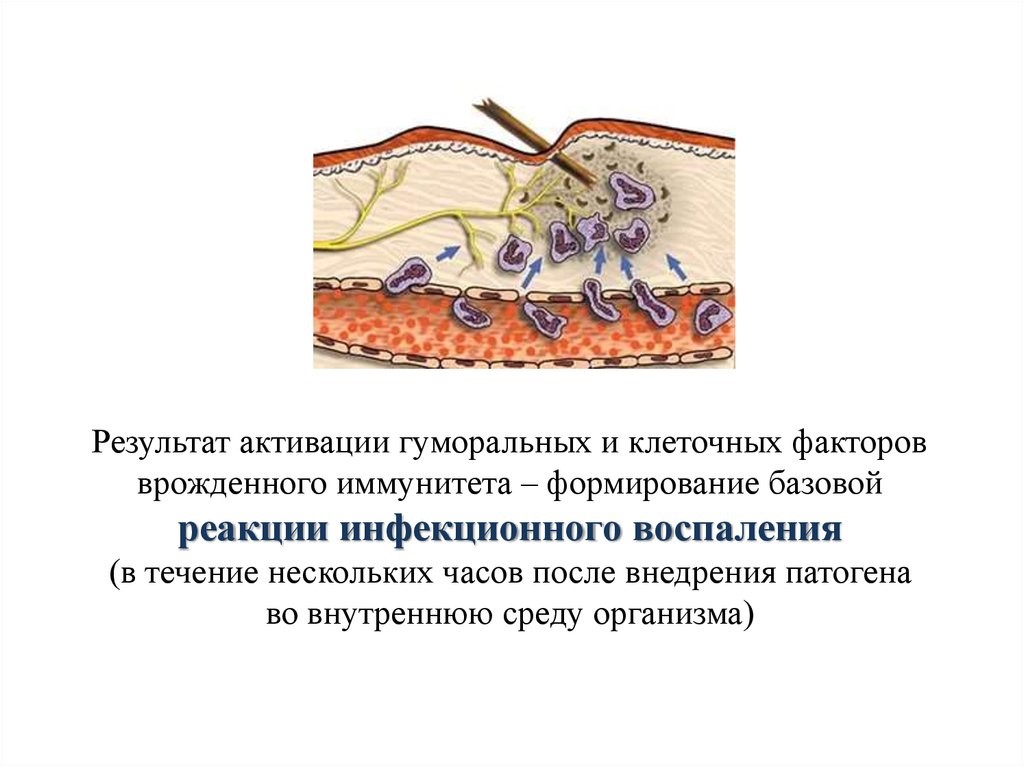
В результате активации гуморальных и клеточных факторов врожденного иммунитета в течение нескольких часов после внедрения патогена во внутреннюю среду организма формируется базовая реакция инфекционного воспаления (рис. 15)
Рис. 15. Инфекционное воспаление ткани на месте внедрения инородного тела с целью его удаления
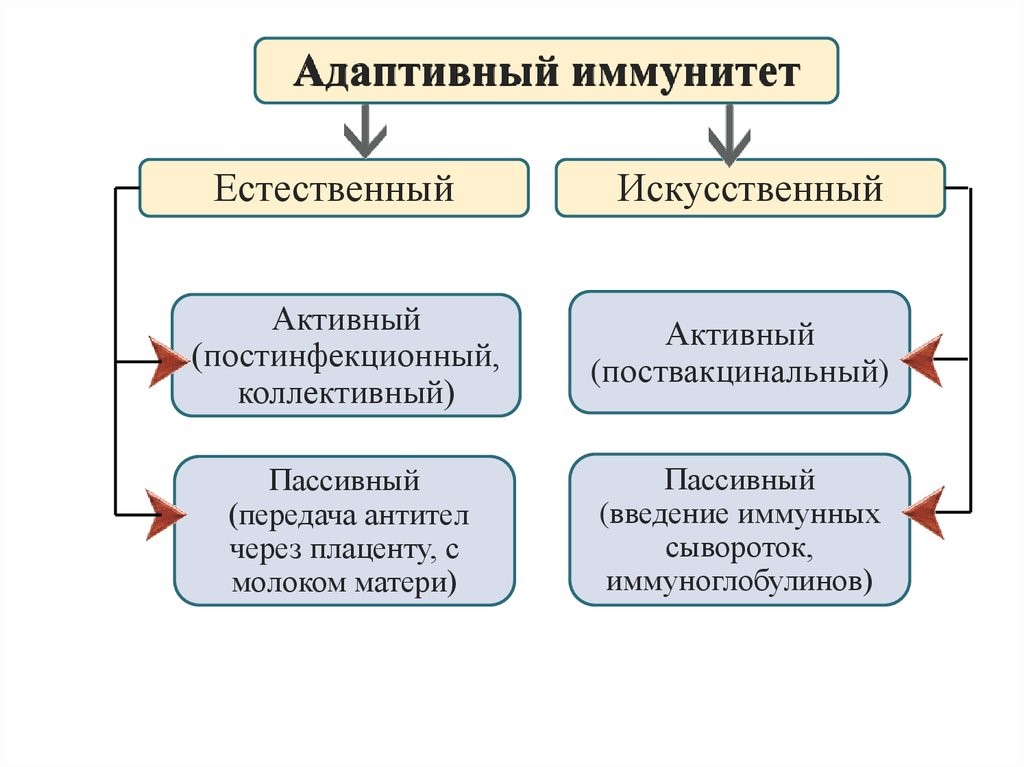
Приобретенный иммунитет (или адаптивный – от франц. adapter «приспосабливать») формируется индивидуально в течение жизни под влиянием антигенной стимуляции и, в свою очередь, подразделяется на естественный и искусственный (рис.16).
Естественный иммунитет формируется при встрече с патогеном, в результате чего в организме вырабатываются защитные иммунные факторы (активный естественный иммунитет), либо они попадают в готовом виде из материнского оргазма в период внутриутробного развития или при грудном вскармливании (пассивный естественный иммунитет).
Искусственный иммунитет создается путем введения вакцин или анатоксинов, которые стимулируют выработку антител против конкретных патогенов или их ядов. При этом с профилактической целью воспроизводится процесс реакции иммунной системы пациента на патоген, но в бессимптомной или легкой клинической форме с сохранением их защитной иммунной силы в течение нескольких месяцев, лет или даже пожизненно (искусственный активный иммунитет). Когда необходимо быстро и на короткое время защитить пациента от реального риска встречи с патогеном во время эпидемии или нейтрализовать уже проникший в его организм патоген применяются иммуноглобулины (антитела) как в очищенном виде, так и в дозированных объемах плазмы или сыворотки, полученных из крови донора (человека или животного). Применение готовых антител формирует пассивный искусственный иммунитет, сохраняющийся 2-3 недели.
Адаптивный иммунитет основывается на трех главных процессах:
- распознавание антигенов (как правило чужеродных для организма) с помощью рецепторов;
- удаление (элиминация) распознанных чужеродных агентов (рис. 17);
- формирование иммунологической памяти о контакте с антигеном, позволяющей быстрее и эффективнее удалять этот антиген при повторном его распознавании.
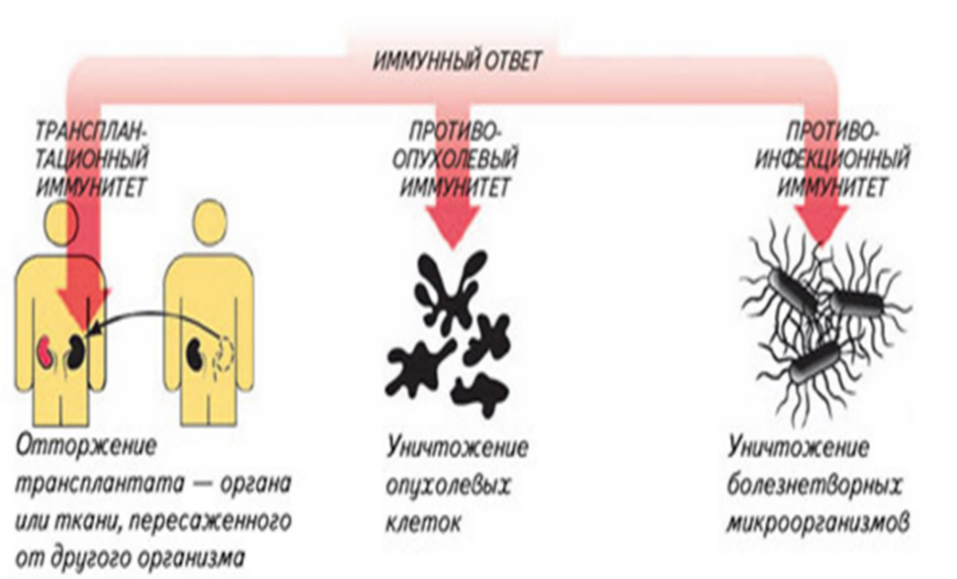
Рис.17.Варианты реагирования иммунной системы на пересадку органов или тканей, возникновение злокачественных новообразований и инфекций
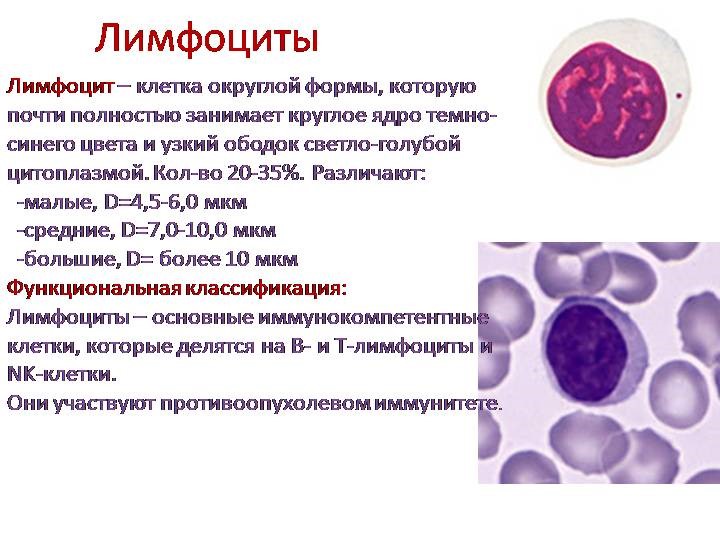
Иммунокомпетентными клетками адаптивного иммунитета являются лимфоциты, которые живут в организме человека от нескольких месяцев до несколько лет. По функциям клетки подразделяются на Т-лимфоциты – 80% и В-лимфоциты – 20%.
То, что Т-лимфоцит распознает только чужеродные антигены, а не молекулы собственного организма, является следствием процесса, называемого селекцией, которая происходит в тимусе, где завершают свое развитие Т-клетки. Суть селекции такова: клетки, окружающие юный, или наивный, лимфоцит, показывают (презентируют) ему пептиды собственных белков. Тот лимфоцит, который слишком хорошо или слишком плохо узнает эти белковые фрагменты, уничтожается. Выжившие же клетки (а это менее 1% всех предшественников Т-лимфоцитов, пришедших в тимус) обладают промежуточным сродством к антигену, следовательно, они, как правило, не считают собственные клетки мишенями для атаки, но имеют возможность среагировать на подходящий чужеродный пептид.
Для активации Т-лимфоцита нужно, чтобы он получил специальные сигналы от рецепторов лейкоцитарной антигенной системы и коктейля из множества провоспалительных цитокинов.
С помощью специальных реагентов определяются маркеры поверхностных белков лейкоцитов определенного типа, которые называются кластерами дифференциации (Сluster of differentiation) – CD. В настоящее время известно 350 CD-антигенов и их подтипов (табл. 1).
Таблица 1. Главные идентификациионные СD-маркёры клеток
Лимфоидная стволовая клетка
CD19, CD72, CD79 и др.
Т-лимфоциты распознают клетки, несущие чужеродные антигены, и уничтожают их после непосредственного контакта (атаки), а также выполняют функцию регуляции иммунного ответа.
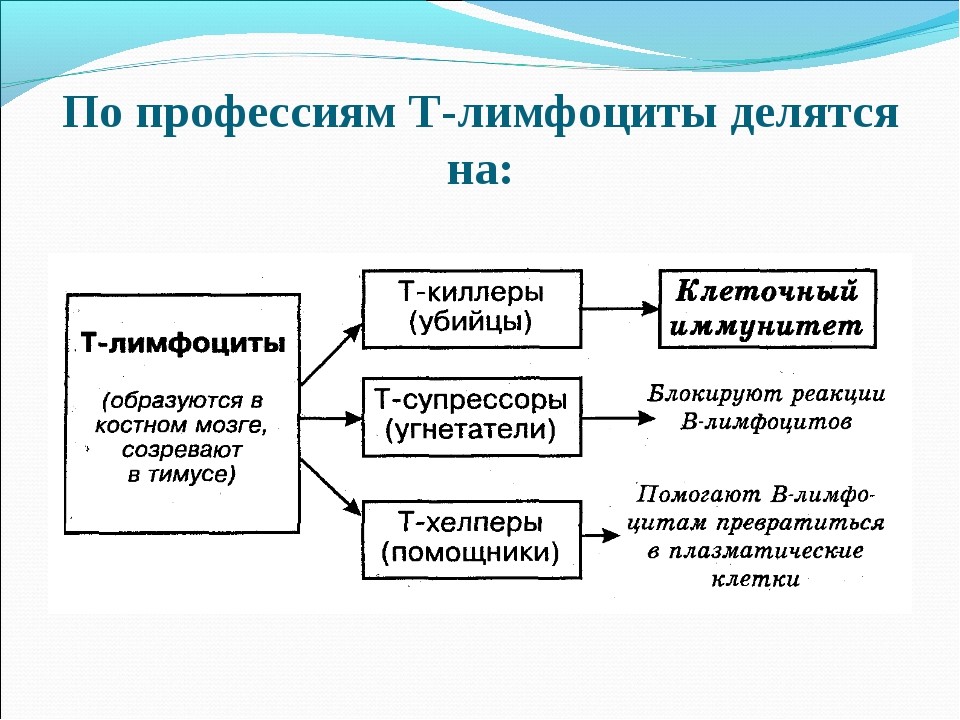
Т-лимфоциты имеют подтипы (рис. 18):
Рис. 18. Подтипы Т-лимфоцитов и их функции
- Т-киллеры (их еще называют CD8+ Т-лимфоциты), которые подобно NK-клетке (натуральному киллеру), выделяет белки перфорин и гранзим, что приводит к лизису клетки-мишени;
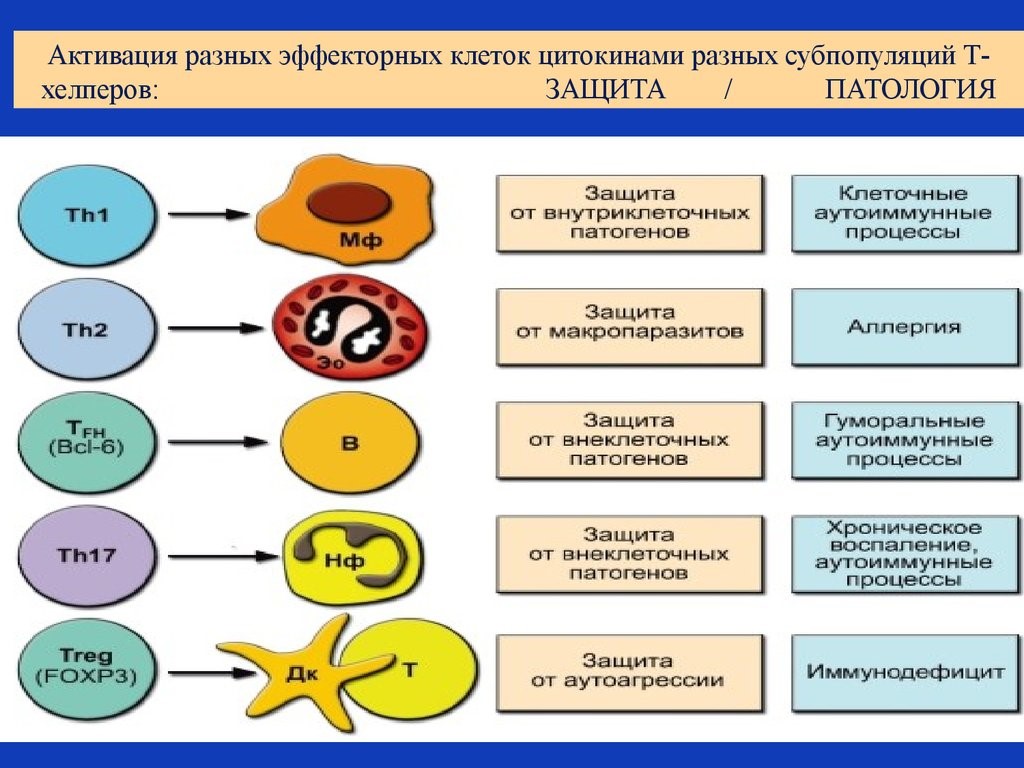
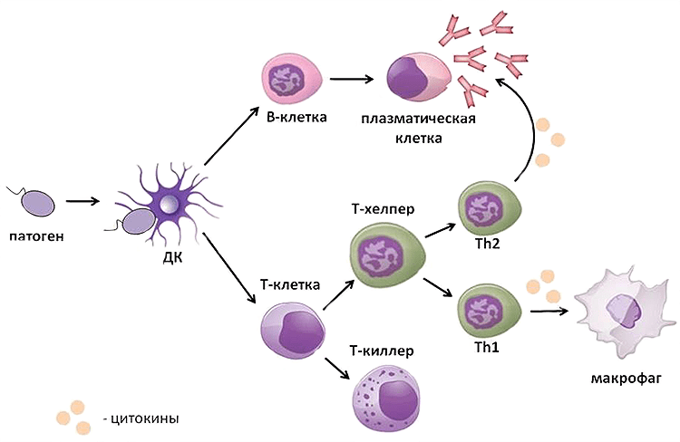
- Т-хелперы (от английского helper – помощник). Они еще обозначаются как Th-клетки, CD4+ T-лимфоциты. Активированные Т-хелперы продуцируют хемокины и цитокины, участвующие в иммунном процессе (рис.19);
Рис. 19. Активация цитокинами разных субпопуляций Т-хелперов
- Т-супрессоры (Ts) подавляют (супрессируют) реакции В-лимфоцитов и блокируют Т-хелперы. Притом эти клетки вовсе не устраивают саботаж иммунным процессам и не вредят здоровью. Они просто регулируют силу иммунного ответа, что позволяет иммунной системе сдержанно и с умеренной силой отвечать на раздражители (тушить пожар, а не костер);
- Т-регуляторные клетки (Tr1) влияют на образование зернистых лейкоцитов (гранулоцитов), которых мы уже представляли в качестве макрофагов.
Соотношение количества клеток CD4/CD8 называют иммунорегуляторным индексом (ИРИ). Если у пациента ИРИ повышен (более 2,2), то это говорит о чрезмерной активности T-хелперов и ослаблении регулирующей функции T-киллеров. При таком показателе иммунные клетки могут разрушать собственные ткани организма. Повышенный ИРИ чаще всего отмечается у пациентов с аутоиммунными болезнями (системной красной волчанкой, склеродермией, ревматоидным артритом и др.). Причиной чрезмерной активности T-хелперов может также стать опухоль вилочковой железы. При этой патологии продуцируется избыточное количество лимфоцитов. Высокие показатели ИРИ отмечаются при остром лимфобластном лейкозе. Это тяжелое онкологическое заболевание сопровождается неконтролируемым увеличением количества незрелых лимфоцитов.
Если иммунорегуляторный индекс понижен (менее1,6), то это говорит о серьезном ухудшении работы иммунитета. Низкие показатели ИРИ свидетельствуют о том, что в организме ослаблена функция защитных клеток, а регуляция со стороны T-киллеров чрезмерна. Обычно это отмечается при следующих патологиях, сопровождающихся иммунодефицитом: инфекционных болезнях (в том числе ВИЧ-инфекции); врожденном иммунодефиците; любых затяжных и хронических болезнях; опухолях костного мозга.
В-лимфоциты ответственны за гуморальное звено иммунитета – продукцию антител. После антигенного стимула В-лимфоцит превращается в лимфобласт – клетку, способную к делению. Часть лимфобластов дифференцируется в В-лимфоциты памяти, другая часть превращается в плазматические клетки, которые осуществляют продукцию антител.
В-лимфоциты несут на своей поверхности В-клеточный рецептор. При контакте с антигеном эти клетки активируются и превращаются в особый клеточный подтип – плазматические клетки, живущие до трех недель и обладающие уникальной способностью секретировать в этот срок тысячи антител.
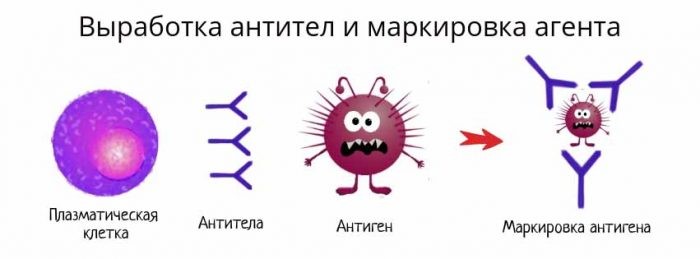
Антитело имеет сродство к распознаваемому им антигену, как бы «прилипает» к нему. Это дает возможность антителам обволакивать (опсонизировать) клетки и вирусные частицы, покрытые молекулами антигена, привлекая макрофаги и другие иммунные клетки для уничтожения патогена. Антитела также умеют активировать специальный каскад иммунологических реакций, называемый системой комплемента, который приводит к перфорации клеточной мембраны патогена и его гибели.
Рис. 20. Выработка антител и маркировка патогена
Различают несколько классов антител (иммуноглобулинов). Первыми после антигенного раздражения, вызывающих агглютинацию бактерий и нейтрализацию вирусов, появляются иммуноглобулины М (IgM). В длительном иммунитете участвуют иммуноглобулины G(IgG).
В табл.2 представлена интерпретация лабораторных исследований на наличие патогена на молекулярном уровне и с помощью тестов на иммуноглобулины М и G.
Таблица 2. Интерпретация лабораторных исследований на наличие патогена на молекулярном уровне
Результат молекулярного исследования
Тест на антитела
Инфицированный или повторно инфицированный пациент
Ранние стадии инфекции. Требуется дополнительное исследование
Инфекция. Требуется дополнительное исследование
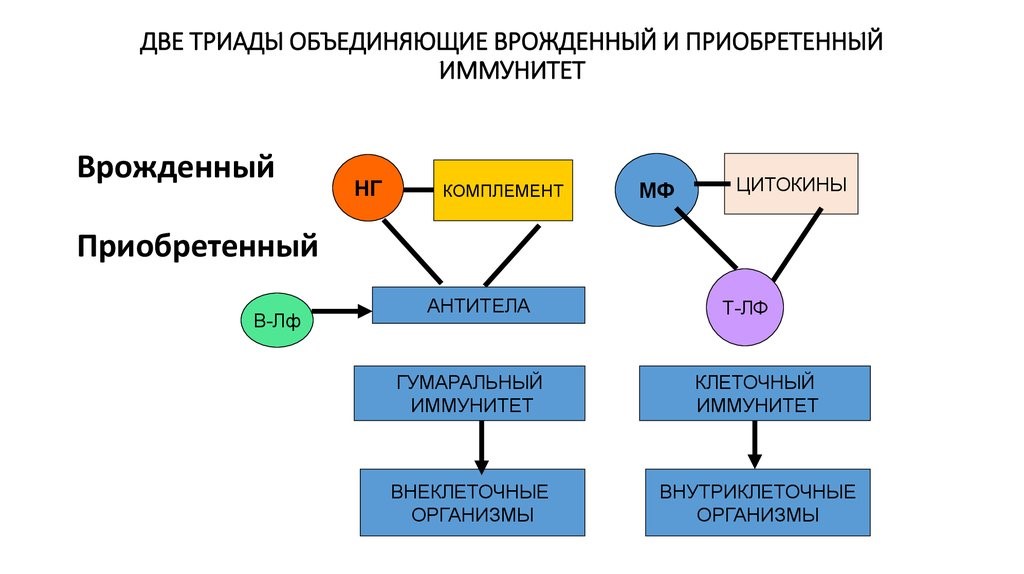
Врожденный и приобретенный виды иммунитета имеют точки соприкосновения, которые представляют две триады (рис.21)
Рис. 21. Две триады, объединяющие врожденный и приобретенный виды иммунитета
Развитие адаптивного иммунного ответа требует достаточно много времени (от нескольких дней до двух недель), и для того чтобы организм мог защищаться от уже знакомой инфекции быстрее, из Т- и В-клеток, участвовавших в прошлых битвах, формируются так называемые клетки памяти. Они, подобно ветеранам, в небольшом количестве присутствуют в организме, и, если появляется знакомый им патоген, вновь активируются, быстро делятся и целой армией выходят на защиту границ (рис.22).
Рис.22. Т-клетки памяти быстро формирует вторичный иммунный ответ
Иммунологическая толерантность
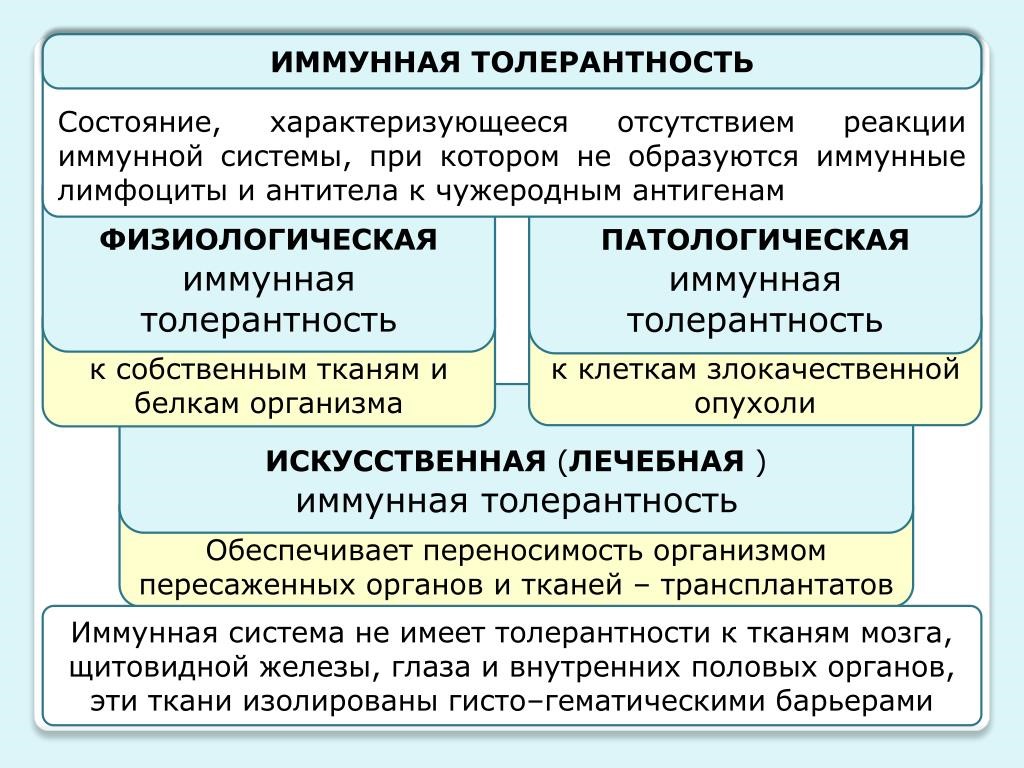
Под иммунологической толерантностью (терпимостью, ареактивностью) понимают отсутствие иммунного ответа на специфический антиген. Перечень антигенов, к которым может развиваться толерантность, практически неотличим от набора антигенов, против которых развивается специфический иммунный ответ (рис.23).
Рис. 23. Иммунная толерантность
Механизмы толерантности необходимы, поскольку иммунная система продуцирует огромное число разнообразных антиген специфичных рецепторов, и некоторые из них оказываются специфичными к собственным антигенам организма; толерантность предотвращает нежелательные реакции против собственных органов и тканей, также для нормального протекания беременности.
Нарушения иммунной системы у человека
Нарушения в работе иммунной системы можно подразделить на три категории: иммунодефициты, аутоиммунные заболевания и реакции гиперчувствительности.
Иммунодефициты
Иммунодефицит – снижение количественных показателей и/или функциональной активности основных компонентов иммунной системы, приводящее к нарушению защиты организма от патогенных микроорганизмов и проявляющееся повышенной инфекционной заболеваемостью.
Первичные иммунодефициты (ПИД) – наследственные заболевания, обусловленные дефектами генов, контролирующих иммунный ответ. В основном ПИД заявляют о себе уже в раннем детском возрасте, но иногда лишь к 30-40 годам жизни.
- симптомов, которые могут быть признаками первичных иммунодефицитов:
- 4 и более случаев отита в течение года;
- 2 и более синусита в течение года;
- низкая эффективность антибиотиков в течение двух и более месяцев приема;
- 2 и более случаев пневмонии в течение года;
- невозможность ребенка набирать вес и нормально расти;
- частые и глубокие абсцессы кожи и внутренних органов
- постоянный кандидоз полости рта и кожи;
- необходимость внутривенного введения антибиотиков для разрешения инфекции;
- две и более системных инфекции, включая сепсис;
- наследственная предрасположенность.
По механизмам развития выделяют 4 основные группы ПИД (табл.3):
- 1-я группа – преимущественно гуморальные, или В-клеточные ПИД;
- 2-я группа – комбинированные ПИД (при всех Т-клеточных иммунодефицитах есть нарушение функции В-клеток);
- 3-я группа – ПИД, обусловленные дефектами фагоцитоза;
- 4-я группа – ПИД, обусловленные дефектами в системе комплемента.
Таблица 3. Некоторые первичные иммунодефициты
Частые бактериальные инфекции
Дефицит или полное отсутствие В-лимфоцитов
Антибиотики, пожизненное введение IgG
Частые респираторные инфекции, отиты
Дефекты Т- и В- лимфоцитов
Антибиотики, пожизненное введение IgG
Атаксия-телеангиоэкстазия (синдром Луи-Бар)
Аномалия двигательной функции, слабость мышц, нарушение речи
Дефицит Т- и В- лимфоцитов
ПИД, обусловленные дефектами фагоцитоза
Хроническая гранулёматозная болезнь
Частые пневмонии, гнойные инфекции
Пожизненная антибактериальная и противогрибковая терапия, интерферон гамма
ПИД, обусловленные дефектами в системе комплемента
Наследственный ангионевротический отек
Отеки губ и век при отсутствии зуда. Отеки гортани, носа, языка опасны для жизни
Низкая концентрация ингибитора эстеразы С1
Введение концентрата ингибитора эстеразы С1
Как следует из табл.3, основным и часто единственным методом лечения большинства пациентов с первичными В-клеточными иммунодефицитами являются иммуноглобулины. Это лекарственные средства, получаемые из плазмы крови человека. Они призваны заменить защитные антитела, отсутствующие в иммунной системе, с целью предотвращения или остановки развития тяжелых инфекционных заболеваний. Сегодня в арсенале врача имеются иммуноглобулины, различающиеся по концентрации активного вещества (5 и 10%), а также по способу введения (внутривенный и подкожный).
ПИД может проявиться в любом возрасте. В зависимости от этого у пациента возникают своеобразные проблемы, требующие определенных видов поддержки на протяжении всей жизни (табл. 4).
Таблица 4. Необходимость в видах поддержки пациента с ПИД в различных возрастных группах
В возрасте от 0 до 14 лет требуется уход со стороны родителей, направленный на профилактику инфекций и на период лечения. Могут потребоваться: обучение на дому; оказание психологической помощи; социальная поддержка в приобретении лекарственных средств.
В подростковом возрасте (14-18 лет) дополнительно могут возникнуть потребности в продолжении непрерывного обучения, профессиональной ориентации, налаживании взаимоотношений со сверстниками, организации досуга.
В возрасте от 18 до 65 лет у пациентов чаще возникают инфекционные осложнения, а с ними и расходы на приобретение лекарственных средств, не подлежащих восполнению, а также проблемы с трудоустройством.
В пожилом возрасте (старше 65 лет) возникают потребности в материальной, социальной и психологической поддержке пациента с ПИД.
Аутоиммунная патология
Повреждение собственных органов и тканей организма иммунной системой называется аутоиммунным процессом. Заболеваниями такого типа страдает около 5% человечества. В организме пациента развиваются боевые действия, напоминающие гражданскую войну: в атаку идут «свои против своих». В этой борьбе победителей нет – одни страдания.
Селекция Т-лимфоцитов в тимусе, а также удаление аутореактивных клеток на периферии (центральная и периферическая иммунологическая толерантность), о которых мы говорили ранее, не могут полностью избавить организм от аутореактивных Т-лимфоцитов. Что же касается В-лимфоцитов, вопрос о том, насколько строго осуществляется их селекция, до сих пор остается открытым. Поэтому в организме каждого человека обязательно присутствует множество аутореактивных лимфоцитов, которые в случае развития аутоиммунной реакции могут повреждать собственные органы и ткани.
В качестве аналога можно привести созданную турками в ХIV веке янычарскую пехоту, в которую набирали юношей-христиан 8-16 лет, воевших против своих сородичей.
Т-клеточная аутоиммуннная агрессия хорошо изучена при ревматоидном артрите, сахарном диабете первого типа, рассеянном склерозе и многих других болезнях.
Такие же клетки-янычары, не помнящие своего родства, прослеживаются среди В-лимфоцитов:
- аутоантитела могут вызывать гибель клеток, активируя на их поверхности систему комплемента или же привлекая макрофаги;
- мишенями для антител могут стать рецепторы на поверхности клетки.
Например, вследствие срыва иммунологической толерантности происходит активация В-лимфоцитов, продуцирующих антитела. Это приводит к выраженному повышению выработки тиреоидных гормонов (Т4 и Т3), а также к увеличению щитовидной железы в размерах (гипертрофии). Патология носит название болезнь Грейвса.
Еще одним примером может быть миастения гравис, которая характеризуется слабостью скелетной мускулатуры вследствие образования аутоантител против структур, отвечающих за холинергическую передачу и сокращение мышечного волокна;
- аутоантитела вместе с растворимыми антигенами могут образовывать иммунные комплексы, которые оседают в различных органах и тканях (например, в почечных клубочках, суставах, на эндотелии сосудов), нарушая их работу и вызывая воспалительные процессы.
Как правило, аутоиммунное заболевание возникает внезапно, и невозможно точно определить, что стало его причиной. Считается, что триггером для запуска может послужить практически любая стрессовая ситуация, будь то перенесенная инфекция, травма или переохлаждение. Значительный вклад в вероятность возникновения аутоиммунного заболевания вносит как образ жизни человека, так и генетическая предрасположенность – наличие определенного варианта какого-либо гена.
Гиперчувствительность
Под гиперчувствительностью понимают чрезмерный иммунный ответ на какой-либо антиген. Реакции гиперчувствительности подразделяют на несколько типов в зависимости от их длительности и механизмов, лежащих в их основе:
- гиперчувствительность I типа включает немедленные анафилактические реакции, часто связанные с аллергией. Реакции этого типа могут как вызывать небольшой дискомфорт, так и приводить к смерти. Основу гиперчувствительности I типа составляют иммуноглобулины E (IgE), которые вызывают дегрануляцию базофилов и тучных клеток;
- гиперчувствительность II типа характеризуется присутствием антител, распознающих его собственные белки и помечающие экспрессирующие их клетки к разрушению. Гиперчувствительность II типа также называют зависимой от антител или цитотоксической гиперчувствительностью, её основу составляют иммуноглобулины G (IgG) и M (IgM);
- гиперчувствительность III типа обусловлена иммунными комплексами, состоящими из антигенов, белков комплемента, IgG и IgM;
- гиперчувствительность IV типа, также известная как отложенная гиперчувствительность, развивается в течение 2-3 дней. Реакции гиперчувствительности IV типа наблюдаются при многих аутоиммунных и инфекционных заболеваниях, а их основу составляют T-клетки, моноциты и макрофаги.
Эффективные методы воздействия на иммунитет:
- регулярная вакцинация по скорости и качеству реакции превышает естественный процесс формирования иммунитета на конкретную инфекцию;
- сбалансированное питание, обеспечивающее поддержание нормального обмена веществ;
- регулярные физические нагрузки, обеспечивающие физиологическое функционирование всех систем организма, поддержание оптимальных показателей массы тела;
- отказ от вредных привычек, приводящих к зависимостям (алкогольной, никотиновой, наркотической, токсической, компьютерной);
- режим дня, особенно влияние циркадных ритмов (смена дня и ночи): во время бодрствования пика достигает численность T-киллеров и NK-клеток, а также концентрация противовоспалительных веществ, таких как кортизол и катехоламины; во время сна достигает своего пика формирование Т-клеток памяти.
Спекулятивные методы вокруг иммунитета:
- прием иммуностимуляторов клинически не оправдан. Если постоянно стимулировать выработку лейкоцитов лекарственными средствами, иммунная система начнет утрачивать свои непосредственные функции. Вот тогда и наступает момент начала серьезных проблем с иммунитетом. Совершенно не влияют на иммунную систему природные адаптогены: лимонник китайский, женьшень, элеутерококк, радиола розовая. Они воздействуют, как усилители синтеза РНК и белков (основу человеческих клеток), активизируют ферменты обмена и работу эндокринной и вегетативной систем;
- прием витаминов явно переоценен. Положительное влияние на иммунную систему оказывает витамин D, который стимулирует образование Т-киллеров. Все остальные группы витаминов прямого участия в функционировании иммунной системы не принимают;
- банные процедуры и сауна на иммунную систему не влияют;
- народные средства, такие как мед и чеснок обладают легким бактерицидным, но не иммуногенным действием.
Заключение
Иммунная система представлена тремя уровнями: органным, клеточным и молекулярным со сложнейшими взаимодействиями между ними.
Современная иммунология различает два взаимодействующих компонента иммунной системы – врожденный и приобретенный (адаптивный) виды иммунитета, обеспечивающие развитие иммунного ответа на генетически чужеродные субстанции, которые представляют собой микроорганизмы, злокачественные опухолевые клетки, пересаженные органы и ткани.
Адаптивный иммунитет основывается на трех главных процессах: распознавание антигенов, их удаление (элиминация) и формирование иммунологической памяти.
Поломки в структуре иммунной системы приводят к развитию иммунодефицитов, аутоиммунным заболеваниям или реакции гиперчувствительности.
Иммунодефицит на генетическом уровне (первичный) или приобретенный (вторичный) может проявиться в любом возрасте и привести к повышенной инфекционной заболеваемости. В последние годы появились средства заместительной терапии, которые продлевают жизнь этим пациентам. Для повышения качества их жизни требуется не только обеспечение дорогостоящим лечением, но и организация поддержки со стороны семьи, психологов и социальных институтов.
Аутоиммунные заболевания и гиперчувствительность – это неспособность организма противостоять разбушевавшейся иммунной системе, которая перепутала свое и чужое.
К сожалению, ни одно из заболеваний иммунной системы медицина еще не научилась излечивать, а только применять заместительную терапию.
Эффективными профилактическими методами воздействия на иммунную систему являются вакцинация и здоровый образ жизни. Купить иммунитет в аптеке пока никому не удалось.
Источник