Рецепторы обеспечивающие основное действие лекарственного препарата называются
Рецепторы — макромолекулы, функция которых заключается в связывании веществ-посредников и в преобразовании этой связи в действие, т, е. изменение клеточной функции. Рецепторы отличаются по своей структуре и способу преобразования контакта с лигандом в клеточный ответ (преобразование сигнала).
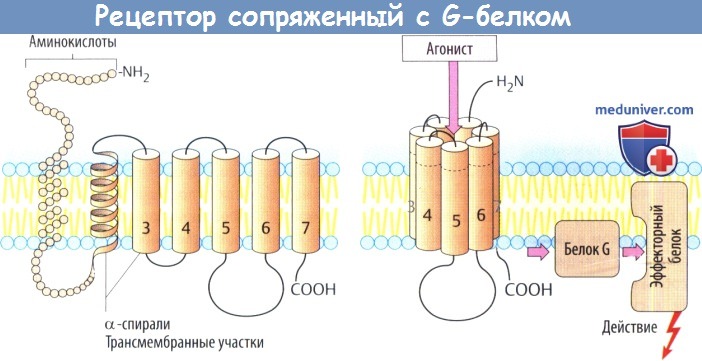
а) Рецепторы, сопряженные с белком G, состоят из цепи аминокислот, которая направлена в сторону мембраны и от нее в виде серпантина. С вне-мембранными петлевыми участками молекулы связаны углеводные остатки через различные точки N-гликозилирования.
Семь а-спиральных, охватывающих мембрану участков образуют окружность возле центральной ниши, которая несет участки для связывания медиаторных веществ. Связывание молекулы медиатора или структурно связанной молекулы агониста вызывает изменение конформации белка, в результате чего он вступает во взаимодействие с белком G (белок, связывающий нуклеотид гуанил).
Белки G располагаются в нижнем слое плазмолеммы и состоят из трех субъединиц, обозначаемых а, β и γ. Существует несколько белков G, которые отличаются в основном своей a-единицей. Контакте рецептором активирует белок G, что, в свою очередь, приводит к активации другого белка (фермента, ионного канала). Многие медиаторы действуют через рецепторы, сопряженные с белком G.
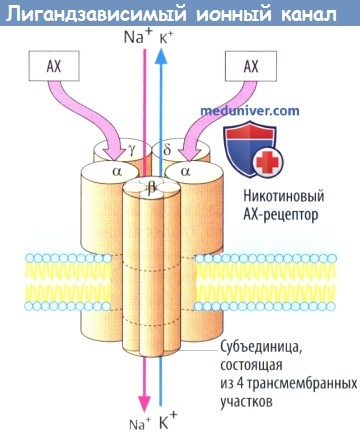
б) Примером лигандзависимого ионного канала является никотиновый холинорецептор на концевой пластинке двигательного нерва. Рецепторный комплекс образован пятью субъединицами, каждая из которых содержит четыре трансмембранных участка.
Одновременное связывание двух молекул АХ двумя а-субъединицами приводит к открытию ионного канала со входом Na + (и выходом некоторого количества К + ), деполяризации мембраны и активации потенциала действия. Нейронные N-холинорецепторы, очевидно, состоят лишь изо- и β-субъединиц.
Ряд рецепторов медиатора γ-аминомасляной кислоты (ГАМК) принадлежат к данной группе: подтип ГАМКA связан с хлорными каналами (и с участком связывания бензодиазепинов). Глутамат и глицин оба действуют через лигандзависимые ионные каналы.
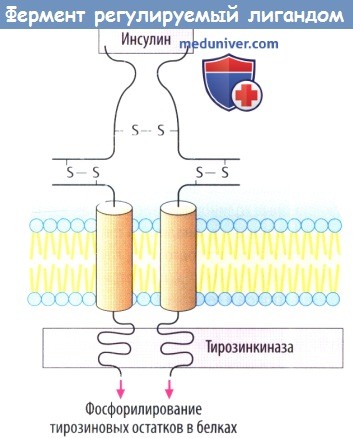
в) Белок инсулинового рецептора представляет собой управляемый лигандом фермент, каталитический рецептор. При связывании инсулина с внеклеточным участком «отключается» активность тирозинкиназы внутри клетки. Фосфорилирование белка приводит к изменению клеточной функции в результате образования других сигнальных белков. Рецепторы гормонов роста тоже принадлежат к классу каталитических рецепторов.
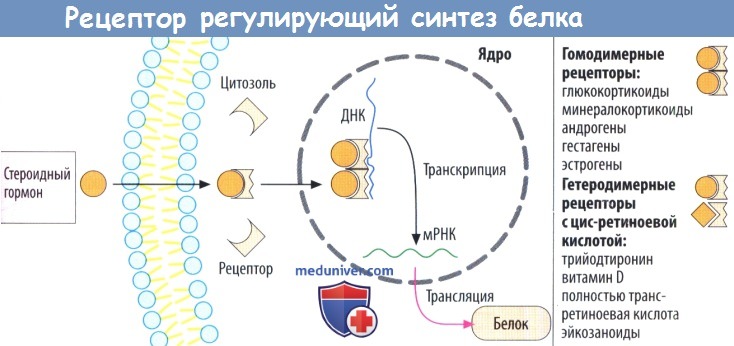
г) Рецепторы, регулирующие синтез белка, стероидов и гормонов щитовидной железы, находятся в цитозоле и в клеточном ядре соответственно. Белки рецепторов также расположены внутриклеточно, в зависимости от гормона — в цитозоле (глюкокортикоиды, минералокортикоиды, андрогены и гестагены) или в клеточном ядре (эстрогены, гормоны щитовидной железы).
При связывании гормона открывается скрытый в норме участок белка рецептора, что дает возможность последнему связаться с особой последовательностью нуклеотидов ДНК в гене и регулировать его транскрипцию. Из этого следует, что комплексы лиганд-рецептор работают как факторы, регулирующие транскрипцию. Обычно происходит активация или усиление и, редко, блокада транскрипции.
Комплексы гормон-рецептор взаимодействуют парно с ДНК. Эти пары (димеры) могут состоять из двух идентичных комплексов гормон-рецептор (гомодимерная форма, например, с гормонами надпочечников или половыми гормонами). Комплекс тиреоидный гормон-рецептор встречается в гетеродимерной форме и сочетается с комплексом цис-ретиноевая кислота-рецептор.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Взаимодействия лекарственного вещества с рецептором
, PhD, PharmD, Columbia Southern University, Orange Beach, AL
Рецепторы – это макромолекулы, участвующие в передаче химических сигналов как между клетками, так и внутри одной клетки; они могут находится на поверхности клеточной мембраны или в цитоплазме (см. таблицу Некоторые типы физиологических рецепторов и рецепторов лекарственных препаратов Влияние возраста на особенности клинических эффектов некоторых лекарственных препаратов Фармакодинамика определяет заданную эффективность лекарственного препарата в организме и реакцию организма на воздействие лекарственного препарата; эти эффекты обусловлены рецепторными связями. Прочитайте дополнительные сведения ). Активированные рецепторы прямо или косвенно регулируют клеточные биохимические процессы (например, проводимость ионных каналов, фосфорилирование белков, транскрипцию ДНК, ферментативную активность).
Молекулы (к примеру, лекарственные препараты, гормоны, нейротрансмиттеры), которые связываются с рецептором, называются лигандами. Связывание может быть специфическим и обратимым. Связывание с лигандом может приводить к активации либо инактивации рецептора; активация может стимулировать либо ингибировать ту или иную клеточную функцию. Каждый лиганд способен взаимодействовать с различными подтипами рецепторов. Почти не существует препаратов, абсолютно специфичных к одному рецептору или его подтипу, но большинство из них имеет относительную селективность. Селективность – это степень, с которой лекарственное средство действует на определенный участок относительно других участков; селективность относится в основном к физико-химическому связыванию препарата с клеточными рецепторами.
Способность лекарственного препарата воздействовать на конкретный тип рецептора зависит от его аффинности (вероятности того, что ЛС займет рецептор в определенный момент времени) и внутренней активности (степени активации рецептора после связывания с лигандом и развития клеточной реакции). Аффинность и внутренняя активность лекарственного вещества в свою очередь определяются его химической структурой.
Фармакологический эффект определяется также длительностью сохранения комплекса «препарат-рецептор» (время удержания). На продолжительность существования комплекса «препарат-рецептор» влияют динамические процессы (изменения конформации), которые контролируют скорость ассоциации и диссоциации лекарственных веществ от своей мишени. Большее время удержания служит объяснением продолжительному фармакологическому действию. К препаратам с длительным временем удержания относятся финастерид и дарунавир. Длительное время удержания может быть потенциальным недостатком, если за этот счет продлевается и токсический эффект препарата. Для некоторых рецепторов транзиторное связывание производит нужный фармакологический эффект, в то время как длительное связывание провоцирует токсичность.
Физиологические функции (такие как сокращение, секреция), как правило, регулируются множественными рецептор-опосредованными механизмами и включают несколько этапов (связывание с рецептором, активация внутриклеточных вторичных мессенджеров и т. д.) между первоначальным взаимодействием лекарственного вещества с рецептором и конечным ответом ткани или органа. По этой причине один и тот же желаемый фармакологический эффект может быть достигнут применением ЛС с разной химической структурой.
На способность препарата связываться с рецептором оказывают влияние внешние факторы, а также внутриклеточные регуляторные механизмы. Исходная плотность рецепторов и эффективность механизмов ответа на стимул варьируют от ткани к ткани. Лекарственные средства, старение, мутации и заболевания могут повышать (активировать) или снижать (подавлять) число и аффинность рецепторов. Например, клонидин снижает активность альфа-2-адренорецепторов; по этой причине быстрая отмена клонидина может спровоцировать гипертонический криз Неотложные состояния К неотложным состояниям относят поражения органов-мишеней (головной мозг, сердечно-сосудистая система и почки) на фоне выраженного повышения АД. Диагностика производится посредством измерения. Прочитайте дополнительные сведения . Длительная терапия бета-блокаторами повышает плотность бета-рецепторов, в связи с чем резкое прекращение приема данного класса препаратов может вызвать развитие тяжелой гипертензии или тахикардии. Стимуляция и ингибирование рецепторов влияют на механизмы приспособления организма к лекарственному средству (например, в виде гипосенсибилизации, тахифилаксии, толерантности, приобретенной резистентности и гиперчувствительности после отмены).
Лиганды связываются с определенными участками на макромолекуле рецептора, называемыми сайтами узнавания. Места связывания лекарственного вещества и эндогенного агониста (гормона или нейротрансмиттера) могут быть идентичными либо различаться. Агонисты, связывающиеся со смежным или другим сайтом, иногда называются аллостерическими агонистами. Также происходит неспецифическое связывание препаратов, т.е. с молекулярными участками, не являющимися рецепторами (например, белками плазмы крови). Связывание лекарственного вещества с подобными неспецифическими участками, например, связывание с белками сыворотки крови, препятствует его связыванию с рецептором, тем самым делая препарат неактивным. Несвязанные препараты способны взаимодействовать с рецепторами и, следовательно, вызывать эффект.
Агонисты и антагонисты
Агонисты активируют рецепторы для реализации желаемого фармакологического эффекта. Традиционные агонисты повышают долю активированных рецепторов. Обратные агонисты стабилизируют рецепторы в их неактивной конформации и действуют аналогично конкурентным агонистам. Многие гормоны, нейротрансмиттеры (например, ацетилхолин, гистамин, норадреналин ) и лекарственные средства (например, морфин, фенилэфрин, изопреналин, бензодиазепины, барбитураты) действуют как агонисты рецепторов.
Антагонисты препятствуют активации рецептора. Предотвращение активации оказывает множество эффектов. Антагонисты усиливают клеточную функцию в том случае, если они блокируют действие вещества, обычно подавляющего данную функцию. Справедлива и обратная закомерность: антагонисты снижают клеточную функцию, если блокируют действие вещества, усиливающего ее.
Антагонисты рецепторов могут быть классифицированы на обратимые и необратимые. Обратимые антагонисты легко диссоциируют от соответствующих рецепторов, необратимые – образуют стабильную, постоянную или почти постоянную химическую связь со своим рецептором (например, при алкилировании). Псевдообратимые антагонисты медленно разрывают связь со своим рецептором.
При конкурентном антагонизме связывание антагониста с рецептором препятствует связыванию с ним агониста.
При неконкурентном антагонизме агонист и антагонист могут связываться одновременно, но связывание антагониста снижает эффект агониста либо препятствует его развитию.
При обратимом конкурентном антагонизме агонист и антагонист образуют кратковременные связи с рецептором, в результате чего достигается равновесное состояние этой трехкомпонентной системы. Такой антагонизм можно преодолеть путем увеличения концентрации агониста. Например, налоксон (антагонист опиоидных рецепторов, структурно схожий с морфином) при введении незадолго до или сразу после введения морфина блокирует действие последнего. Тем не менее конкурентный антагонизм налоксона может быть преодолен с помощью введения морфина в большей дозе.
Такие лекарственные вещества называются частичными агонистами или агонистами-антагонистами. Структурные аналоги молекул агониста часто обладают одновременно свойствами агониста и антагониста. Например, пентазоцин активирует опиоидные рецепторы, но блокирует их активацию другими опиоидами. Таким образом, пентазоцин обеспечивает опиоидное действие, но ослабляет эффект другого опиоида, если последний вводится в период сохранения связи пентазоцина с рецептором. Лекарственное средство, действующее как частичный агонист в одной ткани, может действовать как полный агонист в другой.
Источник
7)Фармакодинамика, определение. Основные принципы действия лекарств. Типы рецепторов. Вторичные мессенджеры.
Фармакодина́мика — раздел фармакологии, изучающий биохимические эффекты и физиологические действия лекарств на тело человека, на микроорганизмы или паразитов, находящихся внутри тела человека или снаружи. Она также изучает механизмы действия лекарств, связь между концентрацией лекарственных веществ и достигнутым ими действием.
Многие лекарства имеют одинаковый механизм действия и, следовательно, могут быть объединены в группы и подгруппы. Количество различных фармакологических групп (подгрупп) ограничивается десятками.
Под действием лекарств в организме не происходит новых биохимических реакций или физиологических процессов. Большинство лекарств только стимулируют, имитируют, угнетают или полностью блокируют действие внутренних посредников, передающих сигналы между различными органами и системами через биологические субстраты.
Каждое звено механизма обратной связи участвует в регулировании функций клетки и целого организма, а, следовательно, может служить “мишенью” – биологическим субстратом – для лекарственных средств.
Многие ферменты являются “мишенями” для лекарств. Лекарства могут угнетать или – реже – повышать активность этих ферментов, а также являться для них “ложными” субстратами. Например, угнетающими активность (ингибирующими) ферментов средствами являются ненаркотические анальгетики и нестероидные противовоспалительные средства, некоторые противоопухолевые препараты (метотрексат), а ложным субстратом – метилдофа. Ингибиторы ангиотензинпревращающего фермента (АПФ) (каптоприл и эналаприл) широко применяются в качестве понижающих артериальное давление (гипотензивных) средств. Изменяя активность ферментов, лекарства изменяют внутриклеточные процессы и тем самым обеспечивают лечебный эффект.
В основе фармакологического действия лекарств лежит их физико-химическое или химическое взаимодействие с такими “мишенями”. Возможность взаимодействия лекарства с биологическим субстратом зависит в первую очередь от химического строения каждого из них. Последовательность расположения атомов, пространственная конфигурация молекулы, величина и расположение зарядов, подвижность фрагментов молекулы относительно друг друга влияют на прочность связи и, тем самым, на силу и продолжительность фармакологического действия. Молекула лекарственного вещества в большинстве случаев имеет очень маленький размер по сравнению с биологическими субстратами, поэтому она может соединяться только с небольшим фрагментом макромолекулы рецептора. При любой реакции между лекарством и биологическим субстратом образуется химическая связь
Итак, есть сигнальные молекулы (медиаторы, гормоны, эндогенные биологически активные вещества), и есть биологические субстраты, с которыми эти молекулы взаимодействуют. Лекарства, введенные в организм, могут воспроизводить или блокировать эффекты естественных сигнальных молекул, изменяя тем самым функции клеток, тканей, органов и систем органов. Этим определяется фармакологическое действие лекарств.
Воспроизведение действия (миметический эффект) наблюдается в тех случаях, когда молекула лекарственного вещества и естественная сигнальная молекула очень похожи: имеют высокое соответствие физико-химических свойств и структуры, обеспечивающих одинаковые внутриклеточные изменения. Результатом взаимодействия лекарства с рецептором в этом случае является активация или торможение определенной функции клеток в полном соответствии с действием эндогенной (внутренней) сигнальной молекулы. Подобным образом действуют очень многие аналоги гормонов и медиаторов. Цель создания подобных лекарств – получение препаратов с более выраженным, стабильным и длительным по сравнению с медиатором (адреналин, ацетилхолин, серотонин и другие) действием, а также восполнение дефицита медиатора или гормона и, соответственно, их функций.
Конкурентное действие (блокирующий, литический эффект) встречается часто и присуще лекарствам, которые лишь частично похожи на сигнальную молекулу (например, медиатор). В этом случае лекарство способно связываться с одним из участков рецептора, но оно не вызывает комплекса реакций, сопутствующих действию естественного медиатора. Такое лекарство как бы создает над рецептором защитный экран, препятствуя его взаимодействию с естественным медиатором, гормоном и так далее. Конкурентная борьба за рецептор, называемая антагонизмом (отсюда и название лекарств – антагонисты), позволяет корректировать физиологические и патологические реакции. Подобным образом действуют адрено-, холино- и гистаминолитики.
Следующий тип взаимодействия лекарства с рецептором называют неконкурентным, и в этом случае молекула лекарства связывается с рецепторной макромолекулой не в месте ее взаимодействия с медиатором, а на рядом расположенном участке, то есть действует опосредованно. При этом происходит изменение пространственной структуры рецептора, вызывающее раскрытие или закрытие его для естественного медиатора. В этих случаях рецептор для лекарства и рецептор для медиатора не совпадают, но находятся в одном рецепторном комплексе, и лекарство не вступает в прямое взаимодействие с рецептором. Ярким примером лекарств, действующих по этому типу, являются бензодиазепины – большая группа структурно родственных соединений, обладающих анксиолитическими, снотворными и противосудорожными свойствами.Соединяясь со специфическими бензодиазепиновыми рецепторами, которые взаимосвязаны с рецепторами гамма-аминомасляной кислоты (ГАМК), лекарственное средство изменяет пространственную конфигурацию ГАМК-рецепторов и увеличивает прочность их связи с субстратом – гамма-аминомасляной кислотой. В результате усиливается тормозящее влияние этого медиатора на центральную нервную систему, чем обеспечивается лечебный эффект препаратов.
В качестве «мишеней» для лекарственных средств служат рецепторы, ионные каналы, ферменты, транспортные системы и гены. Рецепторами называют активные группировки макромолекул субстратов, с которыми взаимодействует вещество. Рецепторы, обеспечивающие проявление действия веществ, называют специфическими.
Выделяют следующие 4 типа рецепторов
I. Рецепторы, осуществляющие прямой контроль за функцией ионных каналов. К этому типу рецепторов, непосредственно сопряженных с ионными каналами, относятся н-холинорецепторы, ГАМКА-рецепторы, глутаматные рецепторы.
II. Рецепторы, сопряженные с эффектором через систему «G-белки — вторичные передатчики» или «G-белки-ионные каналы». Такие рецепторы имеются для многих гормонов и медиаторов (м-холинорецепторы, адренорецепторы).
III. Рецепторы, осуществляющие прямой контроль функции эффекторного фермента. Они непосредственно связаны с тирозинкиназой и регулируют фосфорилирование белков. По такому принципу устроены рецепторы инсулина, ряда факторов роста.
IV. Рецепторы, контролирующие транскрипцию ДНК. В отличие от мембранных рецепторов I-III типов, это внутриклеточные рецепторы (растворимые цитозольные или ядерные белки). С такими рецепторами взаимодействуют стероидные и тиреоидные гормоны.
Вторичные посредники, или «вторичные мессенджеры» — это внутриклеточные сигнальные молекулы, высвобождаемые в тех или иных внутриклеточных сигнальных каскадах в ответ на стимуляцию тех или иных рецепторов и вызванную ею активацию первичных эффекторных белков. Вторичные посредники, в свою очередь, приводят к активации вторичных эффекторных белков. Это, в свою очередь, запускает каскад тех или иных физиологических изменений, которые могут быть важны для обеспечения таких важных физиологических процессов, как рост, развитие и дифференцировка клеток, активация деления клетки, транскрипция или наоборот угнетение транскрипции тех или иных генов, биосинтез тех или иных белков, выделение ею гормонов, нейромедиаторов или цитокинов соответственно типу клетки, изменение биоэлектрической активности клетки, миграция клеток, обеспечение их выживаемости или, наоборот, индукция апоптоза. Вторичные посредники являются инициирующими элементами во множестве внутриклеточных сигнальных каскадов. Вследствие всего этого вторичные посредники играют очень важную роль в жизни клетки, а грубое нарушение работы любой из систем вторичных посредников оказывает неблагоприятное воздействие на клетку (например, может привести к её опухолевой трансформации или наоборот к апоптозу).
Вторичные посредники, как правило, являются малыми небелковыми молекулами. Важнейшие примеры молекул вторичных посредников (но не ограничивающиеся ими) включают в себя циклический АМФ, циклический ГМФ, инозитолтрифосфат, диацилглицерин, кальций, оксид азота (II).
Источник