Разработка лекарственных средств от субстанции
Разработка лекарственного средства начинается с синтеза новых химических соединений. Вещества со сложной структурой можно получить из различных иа очников, например растений (сердечные гликозиды), тканей животных (гепарин), микробных культур (бензилпенициллин), культур человеческих клеток (урокиназа), или посредством генно-инженерных технологий (человеческий инсулин).
Чем больше ясности во взаимоотношениях структуры и активности, тем более направленным оказывается поиск новых веществ.
а) Доклинические испытания дают информацию о биологических эффектах новых веществ. Начальный скрининг может включать биохимические и фармакологические исследования (анализ связывания с рецептором) или эксперименты на культурах клеток, изолированных клетках и изолированных органах.
Поскольку эти модели не способны воспроизвести сложные биологические процессы, происходящие в интактных организмах, любое потенциальное лекарственное средство необходимо проверить на животных. Только эксперименты на животных позволяют выяснить, возникаютли желаемые эффекты при дозах, не вызывающих токсичности или сопровождающихся слабой токсичностью. Цель токсикологических исследований заключается в том, чтобы оценить:
1) токсичность, обусловленную кратковременным или длительным приемом;
2) генетические повреждения (генотоксичность, мутагенез);
3) развитие опухолей (канцерогенность);
4) возникновение врожденных дефектов (тератогенность).
В экспериментах на животных также оценивают всасывание, распределение, метаболизм и элиминацию (фармакокинетика) изучаемых веществ. На уровне доклинического изучение лишь у малой части новых веществ обнаруживается потенциал для применения у человека.
Фармацевтическиетехнологии предлагают методы изготовления лекарственных форм.
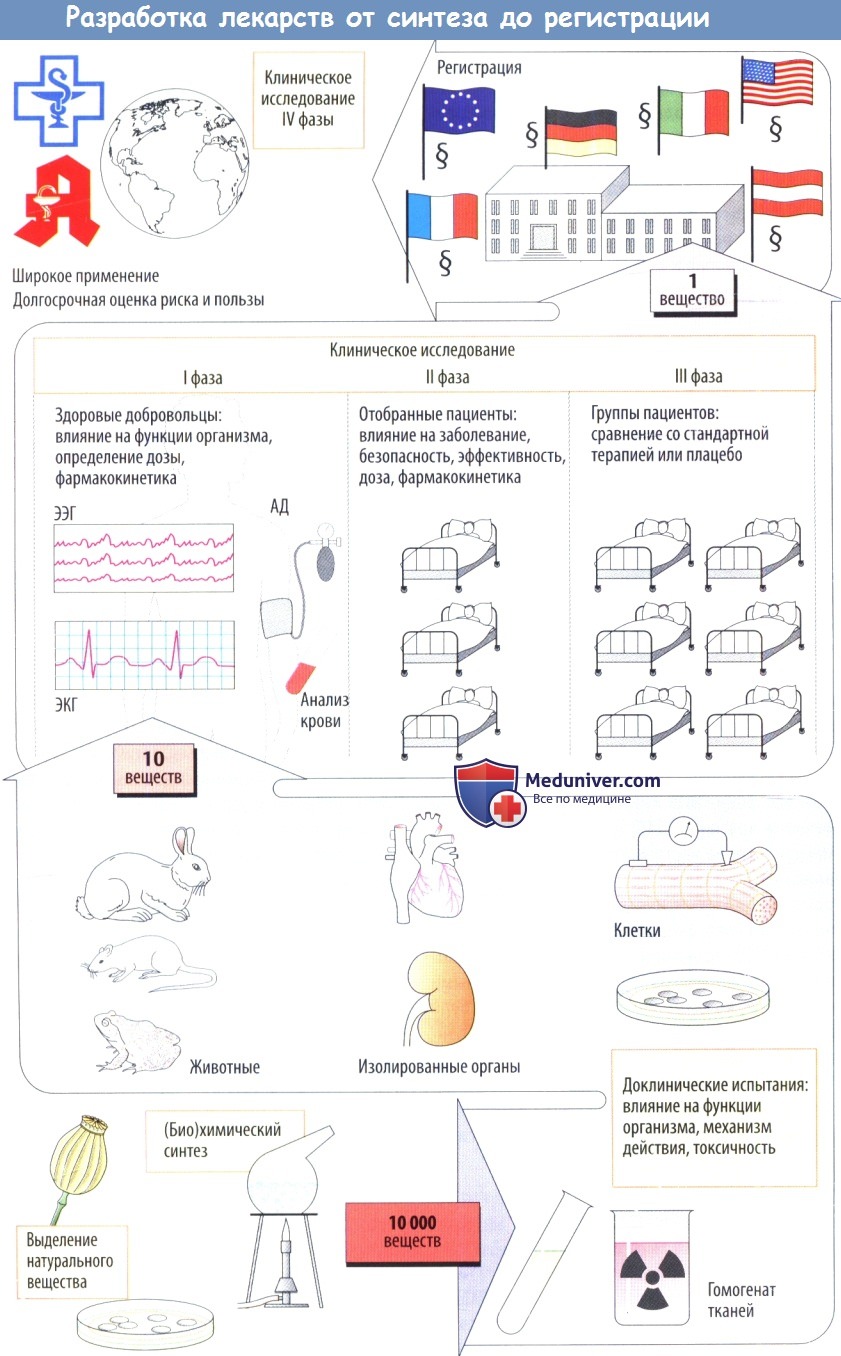
б) Клинические испытания начинаются с исследований I фазы, в которых участвуют здоровые лица; цель этих исследований — определить, будут ли эффекты, наблюдаемые у животных, также возникать у людей. Кроме того, на данном этапе определяется дозозависимость клинических эффектов.
Во II фазе потенциальные лекарственные средства сначала проверяют на отобранных пациентах на терапевтическую эффективность при заболевании, для лечения которого эти препараты предназначались. Если полезное действие очевидно, а частота побочных эффектов приемлема, начинается III фаза, в которой участвует более крупная группа пациентов, у которых новое средство сравнивают с традиционными методами лечения сточки зрения терапевтического результата.
Как форма экспериментов на людях, эти клинические исследования подвергаются анализу и одобрению этическими комитетами медицинских учреждений в соответствии с международными правилами проведения (Хельсинкской, Токийской и Венецианской декларациями). Во время клинических исследований выясняется, что многие вещества нельзя использовать. Как правило, в конце концов примерно из 10 000 вновь синтезированных веществ остается только одно.
в) Решение зарегистрировать новое лекарственное средство выносится национальным регуляторным органом (Food and Drug Administration в США, Health Protection Branch Drugs Directorate в Канаде, комиссией ЕС вместе с European Medicines Agency в Великобритании), которому производители должны подавать регистрационные документы.
Заявители должны документально подтвердить результатами соответствующих испытаний (доклинических и клинических), что критерии эффективности и безопасности удовлетворены и что лекарственные формы продукта (таблетки, капсулы и т. д.) соответствуют всем стандартам контроля качества.
После регистрации новое лекарственное средство может продаваться под торговым названием, оно должно быть доступным, выписываться врачами и отпускаться фармацевтами. В это время наблюдение продолжается в форме постмаркетинговых исследований (IV фаза клинических исследований)
г) Фармакологический надзор — действия, направленные на то, чтобы выявлять и устранять связанные с препаратом риски во время проведения клинических исследований и последующего его выхода на рынок. Фармаконадзор включает отчеты о предполагаемых случаях нежелательных реакций, направляемые в национальные регуляторные органы.
На основе длительного опыта применения можно правильно оценить соотношение риска и пользы и, следовательно, терапевтическую ценность нового лекарственного средства. Если новый препарат имеет небольшое преимущество перед существующими, необходимо принимать во внимание соотношение затрат и пользы от применения лекарственного средства.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Разработка систем доставки лекарственных средств с применением микро- и наночастиц
Полный текст:
Аннотация
Ключевые слова
Для цитирования:
Соснов А.В., Иванов Р.В., Балакин К.В., Шоболов Д.Л., Федотов Ю.А., Калмыков Ю.М. Разработка систем доставки лекарственных средств с применением микро- и наночастиц. Качественная Клиническая Практика. 2008;(2):4-12.
Разработка и внедрение инновационных лекарственных форм (ЛФ) является приоритетной задачей фарминдустрии. В настоящее время около 25% мирового объёма продаж лекарств занимают препараты с улучшенной системой доставки. Имеющиеся на рынке препараты, как правило, продлевают действие и увеличивают биодоступность лекарственного средства (ЛС), а также снижают возможные побочные эффекты [1]. Разрабатываемые и внедряемые в настоящее время системы доставки обладают не только перечисленными выше полезными свойствами, но и обеспечивают направленный транспорт лекарств к очагу патологического процесса. Новые препараты, подготовленные к выпуску на рынок ведущими фармацевтическими компаниями, как правило, уже оснащены транспортной системой. Это позволяет не только в значительной степени увеличить эффективность используемого ЛС, но и существенным образом улучшить его потребительские характеристики.
Очевидно, что финансовый аспект крайне важен для российского потребителя, поскольку доля более дешёвых отечественных лекарств, преимущественно дженериков (от англ. generic – родственный; термин, принятый для обозначения прямых аналогов лекарственных субстанций, на которые закончился срок патентной защиты), на российском рынке составляет не более трети. При этом доля препаратов с улучшенной системой доставки среди них крайне незначительна. По прогнозам экспертов, затраты государства на импорт медикаментов и медицинских изделий к 2010 г. возрастут до 300 миллиардов рублей, при общем росте фармацевтического рынка в РФ до 400-450 миллиардов рублей. В связи с этим, разработка систем доставки ЛС, патентование и производство не только улучшенных лекарственных форм хемодженериков (обеспечивающих быстрое насыщение рынка относительно недорогими отечественными аналогами известных препаратов), но и создание новых, оригинальных ЛС направленного действия является актуальной задачей российской фарминдустрии.
В представленной статье рассмотрены основные направления разработки систем доставки лекарств на основе биоразлагаемых полимеров, мицелл и углеродных наночастиц, включая системы с активной диффузией, обратным ответом и системы направленного транспорта. Влияние свойств частиц на транспорт ЛС проиллюстрировано конкретными примерами, в том числе разработками отечественных ученых Исследовательского Института Химического Разнообразия (ИИХР). Отдельный раздел посвящён возможности использования наночастиц с целью диагностики заболеваний и визуализации действия транспортных систем in vivo с применением передового метода флуоресцентной ЯМР-томографии, активно используемого в ИИХР при создании новых ЛС.
Краткий обзор современных систем доставки лекарств на основе микро- и наночастиц
Как правило, традиционные ЛФ содержат одно или несколько индивидуальных лекарственных веществ (ЛВ) в формах, пригодных для энтерального или парентерального введения. Применяемые подходы к введению лекарств в организм человека, основанные на использовании традиционных ЛФ, имеют целый ряд существенных недостатков, таких как:
- Повышенный расход ЛВ, вызванный тем, что ЛВ не достигает всех необходимых биологических мишеней или достигает, но в концентрации значительно меньшей по сравнению с необходимой терапевтической. Поэтому приходится использовать дозы, которые на 1-2 порядка превышают теоретически необходимые.
- Ненаправленное действие ЛВ, т.е. взаимодействие с нецелевыми биообъектами, часто приводит к побочным эффектам, обусловленным его метаболитами, и к нецелевому, иррациональному расходу ЛС.
- Невозможность поддержания оптимальной терапевтической концентрации ЛВ в течение необходимого времени и, как следствие, необходимость частого приёма лекарственного препарата.
- Недостаточная биосовместимость и нежелательные физиологические эффекты в области введения ЛС. Необходимость использования специальных методик введения лекарственного препарата.
- Значительные трудности в использовании ЛВ с неоптимальными транспортными свойствами (например, высокая липофильность).
Наиболее ярко перечисленные недостатки проявляются при использовании ЛВ с выраженным побочным действием (большинство противоопухолевых препаратов) и лекарств, действующих на центральную нервную систему (ЦНС): наркотические анальгетики, средства лечения болезни Альцгеймера и др., т.е. лекарственных агентов, действие которых требует преодоления гематоэнцефалического барьера (ГЭБ). К сожалению, существенные ограничения в применении значительной доли традиционных ЛФ связаны с наличием именно этих нежелательных последствий. Более того, использование традиционных ЛФ нецелесообразно при создании высокотехнологичных и дорогостоящих лекарственных препаратов, обладающих высоким сродством, высокой активностью и селективностью по отношению к целевым биологическим мишеням.
Таким образом, традиционные ЛФ уже не отвечает жёстким современным требованиям, их производство и использование в значительной степени тормозит развитие медицины, фармацевтической науки и индустрии.
Современное развитие исследовательских методов и технологий подготовило основу для создания новых, инновационных ЛФ, не только лишённых перечисленных выше недостатков, но и способных к направленному транспорту ЛВ в очаг патологического процесса. Кроме того, они способствуют снижению крайне нежелательных побочных эффектов ЛВ, а также их токсичных метаболитов. Некоторые передовые ЛФ позволяют визуализировать процесс диагностики и лечения.
В настоящее время методы и технологии, развивающиеся на стыке органической химии и химии высокомолекулярных соединений (полимеров), медицинской и физической химии, инструментальных методов исследований и аналитической химии, молекулярной биологии и молекулярной генетики, позволяют эффективно решать большинство научных и технологических задач, связанных с созданием эффективных ЛФ. Бурное развитие микро-, нано- и биотехнологий позволяет создавать частицы с заданными свойствами, такими как: размер частиц, свойства «тела» частицы и её поверхности, зависимый «отклик» на местные и удалённые воздействия, а также возможность визуализации действия ЛВ и результатов диагностики [2, 3]. Перечисленные свойства позволяют эффективно использовать микро- и наночастицы при создании новых эффективных форм доставки ЛВ целенаправленно в очаг воспалительного или патологического процесса [4]. Ниже перечислены основные значимые характеристики подобных частиц, применительно к созданию лекарственных транспортных систем:
- капсуляция «сложных» ЛВ;
- визуализация, сенсоры;
- клеточная/тканевая специфичность;
- местная активация (pH, температура и т.д.);
- удалённая активация;
- магнитные свойства;
- контролируемое выделение;
- защита от внешней среды;
- механические свойства/поддержка ткани.
В комплексе применение подобных методов и технологий позволяет:
- пролонгировать действие ЛC, и как следствие, снизить частоту приёма препарата;
- обеспечить необходимую биосовместимость;
- защитить ЛC от преждевременной биодеградации;
- увеличить биодоступность веществ с неоптимальными транспортными свойствами;
- преодолеть биологические барьеры, включая ГЭБ и стенки ЖКТ;
- осуществлять направленный транспорт ЛС (ткане- и/или мишень-специфичная доставка);
- обеспечить контролируемое высвобождение ЛС (обратный ответ, местная или удаленная активация);
- поддержать оптимальную терапевтическую концентрацию ЛВ;
- минимизировать побочные эффекты ЛВ и их метаболитов;
- обеспечить возможность визуализации очага патологического процесса, контроля взаимодействия ЛВ с целевыми биологическими мишенями и результатов лечения на клеточном уровне.
Уже сегодня разработаны новые ЛФ с обратным ответом, например, выделяющие инсулин в зависимости от концентрации глюкозы в крови [5]. Сравнительно недавно были разработаны наномолекулярные модификации камптотецина, ингибитора топоизомеразы, которые в значительной степени повышают его эффективность и селективность [6]. Основные типы транспортных частиц и их размеры представлены на рис. 1.
Рис. 1. Типы и размеры транспортных частиц для доставки ЛВ на основе полимеров, липидов, углеродных наночастиц и коллоидов
На сегодняшний день наибольшее распространение получили ЛФ продолжительного действия с увеличенной биодоступностью и пониженным побочным эффектом. Как правило, такие ЛФ представляют собой микрочастицы, созданные на основе биосовместимых и биоразлагаемых полимерных композиций, мицелл и липосом. ЛВ, не образующее ковалентных связей с носителем, может быть распределено в «теле» частицы, капсулировано, интегрировано в отдельных областях частицы, например, в виде условного комплекса «гость-хозяин» на основе дендримеров, или адсорбировано на его поверхности. Частица также может быть покрыта дополнительным слоем полимера, например, на основе липосом с включением молекул полиэтиленгликоля (ПЭГ) и дендримеров [7, 8]. Также разработаны транспортные системы на основе полимерных мицелл [9]. На рис. 2 представлено образование некоторых типов полимера из мономера, который ковалентно связан с ЛВ, в результате различных химических реакций.
Рис. 2. Принципиальная схема образования различных типов полимер-ЛВ комплексов
Активация действующего вещества происходит при разрыве химической связи полимер-ЛВ. Таким образом, зная природу и свойства такой связи, а также характер поведения полимера в организме, можно регулировать выделение лекарственного вещества [10, 11].
Показательным примером ЛФ на основе ковалентно-связанного ЛВ с наночастицей (фуллерен С60) может служить транспортная форма широко используемого противоопухолевого агента – паклитаксел [12]. Использование такой ЛФ связано с целым рядом преимуществ, например значительным увеличением периода полураспада коньюгата в сыворотке, который составляет около полутора часов (рис. 3).
Рис. 3. Биоразложение коньюгата С60-паклитаксел
Состав и конструкция ЛФ являются компромиссом между жёсткими требованиями к ЛФ и уровнем развития современных технологий. Требования, предъявляемые к ЛФ, зависят от следующих основных факторов:
- вида заболевания;
- локализации очага патологического процесса;
- свойств ЛС;
- способа введения препарата;
- наличия дополнительных требований.
В табл. 1 представлены основные требования, предъявляемые к ЛФ, в зависимости от вида заболевания, а также возможные пути решения поставленных задач, с привлечением передовых микро- и нанотехнологий. Одной из наиболее важных задач является оптимизация липофильности транспортных частиц, которая связана с проникновением через биологические барьеры [1]. Способ введения ЛС часто является определяющим фактором в процессе создания новых ЛФ, с учётом возможности выбора средства лечения. Химические и физико-химические свойства ЛС так же накладывают определённые требования и ограничения на состав и конструкцию транспортных частиц и ЛФ в целом [1, 2].
Таблица 1. Основные требования к ЛФ и возможные технологические решения
Заболевания
Основные требования к ЛФ
Технологические решения
Злокачественные опухоли
Необходимость увеличения эффективности ЛС и снижения его токсичности.
Необходимость тканеспецифичности и улучшения степени проникновения в опухолевые клетки.
Наночастицы с размерами от 50 до 200 нм, липосомы, мицеллы, ПЭГ-содержащие липосомы.
Инфекционные заболевания
Необходимость увеличения эффективности и тканеспецифичности. Снижение токсичности.
Улучшение степени проникновения в клетки (макрофаги, дендритные кленки и др.) и всасывания через слизистые оболочки ЖКТ.
Защита от биодеградации (антигенные пептиды).
Наночастицы различных размеров, липосомы, мицеллы, ПЭГ-содержащие липосомы, а также антиген-содержащие ЛФ.
Метаболические заболевания
Защита от биодеградации (пептиды и протеины).
Улучшение всасывания через слизистые оболочки ЖКТ.
Контролируемое и непрерывное выделение.
Системы с обратным ответом.
Наночастицы и липосомы.
Аутоиммунные болезни
Контролируемая доставка к мишеням иммунной системы и/или к клеткам очага воспаления.
Контролируемое и непрерывное выделение.
Болевые синдромы
Контролируемое и непрерывное выделение.
Улучшение биодоступности для ЦНС.
Липосомы, ЦНС специфичные липосомы и наночастицы, твёрдые липидные наночастицы.
Генетические заболевания
Защита от биодеградации, упаковка ДНК, улучшение клеточного захвата.
Специфичность к цитоплазматическим/ядерным внутриклеточным областям.
Катионные наносферы, полимеры, липиды, наногели и нанокапсулы.
Возможность проникновения через биологические барьеры и тканеспецифичность может быть достигнута за счёт подбора размеров и поверхностных свойств транспортных частиц. Как было показано ранее, оптимальный размер частиц находится в интервале 10-300 нм [3, 13]. Наночастицы с размерами от 50 до 200 нм обладают специфичностью к большинству опухолевых тканей [3]. Размеры частиц влияют не только на их транспортную функцию и специфичность, но и на скорость выделения ЛВ при прочих равных условиях [13]. Тканевая и клеточная специфичность могут быть достигнуты за счёт применения более сложных модификаций транспортной частицы, например, изменением её заряда [1, 13] или интеграции на её поверхность специализированных транспортных белков (моноклональные антитела, пептидные гормоны, онкофетальные белки, «троянские» пептиды и пр.) [1, 2]. Захват частицы клеткой – эндоцитоз, – может осуществляться по неспецифическому или рецептор-опосредованному механизму [14]. Наиболее распространен рецептор-опосредованный эндоцитоз, общий механизм которого представлен на рис. 4.
Рис. 4. Основные этапы рецептор-опосредованного эндоцитоза
Примечание.
1 – Связывание специфического лиганда с поверхностным рецептором.
2 – Формирование окаймленной ямки.
3 – Образование клатриновой везикулы.
4-6 – Внутриклеточная утилизация.
В качестве примера дополнительных возможностей передовых ЛФ можно указать возможность визуализации очага патологического процесса и контроля протекания лечения на клеточном уровне [15, 16]. Такой подход был разработан в процессе создания диагностических препаратов. Он основан на использовании специфических маркёров (изотопы, органические красители, квантовые точки и т.д.). Интеграция нетоксичных (слаботоксичных) маркёров в транспортные частицы позволяет существенно сократить время на создание новой ЛФ, а при её непосредственном использовании учитывать эффективность и особенности процесса лечения. Для разработки и контроля действия такой ЛФ может быть использован флуоресцентный томограф (ФТ), являющийся наиболее приемлемым технологическим решением, отвечающим предъявляемым критериям безопасности, качества и простоты использования, а также по соотношению цена/качество в экспериментах in vivo, с использованием мелких лабораторных животных. Общий принцип действия активируемых проб представлен на рис. 5. Используемый в ИИХР ФТ KODAK Image Station In Vivo FX System позволяет визуализировать информацию, полученную с применением метода рентгеновской и флуоресцентной томографии. В качестве визуализирующих агентов могут быть использованы наночастицы KODAK X-SIGHT Imaging Agents размером 16-17 нм.
Рис. 5. Концепция и принцип действия активируемых проб
Основные преимущества использования наночастиц для оптической визуализации в экспериментах in vivo представлены в табл. 2.
Таблица 2. Оптические и биохимические свойства агентов для оптической визуализации in vivo
Показатели
Органические флуоресцентные маркёры
Квантовые точки
Нанокристаллы
Оптические свойства
Абсорбция /эмиссия/длина волны
слабая ИК область (Cy5/Cy7)
зависит от размера (регулируемая)
регулируемая (преобразование с повышением частоты)
очень короткое (1-50 нс)
короткое (»100 нс)
длительное (более 200 нс)
Биохимические свойства
Возможность функциональной интеграции
различная в зависимости от типа маркера
различная в зависимости от pH среды
(на стадии определения)
различная в зависимости от типа маркера
Как показано в табл. 2, наночастицы являются наиболее удобным и безопасным средством визуализации очага патологического процесса.
Необходимо отметить, что наряду с вышеперечисленными ЛФ, существует целый ряд других, таких как энтеральные и парентеральные ЛФ, имплантируемые и трансдермальные системы и другие [1, 2].
Разработка новых ЛФ в ИИХР
Создание новых, оригинальных ЛВ и ЛФ в ИИХР в первую очередь обусловлено запросами отечественных производителей ЛС и общей государственной политикой в области отечественной фармацевтической промышленности, разработок и исследований. В начале 2006 г. в ИИХР было сформировано специальное подразделение, оснащённое передовыми техническими средствами и методами, направленными на исследование и создание инновационных ЛВ и ЛФ. Высококвалифицированные учёные ИИХР уже сегодня разрабатывают новые эффективные ЛФ для некоторых анальгетиков, антибактериальных и противоопухолевых лекарственных препаратов. В этом году планируется разработка ЛФ, предназначенной для лечения заболеваний ЦНС.
Показательным примером недавних достижений ИИХР в рассматриваемой области является создание эффективной пероральной ЛФ парацетамола. Парацетамол относится к числу общедоступных ненаркотических анальгетиков, широко востребованных на фармацевтическом рынке медицинских препаратов. Однако с учётом сравнительно слабых фармакологических и фармакодинамических показателей, применение этого лекарства связано с определёнными недостатками и неудобствами. В связи с этим на основе парацетамола разрабатываются новые ЛФ продолжительного действия с применением специальных биополимерных матриц, достоинства которых были описаны выше.
Использованная в ИИХР методика изготовления ЛФ базируется на применении стандартной субстанции парацетамола с размером частиц ≈100 мкм. С помощью механического диспергирования при комнатной температуре, а также в среде жидкого азота специалистами ИИХР были получены два типа измельчённого порошка парацетамола с размерами кристаллов ≈10 и ≈1 мкм. Для получения наночастиц размером ≈0,2 мкм использовалась методика, основанная на замораживании разбавленного водного раствора парацетамола с последующей сублимационной сушкой и специальным механическим измельчением при комнатной температуре. Микрочастицы препарата анализировались при увеличении 700-2000 раз с помощью прецизионного светового микроскопа Axiolab Pol (Carl Zeiss Jena GmbH). Измерения с максимальным увеличением осуществлялись в иммерсионном масле. Для оценки размеров частиц лекарственной субстанции, измельчённой до нанометрового размера, использовали сканирующий зондовый микроскоп Solver P47 (НТ-МДТ). Исследование проводилось в режиме прерывисто-контактной атомно-силовой микроскопии на воздухе, с использованием зондовых датчиков серии NSG11 (НТ-МДТ) с номинальными жёсткостью балок 5,5 и 11,5 Н/м и резонансной частотой 150 и 255 кГц, соответственно. Радиус закругления окончания зонда составлял не более 10 нм, а конический угол при вершине зонда 22°. Сканирование проводили с частотой около 1 Гц с разрешением 512´512 точек.
На следующем этапе работы с применением метода фазовых переходов изготавливались композиционные твёрдые смеси на основе частиц парацетамола различного размера с биосовместимыми и биодеградируемыми полимерными матрицами с целью создания новой пероральной ЛФ продолжительного действия. Использованные при этом методика и материалы являются ноу-хау ИИХР. В результате удалось разработать ЛФ парацетамола с размерами частиц 0.2, 1 и 10 мкм на основе особой биополимерной матрицы.
Изучение фармакокинетических характеристик полученных лекарственных форм парацетамола микрометрового размера проводилось на 9 кроликах самцах породы Шиншилла весом 3 кг согласно протоколу исследования (табл. 3). Исследования фармакокинетики препаратов, содержащих парацетамол с размером частиц ≈ 200 нм, осуществляются в настоящее время.
Таблица 3. Протокол исследования новых ЛФ парацетамола, разработанных в ИИХР
Источник


