Маркировка медицинских и фармацевтических товаров
Все потребительские товары, в том числе медицинские и фармацевтические, должны нести определенную товароведческую информацию, предусмотренную соответствующей НТД. Эта информация реализуется в маркировке.
Маркировка (маркирование) — нанесение на продукцию, тару, упаковку условных рисунков, цифровых, буквенно-числовых или символических знаков, обозначающих наименование предприятия-изготовителя, его местонахождение и подчиненность, марку, сорт изделия и др._
Маркировка (нем. mark — знак, markiren — обозначать, отличать знаком) — это обязательная информация, нанесенная на изделие или упаковку в виде комплексов знаков или символов, характеризующих это изделие.
Маркировка подразделяется на потребительскую и транспортную.
Маркировка потребительская применяется для обозначения различных типов, видов, марок продукции и ее соответствия ГОСТам и ТУ.
Маркировка транспортная содержит данные о перевозке продукции, способах обращения с товаром во время транспортировки.
Основные функции маркировки представлены на К ним относятся информационная, идентифицирующая, мотивационная и эмоциональная функции.
Основные функции маркировки
Основные функции маркировки
Информационная функция состоит в предоставлении нужной информации о товаре, об ответственном субъекте рынка — производителе, а также в рекламе продукции.
Идентифицирующая функция маркировки позволяет определить соответствие продукции НТД, принадлежность к определенному ассортименту, виду, типу товаров, подтверждение гарантии определенного уровня качества.
Мотивационная функция заключается, во-первых, в том, что маркировка формирует мышление покупателей с ориентацией на данную товарную марку; во-вторых, по мере роста общественного признания товарной марки повышается престижность продукции, а это способствует и росту степени конкурентоспособности, и привлекательности данного товара для каналов сбыта.
Эмоциональная функция маркировки позволяет уменьшить влияние ценового фактора, так как потребитель может ориентироваться в различных товарах по маркам, что снижает коммерческий риск для них.
Маркировка наносится непосредственно на изделие или прикрепляется к нему в виде ярлыка, бирки, тканевой ленты и т.д.
Обычно в маркировке приводятся следующие данные:
— товарный знак предприятия-изготовителя;
— наименование и местонахождение предприятия-изготовителя;
— номер ГОСТ Р или ТУ;
— потребительские (технические и размерные) характеристики товара, артикул, сорт, цена, дата выпуска, номер контроля ОТК предприятия и т.д.
В случае необходимости в маркировку включают условные обозначения способов ухода за изделиями или материалами.
Особая роль в маркировке принадлежит товарному знаку. Часто заводы-изготовители имеют длинные названия, не совсем удобные для запоминания и оперативного использования в работе. Гораздо легче удержать в памяти условные обозначения в виде удобно произносимого слова или выразительного графического символа.
Товарные знаки применялись еще в Ассирии и Вавилоне, на каменных плитах высекались имена владельцев или строителей. С расширением ремесел их стали проставлять на товары для обозначения местонахождения изготовителя и охраны его прав на собственность и авторство. В России товарные знаки появились во времена Петра I в XVII—XVIII вв.
Товарная марка или товарный знак, приводимые в маркировке, — это имя, знак или символ (или сочетание их), идентифицирующие продукцию.
Можно встретить другое определение (В. Karlof, 1991).
Товарный знак — это слово, марка, символ или дизайн, которые отличают компанию и ее продукцию от других компаний и их продукции.
Функция товарного знака — способствовать маркетингу, т. е. созданию спроса. Устанавливая торговую марку, компания может формировать спрос без других дополнительных затрат на рекламу.
Применение товарных знаков в России регламентируется Законом РФ №3520-1 «О товарных знаках, знаках обслуживания и наименованиях мест происхождения товаров» (1992). Товарные знаки могут быть словесными, изобразительными, объемными, комбинированными и т.д.
Товарные знаки выполняют правовые и экономические функции —
являются гарантией качества производителя, рекламой и т.д.
Зарегистрированный товарный знак сопровождается латинской буквой ® в круге. Регистрация товарного знака действует в течение 10 лет, но срок может быть продлен по заявлению владельца. На зарегистрированный товарный знак выдается лицензия, которая может
быть продана, что вызывает смену его владельца. Применение товарного знака без разрешения владельца не допускается, так как он находится под правовой защитой.
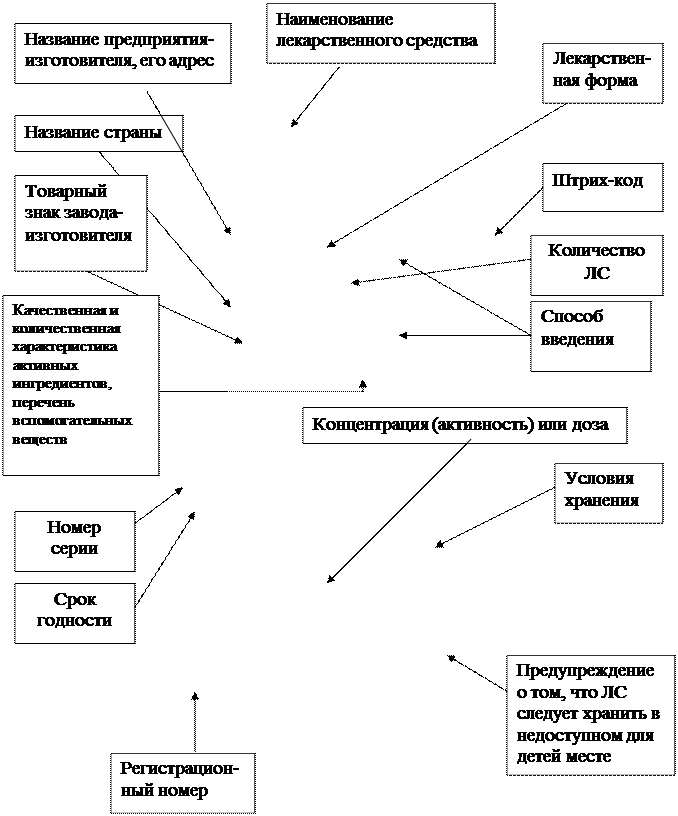
В перечень обязательных маркировочных данных для МФТ входят:
Регистрационный номер — это номер государственного регистрационного удостоверения. Его принято обозначать буквой Р, за которой следуют цифры, указывающие год регистрации ЛС в приказе МЗ РФ; далее через точки указываются номера этого приказа и пункта, относящегося к данному ЛС. Например, регистрационный номер капель «Уролесан» имеет следующий вид: Р 81.761.11; это означает, что препарат утвержден приказом МЗ в 1981 г., номер приказа 761, пункт 11. Группы цифр могут также разделяться косой чертой, например Р81/761/11.
Составной частью маркировки медицинских изделий является клеймо-знак, удостоверяющий качество изделия (ОТК, номер браковщика, личное клеймо, проба металла и т.д.). Клеймо информирует, что изделие подвергнуто контролю, проверено работниками ОТК; оно удостоверяет определенные свойства изделия, материалы, из которых оно изготовлено; подтверждает, что изделие подвергнуто испытаниям согласно установленным правилам.
Серией, согласно ОСТ «Стандарты качества лекарственных средств. Основные положения», называется определенное количество ЛС, полученного в результате одного технологического процесса.
Серия означает, как правило, производственный номер ЛС завода-изготовителя и время его выпуска. Каждой промышленной партии выпускаемой продукции присваивается заводская серия, которая маркируется не менее, чем 5-10 цифрами (большей частью 6-7 знаков).
Номер серии обозначается арабскими цифрами слитно, слово «серия» не проставляется. Последние четыре цифры в номере обозначают месяц и год изготовления ЛС. Цифры, предшествующие последним четырем, являются производственным номером серии.
0601 — июнь 2001 — дата изготовления,
2735 — производственный номер серии.
При производстве ЛС в 2000 г. дата изготовления проставлялась шестью цифрами.
062000 — июнь 2000 г. — дата изготовления,
2735 — производственный номер серии.
При недостаточном печатном поле на упаковке допускалось дату изготовления в 2000 г. указывать четырьмя цифрами.
0600 — июнь 2000 г. — дата изготовления,
2735 — производственный номер серии.
Маркировка сроков годности. Под воздействием внешних факторов (температура, свет и т.п.) происходит разложение и инактивация ЛС, при этом могут образовываться неактивные, более токсичные и даже ядовитые продукты. Поэтому для всех ЛС установлен срок годности.
Срок годности — это период времени, в течение которого ЛС должно полностью отвечать всем требованиям соответствующего Госу-дарственного стандарта качества._
В течение срока годности ЛС должны полностью сохранять свою терапевтическую активность, безвредность и удовлетворять всем требованиям НТД, в соответствии с которой были выпущены и хранились в условиях, предусмотренных этой документацией.
Срок годности исчисляется в месяцах и/или годах и определяется путем вычитания даты выпуска из даты срока хранения, обозначаемой на упаковке.
Срок хранения — календарная дата на индивидуальной упаковке ЛС, до которой его свойства при условии правильного хранения должны отвечать требованиям стандарта качества._
После этой даты ЛС не подлежит употреблению. Чаще всего для ЛС заводского изготовления срок годности равен 2—5 годам, но могут быть и более длительные сроки — до 10 лет, а также менее длительные — 6 мес., 1 год, 1,5 года, 3 года. Срок годности от 1 до 3 лет считается ограниченным. Срок годности можно определить по маркировке. В настоящее время маркировка сроков годности ЛС осуществляется в соответствии с Методическими указаниями МЗ РФ МУ 9467-015-05749470-98 «Графическое оформление лекарственных средств. Общие требования».
После слов «годен до. » римскими цифрами проставляется месяц, а арабскими 2 последние цифры года. Например, годен до декабря 2002 г. — XII.02.
Если в НТД на ЛС указано «препарат контролируется ежегодно» или «активность контролируется ежегодно», то на упаковке вместо «годен до. » делается соответствующая надпись.
Если препарат имеет срок годности более 3-х лет, маркировка «годен до. » не наносится.
Источник
Регистрационный номер — кодовое обозначение, присвоенное лекарственному препарату при его государственной регистрации. (ФЗ № 61 от 12.04.2010 г)
Регистрационное удостоверение лекарственного препарата — документ, подтверждающий факт государственной регистрации лекарственного препарата. (ФЗ № 61 от 12.04.2010 г)
При первой регистрации препарата в России регистрационное удостоверение выдается на 5 лет.
По истечении данного срока производитель подает документы для подтверждения регистрации препарата и тогда уже регистрационное удостоверение выдается бессрочно.
Держатель или владелец регистрационного удостоверения лекарственного препарата — разработчик лекарственного средства, производитель лекарственных средств или иное юридическое лицо, обладающее правом владения регистрационным удостоверением, которые несут ответственность за качество, эффективность и безопасность лекарственного препарата.
(ФЗ № 61 от 12.04.2010 г)
СТАНДАРТИЗАЦИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
В соответствии с ФЗ № 61 от 12.04.2010 г.:
Качество лекарственного средства — соответствие лекарственного средства требованиям фармакопейной статьи либо в случае ее отсутствия нормативной документации или нормативного документа.
Безопасность лекарственного средства — характеристика лекарственного средства, основанная на сравнительном анализе его эффективности и риска причинения вреда здоровью.
Эффективность лекарственного препарата — характеристика степени положительного влияния лекарственного препарата на течение, продолжительность заболевания или его предотвращение, реабилитацию, на сохранение, предотвращение или прерывание беременности.
Стандартизация ЛС — разработка и применение унифицированных требований и методов исследования лекарственных форм (стандартов).
Стандарт качества ЛС — нормативный документ, содержащий перечень нормируемых показателей и методов контроля качества лекарственных средств, утверждаемый Министерством здравоохранения Российской Федерации (Минздравом России).
Стандарты качества ЛС подразделяются на две категории:
1) Государственные стандарты качества ЛС — Общая фармакопейная статья (ОФС) и Фармакопейная статья (ФС);
Фармакопейная статья предприятия (ФСП).
Общая фармакопейная статья — документ, утвержденный уполномоченным федеральным органом исполнительной власти и содержащий перечень показателей качества и (или) методов контроля качества конкретной лекарственной формы, лекарственного растительного сырья, описания биологических, биохимических, микробиологических, физико-химических, физических, химических и других методов анализа лекарственного средства.
Фармакопейная статья — документ, утвержденный уполномоченным федеральным органом исполнительной власти и содержащий перечень показателей качества и методов контроля качества лекарственного средства.
Фармакопейная статья предприятия — это стандарт качества
лекарственного средства на лекарственное средство под торговым названием, содержащий перечень показателей и методов контроля качества лекарственного средства производства конкретного предприятия, учитывающий конкретную технологию данного предприятия и прошедший экспертизу и регистрацию в установленном порядке.
Государственная фармакопея (ГФ) — это сборник государственных стандартов качества ЛС, имеющий законодательный характер.
СЕРТИФИКАЦИЯ И ДЕКЛАРИРОВАНИЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ И МЕДИЦИНСКИХ ИЗДЕЛИЙ.
С целью подтверждения соответствия товара определенному уровню качества, указанному в НТД, проводится сертификация и декларирование соответствия.
Объекты обязательной сертификации определяются Постановлением Правительства РФ № 982 от 1 декабря 2009 г.(ред. 18.06.2012 № 596) «Об утверждении единого перечня продукции, подлежащей обязательной сертификации, и единого перечня продукции, подтверждение соответствия которой осуществляется в форме принятия декларации о соответствии».
Обязательное подтверждение соответствия качества товара осуществляется в двух формах — путем обязательной сертификации, путем принятия декларации о соответствии.
ЛС относятся к видам продукции, несущим потенциальную опасность. Это объясняется тем, что некачественные или фальсифицированные лекарства могут принести вред здоровью.
В единый перечень продукции, подлежащий обязательной сертификации включенынекоторые виды товаров класса 9300 «Медикаменты, химико-фармацевтическая продукция и продукция медицинского назначения» Общероссийского классификатора продукции (ОКП):
— Сыворотки, иммуно- и гаммаглобулины, препараты из крови прочие и полученные методом генетической инженерии, применяемые в медицине;
— Вакцины, анатоксины и токсины, применяемые в медицине.
— Бактериофаги.
В единый перечень продукции, подтверждение соответствия которой осуществляется в форме принятия декларации о соответствии включены:
— Лекарственные средства, зарегистрированные в установленном порядке, (кроме указанных в предыдущем перечне);
— Оборудование медицинское;
Дата добавления: 2018-02-15 ; просмотров: 4309 ; Мы поможем в написании вашей работы!
Источник
Маркировка готовых лекарственных средств



Каждое ГЛС имеет определенное внешнее оформление: этикетку, которая наклеена непосредственно на упаковку, упаковочный лист, бандероль, инструкцию по медицинскому применению, в которой указан способ применения ГЛС.
Маркировка лекарственных средств в Украине должна соответствовать Закону Украине «О лекарственных средствах», ГСТУ 64-7-2000, и Приложению 9 к пункту 6.1 Порядка проведения экспертизы регистрационных материалов на лекарственные средства, подаваемых на государственную регистрацию (перерегистрацию), а также экспертизы материалов о внесении изменений к регистрационным материалам в течение действия регистрационного удостоверения, утвержденного Приказом №426 МЗ Украины от 26.08.2005 (с изменениями и дополнениями в последней редакции).
К требованиям графического оформления упаковки относятся:
§ информационная функция упаковки должна быть обеспечена четкой и контрастной печатью, возможностью легкого считывания информации;
§ производить эстетическое влияние на потребителя;
§ иметь высокий художественный и технологический уровень обеспечения маркировки.
На вторичной упаковке готового лекарственного средства, а при ее отсутствии – на первичной упаковке указываются такие сведения:
| |||||
| |||||
|
|
| |||
| |||||
|
|
| |||
|
| ||||
|
На первичной упаковке в виде блистера, первичной упаковке суппозиториев, тубе и т.п. приводится следующая информация:
 |
На первичной упаковке небольшого размера (ампулы, тюбик-капельницы, шприц-тюбика и т.п.), которая помещается во вторичную упаковку, приводятся такие данные:
Регистрационный номер лекарственных средств, зарегистрированных до августа 2003 г., содержит следующую информацию: буквы «Р» или «П» в зависимости от регистрационной процедуры означают регистрацию или перерегистрацию лекарственного средства соответственно, далее четыре цифры обозначают месяц и год регистрации, после риски пятизначное число показывает порядковый номер регистрации, который вносится в Государственный реестр лекарственных средств Украины.
 |
Согласно Приказу МЗ Украины № 358 от 29 июля 2003 г. регистрационный номер ЛС состоит из буквенного кода Украины «UA», после риски следует четыре цифры порядкового номера ЛС в Государственном реестре, затем по две цифры обозначений каждой новой лекарственной формы и каждой новой силы действия (т.е. каждой новой дозировки) конкретного ЛС. Дата регистрации и номер Приказа МЗ Украины указывается на листке-вкладыше, прилагаемом к ГЛС.
Номер серии ЛС обозначается арабскими цифрами. Слово «серия» не указывается. Последние четыре цифры номера означают месяц и год производства ЛС, цифры перед датой указывают производственный номер серии.
|
Номер серии лекарственного средства должен быть указан на первичной и вторичной упаковке.
Указание номера серии по-английски — Batch. Например:
В. № 020805 (учитывает месяц и год производства);
Ch.- В. 210053 (не учитывает месяц и год производства);
Charge — Nr.: 1530708, №. 0301108 (учитывает месяц и год производства)
В 0615 — месяц и год не учитываются.
В то же время, на упаковках импортных лекарственных препаратов дополнительно наносится дата изготовления (производства).
В английской транскрипции часто используется сокращенный вариант слова “Manufactured “ — “Mfd” — произведено (иногда “Mfg”). В немецкой транскрипции дата изготовления — Herstelldatum. Примеры обозначений даты производства:
Дата произв.: 08/07
Для лекарственных средств, изготовленных одним предприятием (в упаковке «ангро»), а расфасованных другим, указывается номер серии предприятия, которое фасовало лекарственное средство.

Рисунок 14.2. Графическое оформление вторичной упаковки ГЛС
Срок годности следует указывать: «Годен до . » или (при малых размерах печатного поля) — «до . » . Римскими цифрами указывается месяц, арабскими — две последние цифры года. Допускается отмечать месяц арабскими цифрами. Высота цифр должна быть не более 5 мм.
«Годен до X 2001″ («Годен до Х 2001») или «До X 2001» («До Х 2001») — определяет пригодность до октября 2001 года;
Допускается обозначение «Годен до X 01» («пригодный до Х 01») или «До Х 01″(«До Х 01»).
Для лекарственных средств, фасуемых в тубы, допускается обозначение срока годности на тубе.
Например – «Срок годности 2 года».
Для лекарственных средств, в форме капель, при необходимости, следует указывать срок годности лекарственного средства после раскрытия упаковки – «Срок годности после раскрытия . суток».
На упаковке лекарственного растительного сырья необходимо дополнительно указывать требования относительно условий и срока хранения приготовленного настоя.
В случаях маркировки комплекта антибиотика с растворителем, на пачке должен быть указан номер серии антибиотика и номер серии растворителя, а также срок годности лекарственного средства (антибиотика).
Если для лекарственного средства определен ежегодный контроль по показателям качества, то на упаковке указывают «Контролируется ежегодно».
Для лекарственных средств, содержащих сильнодействующие и ядовитые вещества, на потребительской упаковке указывают надпись-предупреждение «Применять по назначению врача».
Условия хранения указываются в соответствии с требованиями, определенными разработчиком лекарственного средства.
Штриховое кодирование, печать и размещение штрих-кодовых пометок на первичной и вторичной упаковке должно быть выполнено в соответствии с требованиями Национальных стандартов Украины и руководящих нормативных документов по штриховому кодированию товарной продукции.
Адрес предприятия-производителя должен быть указан полностью. Допускается не указывать полный адрес предприятия-производителя на первичной упаковке в случаях, если этикетка первичной упаковки имеет малые размеры печатного поля и название предприятия-производителя включает в себя информацию о местонахождении предприятия.
Вторичная упаковка и этикетка групповой тары должны содержать полный адрес предприятия-производителя.
Открытое акционерное общество «Фармак», г. Киев, ул. Фрунзе, 74;
ОАО «Фармак», г. Киев, ул. Фрунзе, 74;
ОАО «Фармак», г. Киев (при малых размерах печатного поля).
Акционерное общество «Киевмедпрепарат»,
г. Киев, ул. Саксаганского, 139;
АО «Киевмедпрепарат», г. Киев, ул. Саксаганского, 139.
АО «Киевмедпрепарат», (при малых размерах печатного поля).
Наименование лекарственного средства должно быть указано на украинском (и русском) и латинском (и/ или английском) языках.
Наименование лекарственного средства и международное непатентованное название должны выделяться среди всех других маркировочных надписей. Для этого используется более крупный и (или) жирный шрифт, контрастный цвет, выбирается удобное для прочтения место на этикетке или на одной из граней упаковки. Вокруг названия не должны располагаться надписи, затрудняющие прочтение названия.
С 1 января 2010 г. в силу вступили изменения к Закону Украины «О лекарственных средствах», обязывающий производителей лекарственных препаратов маркировать упаковку шрифтом Брайля,точнее, наносить на упаковку название препарата, дозы действующего вещества и формы лекарства.
Шрифт Брайля является методом передачи информации – то есть дает возможность пользователю прочитать тактильным способом текст, написанный на украинском, русском или другом языке.
Министерство здравоохранения Украины определяет лекарственные средства, упаковка которых не маркируется шрифтом Брайля или шрифтом Брайля указывается только название лекарственного средства.
К каждому реализуемому лекарственному средству, прикладывается инструкция о применении, которая должна содержать:
— наименование лекарственного средства;
— общую характеристику (химическое название, основные физико-химические свойства, состав);
— сведения о фармакологических свойствах;
— показания для применения;
— взаимодействие с другими лекарственными средствами;
Источник