- Как проверить легальность и регистрацию лекарства, БАДа?
- Как не купить пустышку и не легальный лекарственный препарат?
- Как проверить лекарство через Минздрав России?
- Как проверить лекарство на сайте Росздравнадзора?
- Как проверить БАДы на подлинность на сайте Роспотребнадзора?
- Как проверить лекарство и БАД через справочник лекарств РЛС?
- Лекарственные средства
- Счетчик обращений граждан и организаций
- Лекарственные средства
- Контроль качества лекарственных средств
- Информационные письма
- Лекарственные средства
- Счетчик обращений граждан и организаций
- Лекарственные средства
- Ввод в гражданский оборот лекарственных препаратов
- Информационные письма
- Электронные сервисы
- Нормативные документы
- Какие реестры Росздравнадзора необходимо использовать в работе и где их найти
- Проверяем легальность лекарств
- Мониторим брак
- Осуществляем фармаконадзор
- Разрешительные сервисы
- Ресурсы для контроля
Как проверить легальность и регистрацию лекарства, БАДа?
Каждый день появляются все новые лекарственные препараты их рекламируют по телевидению и в интернете, но не каждое, рекламируемое лекарство несет в себе ту пользу, которую так красочно расписывают в рекламе.
Как не купить пустышку и не легальный лекарственный препарат?
Каждое разрешенное в России лекарство, должно иметь государственную регистрацию Минздраве России и быть в реестре лекарственных средств. Зачем нужна регистрация лекарственных препаратов? Регистрируя препарат, государство берет на себя ответственность за проверку его эффективности и безопасности, плюс проводятся локальные клинические исследования, даже если они уже проводились в других странах.
Как проверить лекарство через Минздрав России?
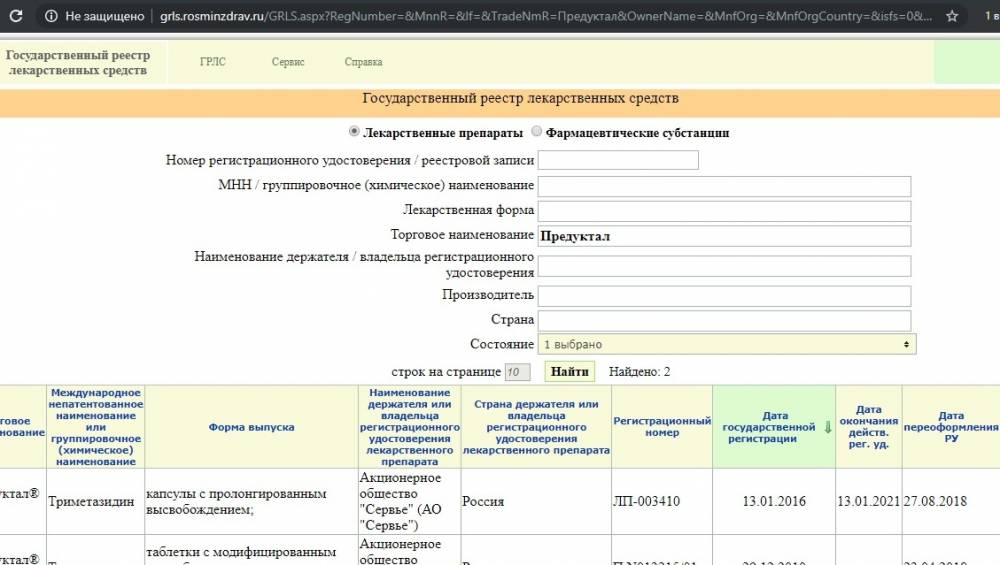
Государственный реестр лекарственных средств
Вводите торговое наименование и нажимаете найти. Если препарат есть реестре, то внизу вы увидите таблицу с данными всех производителей, форм выпуска, даты регистрации и т.п.
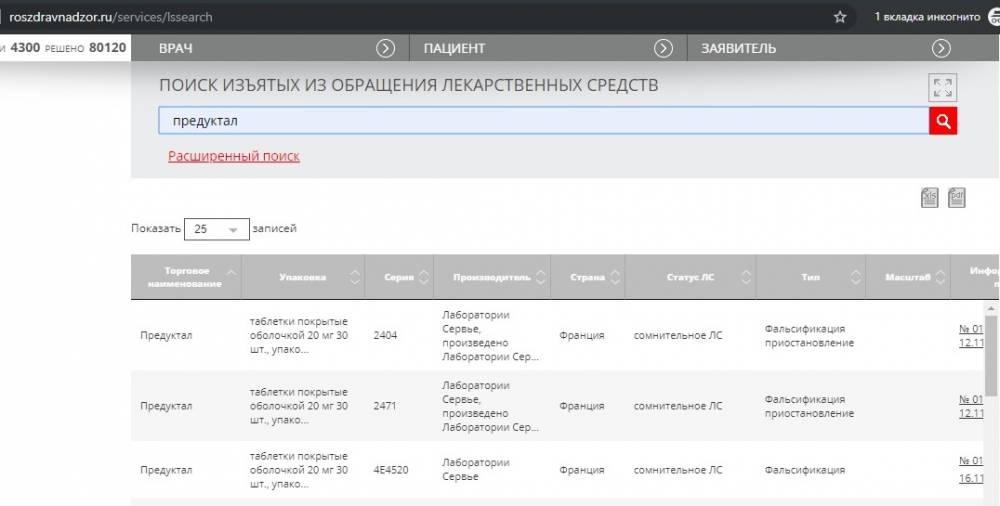
Как проверить лекарство на сайте Росздравнадзора?
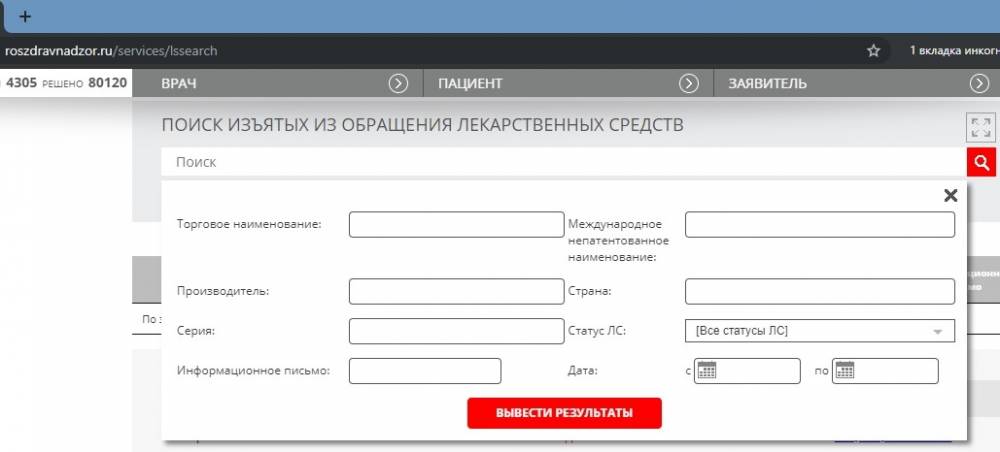
Используя поиск изъятых из обращения лекарственных средств, можно проверить лекарство на подлинность, на подделку. Для точного результата, нужно использовать «расширенный поиск» указывая серию, дату.
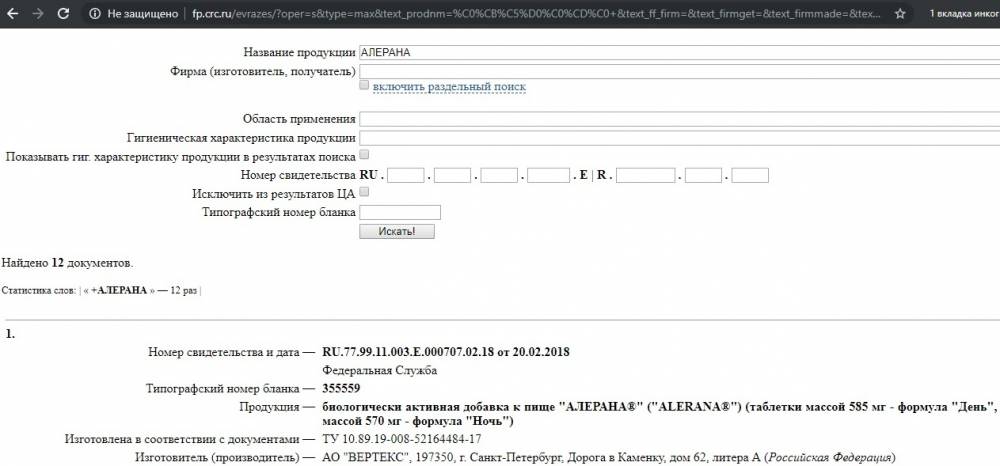
Как проверить БАДы на подлинность на сайте Роспотребнадзора?
БАД относится к компетенции Роспотребнадзора. Получить сведения о биологически активных добавках, прошедших государственную регистрацию и разрешенных к ввозу и обороту на территории Российской Федерации, можно на официальном сайте Роспотребнадзора.
Реестр свидетельств о государственной регистрации (единая форма Таможенного союза, российская часть).
Также там можно проверить и парфюмерно-косметическую продукцию и продукты питания и бытовую химию и многое другое. Если нажать «полный список» вы увидите весь перечень, проверяемых наименований.
Как проверить лекарство и БАД через справочник лекарств РЛС?
РЛС® — Регистр лекарственных средств России. Энциклопедия лекарств и товаров аптечного ассортимента
Здесь можно узнать является препарат лекарством или бадом, действующие вещества, наличие в аптеках. Причем если вы укажете в поиске действующее вещество, то получите полный список аналогов препаратов с данным веществом.
В нашем стремительно развивающемся мире и засилье информационных технологий, нужно быть на чеку. Не доверять красивой рекламе и красочной упаковке. Нужно искать информацию, отзывы, проверять все самому. Только так можно добиться безопасности и не попасться на удочку производителей контрафакта.
Источник
Лекарственные средства
Счетчик обращений граждан и организаций
Лекарственные средства
Контроль качества лекарственных средств
Постановлением Правительства Российской Федерации от 30.06.2004 № 323 «Об утверждении Положения о Федеральной службе по надзору в сфере здравоохранения» на Росздравнадзор возложены полномочия по федеральному государственному надзору в сфере обращения лекарственных средств посредством проведения проверок соответствия лекарственных средств установленным обязательным требованиях к их качеству, и выборочный контроль качества лекарственных средств.
В данном разделе размещены:
Рубрика «Нормативная документация», где можно ознакомиться с нормативными правовыми актами, которые регулируют требования к лекарственным средствам, находящимся в обращении.
Рубрика «Информационные письма», которая содержит письма Росздравнадзора о выявленных недоброкачественных, фальсифицированных лекарственных средствах; об отзыве лекарственных средств; об изменении дизайна упаковок лекарственных препаратов для медицинского применения; о подлежащих изъятию из оборота лекарственных средствах; о результатах проверок соответствия лекарственных средств, проведенных Росздравнадзором, а также о решениях Росздравнадзора о соответствии лекарственных средств установленным требованиям к их качеству и решениях Росздравнадзора, принятым по результатам выборочного контроля качества лекарственных средств.
Рубрика «Справочная информация», в которой опубликованы обобщенные сведения о результатах государственного контроля в сфере обращения лекарственных средств.
Информационные письма
Информационное письмо от 22.09.2021 № 01И-1204/21
Решение о соответствии лекарственных средств требованиям нормативной документации
Источник
Лекарственные средства
Счетчик обращений граждан и организаций
Лекарственные средства
Ввод в гражданский оборот лекарственных препаратов
Информационные письма
Информационное письмо от 25.03.2021 № 02И-373/21
О решении Комиссии Росздравнадзора по качеству ИЛП
Информационное письмо от 09.10.2020 № 01И-1927/20
О предоставлении информации в АИС Росздравнадзора
Информационное письмо от 17.09.2020 № 01И-1817/20
О решении Комиссии Росздравнадзора по качеству ИЛП
Информационное письмо от 25.06.2020 № 01И-1189/20
О проведении совещания по вводу в гражданский оборот иммунобиологических лекарственных препаратов
Информационное письмо от 02.06.2020 № 01И-1022/20
О решении Комиссии Росздравнадзора по качеству ИЛП
Информационное письмо от 16.04.2020 № 01И-678/20
О новых данных по безопасности лекарственных препаратов ранитидина
Информационное письмо от 18.03.2020 № 02И-471/20
О решении Комиссии Росздравнадзора по качеству иммунобиологических лекарственных препаратов
Информационное письмо от 17.02.2020 № 02И-312/20
О предоставлении информации в АИС Росздравнадзора
Информационное письмо от 28.11.2019 № 01И-2906/19
О вводе в гражданский оборот
Электронные сервисы
Нормативные документы
Приказ Росздравнадзора от 11.05.2021 № 4026
О внесении изменений в Административный регламент Федеральной службы по надзору в сфере здравоохранения по предоставлению государственной услуги по выдаче разрешения на ввод в гражданский.
Постановление Правительства Российской Федерации от 26.11.2019 № 1510
О порядке ввода в гражданский оборот лекарственных препаратов для медицинского применения
Приказ Росздравнадзора от 07.07.2020 № 5721
Об утверждении Административного регламента Федеральной службы по надзору в сфере здравоохранения по предоставлению государственной услуги по выдаче разрешения на ввод в гражданский оборо.
Приказ Росздравнадзора от 29.11.2019 № 8966
Об утверждении формы разрешения на ввод в гражданский оборот в Российской Федерации серии или партии произведенного в Российской Федерации или ввозимого в Российскую Федерацию иммунобиоло.
Приказ Росздравнадзора от 17.12.2019 № 9452
Об утверждении Порядка оценки объема испытаний качества иммунобиологических лекарственных препаратов Комиссией Федеральной службы по надзору в сфере здравоохранения по качеству иммунобиол.
Приказ Росздравнадзора от 29.11.2019 № 8967
«О Комиссии Федеральной службы по надзору в сфере здравоохранения по качеству иммунобиологических лекарственных препаратов» (вместе с «Положением о Комиссии Федеральной службы по надзору .
Федеральный закон от 28.11.2018 № 449-ФЗ
О внесении изменений в отдельные законодательные акты Российской Федерации по вопросу ввода в гражданский оборот лекарственных препаратов для медицинского применения
Источник
Какие реестры Росздравнадзора необходимо использовать в работе и где их найти
Дистанционные технологии плотно вошли в жизнь аптек и их контролеров. На смену бумажным лицензиям пришли онлайн-реестры, для поиска брака больше не нужны специальные журналы. Росздравнадзор переходит к реестровым моделям представления обязательной для исполнения информации по контролю за обращением лекарств и медизделий. Рассмотрим, какие сервисы «лекарственного ревизора» нужны аптеке в работе.
Проверяем легальность лекарств
Наиболее востребованными в повседневной практике аптекарей стали сервисы по проверке качества лекарственных препаратов и медицинских изделий.
В конце 2019 года изменились правила поступления лекарств в гражданский оборот. Вместо привычных деклараций и сертификатов качество препаратов стали подтверждать непосредственно в Росздравнадзоре. Лекарства могут легально обращаться на рынке с момента появления данных о конкретных сериях в одном из реестров:
- «Сведения о лекарственных средствах, вводимых в гражданский оборот в Российской Федерации» 1 — для лекарственных препаратов;
- «Реестр разрешений на ввод в гражданский оборот иммунобиологических лекарственных препаратов» 2 — для иммунобиологических препаратов.
Мониторим брак
Решения по качеству и обращению аптечных товаров Росздравнадзор принимает в форме писем, которые размещает в одноименных разделах своего сайта.
Информация о забраковке лекарств аккумулируется в специальном сервисе «Поиск изъятых из обращения лекарственных средств», попасть на который можно по ссылке https://roszdravnadzor.gov.ru/services/lssearch. Используя простой поиск, можно по названию, серии или производителю провести ревизию аптечного ассортимента на наличие запрещенных к продаже препаратов.
Для оптимизации работы можно воспользоваться расширенным поиском, который позволяет искать по нескольким критериям одновременно. Например, вводить названия, серии и производителей только тех товаров, которые есть в аптеке. Поля для ввода дат позволяют получить данные о приостановке или изъятии недоброкачественных, фальсифицированных или контрафактных лекарств за конкретный период. Сервис также позволяет выгружать базу данных в удобном табличном формате. В умелых руках программистов такая база может быть легко интегрирована в аптечную систему и упростит сотрудникам процессы по отслеживанию брака.
Проверка качества препаратов не ограничивается только решениями о браке. Используя сервис «Поиск писем по контролю качества лекарственных средств», аптекари могут получать оперативную информацию об изменениях дизайнов упаковок препаратов, о результатах экспертизы отдельных серий лекарств в ходе выборочного контроля, другую важную информацию об их обращении.
Для поиска запрещенных к обращению медицинских изделий предусмотрен электронный ресурс «Информационные письма о медицинских изделиях» (https://roszdravnadzor.gov.ru/services/unreg). С помощью данного сервиса фармработники могут своевременно выявить и переместить в карантин незарегистрированные, недоброкачественные, фальсифицированные и контрафактные медизделия.
Осуществляем фармаконадзор
Помимо качества аптечной продукции фармацевты и провизоры должны уделять внимание вопросам безопасности лекарств и медицинских изделий. Обязанность по осуществлению фармаконадзора в отношении указанных групп аптечных товаров предусмотрена ФЗ № 323 «Об основах охраны здоровья граждан» и ФЗ № 61 «Об обращении лекарственных средств».
С новыми данными по безопасности шприцев, тонометров и прочих медизделий аптечные работники могут ознакомиться в разделе сайта «Информационные письма о медицинских изделиях». Данные о побочных реакциях на лекарственные препараты служба публикует в специальном подразделе «Мониторинг эффективности и безопасности лекарственных препаратов» 3 .
Знания о безопасности медицинских товаров можно и нужно использовать при аптечном консультировании покупателей.
Часто аптеки становятся своеобразным «входным» окном для коммуникации с пациентами в вопросах эффективности лекарств. Правилами фармаконадзора предполагается, что аптеки должны не только ретранслировать медработникам и фармпроизводителям жалобы, поступающие от пациентов на действие препаратов, но и самостоятельно фиксировать в учетной системе Росздравнадзора или направлять карты-извещения в службу. Для передачи данных нужно пройти несложную регистрацию в автоматизированной системе «Фармаконадзор» 4 .
Разрешительные сервисы
В прошлом году Росздравнадзор продолжил диджитализацию разрешительных сервисов. В первую очередь нововведения касаются вопросов дистанционной торговли лекарствами. Заявление по государственной услуге «Разрешение на дистанционную торговлю лекарственными препаратами» можно подать на официальном сайте Росздравнадзора в разделе «Электронные сервисы» (https://roszdravnadzor.gov.ru/services). Принятые территориальными органами разрешения публикуются в «Реестре выданных разрешений на дистанционную торговлю лекарственными препаратами» 5 .
С переходом на реестровую модель лицензирования возрастает значение «Единого реестра лицензий». С нового года лицензирующие органы перестали выдавать бумажные лицензии, заменив их внесением сведений в единый реестр. От корректности внесенных в реестр данных зависит их интеграция с системой мониторинга движения лекарственных препаратов (ФГИС МДЛП). Также с помощью данного ресурса нужно будет проверять актуальность фармлицензии у дистрибьютора.
Без использования в повседневной практике «Государственного реестра медицинских изделий и организаций (индивидуальных предпринимателей), осуществляющих производство и изготовление медицинских изделий» 6 невозможно правильно организовать оборот данных товаров в аптеке. Приемочный контроль поступающих расходников и медицинских аппаратов должен включать в себя проверку сопроводительных документов и маркировки самих медизделий на соответствие данным государственного реестра.
Особое внимание необходимо уделять подразделу «Наименование медицинского изделия» реестровой записи о конкретном товаре. Отсутствие конкретного вида медизделия в данном реестре при контроле рассматривается как нарушение, а сам товар признается незарегистрированным медизделием.
Ресурсы для контроля
Информационное обеспечение сайта позволяет значительно упростить подготовку к проверочным мероприятиям надзорного органа.
В разделе «Контроль и надзор» 7 размещаются актуальные планы по ежегодному контролю субъектов фармацевтического рынка.
Реформа контрольно-надзорной деятельности изменила подходы к формированию планов проверок. Попадание той или иной аптеки в план зависит от присвоенной ей категории риска, рассчитать который можно самостоятельно с помощью электронного калькулятора 8 , а затем проверить в реестре 9 .
Также на сайте публикуется «Перечень нормативных правовых актов (их отдельных положений)» 10 , за нарушение которых аптеку могут привлечь к административной ответственности.
Источник