— 3 — Механизмы проникновения лекарственных веществ через биомембраны
Молекулы лекарственных веществ через биологические мембраны могут проникать различными способами:
Пассивная диффузия — транспорт через биологические мембраны, вызванный движением частиц, например под влиянием тепла и разности концентраций транспортируемого вещества по обе стороны мембраны. С участием пассивной диффузии транспортируются, например, лекарственные вещества, являющиеся слабыми органическими кислотами (кислота ацетилсалициловая, кислота бензойная) и слабыми органическими основаниями (амидопирин, аминазин).
Облегченная диффузия – это транспорт лекарственных веществ осуществляется с участием молекул специфических переносчиков. Как и при пассивной диффузии, перенос веществ происходит по концентрационному градиенту, но скорость выше, чем при простой диффузии. Транспорту путем облегченной диффузии подвергаются клеточные метаболиты, поступающие из плазмы крови (глюкоза и другие моносахариды, аминокислоты, витамины и др.).
Обменная диффузия — молекулы переносной системы транспортируют молекулы лекарственных веществ на противоположную сторону мембраны, а сами образуют комплекс с другой молекулой подобной структуры и переносят ее на внешнюю сторону мембраны, т.е. в межклеточное пространство.
Активный транспорт — это перенос молекул лекарственных веществ через биомембраны против градиентов их концентраций, сопряженный с затратой энергии (транспорт в фолликулы щитовидной железы из плазмы крови).
Пиноцитоз — это адсорбция, осуществляемая путем выпячивания (инвагинации) поверхности биомембраны с последующим образованием везикулы вокруг транспортируемого вещества, как при фагоцитозе (захват макромолекул — белки и нуклеиновые кислоты с диаметром частиц не более 750 нм), жирные кислоты и жирорастворимые витамины.
Липосомы — лекарственная форма, представляющая собой фосфолипидные пузырьки с включенными в их полость лекарственными и биологически активными веществами.
Распределение лекарственных веществ в организме.
Большинство лекарственных веществ в организме животных распределяется неравномерно. Лекарственные вещества достигают концентрации, обеспечивающей эффективные изменения за разное время в различных органах и тканях. Это объясняется наличием гистогематических барьеров (стенка капилляров, клеточные мембраны, гематоэнцефалический и плацентарный барьеры и др.), функциональным состоянием и кровоснабжением органа, сродством молекул лекарственных веществ с биохимическими структурами органов и тканей.
При отдельных патологических состояниях ослабляются существующие в норме барьеры и возникают патологические барьеры за счет разрастания соединительной ткани вокруг очагов воспаления.
Важным фактором в распределении лекарственных веществ является образование комплексов белок — молекула лекарственных веществ. Они образуются в крови, межклеточных пространствах, в цитоплазме, иногда в ядре (сульфаниламиды, антибиотики и др.).
Связывание лекарственных веществ с белками уменьшает терапевтический эффект, замедляет выведение их из организма, а также участие в процессах биотрансформации, так как в этих процессах могут принимать участие только свободные молекулы.
Некоторые лекарственные вещества в больших количествах аккумулируются в тканях и органах. Например, мышьяк депонируется в волосяном покрове, йод — в щитовидной железе, хром — в эритроцитах. Наркотические вещества обладают липотропным действием, и поэтому депонируются в местах сосредоточения липидов. Кумуляция лекарственных веществ используется в терапевтической и диагностической практике.
Следует учитывать, что накопление лекарственных веществ в определенных органах и тканях может оказывать специфическое действие только при наличии в данной ткани внутриклеточных рецепторов, с которыми и может взаимодействовать лекарство или биологически активное вещество.
Источник
Основные механизмы проникновения лекарства через биологические мембраны. Факторы, влияющие на процессы абсорбции лекарств.
Если лекарственное средство не было введено непосредственно в кровоток, то для того, чтобы оказать системное действие лекарство должно всосаться (абсорбироваться) из места инъекции (введения). Процесс абсорбции вещества представляет собой, фактически, процесс его переноса через биологические мембраны. Все лекарственные средства абсорбируются (транспортируются) через биологические мембраны 4 принципиальными способами:
Фильтрацией (водной диффузией);
Пассивной диффузией (липидной диффузией);
Транспортом при помощи специфических переносчиков;
Эндоцитозом и пиноцитозом.
Фильтрация (водная диффузия).Представляет собой перемещение молекул вещества по градиенту концентрации через заполненные водой поры, которые существуют в мембране каждой клетки, а также между соседними клетками. Процесс протекает без затрат энергии, т.е. является пассивным. Диаметр пор, по которым осуществляется, водная диффузия, равен 0,35-0,4 нм, поэтому процессу фильтрации могут подвергаться лекарства с молекулярным весом не более 100-200 Да. Фильтрация не является основным путем абсорбции лекарств.
Процесс фильтрации подчиняется закону диффузии Фика:

Скорость диффузии – количество переносимых в единицу времени молекул лекарства;
С1 — концентрация вещества снаружи мембраны;
С2 — концентрация вещества изнутри мембраны.
Как следует из этого закона, фильтрация лекарства тем выше, чем больше его концентрация в месте введения и площадь абсорбции. Например, площадь абсорбируемой поверхности в кишечнике несоизмеримо больше, чем площадь слизистой оболочки желудка, поэтому и абсорбция вещества в кишечнике будет протекать более быстро, чем в желудке. С другой стороны, чем более «толстая» биологическая мембрана, тем медленнее через нее проникают лекарства. Например, толщина барьера в альвеолах легких значительно меньше, чем толщина кожи, поэтому и скорость абсорбции в легких будет выше, чем в коже.
Липидная диффузия.Представляет собой процесс растворения лекарства в липидах мембраны и движение через них. Этот путь абсорбции также подчиняется закону Фика, но он не зависит от размеров лекарственного вещества, а определяется лишь их липофильностью. Наиболее липофильными являются незаряженные молекулы. Липидная диффузия – основной путь абсорбции лекарств.
Все лекарственные средства можно рассматривать как слабые кислоты или слабые основания, которые имеют свои значения константы ионизации (рК). Если значение рН среды равно значению рК лекарства, то 50% его молекул будет находится в ионизированном и 50% в неионизированном состоянии и среда для лекарства будет нейтральной.
Схема 1. Распределение лекарственного средства между его ионизированной и неионизированной формами зависит от рН среды и рК лекарственного средства. Для наглядности гипотетическое лекарственное средство представлено со значением рК=6,5. R—COOH – слабая кислота, R—NH2 — слабое основание.
В кислой среде (если рН меньше рК), там где имеется избыток протонов, слабая кислота будет находиться в недиссоциированной форме (R-COOH), т.е. будет связана с протоном – протонирована. Такая форма кислоты незаряжена и хорошо растворима в липидах. Если рН сместиться в щелочную сторону (т.е. рН станет больше рК), то кислота начнет диссоциировать и лишится протона, перейдя при этом в непротонированную форму, которая имеет заряд и плохо растворима в липидах.
R
протонированное основание (заряженное, более водорастворимое)
R
протонированная кислота (незаряженная, более растворима в липидах)
непротонированное основание (незаряженное, более растворимо в липидах)
непротонированная кислота (заряженная, более водорастворимая)
В щелочной среде, там где имеется дефицит протонов, слабое основание будет находиться в недиссоциированной форме (R-NH2), т.е. будет непротонировано и лишено заряда. Такая форма основания хорошо растворима в липидах и быстро абсорбируется. В кислой среде имеется избыток протонов и слабое основание начнет диссоциировать, связывая при этом протоны и образуя протонированную, заряженную форму основания. Такая форма плохо растворима в липидах и слабо абсорбируется.
Следовательно, абсорбция слабых кислот протекает преимущественно в кислой среде, а слабых оснований – в щелочной.
На схеме 2 показано, как повлияет изменение рН различных биологических жидкостей на абсорбцию слабой кислоты с рК=3,5 и слабого основания с рК=7,0.
Схема 2. Этапы движения лекарственного вещества в организме. Слева показано как будет изменяться ионизация слабой кислоты с рК=3,5. Справа – как будет происходить аналогичный процесс для слабого основания с рК=7,0.
Слабая кислота будет находиться в неионизированной форме в кислом содержимом желудка, тогда как в щелочной среде тонкого кишечника будет происходить ее диссоциация и молекулы кислоты приобретут заряд. Поэтому, абсорбция слабых кислот будет наиболее интенсивной в желудке. В крови, среда достаточно щелочная и всосавшиеся молекулы лекарства перейдут в ионизированную форму. Фильтр клубочков почек пропускает как ионизированные, так и неионизированные молекулы, поэтому, несмотря на заряд молекулы кислоты будут выводиться в первичную мочу. Дальнейшая их судьба будет зависеть от реакции мочи: если она щелочная (рН=8,0), то кислота останется в ионизированной форме, не сможет реабсорбироваться обратно в кровоток и выделится с мочой. Однако, если реакция мочи кислая, то лекарство перейдет в неионизированную форму, которая легко реабсорбируется обратно в кровь.
Слабое основание, напротив, практически не будет всасываться из желудка, где для него достаточно кислая среда и оно практически полностью ионизировано. Абсорбция слабых оснований протекает из кишечника. В крови молекулы лекарства не будут ионизироваться и поэтому достаточно легко пройдут через барьер почек и выделятся в первичную мочу. Если реакция мочи щелочная, то, оставаясь неионизированными, молекулы лекарства также быстро подвергнутся реабсорбции, однако, если реакция мочи кислая, то за счет ионизации слабое основание приобретет заряд и будет выделяться с мочой.
Таким образом, для того чтобы ускорить выведение из организма слабой кислоты мочу необходимо ощелачивать, а чтобы ускорить выведение слабого основания ее необходимо подкислить.Данный принцип иногда используют при лечении отравлений, для ускорения элиминации токсического вещества с мочой (детоксикация по Попову).
Количественную зависимость процесса ионизации лекарства при различном рН среды позволяет получить уравнение Henderson—Hasselbach:

если рH=рK, то 
(у кислот эта форма не имеет заряда и высоко липофильна)
если рН>рК на 1,0; то 
(у оснований эта форма не имеет заряда и высоко липофильна)
если рН>рК на 2,0; то 
если рН>рК на 3,0; то 
Несмотря на то, что большинство лекарств ионизируется лишь при определенном значении рН среды, можно выделить еще две небольшие группы лекарственных средств:
лекарственные средства, не имеющие заряда независимо от рН среды (дигоксин, хлорамфеникол) – эти лекарственные средства не имеют групп способных ионизироваться, они высоко липофильны и хорошо проникают через гистогематические барьеры и внутрь клеток;
лекарственные средства с постоянным зарядом (гепарин, тубокурарин, суксаметоний) – обладают химическими группировками с настолько выраженной ионизацией, что остаются заряженными при любом значении рН.
Транспорт при помощи специфических переносчиков.Этот транспорт осуществляется при помощи особых транспортных молекул, встроенных в мембрану клетки. Как правило в роли переносчиков выступают белки, которые необходимы для поступления в клетку естественных метаболитов. Данным видом транспорта могут переноситься лекарственные вещества близкие по структуре к эндогенным молекулам – например, витамины, метотрексат. Различают две разновидности транспорта при помощи переносчиков:
облегченная диффузия – осуществляется по градиенту концентрации;
активный транспорт – осуществляется против градиента концентрации.
Специализированный транспорт не подчиняется закону диффузии Фика и не зависит от наличия заряда у лекарственного вещества. Он является насыщаемым процессом – т.е. скорость абсорбции увеличивается лишь до тех пор, пока количество молекул лекарственного вещества не сравняется с количеством переносчиков. Дальнейшего роста скорости абсорбции, несмотря на повышение концентрации лекарства, при этом не происходит.
Эндоцитоз и пиноцитоз.Этот вид абсорбции характерен для высокомолекулярных веществ – полипептидов. При этом лекарство вначале связывается со специальным распознающим компонентом мембраны клетки, а затем возникает инвагинация (впячивание) мембраны и постепенно формируется вакуоль (пузырек, содержащий молекулы лекарства). Вакуоль перемещается по цитоплазме клетки к ее противоположному полюсу, при этом лекарство может выделяться как в цитоплазму клетки, так и с противоположного полюса клетки (путем экзоцитоза).
Таблица 2. Сравнительная характеристика процессов абсорбции лекарств
Источник
Проникновение лекарственных веществ через биологические мембраны это
Способность проникать сквозь двойные липидные слои является условием для всасывания лекарственных средств, проникновения в клетки или в клеточные органеллы и прохождения через ГЭБ и плацентарный барьер. Благодаря амфифильной природе фосфолипиды образуют двойные слои, характеризующиеся гидрофильной поверхностью и гидрофобной внутренней частью. Вещества могут проникать через такую мембрану тремя разными способами.
а) Диффузия. В зависимости от степени липофильности вещества могут диффундировать непосредственно через двойной липидный слой по градиенту концентрации через мембрану (красные точки). В то же время мембрана практически непроницаема для высокогидрофильных веществ (норадреналина).
б) Пассивный транспорт. Во многих тканях есть транспортные системы для переноса через мембрану веществ, которые самостоятельно не могут через нее пройти. Проникая сквозь мембраны, вещества попадают внутрь клеток и в клеточные отделы, где имеется потребность в них. Эти транспортные системы расположены в мембранах и являются более или менее специфичными для определенной группы веществ.
Пассивный транспорт через мембрану не требует энергии. Каналы или белки-переносчики обеспечивают возможность гидрофильным веществам проникать через мембраны. Примерами являются потенциал- или лиганд-контролируемые ионные каналы (потенциалзависимые Na + -каналы, Са 2+ -каналы) и аквапорины.
Аквапорины — специальные транспортные белки, которые обеспечивают прохождение воды через гидрофобную клеточную мембрану во многих тканях организма.
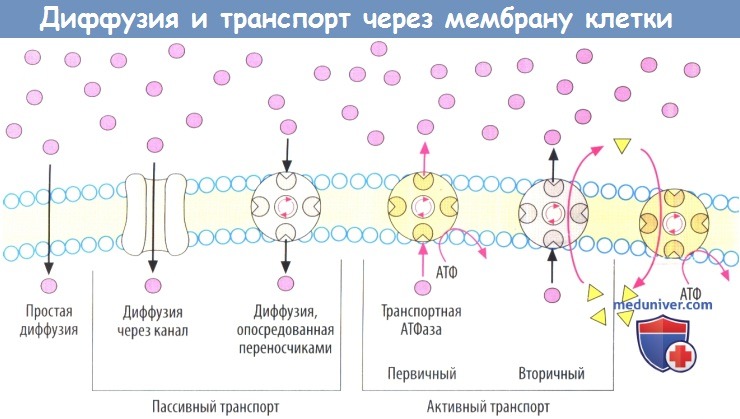
в) Активный транспорт. Многие транспортные процессы в организме осуществляются с прямым или непрямым использованием энергии аденозинтрифосфата (АТФ). Энергия АТФ особенно необходима, когда транспорт веществ через клеточную мембрану осуществляется против градиента концентрации, т. е. с затратой энергии.
В первичном активном транспорте участвуют белки, которые самостоятельно расщепляют АТФ (АТФазы) и таким образом обеспечивают транспорт веществ. Примерами являются Na + /K + -АТФаза или H + /K + -АТФаза.
Некоторые белки первичного активного транспорта выступают в роли мишеней для лекарственных средств; так, гликозиды наперстянки ингибируют Na + /K + -АТФазы] Ингибиторы протонной помпы снижают продукцию кислоты в желудке за счет ингибирования действия H + /K + -АТФазы.
г) При вторичном активном транспорте необходимо функциональное взаимодействие котранспортера с первичным АТФ-зависимым транспортером, В таком случае источником энергии, необходимой для транспорта вещества, служит движение ионов по градиенту концентрации. Градиент Na + обычно служит донором энергии. За поддержание градиента данного иона отвечает, в свою очередь, Na + /К + -АТФаза.
Многие нейромедиаторы и анионные или катионные переносчики используют клеточные градиенты Na + в качестве источника энергии.
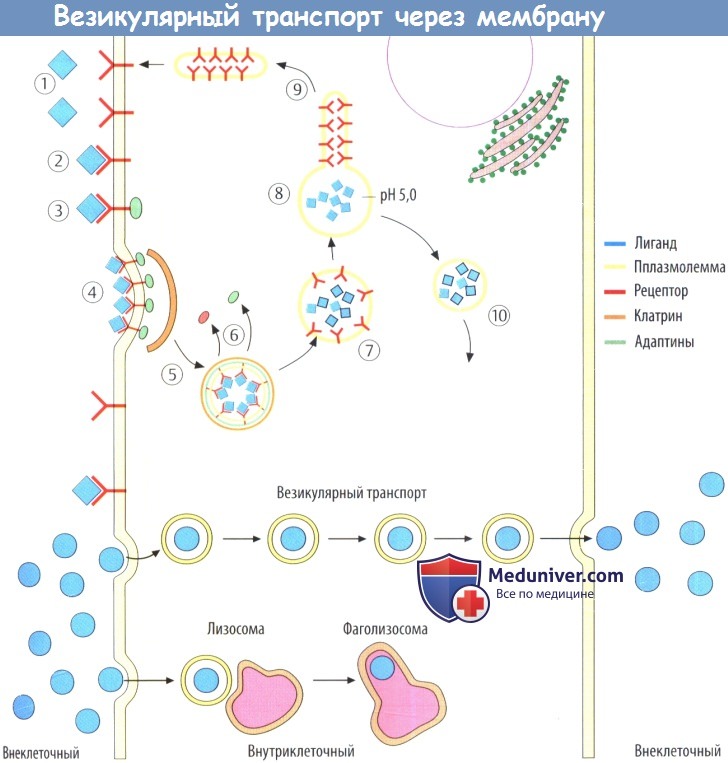
д) Трансцитоз (везикулярный транспорт). Вновь образованные везикулы захватывают растворенные во внеклеточной жидкости вещества и затем переносят их через цитоплазму. В некоторых случаях везикулы (фагосомы) сливаются с лизосомами дообразования фаголизосом, а переносимые вещества метаболизируются.
е) Эндоцитоз, опосредованный рецепторами. Лекарственное средство связывается в первую очередь с рецепторами на поверхности мембраны, а цитозольные участки рецепторов взаимодействуют со специальными белками (адаптины). Комплексы лекарственного вещества с рецептором мигрируют вдоль мембраны и соединяются с другими комплексами на основе клатринзависимого процесс. Область поврежденной мембраны инвагинирует и в конце концов отслаивается до образования обособленной везикулы.
Везикула охватывает клатрин и адаптин, что приводит к образованию ранней эндосомы. Внутри нее повышается концентрация протонов, вызывая диссоциацию комплекса «лекарственное средство-рецептор». Далее участки несущей рецептор мембраны отделяются от эндосомы. Они возвращаются обратно в плазмолемму в то время как эндосома направляется в органеллы мишени.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник




