Проекты по разработке лекарственных средств
Разработка лекарственного средства начинается с синтеза новых химических соединений. Вещества со сложной структурой можно получить из различных иа очников, например растений (сердечные гликозиды), тканей животных (гепарин), микробных культур (бензилпенициллин), культур человеческих клеток (урокиназа), или посредством генно-инженерных технологий (человеческий инсулин).
Чем больше ясности во взаимоотношениях структуры и активности, тем более направленным оказывается поиск новых веществ.
а) Доклинические испытания дают информацию о биологических эффектах новых веществ. Начальный скрининг может включать биохимические и фармакологические исследования (анализ связывания с рецептором) или эксперименты на культурах клеток, изолированных клетках и изолированных органах.
Поскольку эти модели не способны воспроизвести сложные биологические процессы, происходящие в интактных организмах, любое потенциальное лекарственное средство необходимо проверить на животных. Только эксперименты на животных позволяют выяснить, возникаютли желаемые эффекты при дозах, не вызывающих токсичности или сопровождающихся слабой токсичностью. Цель токсикологических исследований заключается в том, чтобы оценить:
1) токсичность, обусловленную кратковременным или длительным приемом;
2) генетические повреждения (генотоксичность, мутагенез);
3) развитие опухолей (канцерогенность);
4) возникновение врожденных дефектов (тератогенность).
В экспериментах на животных также оценивают всасывание, распределение, метаболизм и элиминацию (фармакокинетика) изучаемых веществ. На уровне доклинического изучение лишь у малой части новых веществ обнаруживается потенциал для применения у человека.
Фармацевтическиетехнологии предлагают методы изготовления лекарственных форм.
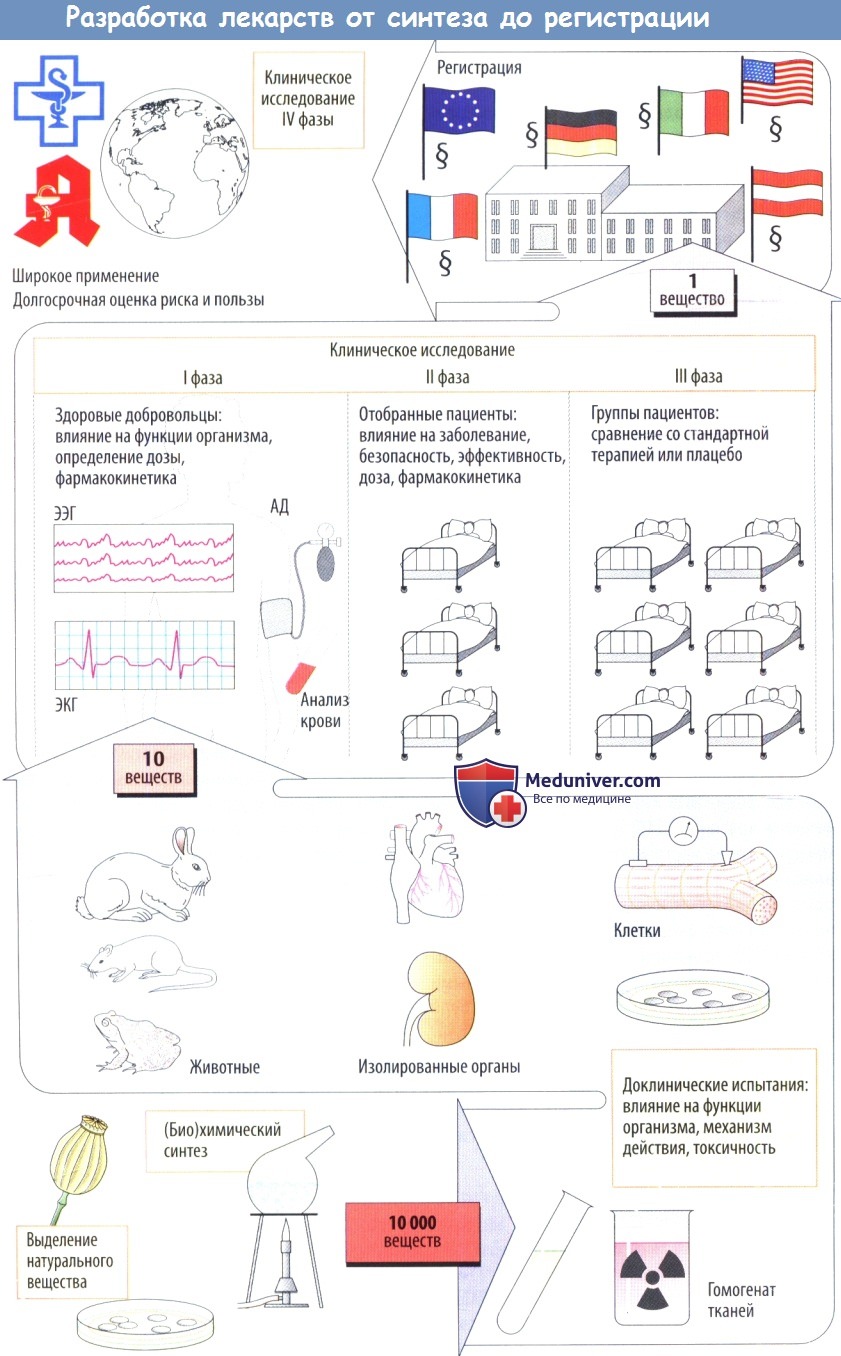
б) Клинические испытания начинаются с исследований I фазы, в которых участвуют здоровые лица; цель этих исследований — определить, будут ли эффекты, наблюдаемые у животных, также возникать у людей. Кроме того, на данном этапе определяется дозозависимость клинических эффектов.
Во II фазе потенциальные лекарственные средства сначала проверяют на отобранных пациентах на терапевтическую эффективность при заболевании, для лечения которого эти препараты предназначались. Если полезное действие очевидно, а частота побочных эффектов приемлема, начинается III фаза, в которой участвует более крупная группа пациентов, у которых новое средство сравнивают с традиционными методами лечения сточки зрения терапевтического результата.
Как форма экспериментов на людях, эти клинические исследования подвергаются анализу и одобрению этическими комитетами медицинских учреждений в соответствии с международными правилами проведения (Хельсинкской, Токийской и Венецианской декларациями). Во время клинических исследований выясняется, что многие вещества нельзя использовать. Как правило, в конце концов примерно из 10 000 вновь синтезированных веществ остается только одно.
в) Решение зарегистрировать новое лекарственное средство выносится национальным регуляторным органом (Food and Drug Administration в США, Health Protection Branch Drugs Directorate в Канаде, комиссией ЕС вместе с European Medicines Agency в Великобритании), которому производители должны подавать регистрационные документы.
Заявители должны документально подтвердить результатами соответствующих испытаний (доклинических и клинических), что критерии эффективности и безопасности удовлетворены и что лекарственные формы продукта (таблетки, капсулы и т. д.) соответствуют всем стандартам контроля качества.
После регистрации новое лекарственное средство может продаваться под торговым названием, оно должно быть доступным, выписываться врачами и отпускаться фармацевтами. В это время наблюдение продолжается в форме постмаркетинговых исследований (IV фаза клинических исследований)
г) Фармакологический надзор — действия, направленные на то, чтобы выявлять и устранять связанные с препаратом риски во время проведения клинических исследований и последующего его выхода на рынок. Фармаконадзор включает отчеты о предполагаемых случаях нежелательных реакций, направляемые в национальные регуляторные органы.
На основе длительного опыта применения можно правильно оценить соотношение риска и пользы и, следовательно, терапевтическую ценность нового лекарственного средства. Если новый препарат имеет небольшое преимущество перед существующими, необходимо принимать во внимание соотношение затрат и пользы от применения лекарственного средства.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Стоимость разработки инновационных лекарственных средств
Сегодня в мире существует около 4300 компаний, которые занимаются разработками в сфере лекарств (новых молекулярных единиц [НМЕ] или новых биологических препаратов (на основе белков) — далее по тексту сокращение НМЕ используется для обоих типов лекарств).
Из 1222 НМЕ, одобренных Управление по контролю над пищевыми продуктами и лекарственными препаратами (Food and Drug Administration, FDA, США) с 1950 по 2008 гг., 1103 являются малыми молекулами и 119 — биопрепаратами.
Активные молекулы-кандидаты сами собой не возникают. Доклиническим испытаниям на клетках и тканях, а затем на животных предшествует работа коллектива учёных, задачей которого является анализ патентной и научно-технической литературы, выбор объектов исследования, разработка удобных методов получения перспективных соединений и их полупродуктов, а также их идентификации и очистки, масштабирование процессов до технологических объёмов, наработка опытных партий для клинических исследований I-III фазы, создание соответствующей научно-технической документации.
По статистике, лекарство-кандидат не доходит до процесса регистрации в следующих случаях: токсичность (30%), недостаточная клиническая эффективность (27%), неприемлемый профиль безопасности (13%), предпочтение другим препаратам (9%), отсутствие дальнейших инвестиций (5%), другие причины (16%).
Затраты на каждую НМЕ повышались в течение десятилетий. Согласно данным Ассоциации фармацевтических исследований и производителей Америки (Pharmaceutical Research and Manufacturers of America, PhRMA), членами которой, в основном, являются крупные фармкомпании, с 1970 г. затраты на R&D (Research and Development; исследования и разработка новейших лекарственных средств) росли с ежегодным совокупным темпом в 12,3%. Так, в 2008 г. только у 27% компаний затраты на НМЕ были ниже 1 млрд. долларов. Масштабы этих цифр беспокоят и требуют более глубокого анализа.
DiMasi оценил, что средние затраты на НМЕ в США составили 802 млн. долларов в 2000 г. для малых молекул (это было примерно в 3,5 раза выше подобного показателя в 1987 г.) и 1,318 млрд. долларов в 2005 г. для биопрепаратов. Министерство здравоохранения и социального обеспечения США, основываясь на данных 2002 г., представило более высокие оценки — 1,7 млрд. долларов, что означало рост за последние пять лет на 55%. Однако, эти средние вычисления не исключают затраты после получения разрешения для исследований IV фазы, которые может потребовать FDA, Европейское агентство по регистрации лекарственных средств (EMA) и другие регуляторные органы; они также упускают затраты на получение регуляторных разрешений на рынках вне США и Европы, и подачи заявок на новые показания к применению.
Наиболее важным является то, что вероятность успешного появления на фармацевтическом рынке новой молекулы после клинических испытаний составляет лишь 11,5%. Когда подсчёты DiMasi были скорректированы, как для инфляции, так и других увеличившихся затрат (например, в связи с более строгими регуляторными требованиями), затраты на каждую НМЕ увеличились значительно. Эти средние подсчёты также скрывают потенциально б`ольшие отличия между компаниями. Например, между 2000 и 2008 гг., фирма Pfizer потратила 60 млрд. долларов США на R&D и получила разрешения на 9 НМЕ. В противоположность, фирма Progenies, которая получила разрешение от FDA на methylnaltrexone bromide (Relistor) в 2008 г., потратила 400 млн. долларов на R&D за тот же период — соответственно, затраты на одну НМЕ значительно ниже, чем у Pfizer.
Большая часть выпускаемых в мире инновационных препаратов была разработана частично, либо полностью именно в маленьких и средних фармкомпаниях. Это стало возможным благодаря высокой мобильности, низким накладным расходам, более эффективному управлению и высокой производительности труда. В подобных компаниях суммарные расходы на разработку нового препарата в несколько раз ниже, чем у фармгигантов. Приведённые в публикациях цифры основаны на статистике транснациональных фармацевтических компаниях (Big Pharma), а фармгиганты известны своим консерватизмом как в поиске новых лекарственных средств, так и в разработке стратегии и дальнейшем следовании жёсткому бизнес-плану.
На стоимость инновационного лекарства влияет не только неэффективное управление научными разработками в фармкомпаниях. Непрямой, но значительный вклад в себестоимость вносят неудачные рыночные и корпоративные действия компаний, а затраты на маркетинг могут достигать 400 млн. долларов США за лекарство (например, Виагра) и обычно составляют до трети всех расходов на разработку нового препарата.
Подсчёт затрат на НМЕ сложен из-за того, что средства, потраченные на R&D, возвращаются в виде прибыли лишь через несколько лет, следовательно, затраты на R&D должны амортизироваться в течение этого периода. Однако, продолжительность этого периода неясна и, вероятно, меняется со временем, так как биофармацевтическая наука и регуляторные органы изменили исследования лекарств. На практике, среди экспертов практически нет согласия по поводу того, как капитализировать и амортизировать R&D лекарств. Опубликованные исследования использовали периоды, варьирующиеся от 4-х до 12 лет.
В настоящее время чистая приведённая стоимость (net present value [NPV]) является основным показателем, используемым для оценки принятия решений относительно выгодности капиталовложений, в том числе и в фарминдустрии. В общих чертах, NPV представляет собой величину денежных средств, которую инвестор ожидает получить от проекта после того, как денежные притоки окупят его первоначальные инвестиционные затраты и периодические денежные оттоки, связанные с осуществлением проекта. Положительная (больше нуля) NPV означает, что проект будет прибыльным для компании. Для установки диапазонов NPV проводится анализ чувствительности и имитационное моделирование методом Монте-Карло. Такой подход необходим для создания полноценных сценариев всех возможных рисков на различных стадиях R&D с помощью рассмотрения разных вариантов и исходов. Таким образом, оценка риска обязательна, а в случае с лекарственным средством она также включает в себя оценку вероятности получения официального разрешения контролирующих органов. NPV используют для сравнения проектов как по отношению к ассортименту лекарств, находящихся в разработке, так и к существующему на рынке общему ассортименту фармацевтической продукции.
Например, среднестатистическая NPV для антибиотиков составляет 100, в то время как этот же показатель для препаратов против рака равен 300; для лекарств, применяемых для терапии неврологических заболеваний – 720; для препаратов, направленных на лечение заболеваний опорно-двигательного аппарата – 1150. Любое лекарство с NPV Стратегия развития фармацевтической промышленности РФ на период до 2020 г. Этот документ предполагает определённые объёмы и источники финансирования. Всего на период 2009-2020 гг. предусматривается выделение 106,4 млрд. руб. (в ценах февраля 2009 г.) по направлению «Разработка лекарственных средств». Безусловно, это серьёзный и обнадёживающий задел на будущее. Много это или мало? Если эти средства были бы у американских разработчиков, то на свет появилось бы как минимум 5 новых блокбастеров, в России же возможно появление 20 и более инновационных препаратов. Посмотрим на развитие событий, в отечестве существуют современные аналитические лаборатории, многие фармфирмы уже перешли на стандарт производства GMP, а качество клинических исследований не уступает зарубежным. Время покажет, куда пошли такие колоссальные ресурсы, ждать осталось 9 лет.
В целом, в разработке новых лекарственных средств посредством инвестирования в R&D есть положительный, но рискованный эффект на прибыль.
При разработке инновационного препарата необходимо так же оценить стоимость будущего лекарства. Для этого проводится анализ «порога готовности платить» (ПГП). ПГП отражает ту сумму, которую общество готово потратить на достижение определённого терапевтического эффекта или неких суррогатных конечных точек для данной категории больных. Порог готовности платить для России в 2010 г. составил 1 062 510 руб., поэтому препараты со стоимостью достижения эффекта превышающий эту цифру вряд ли будут востребованы российским обществом.
Источник
Как создать препарат в лаборатории и перенести его в производство
Все мы ходим в аптеку и покупаем лекарства: таблетки, порошки, мази, растворы и многие другие формы лекарственных веществ. Но мало кто знает, как происходит создание лекарств и какой путь необходимо пройти от научной разработки в руках ученого до получения регистрационного досье на готовый препарат.
Разработка и создание лекарственных препаратов проходят при финансовой поддержке различных государственных и коммерческих структур (фондов) в соответствии с утвержденными приоритетными направлениями развития науки, технологий и техники в Российской Федерации, согласно перечню (указ президента России от 7 июля 2011 года №899). Одним из таких направлений являются «Технологии снижения потерь от социально значимых заболеваний».
Терапия и диагностика онкологических заболеваний — одно из приоритетных направлений. Многие ученые работают над созданием новых низкомолекулярных веществ для химиотерапии, получением новых аналогов уже существующих препаратов для преодоления возникающей резистентности опухолевых клеток, а также созданием новых лекарственных форм препаратов для улучшения биодоступности активного компонента и уменьшения побочных эффектов. В последние годы широко развивается направление адресной доставки препаратов — например, на основе антител.
Нашей научной группой под руководством члена-корреспондента РАН, профессора, доктора химических наук Евгения Северина разработан универсальный подход к созданию препарата для адресной доставки в злокачественные новообразования. Данный метод заключается в синтезе наночастиц, содержащих активное вещество, с последующей конъюгацией векторной молекулой — белка, способного связываться с рецепторами на поверхности опухолевых клеток. Предварительные исследования показали многообещающие результаты, проведенные доклинические испытания подтвердили, что разработанный прототип препарата обладает большей противоопухолевой активностью по сравнению с аналогом, представленным на рынке. Суммируя опыт проведения таких исследований, мы можем описать стандартный протокол проведения исследований при разработке нового препарата и оформления нормативной документации.
Каков же общий путь исследований, позволяющих провести доказательную базу эффективности и безопасности нового препарата, и какое количество времени для этого необходимо? После проведения этапов разработки подхода создания препарата и проведения предварительных экспериментов для доказательства его эффективности коллективом оформляется заявка для участия в конкурсе для предоставления финансирования на проведение доклинических испытаний. Стандартный грант предоставляется на три года, по результатам выполнения которого у группы исследователей, выполняющих данную работу, будет готовый прототип препарата, изучена его эффективность, безопасность и оформлены все необходимые нормативные документы, на основе которых формируется досье и подается на рассмотрение в Министерство здравоохранения России.
Первое, что необходимо сделать при разработке нового препарата,— проведение обширного литературного и патентного поиска в близких и смежных областях, чтобы избежать «изобретения велосипеда». Если патентная чистота подтверждена, можно приступать к экспериментальной работе.
В полученном гранте на проведение доклинических испытаний прописан календарный план и список этапов, которые необходимо выполнить, а затем подготовить отчетную документацию. Все этапы регламентированы соответствующими нормативными документами. Настольными книгами для специалистов являются «Государственная фармакопея Российской Федерации» и «Руководство по проведению доклинических исследований лекарственных средств» под редакцией А. Н. Миронова. В фармакопее прописаны все требования и нормы к разрабатываемым препаратам, какие виды исследования необходимо провести для подтверждения состава, структуры и свойств будущего лекарства или новой лекарственной формы (порошки, таблетки, растворы и пр.). В руководстве по проведению доклинических исследований подробно изложено, как необходимо проводить доклинические испытания, чтобы исследование было стандартизировано: выбор вида животных, их количества, кратность введения, дозы и пр.
Для проведения такого широкого спектра исследований необходимо соответствующее количество будущего препарата. В лабораторных условиях обычно отрабатывают технологические режимы и оптимальные параметры получения — от температурного режима до масштабирования процесса — и изучают влияние этих параметров на свойства получаемого продукта. По оптимизированным условиям пишут лабораторный регламент, где четко описано, как именно и при каких условиях необходимо проводить каждый этап получения препарата и что должно быть на выходе, вплоть до учета потерь производства. Лабораторный регламент является официальным нормативным документом, на его основе составляют опытно-промышленный и промышленный регламенты. Для последних двух необходима специальная производственная площадка, аттестованная под изготовление похожего продукта, как и разработанный препарат (рекомбинантные белки, вакцинные препараты, противоопухолевые препараты и т. д.). Необходимо перенести лабораторную технологию получения продукта в больший масштаб на промышленное оборудование, отработать регламентированный процесс получения и оптимизировать технологию с учетом новых объемов. Таким образом, на промышленных производственных площадках по опытно-промышленному и промышленному регламенту получают опытные партии препарата, которые затем необходимо проверять на соответствие всем показателям, которые были установлены разработчиками после получения оптимальной партии по лабораторному регламенту. Все требования к полученному препарату описаны в нормативном документе — фармацевтической статье предприятия (ФСП).
ФСП пишут по тем методам, с помощью которых анализируют полученный препарат в соответствии с государственной фармакопеей. Для включения метода в ФСП необходимо использовать либо стандартизированные методы, приведенные в фармакопее, либо валидированные методы, которые были использованы, но отсутствуют в фармакопее или отличаются по условиям проведения от описанных. Чем больше активных (целевых) и вспомогательных компонентов в препарате, тем больше методов содержит ФСП. Необходимо провести количественный анализ активного компонента и примесей, полный качественный анализ, а также подтвердить сохранение функциональной активности основного компонента.
Зачем нужна фармацевтическая статья предприятия? В технологическом процессе получения препарата могут возникнуть непредвиденные неполадки на какой-либо стадии производства. Для выявления несоответствия продукта (брака производства) необходимо проводить анализ каждой партии. Если была получена бракованная партия, ее можно будет легко выявить, проведя все анализы и сравнив с установленными нормами в ФСП.
После получения опытных партий необходимо изучить стабильность полученного препарата, чтобы доказать, что за указанный промежуток времени (срок годности) не происходит никаких существенных изменений и свойства будущего лекарства остаются неизменными. Стандартный срок хранения лекарственных средств — от полугода до трех лет. Для противоопухолевых препаратов — два года. Для конкурентоспособности и рентабельности будущего лекарства необходимо придерживаться таких же сроков годности, а также ориентироваться на аналоги. Однако ждать два года, чтобы узнать, стабилен ли препарат и проходит ли он по всем нормам и стандартам, нет необходимости. Существуют протоколы, описанные в фармакопее (ОФС.1.1.0009.15 «Сроки годности лекарственных средств»), позволяющие сократить период исследования до года и даже шести месяцев, используя более агрессивные условия исследования. Если препарат по всем показателям сохраняет количественные, качественные и функциональные характеристики, указанные в ФСП, следующий этап — проведение доклинических исследований на животных. На все перечисленные стадии оформляют нормативные документы: регламенты на производство, отчеты о валидации, акты наработки, ФСП, протоколы анализа партий, подтверждающие соответствие полученного продукта описанному в документах.
Для изучения безопасности и эффективности полученного препарата на лабораторных животных утверждается план доклинических исследований, в котором перечислены все этапы исследования и их последовательность. План и модели проведения исследований составляются в зависимости от типа разработанного препарата и описаны в «Руководстве по проведению доклинических исследований лекарственных средств». Для оформления регистрационного досье необходимо провести полные доклинические исследования: исследование нескольких видов токсичности (общетоксическое действие, аллергизирующие свойства, иммунотоксическое действие, репродуктивная токсичность и др.), эффективности действия (например, противоопухолевый эффект нового препарата в сравнении с аналогами), изучить фармакокинетику. Все полученные данные обрабатывают статистически и оформляют в нормативный документ — отчет о доклинических исследованиях с прикреплением первичных результатов. На основании полученных данных, в случае если препарат обладает эффективностью и при этом безопасен для применения, разработчики пишут план проведения первой стадии клинических испытаний, проект инструкции по применению и проект брошюры исследователя. Из составленных документов формируется регистрационное досье, которое и подается на рассмотрение в Министерство здравоохранения России с другими сопутствующими документами.
До последнего этапа, описанного в данной статье, доходят немногие разработки. Путь от научной идеи до регистрации может занимать от трех лет до десятилетий. При наличии оформившейся идеи, прошедшей предварительные фундаментальные исследования, все описанные этапы исследования можно провести за три-пять лет. А дальше препарат ждет еще более сложный, но не менее интересный путь: клинические испытания, регистрация, производство и выход на рынок — при условии наличия хороших результатов на этапе клинических испытаний.
Елена Никольская, кандидат химических наук, старший научный сотрудник ИБХФ РАН
Источник



