Медленно и нервно: в ЕМА объяснили задержку одобрения «Спутника V»
«Спутник V» продолжают исследовать европейские эксперты совместно с ВОЗ. Об этом «Известиям» заявили в пресс-службе Европейского агентства лекарственных средств (EMA). Как пояснил официальный представитель регулятора, европейские эксперты уже провели проверки надлежащей клинической практики (GCP) в России, но на этот месяц еще запланированы проверки надлежащей производственной практики (GMP). Тем временем страны ЕС уже открываются для туристов, вакцинированных одобренными ЕМА и ВОЗ препаратами. Однако, как отмечают опрошенные «Известиями» местные жители, пока темпы прививочной кампании в самой Европе оставляют желают лучшего.
Сорок сороков
Одобрения вакцины от коронавируса «Спутник V» Европой ожидают многие россияне. Недавно страны ЕС согласовали план по возобновлению международного туризма, согласно которому на территорию объединения пока смогут попасть только путешественники из третьих стран, привитые одобренными в ЕМА и ВОЗ препаратами.
Процедуру исследования российской разработки от коронавируса ЕМА запустило в начале марта. Как ранее предполагалось, Европу «Спутник V» в любом случае смог бы увидеть не раньше мая. На пресс-конференции 12 мая глава департамента ЕМА Марко Кавалери не исключил, что в ближайшие недели сможет определить сроки одобрения российского препарата. Тем не менее, как сообщили «Известиям» в пресс-службе регулятора, в этом месяце «Спутнику V» предстоит пройти еще одну стадию исследования.
— Сейчас проходит циклический обзор (rolling review) российской вакцины. Текущие исследования будут продолжаться до тех пор, пока не будут получены все необходимые доказательства для оформления заявки на получение разрешения на продажу препарата в Европе, — сообщили в ЕМА.
Как пояснил официальный представитель агентства в беседе с «Известиями», для оценки вакцины европейские инспекторы уже провели проверки надлежащей клинической практики (GCP) в России, тем не менее на этот месяц запланированы проверки надлежащей производственной практики (GMP). Точные сроки одобрения вакцины при этом назвать в ЕМА не смогли, поскольку совместное исследование препарата европейскими экспертами и ВОЗ все еще продолжается.
3 мая эксперт ВОЗ Марианджела Симао в ходе брифинга заявила, что они планируют оценить безопасность российской вакцины в конце июня — в июле. Представитель ВОЗ в России Мелита Вуйнович отметила позже, что эксперты организации смогут завершить оценку безопасности вакцины «Cпутник V» в течение лета.
Такой прогноз тем не менее не утешает россиян, которые планировали провести отпуск на курортах Испании и Италии, ведь эти страны подавали надежду на открытие границ с РФ. С 12 мая визовый центр Испании стал выдавать краткосрочные визы россиянам, но уже 21 мая стало окончательно понятно, что свободно на Иберийский полуостров смогут пробраться только те, кто привит одобренными ВОЗ и ЕМА препаратами. Об обсуждении возможности допуска российских граждан в Италию этим летом сообщал посол страны в Москве Паскуале Терраччано. Подтверждений этому заявлению не появилось. Сообщение о восстановлении авиаперелетов с Мальтой с 25 мая — еще одна ложная надежда. В Минтуризме государства «Известиям» напомнили, что РФ все еще находится в красном списке из-за эпидситуации, так что пока правом на допуск туристов, привитых другими вакцинами, из европейских курортных стран воспользовалась только Греция.
Между тем, как допустили 23 мая в МИД Мальты, «Спутник V» может быть сертифицирован в ЕС до конца июня.
Кто последний?
Европа тем временем пытается нарастить темпы вакцинации, демонстрируя отсутствие необходимости в расширении портфеля вакцин китайской Sinopharm и российским «Спутником V». Еще недавно эксперты говорили о катастрофически низких темпах прививочной кампании в этом регионе. В апреле глава европейского бюро ВОЗ Ханс Клюге назвал распределение вакцин в Европе «неприемлемо медленным». Лето уже на носу, но пока только 40% взрослого населения ЕС получили первую дозу вакцины.
В надежде решить эту проблему ЕС даже подал иск в отношении AstraZeneca из-за срыва графика поставок. Другие страны наконец открыли доступ для записи на вакцину не только группам риска. Так, с 7 июня в Германии отменяется очередность вакцинации. Теперь фактически все жители с 16 лет будут иметь право записаться на прививку. Однако в документе подчеркивается, что не все желающие смогут поставить укол уже в июне в связи с ограниченным количеством препаратов.
— Мне 22 года, поэтому только сейчас у меня появляется возможность вакцинироваться. Пока я только получил талон, то есть встал в очередь на прививку, — заявил «Известиям» житель Магдебурга Кристиан.
Он также добавил, что его ровесники на самом деле готовы вакцинироваться любым препаратом, в том числе и «Спутником V», только бы быстрее, ведь в ФРГ привитые граждане пользуются некоторыми привилегиями при посещении общественных мест. Как подчеркнул собеседник, в любом случае к препарату от AstraZeneca в Германии многие относятся с гораздо большим скепсисом, чем к российской вакцине.
— Уверяю вас: если бы была бы возможность, многие итальянцы привились бы «Спутником V», поскольку новости о летальных исходах от AstraZeneca и Pfizer насторожили население, — рассказала «Известиям» жительница Триеста Гала Росси.
О том, что затягивание регистрации «Спутника V» в Евросоюзе связано с политическими аспектами, недавно сообщил директор Службы внешней разведки России Сергей Нарышкин. По его словам, это объясняется «сигналами из высоких кабинетов». Кроме того, политик заявил, что ЕС готовит «очередную клеветническую кампанию против России» и планирует обвинить Москву в разжигании антипрививочного движения за рубежом. Тем временем, по данным правительства, на 12 мая в России как минимум первую прививку сделали уже более 24 млн человек.
Источник
Какие вакцины от коронавируса используют в мире
В России массовая вакцинация от COVID-19 началась 18 января. В мире на конец марта прививают население уже в 141 стране. Какие вакцины используют — в обзоре РБК
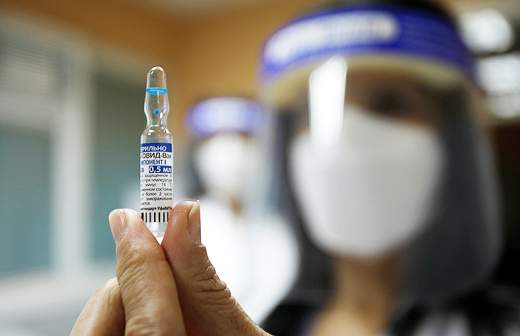
«Спутник V», разработанная Центром эпидемиологии и микробиологии имени Н.Ф. Гамалеи, получила госрегистрацию Минздрава в августе. Вакцину зарегистрировали после второй фазы испытаний, а третий финальный этап стартовал в сентябре.
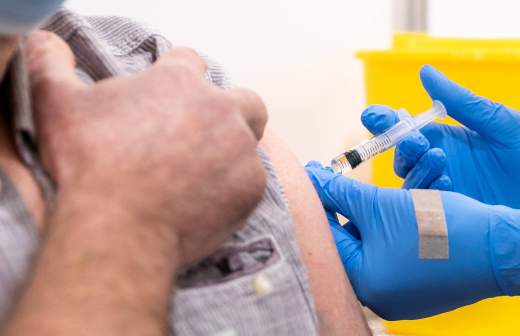
Эффективность «Спутника V» разработчики оценили выше, чем в 95%. Эти данные были получены при исследовании добровольцев, получивших две инъекции препарата. «Спутник V» разработан в двух видах: замороженном (жидкая «Гам-КОВИД-Вак» хранится при температуре не выше минус 18 °С) и лиофилизированном (порошок «Гам-КОВИД-Вак-Лио» хранится при температуре от плюс 2 до 8 °С). Препарат вводится двукратно с интервалом в три недели. В ФАС заявили, что стоимость инъекции «Спутником V» не превысит 1 тыс. руб.
5 декабря Москва стала первым российским регионом, начавшим масштабную вакцинацию «Спутником V», а с 18 января началась массовая вакцинация во всей России. Первой среди зарубежных стран, зарегистрировавших российский препарат, стала Белоруссия. Такое же решение приняли власти Аргентины, Венесуэлы и некоторых других стран
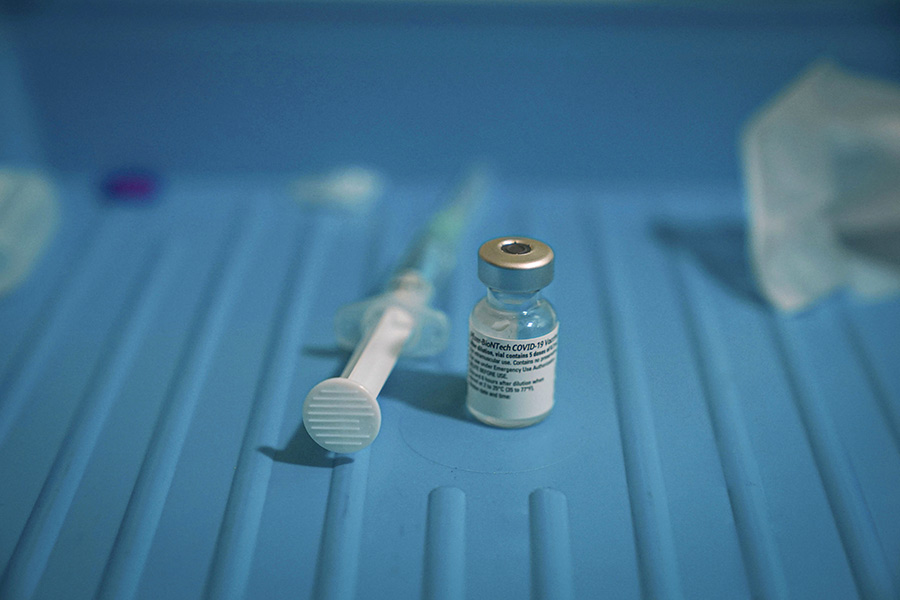
Немецкая компания BioNtech разработала вакцину совместно с американской Pfizer. На третьей фазе клинических испытаний препарат показал эффективность на уровне 95%. У вакцины есть обязательное условие использования: ее нужно хранить при температуре не выше минус 70 градусов Цельсия, а после разморозки она пригодна в течение пяти дней. Разработка Pfizer-BioNTech вводится в два приема с промежутком в три недели. Великобритания стала первой страной, одобрившей применение Pfizer и BioNTech, за ней последовали Канада, США и страны Европы и Ближнего Востока. Массовая вакцинация в США и Канаде началась 14 декабря, а в европейских странах — 27 декабря
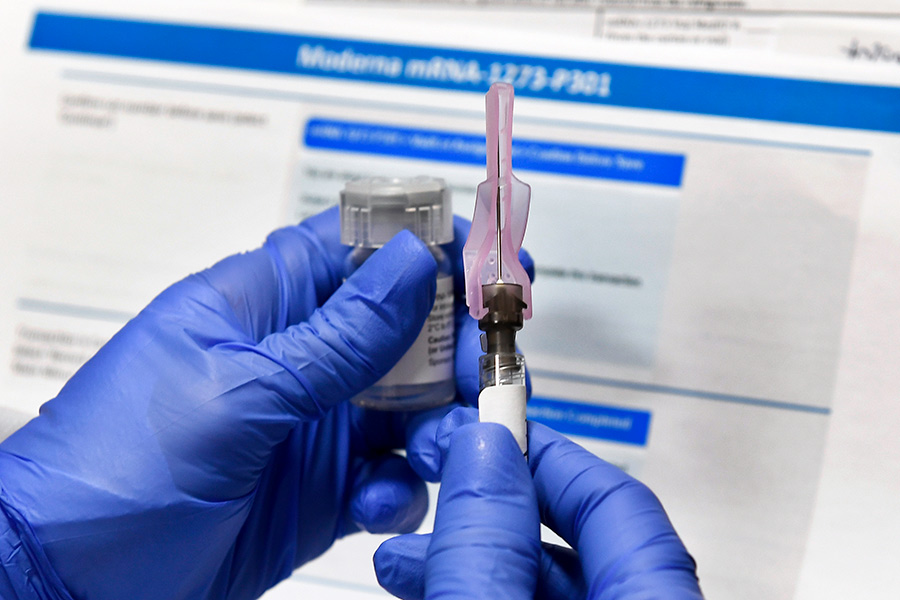
Эффективность вакцины американской фармацевтической компании Moderna составила 94,5%, а при тяжелых случаях заболевания — 100%. Вакцин вводят в два приема с интервалом в четыре недели. Препарат можно до 30 дней хранить при 2–8 градусах Цельсия. В этом году Moderna планирует выпустить 600 млн доз.
18 декабря США одобрили использование Moderna и заказали 200 млн доз с возможностью покупки еще 300 млн. Следом разрешение на использование она получила в Канаде, Израиле, Великобритании и Швейцарии. 6 января Европейский регулятор одобрил препарат американского производства
Вакцина, разработанная британской компанией AstraZeneca вместе с Оксфордским университетом, показала эффективность на уровне 70%, а при одном из способов введения (сначала вводят половину дозы, а через месяц — полную) — 90%.
У препарата есть два преимущества: его можно хранить при той же температуре, которую позволяет создать обычный холодильник, а его стоимость составляет $4–5. Вводится два раза с интервалом в 4–12 недель.
Великобритания первой в мире разрешила использовать AstraZeneca и заказала 100 млн доз. Препарат получил разрешение на использование в Индии, Аргентине, Доминиканской Республике, Сальвадоре, Мексике и Марокко.
В марте 2021 года вокруг препарата AstraZeneca разразился скандал. Более 15 стран Европы, в том числе Германия, Франция, Испания, и некоторые страны Азии и Африки частично или полностью отказались от препарата. Такое решение власти приняли на фоне сообщений об образовании тромбов у привившихся и смертельных исходах.
В самой компании указывают на отсутствие доказательств, что к смерти пациентов привела именно вакцинация. 18 марта вышло заключение Европейского агентства лекарственных средств (EMA) о том, что AstraZeneca не увеличивает риски по образованию тромбов. ВОЗ также продолжает рекомендовать использование препарата. После этих заявлений европейские страны, кроме некоторых скандинавских, возобновили иммунизацию AstraZeneca.
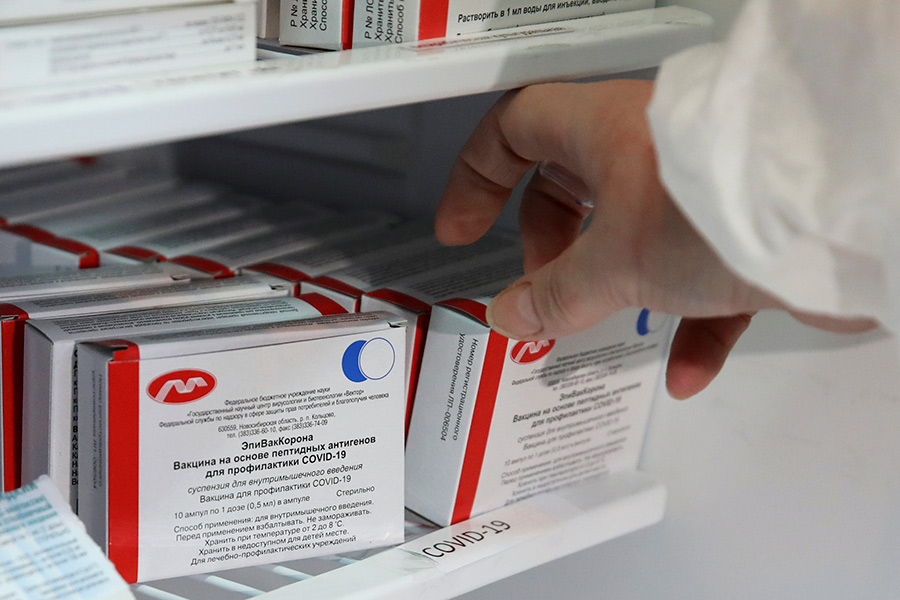
Пептидная вакцина новосибирского научного центра «Вектор» «ЭпиВакКорона» получила регистрационное удостоверение в октябре 2020 года. Она, как и «Спутник V», была зарегистрирована после двух стадий клинических испытаний.
Вакцину вводят двукратно внутримышечно с интервалом в две-три недели. Препарат можно хранить при температуре от 2 до 8 градусов выше нуля. В Роспотребнадзоре отмечают, что вакцина подходит для пожилых и людей с хроническими заболеваниями. В центре «Вектор» заявили, что стоимость препарата будет эквивалента стоимости «Спутника V», то есть около 1 тыс. руб.
Глава Роспотребнадзора Анна Попова сообщала, что «ЭпиВакКорона» поступила в гражданский оборот в пяти городах — Москве, Санкт-Петербурге, Ростове-на-Дону, Туле и Новосибирске. После завершения пострегистрационных клинических испытаний в 2021 году может начаться массовая вакцинация «ЭпиВакКороной»
Инактивированная вакцина CoronaVac, разработанная китайской Sinovac Biotech, хранится в холодильнике при плюс 2–8 градусах Цельсия. В Sinovac заявили, что обеспечат производство 300 млн доз в год. Для иммунизации требуется две дозы, а это означает, что CoronaVac смогут привиться 150 млн человек — чуть больше десятой части населения Китая.
Данные об эффективности вакцины от Sinovac разнятся. Последние испытания в Бразилии показали 50,4% эффективности, а в Индонезии и Турции — 65,3% и 91,5% соответственно.
Вакцина была одобрена для экстренного применения в группах высокого риска в Китае с июля. Использование этой вакцины 13 января разрешили власти Турции. Несколько азиатских стран — Сингапур, Малайзия и Филиппины, а также Бразилия и Украина подписали соглашения о закупках CoronaVac
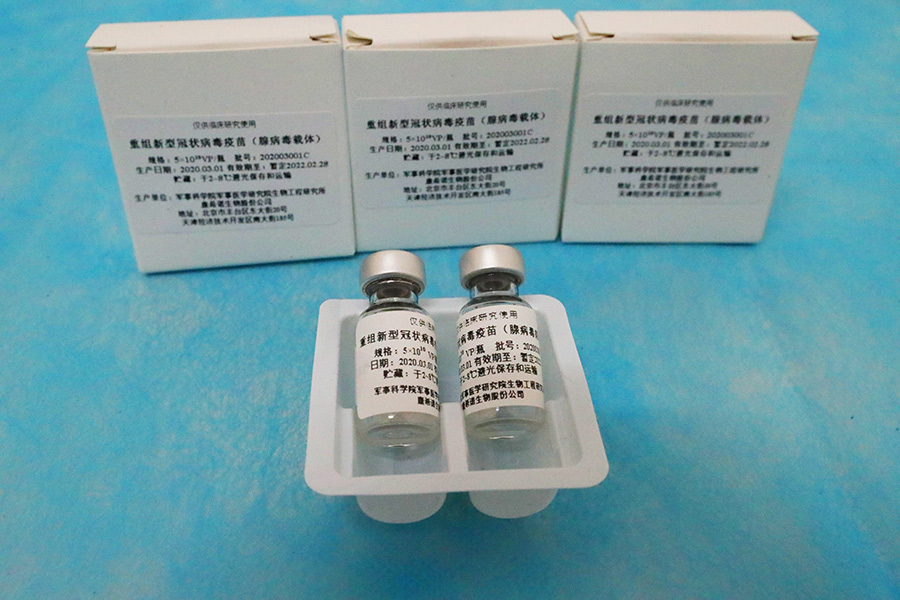
Еще одна китайская вакцина Ad5-nCoV («Конвидеция»), на основе человеческого аденовируса типа 5, разработана фармкомпанией CanSino Biologics. Преимуществом этого препарата является однократное введение, а также возможность хранения при температуре от плюс 2 до плюс 8 градусов Цельсия.
В ноябре 2020 года были поданы документы в Минздрав России для регистрации вакцины. В декабре Минздрав выдал разрешение на проведение третьего международного этапа клинического исследования Ad5-nCov. В случае, если вакцина покажет высокую эффективность и безопасность, CanSino Biologics с российским «Петроваксом» организуют ее производство в России.
Согласно промежуточным результатам третьей фазы клинических испытаний в России, Ad5-nCoV показала эффективность в 92,5%. Окончательные результаты исследования появятся в середине 2021 года
Другую китайскую инактивированную вакцину разработала China National Biotec Group (CNBG) (подразделение Sinopharm). Она не требует отрицательной температуры хранения и вводится двумя дозами с интервалом в две недели.
30 декабря Sinopharm объявила, что на третьем этапе испытаний препарат показал эффективность на 79%. Однако Объединенные Арабские Эмираты, которые одобрили вакцину Sinopharm в этом месяце, заявили, что эффективность вакцины составила 86%. Кроме Китая и ОАЭ вакцина Sinopharm проходит клинические испытания в Бахрейне, Иордании, Перу и Аргентине.
В Китае препарат Sinopharm с июля используется в рамках программы по экстренному вакцинированию, а 31 декабря Государственное управление по лекарственным средствам Китая одобрило препарат для широкого использования
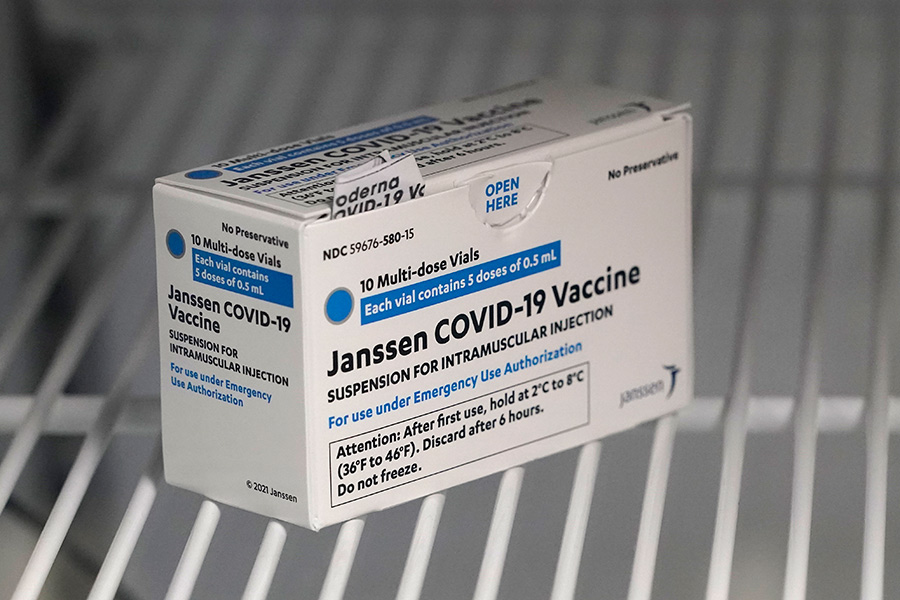
Вакцину Janssen американской корпорации Johnson & Johnson 11 марта одобрил ЕС. Чуть раньше экстренное применение препарата разрешило Управление США по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). Препарат также включен в список для экстренного применения ВОЗ.
В ходе клинических испытаний с участием 44 тыс. человек из США, Южной Африки и стран Латинской Америки препарат показал эффективность в 67%.
Вакцина Janssen хранится при температуре -20 градусов по Цельсию. Но у нее есть особенность — на протяжении трех месяцев она может находиться в условиях от 2 до 8 градусов по Цельсию. Главное преимущество — однодозное введение.
Источник