Природа лекарств. Основные понятия лекарствоведения.



Определение фармакологии и ее место среди других медико-биологических наук.
Цели и задачи фармакологии.
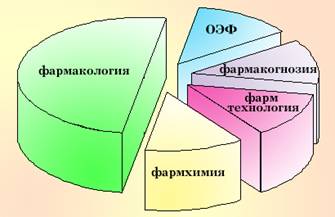 Схема 1. Компоненты лекарствоведения. ОЭФ – организация и экономика фармации. Схема 1. Компоненты лекарствоведения. ОЭФ – организация и экономика фармации. |
Фармакология (греч. pharmakon – лекарство) – наука о взаимодействии лекарственных веществ с живыми системами. Фармакология является одной из частей лекарствоведения – науки о лекарствах вообще. Лекарствоведение помимо фармакологии включает в себя фармацию, состоящую из фармацевтической химии (науки о физико-химических свойствах лекарства), фармакогнозии (науки о лекарственных веществах растительного происхождения), технологии лекарственных форм (науки об изготовлении лекарственных препаратов) и организации фармации.
При изучении биологических свойств лекарств фармакология опирается на достижения в области химии (в настоящее время большинство лекарств – продукты химического синтеза), биологической химии, нормальной и патологической физиологии (использует их концепции для объяснения механизмов действия лекарств, а методики – для оценки эффектов, которые вызывает в организме лекарство).
В свою очередь, та сумма знаний, которую создает фармакология, служит базой для фармакотерапии (т.е. лечения заболеваний с помощью лекарств).
Основная цель фармакологии – изыскание новых высокоэффективных и безопасных лекарственных средств.
Задачами фармакологии являются:
· Изучение механизма действия и влияния лекарственных веществ на органы и системы организма.
· Исследование нежелательных (побочных) и токсических реакций лекарственных веществ.
· Установление показаний и противопоказаний к назначению лекарств.
· Разработка схем рационального дозирования лекарств.
Фармакологию подразделяют на:
1. Экспериментальную (базисную) фармакологию – изучает действие лекарств в эксперименте.
2. Клиническую фармакологию – изучает клиническую эффективность и безопасность применения лекарств у пациентов, оптимизирует программу лечения пациента с учетом его состояния.
3. Токсикологию – изучает токсическое действие на органы различных веществ (в том числе и лекарственных).
Природа лекарств. Основные понятия лекарствоведения.
· Лекарственное средство (лекарство) – одно или несколько лекарственных веществ разрешенных в установленном порядке для практического применения с целью лечения, профилактики, диагностики заболеваний у человека и животных, а также для применения с целью контрацепции. Лекарственное вещество – индивидуально чистое химическое соединение. Лекарственное средство необходимо отличать от фармакологического средства – вещества с установленной биологической активностью, которое может быть или является предметом клинических испытаний (т.е. в отличие от лекарственных средств фармакологические средства это еще не разрешенные для практического применения соединения).
· Лекарственная форма – придаваемое лекарственному средству удобное для практического применения состояние, при котором достигается необходимый терапевтический эффект. Лекарственные формы делят на твердые, жидкие, мягкие и лекарственные формы для инъекций.
· Лекарственный препарат – лекарственное вещество (средство) в приданной ему определенной лекарственной форме.
· Лекарственное сырье – необработанные природные материалы минерального, растительного, животного или микробиологического происхождения, которые используются для выделения лекарственных веществ. По способу получения лекарственных препаратов из лекарственного сырья выделяют: 1) простые лекарственные формы – получают механической обработкой лекарственного сырья (сборы, порошки); 2) галеновы препараты – получают при помощи сложной обработки, которая позволяет извлечь из сырья действующее начало в относительно чистом виде (настои, отвары, экстракты и настойки); 3) новогаленовы препараты – получают из галеновых лекарственных препаратов путем их дальнейшей очистки, они могут применяться для парентерального введения.
Например: лекарственным веществом является антибиотик ампициллин, лекарственным средством – ампициллина тригидрат, который может выпускаться в форме таблеток или капсул. Лекарственным препаратом являются таблетки ампициллина тригидрата по 0,25 г.

В самом общем виде лекарство можно определить как вещество, которое вызывает полезные изменения биологической функции за счет химического взаимодействия. Для того, чтобы обеспечить такое взаимодействие лекарство должно иметь определенную структуру, размеры и форму молекулы, реакционную способность, а также липофильность. Остановимся на каждом из этих факторов подробнее.
[ Структура лекарств. Молекулы лекарственного вещества принадлежат к различным классам органических соединений. Однако, подавляющее большинство лекарств содержит кислотные или оснóвные группировки и, поэтому, могут рассматриваться как слабые кислоты или основания.
[ Размеры молекулы лекарства. Молекулярные массы лекарств колеблются от очень малых (масса иона лития 7 Да), до чрезвычайно больших (молекула фибринолитического средства альтеплазы имеет молекулярную массу 59.050 Да). Однако, масса большинства лекарств лежит в пределах 100-1000 Да. Нижний уровень этого диапазона определяется, по-видимому, требованиями к избирательности действия лекарства: чтобы точно соответствовать лишь одному типу рецептора молекула лекарства должна иметь какой-то минимальный набор функциональных группировок, формирующих ее реакционный центр.
Верхняя граница массы определяется необходимостью проникновения лекарства через гисто-гематические барьеры в ткани. Лекарственные вещества с массой более 1000 Да чрезвычайно плохо проникают в патологические очаги и их применение может быть затруднено. Однако, высокая масса лекарства может рассматриваться и как позитивный фактор. Так, через плаценту практически не проникают лекарственные вещества с массой более 600 Да, поэтому при лечении инфекций у беременных женщин можно применять эритромицин (молекулярная масса 733 Да), назначать дигоксин для лечения сердечной недостаточности (молекулярная масса 780 Да).
[ Реакционная способность лекарства. Большинство лекарств не относится к классу высокореакционных соединений. Наиболее распространенный тип связи, который устанавливает лекарство со своим биологическим субстратом – электростатическое взаимодействие.
[ Форма молекул лекарства. В идеальном лекарственном средстве форма молекулы должна быть полностью комплиментарна форме биологического субстрата, с которым она взаимодействует, т.е. подходить к нему как «ключ к замку». Большинство лекарств являются хиральными соединениями, т.е. имеют центр ассимметрии и существуют в виде нескольких пространственных конфигураций. При этом возможно 4 принципиальных ситуации:
º Оба изомера являются фармакологически активными молекулами, хотя могут и отличаться по способности к метаболизму, токсичности и др. факторам. Например, хинин и его правовращающий изомер хинидин являются одинаково мощными противоаритмическими и противомалярийными средствами (хотя хинидин обладает лучшей переносимостью).
º Только один из изомеров является фармакологически активным, а второй – лишен фармакологического эффекта или оказывает его в незначительной степени. Например, l-пропранолол является b-адреноблокатором, тогда как d-пропранолол не способен блокировать адренорецепторы.
º Каждый из изомеров обладает уникальным фармакологическим действием. Например, l-соталол блокирует b-адренорецепторы, а d-соталол – не действует на адренорецепторы, но блокирует калиевые каналы.
º Один из изомеров оказывает фармакологическое, а другой – токсическое действие. Например, R-талидомид является снотворным, а S-талидомид – вызывает фокомелию (тератогенный эффект).
В настоящее время подавляющее большинство лекарственных средств выпускается в виде рацемических смесей. Как правило, так поступают из экономических соображений – производство лекарства в виде чистого изомера дорогостоящий процесс. Однако, в ряде случаев осуществляется производство именно чистых изомеров (гормон щитовидной железы l-тироксин, l-хлорамфеникол или левомицетин).
[ Липофильность лекарства. Для того, чтобы лекарственное вещество проникло из места введения к органам и тканям мишеням оно должно пройти через ряд клеточных биологических мембран, которые представляют собой липидные структуры. Поэтому, чем более липофильным является лекарственное вещество, тем оно быстрее проникает из места введения к месту своего действия.
Источник
Природа лекарственных средств это
Автор: К.С.ДАВЫДОВА, филиал «Клиническая фармакология» НЦ БМТ РАМН
Большая часть лекарственных средств ( ЛС ) на современном фармрынке являются воспроизведенными (генерическими) препаратами. Согласно данным розничного аудита (IMS Health и DSM Group) доля дженериков в настоящее время составляет от 77 до 88% в натуральном выражении [5] (существуют данные и про долю в 95% [9], однако ее достоверность вызывает сомнения), при этом согласно прогнозам эта доля будет неуклонно расти. По объему генерического сектора Россия занимает 3 место в мире после Китая и Индии [2,3]. В то же время структура рынка стран большой семерки формируется следующим образом: в США — 12% дженериков, в Японии — 30%, в Германии — 35%, во Франции — 50%, в Англии — 55%, в Италии — 60%, в Канаде — 64% (рис. 1) [8].
Среди препаратов, которые ежегодно регистрируются в России, отмечается значительно большее количество дженериков, чем оригинальных препаратов. Отдельные оригинальные препараты имеют значительное количество воспроизведенных ЛС. Так, оригинальное лекарственное средство Вольтарен (действующее вещество – диклофенак натрия) сегодня имеет 207 дженериков, зарегистрированных к медицинскому применению. Также в РФ зарегистрировано около 150 генерических ЛС эналаприла, около 100 — нифедипина, атенолола, ципрофлоксацина и порядка 50 – нитроглицерина, аспирина и парацетамола (причем количество комбинированных генерических последних двух ЛС превышает 300) [1,4]. В ряде стран с развитой системой контроля качества, эффективности и безопасности ЛС, число дженериков инновационного препарата в большинстве случаев не превышает 4-5 [10,19].
Генерические ЛС выводятся на рынок после истечения срока патентной защиты. Они должны полностью соответствовать оригинальному продукту по составу действующих веществ (вспомогательные вещества могут быть иными) и лекарственной форме, соответствовать фармакопейным требованиям, быть произведенными в условиях GMP. В Федеральном законе о лекарственных средствах №86-ФЗ от 1998 г. дается определение воспроизведенных ЛС: «воспроизведенные лекарственные средства — лекарственные средства, поступившие в обращение после истечения срока действия исключительных патентных прав на оригинальные лекарственные средства». Однако такое определение не характеризует дженерик как копию или аналог инновационного препарата. В новом Федеральном законе «Об обращении лекарственных средств» №61-ФЗ от 2010 г. смысл термина раскрывается более полно, согласно современным международным рекомендациям: «воспроизведенное лекарственное средство — лекарственное средство, содержащее такую же фармацевтическую субстанцию или комбинацию таких же фармацевтических субстанций в такой же лекарственной форме, что и оригинальное лекарственное средство, и поступившее в обращение после поступления в обращение оригинального лекарственного средства».
Воспроизведенные ЛС имеют ряд равнозначных общеупотребляемых синонимов – «генерики», «дженерики», «генерические лекарственные средства», «многоисточниковые (мультиисточниковые) лекарственные средства» [8,9], однако согласно Федеральному закону № 61-ФЗ именно термин «воспроизведенные лекарственные средства» должен применяться в первую очередь. В то же время Всемирная организация здравоохранения в качестве основного понятия таких ЛС рекомендует употреблять термин «многоисточниковые лекарственные средства» (multisource drugs) [20]. Оригинальное (инновационное) лекарственное средство – это ЛС, которое было впервые зарегистрировано на основе полной документации в отношении его качества, безопасности и эффективности, защищенное патентом на срок до 20 лет [11].
Основными характеристиками оригинального ЛС являются: длительность разработки (10-15 лет) на основании отбора действующего вещества из значительного количества молекул; фармакологический эффект, токсичность, мутагенность и тератогенность которого проверены в доклинических исследованиях на животных; прохождение всех фаз клинических исследований в соответствии со стандартами GСP.
Несмотря на то что инновационное и воспроизведенное ЛС содержат одно и то же действующее вещество в одинаковой дозировке и лекарственной форме, эффективность и безопасность генерических препаратов может существенно различаться. Основными причинами таких различий могут быть фармацевтическая технология производства лекарственного препарата, вспомогательные вещества (неактивные ингредиенты, наполнители, консерванты, красители и др.), их природа и количество, полиморфизм, солевая форма, упаковка препарата, условия его хранения и транспортировки. Из-за этих отличий эффективность генерических препаратов и выраженность их побочных эффектов может сильно варьировать.
При этом следует отметить, что стоимость воспроизведенного ЛС ниже, чем оригинального, что определяется рядом причин. Для этого необходимо рассмотреть, из чего складывается стоимость оригинальных ЛС и дженериков. 80% стоимости оригинального ЛС составляет стоимость исследований эффективности и безопасности препарата, а 20% стоимости – это стоимость синтеза лекарственного вещества. Процесс создания оригинального ЛС является очень длительным и дорогостоящим. Сначала создается молекула, потом она оценивается в исследованиях на клетках и тканях, затем на животных. После этого следуют три этапа клинических исследований на здоровых добровольцах и пациентах. После завершения клинических исследований ЛС проходит регистрацию. Исследование оригинального ЛС продолжается и после регистрации. С соблюдением правил GCP проводятся и пострегистрационные исследования [23].
Известно, что только 1 из 5 000 молекул доходит до рынка в виде ЛС. Этот путь продолжается 12-15 лет, его стоимость составляет от 800 млн. до 1 млрд. долл. Прибыльными являются только 1-2 из вновь созданных ЛС [8]. Объяснением более низкой стоимости генерических ЛС являются: отсутствие клинических исследований; отсутствие масштабных доклинических исследований фармакологической активности, поисковых исследований; отсутствие изучения полного профиля безопасности.
Несмотря на широкое использование понятия эквивалентность, «эквивалентности» дженериков как термина не существует. Всемирная организация здравоохранения предлагает применять термин «взаимозаменяемость» (interchangeability) воспроизведенных лекарственных препаратов [23]. Взаимозаменяемое генерическое ЛС – это терапевтически эквивалентное генерическое ЛС, которым можно заменить препарат сравнения в клинической практике [22]. Видов «эквивалентности» воспроизведенных ЛС выделяют несколько – терапевтическая, фармацевтическая, биологическая, а также т.н. «эквивалентность in vitro» (in vitro equivalence), введенная в употребление в документе «WHO Technical Report Series 937. WHO Expert Committee on Specifications for Pharmaceutical Preparations (2006). Annex 7. Multisource (generic) pharmaceutical products: guidelines on registration requirements to establish interchangeability» [23].
Терапевтически эквивалентными лекарственные препараты могут считаться только в том случае, если они фармацевтически эквивалентны и можно ожидать, что они будут иметь одинаковый клинический эффект и одинаковый профиль безопасности при использовании пациентами в соответствии с указаниями инструкции по применению [7,22]. Терапевтическая эквивалентность означает, что два препарата обеспечивают одинаковый терапевтический эффект и безопасность. Терапевтически эквивалентные лекарственные препараты должны отвечать следующим требованиям: иметь доказанную эффективность и безопасность; быть фармацевтически эквивалентными; быть биоэквивалентными; иметь сходные инструкции по применению; производиться в условиях стандарта GMP [6]. Доказанную клиническую эффективность и безопасность устанавливают на основании клинических исследований.
ЛС считаются фармацевтически эквивалентными, если они содержат одни и те же действующие вещества в одинаковом количестве и в одинаковой лекарственной форме и отвечают требованиям одних и тех же или сходных стандартов [1]. То есть фармацевтическая эквивалентность – это полное соответствие состава и лекарственной формы препаратов. Для некоторых лекарственных форм фармацевтическая эквивалентность будет обеспечивать терапевтическую эквивалентность и, соответственно, взаимозаменяемость двух препаратов (препараты для местного применения, порошки для изготовления растворов, инъекционные растворы и некоторые другие) [23].
Отдельно стоит выделить фармацевтическую альтернативность ЛС. Лекарственные средства являются фармацевтически альтернативными, если они содержат одинаковое количество одной и той же активной субстанции (субстанций), но различаются по лекарственной форме (например, таблетки и капсулы) и/или по химической форме (различные соли, эфиры) [1].
Оценка биоэквивалентности ЛС является основным видом медико-биологического контроля воспроизведенных (генерических) ЛС, не отличающихся лекарственной формой и содержанием действующих веществ от соответствующих оригинальных ЛС. Биоэквивалентность ЛС обозначает их одинаковую биодоступность. Под биодоступностью понимают количество неизмененного действующего вещества, достигающего системного кровотока (степень всасывания) относительно исходной дозы ЛС. Исследования биоэквивалентности позволяют сделать обоснованные заключения о качестве сравниваемых препаратов по относительно меньшему объему первичной информации и в более сжатые сроки, чем при проведении клинических исследований [17,18,21].
В некоторых международных руководствах введено понятие регуляторной процедуры «биовейвер», в соответствии с которой определение взаимозаменяемости генерических ЛС проводится на основании оценки их биофармацевтических свойств и эквивалентности in vitro (изучение сравнительной кинетики растворения) либо другими методами in vitro в качестве альтернативы исследованиям биоэквивалентности in vivo при их государственной регистрации [16].
Самое главное, к чему надо стремиться, — дженерики, как и инновационные (оригинальные) препараты, должны отвечать требованиям, предъявляемым в рамках Общего (или единого) технического документа (CTD): эффективность, безопасность, качество 14, поэтому весь объем исследований должен быть достаточным для подтверждения данных требований.
Литература
1. Арзамасцев А.П., Дорофеев В.Л. Эквивалентность воспроизведенных лекарственных средств: фармацевтические аспекты. // Ведомости НЦЭСМП. – М., 2007. – №1. – С. 27-35.
2. Баула О.Ю. Современные регуляторные требования к исследованиям и регистрации генерических лекарственных средств. – М., «Фармсодружество», 2007.
3. Белоусов Ю.Б. Дженерики – мифы и реалии. «Ремедиум». – 2003. — № 7–8. — С. 4–9.
4. Верткин А.Л., О.Б.Талибов. Генерики и эквивалентность – что стоит за терминами. Неотложная терапия. — 2004; — № 1–2. – С.16–17.
5. Новикова Н.Н. // Фармацевтический Вестник. – М., 2008. – №4. – С. 4.
6. Рудык Ю.С. К вопросу о терапевтической эквивалентности лекарственных средств // Рациональная фармакотерапия. – Киев, 2007. — №2. – С. 40-48.
7. Семинар-тренинг ВОЗ по проведению теста растворения, взаимозаменяемости лекарственных средств и системе биофармацевтической классификации. // Аптека, — Киев, 2007. – № 31. – С. 10-17.
8. Талибов О.Б. Генерики и эквивалентность лекарственных препаратов. // Медицинская газета «Здоровье Украины». – Киев, 2008. – №5. – С. 12-16.
9. Тарловская Е.И. Генерики и оригинальные препараты: взгляд практического врача. // Российский Медицинский Журнал. – М., 2008, – т. 16. – №5. – С. 30 – 35.
10. Чумак В.Т. Оборот лекарственных средств в Украине. Проблемы и перспективы. Материалы І Международной конференции «Клинические испытания лекарственных средств в Украине». — Киев, 2006.
11. Directive 2004/27/EC of the European Parliament and of the Council, Art. 10.1. – 2004.
12. ICH Harmonised Tripartite Guideline: The Common Technical Document for the Registration of Pharmaceuticals for Human Use: Quality M4Q (R1). – Geneva: ICH, 2002.
13. ICH Harmonised Tripartite Guideline: The Common Technical Document for the Registration of Pharmaceuticals for Human Use: Safety. M4S (R2). – Geneva: ICH, 2002.
14. ICH Harmonised Tripartite Guideline: The Common Technical Document for the Registration of Pharmaceuticals for Human Use: Efficacy. M4E (R1). – Geneva: ICH, 2002.
15. Interchangeability of multisource drug products containing highly variable drugs. WHO/FIP Training Workshop on Dissolution, Pharmaceutical Product Interchangeability and Biopharmaceuticals Classification System (BCS) — Kiev, 2007.
16. Yu G., Amidon J. Polli. Biopharmaceutics Classification System: The Scientific Basis for Biowaiver Extensions. // Pharmaceutical Research. – 2002. – Vol. 19, №. 7.
17. Chen M., Lesko L. Individual bioequivalence revisited. // Clin Pharmacokinet – 2001. – № 40: – pp. 701-706.
18. Chen M., Shah V., Patnaik R. Bioavailability and Bioequivalence: An FDA Regulatory Overview. // Pharmaceutical Research. – 2001. – Vol. 18, №. 12.
19. Laroche M., Merle L. Generic and brand-name drugs. Are different criteria sufficiently taken into account before granting market authorisation? // Acta Clin Belg Suppl. – 2006. – № 1: – pp. 48-50.
20. Multisource (Generic) Pharmaceutical Products: Guidelines on Registration Requirements to Establish Interchangeability. — WHO Technical Report Series, № 937. – WHO, 2006.
21. Quality of bioequivalence data. WHO workshop on assessment of bioequivalence data submitted to regulatory authorities – Kiev, 2009.
22. WHO Technical Report Series 937. WHO Expert Committee on Specifications for Pharmaceutical Preparations. – WHO, 2006.
23. WHO Technical Report Series 937, annex 7 « Multisource (generic) pharmaceutical products: guidelines on registration requirements to establish interchangeability». WHO Expert Committee on Specifications for Pharmaceutical Preparations. – WHO, 2006.
Рисунок — в приложении
Файл: Загрузить (85 кбайт)
Источник



