- Биотрансформация лекарственных веществ в организме
- Примеры биотрансформации лекарственных веществ в организме
- Пути выведения лекарственных веществ из организма
- БХ — 3 семестр / ()Лекции / ()Общие / Углеводы / БИОТРАНСФОРМАЦИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ В ОРГАНИЗМЕ
- Биотрансформация лекарственных веществ. Реакции I и II этапов метаболизма. Индукторы и ингибиторы микросомальных ферментов (примеры).
Биотрансформация лекарственных веществ в организме
ЛС, поступившие в организм, являются для него ксенобиотиками, т. е. чужеродными агентами, следовательно, они подлежат выведению. Комплекс физико-химических и (или) биохимических реакций, в результате которых ЛС превращается в более полярное (водорастворимое) соединение называется биотрансформацией.
Выделяют два основных вида превращения лекарственных препаратов:
Метаболическая трансформация (реакции I фазы, несинтетические реакции метаболизма).
Коньюгация (реакции IIфазы, синтетические рекции метаболизма).
Примеры биотрансформации лекарственных веществ в организме
— с глюкуроновой кислотой
Метаболизм лекарственных веществ в организме приводит к следующим последствиям:
Л.В. становятся гидрофильными, что ускоряет их выведение из организма через почки, так как снижается их реабсорбция в почечных канальцах.
Образующиеся метаболиты лекарственных веществ обычно обладают меньшей активностью, чем сами лекарства. Иногда метаболиты Л.В. более активны (диазепам метаболизируется в активный нордиазепам и оксазепам).
Ряд Л.С. выпускается как про-лекарства, в организме в процессе метаболизма они превращаются в активные вещества (леводопа → дофамин; метилдопа → метилнорадреналин)
Нередки случаи когда, под действием ферментов ксенобиотики превращаются в токсические вещества. Лидокаин → ксилид моноэтилглицид (обладает судорожной активностью); токсичны метаболиты метронидазола, нитрофурана.
На биотрансформацию Л.С. в организме влияет множество факторов: возраст, пол, питание, сопутствующие заболевания.
Поскольку печень – основной орган метаболизма ЛС, то любое нарушение ее функционального состояния отражается на фармакокинетике препарата. Многие ЛС оказывают влияние на метаболизм в печени, угнетая или стимулируя активность микросомальных ферментов, так фенобарбитал, бутадион стимулируют активность; верапамил, пропроналол ингибируют активность микросомальной системы.
Курение способствует индукции оксидаз ферментной системы цитохрома Р450 , в результате ускоряется метаболизм ЛС, подвергающихся окислению с участием этого фермента (теофиллин, дифенин, варфарин).
Влияние пищи – у вегетарианцев скорость биотрансформации снижена. При высоком содержании в пище белков – повышается.
Пути выведения лекарственных веществ из организма
Экскреция– выведение лекарственных средств из организма.
Лекарственные вещества и их метаболиты выводятся из организма различными путями:
через почки (гидрофильные лекарственные вещества) – основной путь выведения ЛС;
через печень (пенициллины, тетрациклины, стрептомицин);
через кишечник с калом (доксициклин);
через легкие (этиловый спирт, средства для ингаляционного наркоза);
с молоком матери (снотворные, болеутоляющие, никотин, спирт этиловый);
через слюнные, сальные, потовые железы (сульфаниламидные препараты, витамины группы В, галогеносодержащие).
Факторы, влияющие на процесс экскреции:
рН мочи, степень ионизации ЛВ;
При интоксикации организма процессом экскреции можно управлять, изменяя рН мочи. Так, при отравлении фармакологическими веществами основного характера, сдвиг рН мочи в кислую сторону, увеличит ионизацию вещества, что обеспечит усиление экскреции и наоборот.
Биотрансформация и экскреция ЛВ объединяются термином «элиминация». Наиболее значащей величиной, характеризующей элиминацию лекарства, является системный, или общий, клиренслекарственного вещества (Сl).Клиренс – это объем плазмы, полностью освобождающийся от вещества в единицу времени. Является главным параметром для управления режимом дозирования, определяется по формулам:
где Vd– объем распределения;
Кel — константа элиминации, мл/мин; л/ч.
Для большинства лекарств клиренс – величина постоянная и его можно найти в справочниках.
Источник
БХ — 3 семестр / ()Лекции / ()Общие / Углеводы / БИОТРАНСФОРМАЦИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ В ОРГАНИЗМЕ
БИОТРАНСФОРМАЦИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ В ОРГАНИЗМЕ.
Печень – самая крупная железа пищеварительного тракта. Она выполняет в организме функцию биохимической лаборатории и играет важную роль в белковом, углеводном и липидном обменах.
А). Участие в пищеварении: связано с образованием желчных кислот, способствующих эмульгации, расщеплению и всасыванию жиров и жирорастворимых веществ (например, витаминов А, D, E, K), а также активации липаз.
Б). Система гемостаза: печень поддерживает оптимальное состояние (содержание и/или активность) факторов системы гемостаза и агрегатного состояния крови (например, через образование компонентов свёртывающей системы, путём депонирования и выброса крови в сосудистое русло).
В). Участие в реакциях системы ИБН (иммунобиологического надзора): в связи с наличием в печени фагоцитирующих клеток фон Купффера, способных также к процессингу и презентации антигена лимфоцитам.
Г). Дезинтоксикация (барьерная функция): в печени проходит связывание токсичных веществ с глюкуроновой кислотой и сульфатами, инактивация аммиака, индола, скатолов, фенолов и др. соединений, поступающих из ЖКТ, а также попадающих в организм извне.
Вещества, поступающие в организм из окружающей среды и не используемые им для построения тканей организма или как источники энергии, называют чужеродными веществами, или ксенобиотиками. Эти вещества могут попадать в организм с пищей, через кожу, слизистые оболочки.
Чужеродные вещества, или ксенобиотики делят на две группы:
— продукты хозяйственной деятельности человека (промышленность, сельское хозяйство, транспорт).
— вещества бытовой химии (моющие средства, вещества для борьбы с насекомыми, парфюмерия и парафармация).
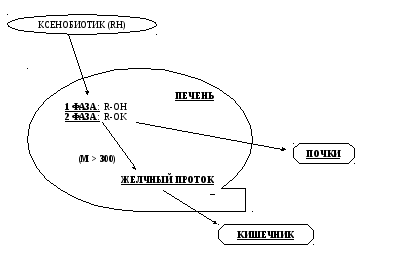
В зависимости от химического строения ксенобиотика, он претерпевает различные изменения в организме и в дальнейшем, при условии нормального гомеостаза выводится им (организмом). Гидрофильные ксенобиотики выводятся из организма в неизменном виде в мочой, в то время как гидрофобные задерживаются в тканях, связываясь с белками или образуя комплексы с липидами мембран, затем претерпевают ряд биохимических изменений и уже в изменённом состоянии выводятся из организма.
Как уже было упомянуто выше, большинство гидрофильных ксенобиотиков выводится из организма с мочой. Вещества, более гидрофобные или обладающие большей молекулярной массой (> 300 кД) выводятся с желчью в кишечник, а затем уже удаляются с фекалиями. Система обезвреживания включает множество разнообразных ферментов, под воздействием которых практически любой ксенобиотик может быть модифицирован.
Изменение химической структуры лекарственных веществ в организме называется их метаболизмом, а продукты метаболизма – метаболитами. В организме лекарственное вещество может подвергаться всем известным типам химических превращений. В результате метаболизма лекарственные вещества, как правило, теряют свою активность и приобретают более гидрофильные свойства.
Метаболизм лекарственных веществ может происходить во всех тканях и жидких средах организма, однако наиболее активно этот процесс происходит в полостях и слизистых оболочках желудка, а также печени.
МЕХАНИЗМ ВЫВЕДЕНИЯ КСЕНОБИОТИКОВ ИЗ ОРГАНИЗМА:
БИОТРАНСФОРМАЦИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ:
Лекарства, поступившие в организм, проходят ряд следующих превращений:
— связывание с белками и транспорт кровью
— взаимодействие с рецепторами
— распределение в тканях
— метаболизм и выведение из организма
Механизм первого этапа (всасывание) определяется физико-химическими свойствами лекарства. Гидрофобные соединения легко проникают через мембраны простой диффузией, в то время как лекарственные вещества, не растворимые в липидах, проникают через мембраны путём трансмембранного переноса при участии различных типов транслоказ. Некоторые нерастворимые крупные частицы могут проникать в лимфатическую систему путём пиноцитоза. Следующие этапы метаболизма лекарственного вещества в организме тоже определяются его химическим строением – гидрофобные молекулы перемещаются по крови в комплексе с альбумином, кислым а1-гликопротеином или в составе липопротеинов. В зависимости от структуры лекарственное вещество может поступать из крови в клетку или, являясь аналогами эндогенных веществ, связываться с рецепторами клеточной мембраны.
Действие на организм большинства веществ прекращается через некоторое время после их приёма. Прекращение действия может быть вызвано тем, что лекарственное вещество выводится из организма либо в неизменном виде (гидрофильные соединения), либо подвергается биотрансформации.
ИЗМЕНЕНИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ ПРИ БИОТРАНСФОРМАЦИИ:
Биохимические превращения лекарственных веществ в организме человека, обеспечивающие их инактивацию и детоксикацию, являются частичным проявлением биотрансформации ксенобиотиков. В результате биотрансформации лекарственных веществ может произойти:
— инактивация лекарственных веществ (снижение фармакологической активности)
— повышение активности лекарственных веществ
— образование токсических метаболитов
ИНАКТИВАЦИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ:
Инактивация лекарственных веществ, как и всех ксенобиотиков, происходит в две фазы. Первая фаза – химическая модификация под действием ферментов монооксигеназной системы ЭР. Например, лекарственное вещество барбитурат в ходе биотрансформации превращается в гидроксибарбитурат, который далее участвует в реакции конъюгации с остатком глюкуроновой кислоты. Фермент глюкуронил-трансфераза катализирует образование барбитуратглюкуронида, в качестве источника глюкуроновой кислоты используется УДФ-глюкуронил.
Другой пример инактивации лекарственного вещества – процесс метаболизма толуола. Толуол ферментами ЭР окисляется в бензиловый спирт. Затем из него в цитоплазме путём окисления образуется бензойная кислота, которая в митохондриях конъюгирует с глицином и в виде бензоглицина элиминирует в кровь, а затем выводится с мочой.
Некоторые лекарственные вещества способны индуцировать синтез микросомальных ферментов в ЭР. При этом лекарственное вещество в первые дни после приёма циркулирует в крови в количестве, достаточном для развития фармакологического эффекта, а затем начинает быстро разрушаться индуцированным ферментом. Таким свойством обладает бутадион, барбитураты (особенно фенобарбитал). Индуцированные ферменты, вызвавшие разрушение лекарственных средств могут сохраняться до двух месяцев. Некоторые хлорированные инсектициды (гексахлоран) оказались активными индукторами ферментов, разрушающих лекарственные вещества и даже естественные стероидные гормоны.
Путём образования эфирно-серных и эфирно-глюкуроновых кислот обезвреживаются фенолсодержащие соединения (например, камфора), хлоралгидрат, ароматические кислоты.
Многие ароматические соединения, соли тяжёлых металлов, образуют ковалентную связь с сульфгидридными группами цистеина и в таком виде выводятся из организма.
ПОВЫШЕНИЕ АКТИВНОСТИ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ:
Очень редко в процессе метаболизма образуются более активные лекарственные вещества, например, из противосифилитического средства новарсенола образуется арсеноксид.
Ещё одним примером образования более активного вещества является образование дезметилимипрамина из имипрамина, который имеет способность ослаблять депрессивное состояние при психических расстройствах.
При таких превращениях возможно не только усиление основного фармакологического действия, но и его подмена на совершенно противоположный усиленный в сотни раз эффект. Особенно эти эффекты могут быть выражены при неправильном лечении комплексами различных антагонистичных препаратов.
ОБРАЗОВАНИЕ ТОКСИЧЕСКИХ ПРОДУКТОВ ИЗ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ:
В отдельных случаях химические превращения лекарственных веществ в организме могут приводить к появлению у них токсических свойств. Так, жаропонижающее, болеутоляющее, противовоспалительное средство фенацетин превращается в парафенацетин, вызывающий гипоксию за счёт образования метгемоглобина – неактивной формы Hb.
ФАКТОРЫ, ВЛИЯЮЩИЕ НА АКТИВНОСТЬ ФЕРМЕНТОВ БИОТРАНСФОРМАЦИИ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ:
Скорость метаболизма лекарственных веществ зависит от состояния организма. У утомлённых и ослабленных людей обезвреживание происходит медленнее. Метаболизм некоторых ЛС снижается при недостатке кислорода. Например, этаминал-натрий (снотворное) разрушается быстрее в присутствии кислорода, поэтому увеличение парциального давления кислорода во вдыхаемом воздухе уменьшает длительность сна.
При заболеваниях печени инактивация ЛС замедляется, поэтому в организме при понижении скорости метаболизма уровень ЛС в крови повышается, а длительность нахождения их увеличивается. В таких случаях значительно снижают дозу.
Чувствительность к ЛС меняется в зависимости от возраста. Например, у новорождённых активность метаболизма в первый месяц жизни существенно отличается от взрослых. Это связано с недостаточностью многих ферментов, участвующих в биотрансформации ЛС, функции почек, повышенной проницаемости гематоэнцефалического барьера, недоразвитием ЦНС. В пожилом возрасте метаболизм ЛС протекает менее эффективно, чем у молодых. Снижается функциональная активность печени, нарушается скорость экскреции препаратов почками, В целом чувствительность в старческом возрасте к большинству препаратов понижена, в связи с чем их доза должна быть снижена.
В ряде случаев повышенная чувствительность к ЛС может быть обусловлена наследственной недостаточностью некоторых ферментов (энзимопатии), участвующих в их метаболизме. Например, при генетической недостаточности холинэстеразы плазмы крови длительность действия миелорелаксанта дитилина резко возрастает и может достигать 6-8 часов, вместо 5-7 минут. Известно, что скорость ацетилирования противотуберкулёзного средства изониазида варьирует довольно широко. Выделяют лиц с медленной и быстрой инактивацией. Считают, что у лиц с медленной инактивацией нарушена структура белков, регулирующих синтез фермента ацетилтрансферазы, обеспечивающего конъюгацию с ацетильным остатком.
Существенное влияние на метаболизм в организме оказывают также факторы окружающей среды, такие как ионизирующее облучение, температура, состав пищи и особенно различные химические вещества (ксенобиотики), в том числе и сами лекарственные вещества.
Источник
Биотрансформация лекарственных веществ. Реакции I и II этапов метаболизма. Индукторы и ингибиторы микросомальных ферментов (примеры).
Биотрансформация (метаболизм) — изменение химической структуры лекарственных веществ и их физикохимических свойств под действием ферментов организма. Основной направленностью этого процесса является превращение липофильных веществ, которые легко реабсорбируются в почечных канальцах, в гидрофильные полярные соединения, которые быстро выводятся почками (не реабсорбируются в почечных канальцах). В процессе биотрансформации, как правило, происходит снижение активности (токсичности) исходных веществ. Биотрансформация липофильных ЛВ в основном происходит под влиянием ферментов печени, локализованных в мембране эндоплазматического ретикулума гепатоцитов. Эти ферменты называются микросомальными, потому что они оказываются связанными с мелкими субклеточными фрагментами гладкого эндоплазматического ретикулума (микросомами), которые образуются при гомогенизации печеночной ткани или тканей других органов и могут быть выделены центрифугированием (осаждаютсяв так называемой «микросомальной» фракции). В плазме крови, а также в печени, кишечнике, легких, коже, слизистых оболочках и других тканях имеются немикросомальные ферменты, локализованные в цитозоле или митохондриях. Эти ферменты могут участвовать в метаболизме гидрофильных веществ. Различают два основных вида метаболизма лекарственных веществ (этапы): • несинтетические реакции (метаболическая трансформация); • синтетические реакции (конъюгация).
биотрансформация (реакции метаболизма 1-й фазы), происходит под действием ферментов — окисление, восстановление, гидролиз.
конъюгация (реакции метаболизма 2-й фазы), при которой происходит присоединение к молекуле вещества остатков других молекул (глюкуроновой, серной кислот, алкильных радикалов), с образованием неактивного комплекса, легко выводимого из организма с мочой или калом.
Лекарственные вещества могут подвергаться или метаболической биотрансформации (при этом образуются вещества, называемые метаболитами), или конъюгации (образуются конъюгаты). Но большинство Л В сначала метаболизируется при участии несинтетических реакций с образованием реакционноспособных метаболитов, которые затем вступают в реакции конъюгации. Кметаболической трансформации относятся следующие реакции: окисление, восстановление, гидролиз. Многие липофильные соединения подвергаются окислению в печени под влиянием микросомальной системы ферментов, известных как оксидазы смешанных функций, или монооксигеназы. Основными компонентами этой системы являются цитохром Р450 редуктаза и цитохром Р450 гемопротеин, который связывает молекулы лекарственного вещества и кислород в своем активном центре. Реакция протекает при участии НАДФН. В результате происходит присоединение одного атома кислорода к субстрату (лекарственному веществу) с образованием гидроксильной группы (реакция гидроксилирования).
Под действием некоторых лекарственных веществ (фенобарбитал, рифампицин, карбамазепин, гризеофульвин) может происходить индукция (увеличение скорости синтеза) микросомальных ферментов печени. В результате при одновременном назначении с индукторами микросомальных ферментов других препаратов (например, глюкокортикоидов, пероральных контрацептивов) повышается скорость метаболизма последних и снижается их действие. В некоторых случаях может увеличиваться скорость метаболизма самого индуктора, вследствие чего уменьшаются его фармакологические эффекты (карбамазепин). Некоторые лекарственные вещества (циметидин, хлорамфеникол, кетоконазол, этанол) снижают активность (ингибиторы) метаболизирующих ферментов. Например, циметидин является ингибитором микросомального окисления и, замедляя метаболизм варфарина, может повысить его антикоагулянтный эффект и спровоцировать кровотечение. Известны вещества (фуранокумарины), содержащиеся в грейпфрутовом соке, которые угнетают метаболизм таких лекарственных веществ, как циклоспорин, мидазолам, алпразолам и, следовательно, усиливают их действие. При одновременном применении лекарственных веществ с индукторами или ингибиторами метаболизма необходимо корректировать назначаемые дозы этих веществ.
Пути выведения лекарственных веществ из организма, значение, понятие о квоте элиминации, периоде полувыведения (Т 1/2) и общем плазматическом клиренсе. Зависимость действия лекарственных веществ от пути выведения, примеры.
Выведение неизмененного лекарственного вещества или его метаболитов осуществляется всеми экскреторными органами (почками, кишечником, легкими, молочными, слюнными, потовыми железами и др.).
Основным органом выведения лекарств из организма являются почки. Выведение лекарств почками происходит путем фильтрации и с помощью активного или пассивного транспорта. Липоидорастворимые вещества легко фильтруются в клубочках, но в канальцах они вновь пассивно всасываются. Препараты, слабо растворимые в липоидах, быстрее выводятся с мочой, поскольку они плохо реабсорбируются в почечных канальцах. Кислая реакция мочи способствует выведению щелочных соединений и затрудняет экскрецию кислых. Поэтому при интоксикации лекарствами кислого характера (например, барбитуратами) применяют натрия гидрокарбонат или другие щелочные соединения, а при интоксикации алкалоидами, имеющими щелочной характер, используют аммония хлорид. Ускорить выведение лекарств из организма можно и назначением сильнодействующих мочегонных средств, например, осмотических диуретиков или фуросемида, на фоне введения в организм большого количества жидкости (форсированный диурез). Выведение из организма оснований и кислот происходит путем активного транспорта. Этот процесс идет с затратой энергии и с помощью определенных ферментных систем-переносчиков. Создавая конкуренцию за переносчик каким-либо веществом, можно замедлить выведение лекарства (например, этамид ипенициллин секретируются с помощью одних и тех же ферментных систем, поэтому этамидзамедляет выведение пенициллина).
Препараты, плохо всасывающиеся из желудочно-кишечного тракта, выводятся кишечником и применяются при гастритах, энтеритах и колитах (например, вяжущие средства, некоторыеантибиотики используемые при кишечных инфекциях). Кроме того, из печеночных клеток лекарства и их метаболиты попадают в желчь и с нею поступают в кишечник, откуда либо повторно всасываются, доставляются в печень, а затем с желчью в кишечник (кишечно- печеночная циркуляция), либо выводятся из организма с каловыми массами. Не исключается и прямая секреция ряда лекарств и их метаболитов стенкой кишечника.
Через легкие выводятся летучие вещества и газы (эфир, закись азота, камфора и т.д.). Для ускорения их выброса необходимо увеличить объем легочной вентиляции.
Многие лекарственные препараты могут экскретироваться с молоком, особенно слабые основания и неэлектролиты, что следует учитывать при лечении кормящих матерей.
Некоторые лекарственные вещества частично выводятся железами слизистой оболочки полости рта, оказывая местное (например, раздражающее) действие на путях выведения. Так, тяжелые металлы (ртуть, свинец, железо, висмут), выделяясь слюнными железами, вызывают раздражение слизистой оболочки полости рта, возникают стоматиты и гингивиты. Кроме того, они вызывают появление темной каймы по десневому краю, особенно в области кариозных зубов, что обусловлено взаимодействием тяжелых металлов с сероводородом в полости рта и образованием практически нерастворимых сульфидов. Такая «кайма» является диагностическим признаком хронического отравления тяжелыми металлами.
При длительном применении дифенина и вальпроата натрия (противосудорожныепрепараты) раздражение слизистой оболочки десны может быть причиной возникновения гипертрофического гингивита («дифениновый гингивит»).Уровень элиминации любого лекарственного вещества оценивают при помощи двух основных тестов:
во-первых, определяют время, в течение которого элиминирует половина введенной дозы химиопрепарата, то есть находят полупериод жизни последнего (Т 1/2);
во-вторых, вычисляют процент той части однократной дозы препарата, которая элиминирует на протяжении суток (коэффициент, или квота, элиминации).
Эти два критерия элиминации любого лекарственного вещества не являются стабильными, ибо зависят от комплекса условий. Среди последних существенная роль отводится свойствам самого препарата и состоянию организма. Они зависят от скорости метаболизма лекарственного вещества в тканях и жидких средах организма, интенсивности его экскреции, функционального состояния печени и почек, пути введения химиопрепарата, длительности и условий хранения, липоидорастворимости, химического строения и т. д. Элиминация жирорастворимых, ионизированных лекарственных веществ, связанных с белками, осуществляется медленнее» чем препаратов водорастворимых, ионизированных, не связанных с белками. При введении высоких доз лекарственных средств элиминация их удлиняется, что обусловлено интенсификацией всех процессов, участвующих в транспорте, распределении, метаболизме и выделении химиопрепаратов. Элиминация большинства лекарственных средств у детей значительно ниже, чем у взрослых. Особенно замедлена она у недоношенных детей первых месяцев жизни. Резко удлиняют элиминацию врожденные и приобретенные энзимопатии (недостаточность глюкозо-6-фосфатдегидрогеназы, N-ацетилтрансферазы в др.), заболевания печени и почек, протекающие с недостаточностью их функций. На скорость элиминации влияют и другие факторы: пол больного, температура тела, физиологические биоритмы, пребывание ребенка в постели и т. д. Данные о полупериоде жизни препаратов позволяет врачу более обоснованно назначать разовую и суточную, дозу того или иного лекарственного средства, кратность введения его.
Источник