Первая помощь при тяжелой преэклампсии
Беременные с преэклампсией или эклампсией, должны госпитализироваться в акушерско-гинекологическое отделение.
Перед транспортировкой в стационар на месте купируется судорожная готовность. Для этого используется в/в ведение 1—2 мл 0,1% р-ра рауседила, 2—4 мл 0,5% р-ра седуксена (сибазон), 2—4 мл 0,25% р-ра дроперидола или I мл 2% р-ра промедола. Для поддержания работы сердца в/в на физиологическом растворе вводятся сердечные гликозиды типа корглюкона в общепринятых дозировках. Высокое АД купируется в/м введением ганглиоблокаторов типа пентамина. По пути следования, при необходимости, больной проводится превентивное лечение судорожной готовности.
При поступлении в стационар в приемном отделении все необходимые манипуляции следует выполнять под наркозом закисью азота в смеси с кислородом.
В отделении интенсивной терапии больную помещают в индивидуальную палату, исключают возможность воздействия внешних раздражителей (громкий звук, боль, яркий свет) и, в зависимости от вида гестоза, проводят специфическую терапию.
1. Седативная терапия при гестозе. Оптимальным препаратом воздействия на ЦНС является рауседил, обладающий седативным и гипотензивным действием (ампулы по 1 мл 0,1% или 0,25% р-ра); его вводят по 1—2,5 мг в/в медленно. Рауседил с успехом можно заменить транквилизатором сибазоном (синонимы: седуксен, реланиум). Препарат вводится медленно, в/в, в разведении на 10—20 мл физиологического раствора в количестве 10—20 мг (2—4 мл). Хорошим эффектом обладает нейролептик дроперидол. Его вводят также в/в медленно, в разведении, в дозе 5—10 мг (2—4 мл 0,25% р-ра). Данные препараты снижают возбудимость центров головного мозга, способствуют стабилизации АД. Для усиления действия седативных препаратов, с целью десенсибилизации и получения антигистаминного эффекта, показано использование препаратов типа димедрола (1—2 мл 1% р-ра). При высокой судорожной готовности и необходимости проведения неотложных манипуляций, показан кислородно-закис-ный наркоз. При необходимости быстрого ввода больной в наркоз в качестве вводного наркоза можно использовать фторотан, с последующим переходом на другой анестетик.
2. Спазмолитическая и гипотензивйая терапия при преэклампсии, эклампсии. При проведении гипотензивной терапии следует проводить сочетанное использование мощных, быстродействующих, но с коротким клиническим эффектом препаратов типа ганглиоблокаторов, с постоянным фоновым введением препаратов, обладающих менее мощным эффектом, но большей продолжительностью действия (дибазол, но-шпа, эуфиллин).
Лечение при преэклампсии, эклампсии следует начинать с в/в медленного введения 3—4 мл 1% р-ра дибазола (см. также тему ГИПЕРТОНИЧЕСКИЕ КРИЗЫ), а затем 10—20 мл 2,4% р-ра эуфиллина. Фоновыми препаратами могут являться спазмолитики типа но-шпы в общепринятых дозах. При отсутствии должного эффекта от вышеуказанной гипотензивной терапии можно попробовать применить ганг-лиоблокаторы типа бензогексоний в виде 1 мл 1% р-ра в/в или в/ м или арфонад (250 мг в разведении на 150—200 мл физраствора, в/в медленно, капельно, под постоянным контролем АД).
Хорошим многосторонним эффектом обладает сульфат магния. В. Н. Серов (1989) рекомендует придерживаться следующих принципов подбора и скорости введения данного препарата в зависимости от величины среднего АД: до 120 мм рт. ст. — 30 мл 25% р-ра магния сульфата; от 121 до 130 мм рт. ст. — 40 мл 25% р-ра, выше 130 мм рт. ст. — 50 мл в 400 мл реополиглюкина. Рекомендуемая скорость введения — около 100 мл/час, следовательно, на всю инфузию потребуется 4 часа.
3. Инфузионная терапия при преэклампсии, эклампсии. В патогенетической терапии эклампсии одно из первых мест занимает инфузионная терапия (ИТ), целью которой является восполнение ОЦК, восстановление нормальной тканевой перфузии и органного кровотока, устранение гемокон-центрации и гиперпротеинемии, коррекция КЩС. Их проводят под контролем Ht и диуреза. Гематокрит не рекомендуется снижать ниже 30%. Общее количество вводимой при ИТ жидкости не должно превышать 1200—1400 мл/сут., а скорость введения — 20—40 кап./ мин. Коррекцию гипопротеинемии осуществляют капельным в/в введением кровезамещаюших растворов, 100—200 мл альбумина или 150—200 мл сухой плазмы. Для нормализации реологии крови применяют в/в капельное введение 400 мл реополиглюкина. 4. Другие виды терапии. Для нормализации сосудистой проницаемости назначается 5—8 мл 5% р-ра аскорбиновой к-ты, гормоны типа преднизолон в дозе 60— 100 мг. Для нормализации реологических и коагуляционных свойств крови используют гепарин в дозе 350 ЕД/кг/сутки, трентал, курантил. Дегидратационная терапия включает в/в назначение 40—60 мг лазикса. Для снятия интоксикации применяют в/в введение 200—400 мл гемодеза и 200—400 мл глюкозо-новокаиновой смеси (200 мл 20% р-ра глюкозы, 200 мл 0,5% р-ра новокаина, инсулин 14—16 ЕД). Одновременно проводят профилактику внутриутробной гипоксии плода: ингаляция кислорода, в/в введение растворов глюкозы, рибоксин и т. д.
Источник
Преэклампсия (гестоз) — симптомы и лечение
Что такое преэклампсия (гестоз)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Дубовой А. А., акушера со стажем в 13 лет.
Определение болезни. Причины заболевания
Преэклампсия — осложнение второй половины беременности, при котором из-за увеличения проницаемости стенки сосудов развиваются нарушения в виде артериальной гипертензии, сочетающейся с потерей белка с мочой (протеинурией), отеками и полиорганной недостаточностью. [1]
По сути, причиной преэклампсии является беременность: именно при ней возникают патологические события, в конечном счете приводящие к клинике преэклампсии. У небеременных преэклампсии не бывает.
В научной литературе описывается более 40 теорий происхождения и патогенеза преэклампсии, а это указывает на отсутствие единых взглядов на причины ее возникновения. Установлено, что преэклампсии чаще подвержены молодые и нерожавшие женщины (от 3 до 10%). [2] У беременных с планируемыми вторыми родами риск ее возникновения составляет 1,4-4%. [3]
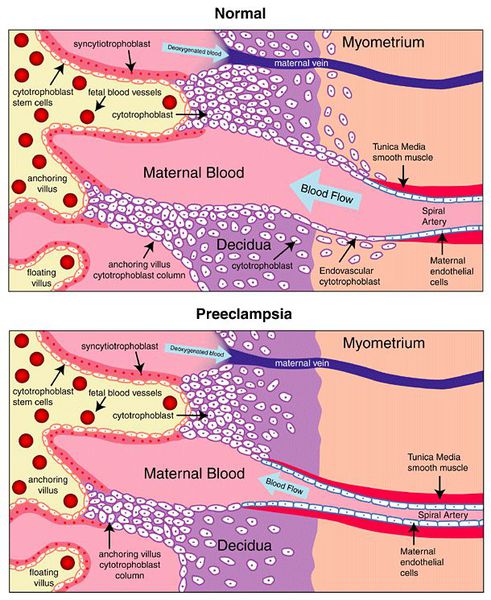
Пусковым моментом в развитии преэклампсии в современном акушерстве считается нарушение плацентации. Если беременность протекает нормально, с 7 по 16 неделю эндотелий (внутренняя оболочка сосуда), внутренний эластичный слой и мышечные пластинки участка спиральных артерий, вытесняется трофобластом и фибриносодержащим аморфным матриксом (составляющие предшественника плаценты — хориона). Из-за этого понижается давление в сосудистом русле и создается дополнительный приток крови для обеспечения потребностей плода и плаценты. Преэклампсия связана с отсутствием или неполным вторжением трофобласта в область спиральных артерий, что приводит к сохранению участков сосудистой стенки, имеющей нормальное строение. В дальнейшем воздействие на эти сосуды веществ, вызывающих вазоспазм, ведет к сужению их просвета до 40% от нормы и последующему развитию плацентарной ишемии. При нормальном течении беременности до 96% из 100-150 спиральных артерий матки претерпевают физиологические изменения, при преэклампсии же — всего 10%. Исследования подтверждают, что наружный диаметр спиральных артерий при патологической плацентации вдвое меньше, чем должно быть в норме. [4] [5]
Симптомы преэклампсии
Раньше в отечественном акушерстве то, что сейчас называется термином «преэклампсия», называлось «поздний гестоз», а непосредственно под преэклампсией понимали тяжелую степень позднего гестоза. Сегодня в большинстве регионов России перешли на классификацию, принятую ВОЗ. Ранее говорили о так называемом ОПГ-гестозе (отеки, протеинурия и гипертензия).
1. Артериальная гипертензия
Преэклампсия характеризуется систолическим АД>140 мм рт. ст. и/или диастолическим АД>90 мм рт. ст., измеряется дважды с интервалом 6 часов. По меньшей мере два повышенных значения АД являются основанием для диагностики АГ во время беременности. Если есть сомнения, рекомендуется провести суточное мониторирование АД (СМАД).
2. Протеинурия
Чтобы диагностировать протеинурию, необходимо выявить количественное определение белка в суточной порции (в норме при беременности — 0,3 г/л). Клинически значимая протеинурия во время беременности определена как наличие белка в моче ≥ 0,3 г/л в суточной пробе (24 часа) либо в двух пробах, взятых с интервалом в 6 часов; при использовании тест-полоски (белок в моче) — показатель ≥ «1+».
Умеренная протеинурия — это уровень белка > 0,3 г/24 часа или > 0,3 г/л, определяемый в двух порциях мочи, взятой с интервалом в 6 часов, или значение «1+» по тест-полоске.
Выраженная протеинурия — это уровень белка > 5 г/24 часа или > 3 г/л в двух порциях мочи, взятой с интервалом в 6 часов, или значение «3+» по тест-полоске.
Чтобы оценить истинный уровень протеинурии, нужно исключить наличие инфекции мочевыделительной системы, а патологическая протеинурия у беременных является первым признаком полиорганных поражений. [1]
3. Отечный синдром
Триада признаков, описанная Вильгельмом Цангемейстером в 1912 г. (ОПГ-гестоз), сегодня встречается лишь в 25-39%. Наличие отеков в современном акушерстве не считается диагностическим критерием преэклампсии, но важно, когда нужно оценить степень ее тяжести. Когда беременность протекает нормально, отеки встречаются в 50-80% случаев, амбулаторное ведение безопасно для лёгкого отечного симптома. Однако генерализованные, рецидивирующие отеки зачастую являются признаком сочетанной преэклампсии (нередко на фоне патологии почек). [6]
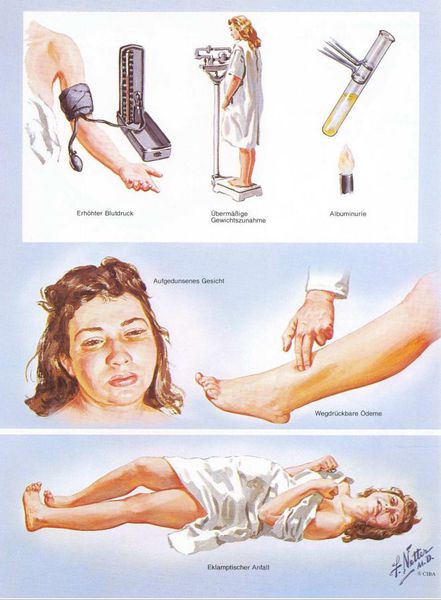
Американский врач-хирург и художник-иллюстратор Фрэнк Генри Неттер, которого справедливо прозвали «Микеланджело медицины», очень наглядно изобразил основные проявления преэклампсии. [7]
Патогенез преэклампсии
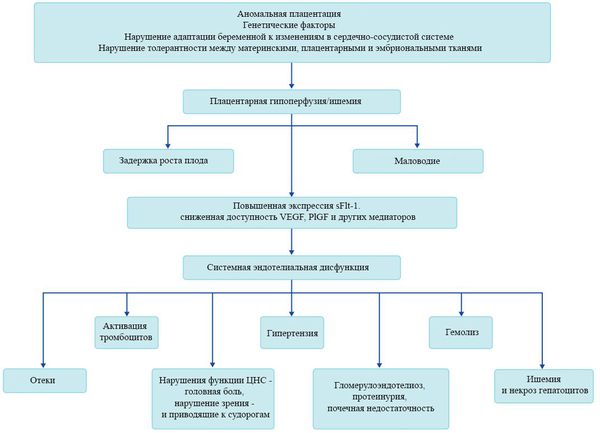
В ответ на ишемию при нарушении имплантации (см. рисунок) начинают активно вырабатываться плацентарные, в том числе антиангиогенные факторы и медиаторы воспаления, повреждающие клетки эндотелия. [8] Когда компенсаторные механизмы кровообращения на исходе, плацента с помощью прессорных агентов активно «подстраивает» под себя артериальное давление беременной, при этом временно усиливая кровообращение. В итоге этого конфликта возникает дисфункция эндотелия. [9]
При развитии плацентарной ишемии активируется большое количество механизмов, ведущих к повреждению эндотелиальных клеток во всем организме, если процесс генерализуется. В результате системной эндотелиальной дисфункции нарушаются функции жизненно важных органов и систем, и в итоге мы имеем клинические проявления преэклампсии.
Нарушение плацентарной перфузии из-за патологии плаценты и спазма сосудов повышает риск гибели плода, задержки внутриутробного развития, рождения детей малых для срока и перинатальной смертности. [10] Кроме того, состояние матери нередко становится причиной прерывания беременности на раннем этапе — именно поэтому дети, родившиеся от матерей с преэклампсией, имеют более высокий показатель заболеваемости респираторным дистресс-синдромом. Отслойка плаценты очень распространена среди больных преэклампсией и связана с высокой перинатальной смертностью.
Классификация и стадии развития преэклампсии
| Умеренная преэклампсия | Сочетание двух основных симптомов: I. Систолическое АД 141-159 мм рт. ст. и/или диастолическое АД,91-99 мм рт. ст. при двукратном измерении с интервалом 6 часов II. Содержание белка в суточной моче 0,3 гр. и более |
|---|---|
| Тяжелая преэклампсия | I. Цифры АД 160/100 мм рт. ст. и выше, измеренного как минимум дважды с интервалом 6 часов в горизонтальном положении беременной и/или II. Протеинурия 5 грамм в сутки и более или 3 грамма в отдельных порциях мочи, полученных дважды с разницей 4 часа и более и/или присоединение к симптомам умеренной преэклампсии хотя бы одного из следующих: — олигурия, 500 мл в сутки и менее; — отек легких или дыхательная недостаточность, (цианоз); — боль в эпигастрии или правом подреберье, тошнота, рвота, ухудшение функции,печени; — церебральные нарушения (головная боль, нарушение сознания, ухудшения зрения — фотопсии); — тромбоцитопения (ниже 100х109/мл); — выраженная задержка роста плода; — начало до 32-34 недель и наличие признаков фетоплацентарной недостаточности. |
| Диагноз тяжелой преэклампсии устанавливается при наличии: — двух основных критериев тяжелой степени (АГ и протеинурия) или — одного основного критерия любой степени и дополнительного критерия. | |
Эклампсия – состояние, при котором в клинических проявлениях преэклампсии преобладают поражения головного мозга, сопровождаемые судорожным синдромом, который не может быть объяснен другими причинами, и следующим после него периодом разрешения. Эклампсия может развиться на фоне преэклампсии любой степени тяжести, а не является проявлением максимальной тяжести преэклампсии.
Осложнения преэклампсии
Основные осложнения преэклампсии:
- гипертоническая энцефалопатия;
- геморрагический инсульт;
- субарахноидальное кровоизлияние;
- преждевременная отслойка плаценты (7-11%);
- ДВС-синдром (8%);
- острая гипоксия плода (48%) и внутриутробная гибель плода;
- отек легких (3-5%);
- легочно-сердечная недостаточность (2-5%);
- аспирационная пневмония (2-3%);
- нарушения зрения;
- острая почечная недостаточность (5-9%);
- гематома печени (1%);
- HELLP-синдром (10-15%);
- послеродовый психоз.
Диагностика преэклампсии
Диагностика преэклампсии заключается прежде всего в установлении наличия указанных выше симптомов. В ряде случаев представляет сложность дифференциальная диагностика преэклампсии и существовавшая до беременности артериальная гипертензия.
Дифференциальная диагностика гипертензивных осложнений беременности
| Клинические признаки | Хроническая гипертензия | Преэклампсия |
|---|---|---|
| Возраст | часто возрастные (более 30 лет) | часто молодые ( [1] |
- При умеренной преэклампсии беременную следует госпитализировать, чтобы уточнить диагноз и провести тщательный мониторинг ее состояния и плода, но при этом возможно продолжение вынашивания до 37 недель. При ухудшении состояния матери и плода показано родоразрешение.
- При тяжелой преэклампсии нужно сначала стабилизировать состояние матери, а затем решать вопрос о родоразрешении, желательно после проведения профилактики респираторного дистресс-синдрома плода, если беременность менее 34 недель.
2. Антигипертензивная терапия
Цель лечения — поддерживать АД в пределах, которые сохраняют на нормальном уровне показатели маточно-плодового кровотока и снижают риск развития эклампсии.
Антигипертензивную терапию следует проводить, постоянно контролируя состояние плода, потому что снижение плацентарного кровотока провоцирует у него прогрессирование функциональных нарушений. Критерием начала антигипертензивной терапии является АД ≥ 140/90 мм рт. ст.
Основные лекарственные средства, используемые для лечения АГ в период беременности:
- Метилдопа (допегит) — антигипертензивный препарат центрального действия, α2-адреномиметик (препарат первой линии);
- Нифедипин — блокатор кальциевых каналов (препарат второй линии);
- β-адреноблокаторы: метопролол, пропранолол, соталол, бисопролол;
- По показаниям: верапамил, клонидин, амлодипин.
3. Профилактика и лечение судорог
Для профилактики и лечения судорог основным препаратом является сульфат магния (MgSO4). Показанием для противосудорожной профилактики является тяжелая преэклампсия, если есть риск развития эклампсии. При умеренной преэклампсии — в отдельных случаях решает консилиум, потому что при этом повышается риск кесарева сечения и есть ряд побочных эффектов. Механизм действия магния объясняется нарушением тока ионов кальция в гладкомышечную клетку.
Кроме того, необходимо контролировать водный баланс, уделять внимание лечению олигурии и отека легких при их возникновении, нормализации функции ЦНС, реологических свойств крови, улучшение плодового кровотока.
Прогноз. Профилактика
Сегодня до 64% смертей от преэклампсии предотвратимы.
Основные факторы качественной и своевременной помощи:
- выявление женщин, входящих в группу высокого риска;
- качественное ведение беременности до клинических появлений осложнения беременности;
- адекватная тактика после клинической манифестации акушерского осложнения.
К сожалению, сегодня нет достаточно чувствительных и специфичных тестов, которые бы обеспечивали раннюю диагностику/выявление риска развития преэклампсии.
Факторы риска развития преэклампсии: [2]
1. антифосфолипидный синдром;
2. заболевания почек;
3. преэклампсия в анамнезе;
4. предстоящие первые роды;
5. хроническая гипертензия;
6. сахарный диабет;
7. жительницы высокогорных районов;
8. многоплодная беременность;
9. сердечно-сосудистые заболевания в семье (инсульты/инфаркты у близких родственников);
10. системные заболевания;
12. преэклампсия в анамнезе у матери пациентки;
13. возраст 40 лет и старше;
14. прибавка массы тела при беременности свыше 16 кг.
Установлено, что для преэклампсии характерен недостаточный ангиогенез — процесс образования сосудов. [11] В нем участвуют около 20 стимулирующих и 30 ингибирующих ангиогенез факторов, их список постоянно пополняется. Наиболее изучен и представляют особый интерес с точки зрения исследования патогенеза преэклампсии два проангиогенных фактора: сосудисто-эндотелиальный фактор роста (VEGF) и плацентарный фактор роста (PlGF), антиангиогенный фактор — Fms-подобная тирозинкиназа (Flt-1) и ее растворимая форма (sFlt-1).
Повышение содержания этого sFlt-1 с одновременным снижением VEGF и PlGF начинается за 5-6 недель до клинических проявлений преэклампсии. [12] Данный факт позволяет прогнозировать развитие преэклампсии у женщин из группы риска в первом триместре беременности. Однако другими исследователями отмечено, что несмотря на высокую чувствительность теста (96%), изолированное определение sFlt-1 не может быть использовано при диагностике преэклампсии из-за низкой специфичности. Таким образом, обнаружение изменений в соотношении уровня PlGF и sFlt-1 в течение беременности может сыграть важную вспомогательную роль для подтверждения диагноза преэклампсии.
Сегодня существуют коммерческие наборы, которые позволяют проводить иммуноферментное исследование, чтобы определить вероятность развития преэклампсии, на основании определения содержания PlGF (DELFIA Xpress PlGF kit, PerkinElmer; США), предложены скрининговые тесты для прогнозирования и ранней диагностики преэклампсии, основанные на определении соотношения sFlt-1 и PlGF (Elecsys sFlt-1/PlGF, Roche, Швейцария).
Из-за нарушения инвазии трофобласта увеличивается сосудистое сопротивление в маточной артерии и снижается перфузия плаценты. Повышение пульсационного индекса и систолодиастолического отношения в маточной артерии в 11-13 недель беременности является лучшим предиктором преэклампсии, и его настоятельно рекомендуется использовать в клинической практике у беременных из группы риска.
Из-за того, что исчерпывающая информация об этиологии и патофизиологии преэклампсии отсутствует, разработка эффективных профилактических мер представляет определенные трудности.
Сегодня доказан прием только 2 групп препаратов для профилактики преэклампсии: [1] [2]
• Аспирин в низких дозах (75 мг в день), начиная с 12 недель до родоразрешения. При этом необходимо брать письменное информированное согласие пациентки, поскольку согласно инструкции по применению, прием аспирина противопоказан в первом триместре.
• Беременным с низким потреблением кальция (
Источник