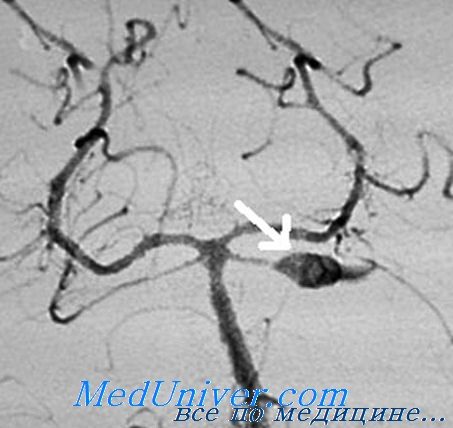
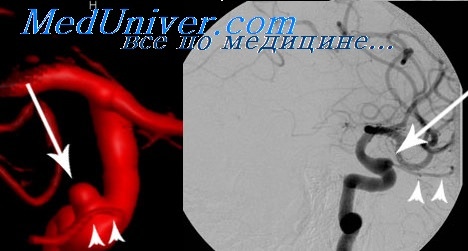
Первая помощь при разрыве аневризмы головного мозга
Повторный разрыв аневризмы. По нашему опыту, достоверных различий в частоте повторных кровоизлияний в различных возрастных группах нет, что согласуется с данными других авторов. Это осложнение мы наблюдали у 15,3% пациентов моложе 60 лет и у 16,2% пожилых больных. На риск возникновения повторного разрыва АА не влияли локализация аневризмы, объем ВМГ, выраженность САК (по Fisher) и ВЖК (по Graeb). У пожилых пациентов повторный разрыв чаще приходился на 10-е сутки, у пациентов молодого и среднего возраста — на 12-е сутки.
Ишемия головного мозга в результате развития ангиоспазма. Вазоспазм после перенесенного субарахноидального кровоизлияния приводит к существенной инвалидизации и смертности пациентов, переживающих первый разрыв аневризмы. У пожилых пациентов компенсаторные возможности мозгового кровотока ограничены вследствие возрастных изменений сосудов и цереброваскулярной болезни, поэтому в этой группе больных можно чаще ожидать возникновение отсроченного неврологического дефицита, обусловленного вазоспазмом.
Например, М. Matsuda и соавт., изучая особенности мозгового кровотока после субарахноидального кровоизлияния в разных возрастных группах, отметили, что у 60-летних пациентов мозговой кровоток остается сниженным от 3 мес до года, в отличие от более молодых больных, у которых мозговой кровоток возвращается к норме в течение нескольких недель.
По данным Т. Inagawa, несмотря на то что у пожилых пациентов выраженность вазоспазма, наблюдаемого при ангиографии, меньше, клинические проявления его встречаются так же часто, как и у молодых. К. Ока и соавт., оценивая проявления вазоспазма, приводят следующие данные: церебральная ишемия после САК наблюдалась у 27,5% пожилых и 24,6% молодых больных. Из этих групп клинически выраженный и подтвержденный при КТ инфаркт мозга был найден у 92,9% пожилых и у 58% молодых больных. Вазоспазм заканчивался распространенной ишемией чаще у больных старше 60 лет, но ишемия не была для них фатальной.
Н. G. Boecher-Schwarz в своих наблюдениях у больных моложе 60 лет, перенесших субарахноидальное кровоизлияние, чаще выявлял увеличение скорости кровотока по мозговым сосудам, чем у пожилых пациентов. В наших наблюдениях при ЦАГ и ТКДГ у пожилых больных в 1,5 раза реже выявляли ангиоспазм, однако проявления ишемии мозга в виде очагов инфаркта мозга при КТ и неблагоприятных типов (III-IV) на ЭЭГ у этой группы больных встречались в 1,25 раза чаще, чем у молодых пациентов. Очаги ишемии в полушариях головного мозга по данным КТ чаще выявляли у пациентов пожилого возраста, чем у больных моложе 60 лет — в 22,6 и 16,7% случаев соответственно.
Линейная скорость кровотока (ЛСК), при которой мы наиболее часто наблюдали клинические проявления ангиоспазма у пожилых, составила 120 см/с, у пациентов моложе 60 лет — 160 см/с.
Вероятно, с возрастом вследствие атеросклероза сосуды головного мозга теряют свою прежнюю эластичность и сократительную способность за счет уменьшения медиального (мышечного) слоя. Поэтому диаметр просвета сосуда изменяется в меньшей степени под воздействием САК и продуктов распада крови, и ЛСК увеличивается незначительно. Однако даже негрубая трансформация просвета сосуда в результате ангиоспазма у пожилых пациентов чаще приводит к появлению клинически значимой ишемии.
Гидроцефалия после разрыва аневризмы сосуда головного мозга. Хроническая дизрезорбтивная гидроцефалия после субарахноидального кровоизлияния развивается у 20-33% больных. У пожилых этот показатель значительно выше и достигает 44%.
Сроки развития синдрома Хакима-Адамса, обусловленного гидроцефалией, варьируют от нескольких дней до месяцев. Установление давности клинических проявлений синдрома очень важно, так как лучшие результаты ликворошунтирующих операций отмечаются при длительности симптомов не более 6 мес.
Расширение желудочков мозга на КТ, по данным К. Ока и соавт., у пожилых пациентов встречалось в 33,3% случаев после перенесенного САК, в сравнении с 24,5% у более молодых. Из них 82,4% пожилых нуждались в шунтировании ликворной системы и были оперированы. Необходимость дренирования ЦСЖ после САК была значительно обусловлена возрастом, наличием ВЖК, ранней гидроцефалией.
По данным Y. Yoshimoto, наружная гидроцефалия после САК встречается также чаще у пожилых больных (38% в сравнении с 14% в конрольной группе). В 81% случаев субдуральное скопление ЦСЖ было связано с одновременным расширением желудочков. Наличие наружной гидроцефалии коррелировало с необходимостью шунтирования желудочковой системы (48% в сравнении с 21% в контрольной группе). Причем после установки вентрикулоперитонеального дренажа значительно регрессировала и наружная гидроцефалия. Патогенетическими факторами в появлении субдурального скопления ЦСЖ являются сниженная абсорбция ее после САК и наличие отверстий в паутинной оболочке после хирургического лечения АА.
Послеоперационная летальность в соответствующих 4 группах пожилых пациентов была следующей: у пациентов 1-й группы — 14,3%, 2-й группы — 16,6%, 3-й группы — 7,7%, 4-й группы — 20,3%. Самая высокая летальность среди пациентов, которым не было выполнено оперативное вмешательство, наблюдалась в наиболее тяжелой группе больных — с осложненным течением аневризматической болезни и декомпенсацией соматической патологии (4-й вариант) — в 100% случаев.
Мы также сравнили функциональные исходы в выделенных группах пожилых больных и проанализировали летальность в зависимости от сроков оперативного лечения.
В этой группе пациентов в 35,2% случаев отмечена умеренная или глубокая инвалидизация в послеоперационном периоде. Ранние сроки оперативного лечения ухудшали прогноз оперативного лечения пациентов 4-й группы и увеличивали летальность до 29,6%.
Подобные исходы оперативного лечения мы наблюдали и во 2-й группе пожилых больных, с осложненным течением основного заболевания, но с компенсированной соматической патологией. В этой группе отмечена высокая инвалидизация оперированных больных — до 50% и значительная послеоперационная летальность в остром периоде кровоизлияния — 40%.
В настоящее время существующие данные о соотношении возраста и исхода субарахноидального кровоизлияния противоречивы. Большинство авторов указывает, что пожилой возраст предполагает неблагоприятный исход САК. Однако существуют работы, которые демонстрируют, что исход лечения зависит, как правило, больше от исходного клинического состояния и тяжести больного, нежели от возраста.
Есть несколько важных моментов, которые следует учитывать при анализе соотношений между возрастом и исходом заболевания:
1. Пациенты старше 60 лет часто исключаются из группы больных, которых готовят для раннего оперативного вмешательства.
2. Пожилые пациенты чаще находятся в более тяжелом состоянии после субарахноидального кровоизлияния, что имеет более определяющее значение для результата лечения, чем сам возраст.
3. Гипертоническая болезнь и атеросклероз чаще наблюдаются у пожилых пациентов. Эти патологические состояния сами по себе могут непосредственно влиять на неблагоприятный исход независимо от возраста.
Результаты консервативного лечения разорвавшейся аневризмы сосуда головного мозга у пожилых являются неудовлетворительными. В 60-х годах прошлого столетия Н. Locksley показал, что ранняя смертность у пожилых, получавших лишь консервативное лечение после разрыва аневризмы, была приблизительно 50%. В. Ellenbogen также сообщил о летальных исходах у больных старше 65 лет более чем в половине случаев. 5-летняя выживаемость после консервативного лечения у пожилых пациентов после САК была менее 20%. Причиной смертельных исходов у них чаще являлся повторный разрыв аневризмы. Раннее применение антифибринолитической терапии для уменьшения объема кровотечения у пожилых оказалось неэффективным и даже увеличивало смертность и ухудшало результаты в сравнении с группой более молодых пациентов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Хирургическое лечение церебральных аневризм в остром периоде кровоизлияния
- Post author:Anton Vorobyev
- Post category:• Статьи
- Post comments:0 комментариев

Фото справа налево: В. Доленс, А. Королев (зав. нхо КОКБ), Ю. Хернисниеми, А. Воробьев
Нетравматические внутричерепные кровоизлияния при разрывах аневризм относятся к одним из наиболее тяжелых форм нарушений мозгового кровообращения.
В России ежегодно регистрируется около 18000 субарахноидальных кровоизлияний (САК), т.е. 13 на 100000 населения в год.
Что такое аневризма и у кого она чаще встречается.
Наиболее часто САК развивается у лиц среднего и пожилого возраста. У больных в возрасте от 40 до 59 лет его частота достигает 50%.
Аневризма представляет собой выпячивание стенки артерии, обычно в области бифуркации сосуда или в месте отхождения от нее крупных ветвей. Характерным для аневризмы является отсутствие трехслойной сосудистой стенки — отсутствие мышечного слоя и эластической мембраны. Стенка аневризмы состоит из соединительной ткани, прорастающей наружную и внутреннюю оболочки. Купол представлен одним тонким внутренним слоем, поэтому кровотечение возникает именно отсюда.
По конфигурации они бывают мешотчатыми, вёретенообразными и фузиформными а также однокамерными и многокамерными. По величине аневризмы делят на милираные (до 3 мм), обычные (от 4 до 15 мм), большие (от 15 до 25 мм), гигантские (более 25 мм). Аневризмы обычно бывают одиночными, но могут быть и множественными (в 15% случаев), располагаясь на различных артериях. В подавляющем числе наблюдений (90-91%) аневризмы располагаются в переднем отделе
артериального круга большого мозга (виллизиева круга) и толь¬ко 9-10% аневризм локализуются в ВББ.
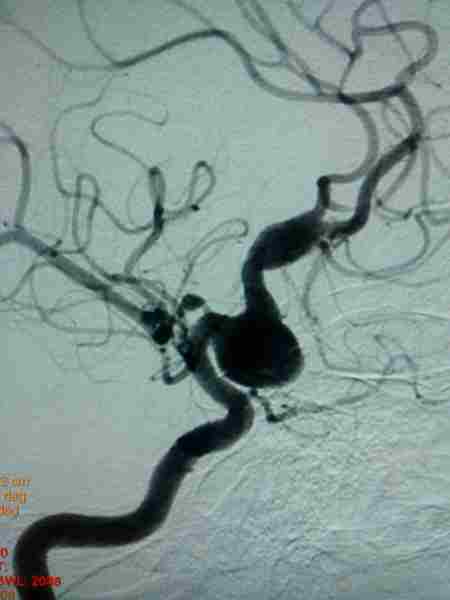
Пример множественных аневризм. Мешотчатая и фузиформная (веретенообразная) аневризмы правой передней мозговой артерии (ПМА).
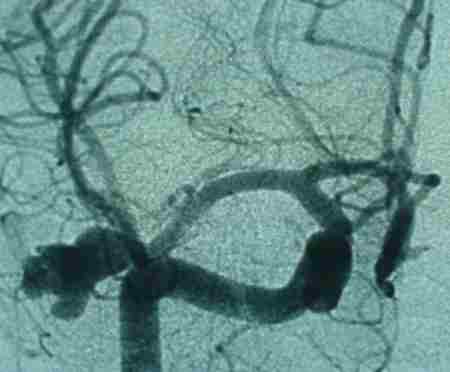
Пример многокамерной аневризмы развилки правой СМА.
При САК кровь поступает под паутинную оболочку и распространяется по базальным цистернам большого мозга. Кровь попадает также в цистерны задней черепной ямки (препонтинную, большую затылочную, мостомозжечкового угла) и далее поступает в позвоночный канал. Источник и интенсивность кровоизлияния определяют характер распространения крови по субарахноидальным пространствам — оно может быть локальным, а может заполнять все субарахноидальные пространства головного мозга с образованием сгустков крови в цистернах. При разрушении мозговой ткани в области кровоизлияния появляются участки паренхиматозного кровоизлияния в виде пропитывания мозгового вещества кровью или формирования гематомы в веществе мозга (субарахноидально-паренхиматозное кровоизлияние).

Разрыв аневризмы ПСА с массивным базальным и паренхиматозным (и немного вентрикулярным) кровоизлиянием.
При значительном поступлении крови в субарахноидальное пространство может возникнуть рефлюкс крови в желудоч¬ковую систему через вывороты IV желудочка (отверстия Мажанди и Люшка) и далее — через водопровод мозга в III и бо¬ковые желудочки. Возможно и прямое проникновение крови в желудочки мозга через поврежденную конечную пластину, что чаще бывает при разрывах аневризмы передней соединительной артерии (субарахноидально-вентрикулярное кровоизлияние). При значительном паренхиматозном кровоизлиянии на фоне САК возможен прорыв гематомы в желудочки мозга (субарахно- идально-паренхиматозно-вентрикулярное кровоизлияние).
Клиника разрыва аневризм мозга.
Клиническая картина САК при разрыве аневризмы развивается остро, иногда на фоне или после физического и эмоционального напряжения. Возникает сильная головная боль. Чаще пациенты описывают ее как головную боль «жгучего», «распирающего» характера, «как будто в голове разлился кипяток». На фоне головной боли развивается кратковременное или длительное угнетение сознания от умеренного оглушения до комы. В остром периоде кровоизлияния нередко возникают психомоторное возбуждение, гипертермия, тахикардия, повышение артериального давления. Неврологическая картина характеризуется развитием менингеального синдрома (ригидность мышц затылка, положительный симптом Кернига, светобоязнь, повышенная чувствительность к шуму и др.). Подобная типичная клиническая картина САК отмечается у 72% пациентов. Однако почти у каждого третьего больного с САК наблюдается иная клиника. Выделяют следующие атипичные варианты САК, для которых характерным является один из ведущих синдромов:
— мигренеподобный;
— ложновоспалительный;
— ложногипертонический;
— ложнорадикулярный;
— ложнопсихотический;
— ложнотоксический.
Неврологическая симптоматика которая развивается при разрывах аневризм той или иной локализации, бывает обусловлена не только эффектом самого САК или паренхиматозного кровоизлияния, но и ишемическими изменениями в мозговой ткани вследствие сосудистого спазма, и тогда клиническая картина заболевания определяется бассейном спазмированных артерий, степенью сужения артерий и особенностями коллатерального кровообращения. Кроме того, при оценке клинических проявлений необходимо учитывать и сроки заболевания, каждый этап которого характеризуется определенной частотой возникновения и формой течения осложнений (повторные кровотечения из аневризмы, внутримозговая гематома, кровоизлияние в желудочки, гидроцефалия, спазм артерий и ишемия мозга, электролитные и эндокринные нарушения, кардиоваскулярные и легочные осложнения и др.).
При всем многробразии клинической картины в практической неврологии и нейрохирургии используют классификации тяжести состояния. К настоящему времени известно более 50 классификаций, которые применяют для оценки тяжести состояния при САК. Наиболее распространенной из них является классификация, предложенная
W. Hunt и R. Hess
I. Бессимптомное течение или слабая головная боль и легкая ригидность мышц затылка.
II. Умеренная или сильная головная боль, ригидность мышц затылка, парез черепно-мозговых нервов.
III. Оглушение, сонливость, спутанность. Умеренный неврологический дефицит.
IV. Сопор, умеренный или выраженный гемипарез, ранняя децеребрационная ригидность.
V. Глубокая кома, децеребрационная ригидность, внешний вид умирающего.
Диагностика субарахноидальных кровоизлияний.
Верификацию кровоизлияния традиционно выполняют путем поясничной пункции.
Компьютерная томография (КТ) головного мозга.
Является ведущим методом в диагностике САК, особенно в первые часы и сутки кровоизлияния. С помощью КТ определяют не только интенсивность базального кровоизлияния и его распространенность по цистернам, но и наличие и объем паренхиматозного и вентрикулярного кровоизлияний, выраженность гидроцефалии, наличие и распространенность очагов ишемии мозга, выраженность и характер дислокационного синдрома.
Кроме того, с помощью КТ иногда удается диагностировать и истинную причину кровоизлияния. Выявляемость САК в первые 12 часов после кровоизлияния достигает 95,2%, в течение 48 часов 80-87%; на 3-и-5-е сутки — 75% и на 6-21-е сутки — всего 29%. Степень выявляемости сгустков крови при САК зависит не только от интенсивности самого кровоизлияния, но и от соотношения сгустков крови и плоскости срезов на КТ. Оптимальным для диагностики САК считается условие, когда плоскость сгустков перпендикулярна плоскости срезов на КТ и толщина сгустков превышает ширину среза КТ. Поэтому САК чаще обнаруживают при сгустках крови толщиной более 1,5 мм.
Наиболее распространенной КТ-классификацией кровоизлияния является классификация, предложенная С.М Fisher et al. в 1980 г.
Данные КТ четко — коррелируют с тяжестью состояния и прогнозом заболевания.
Чем выраженнее кровоизлияние по КТ, тем более вероятно развитие церебрального ангиоспазма и соответственно фатальных ишемических осложнений.
Диагностика источника кровотечения.
Непосредственная визуализация аневризмы возможна тремя методами диагностики: дигитальной субтракционной ангиографией (ДСА), магнитно-резонансной ангиографией (МРА), компьютернотомографической ангиографией (КТА).
Диагностику церебральных аневризм (ЦА) следует начинать с неинвазивных методов.
Компьютерно-томографическая ангиография.
Современная трехмерная КТА с ЗD-реконструкцией (KT-3D-A) обладает чувствительностью в пределах от 87,9 до 97% и специфичностью от 95 до 100%.
При КТА можно получать трехмерное изображение и определять пространственную конфигурацию аневризмы, взаиморасположение с близлежащими структурами.
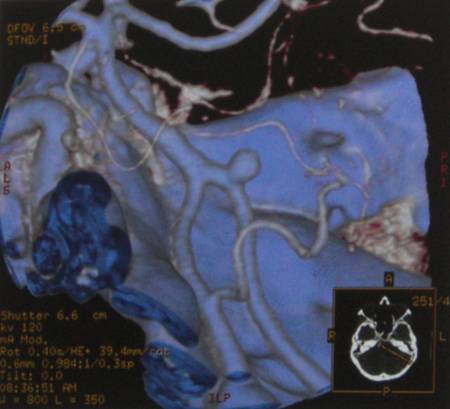
КТА. Аневризма правой позвоночной артерии.
Магнитно-резонансная ангиография.
МРА обеспечивает верификацию внутричерепных аневризм с чувствительностью в пределах от 74 до 100% и специфичностью от 74 до 100%. Чувствительность МРА в обнаружении аневризм диаметром более 3 мм составляет 86%, что сравнимо с результатами ДСА. Отмечено снижение чувствительности МРА при диаметре аневризмы менее 3-5 мм.
Имеется ряд параметров, которые влияют на способность МРА обнаруживать аневризмы: размер ЦА, скорость и направление кровотока в аневризме относительно магнитного поля, тромбоз и кальциноз, — поэтому МРА предпочтительно выполнять в первые 3 суток после кровоизлияния. В сроки от 3 суток до 3 недель после кровоизлияния ее точность снижается из-за биотрансформации молекулы гемоглобина.
Как неинвазивный метод МРА широко применяют в качестве скринингового исследования у пациентов с высоким риском наличия ЦА.
Дигитальпая субтракционная ангиография.
Селективную ДСА необходимо выполнять в следующих случаях: нет возможности проведения КТА или МРА; если эти исследования не выявили источник кровоизлияния или полученные данные недостаточны для проведения хирургического вмешательства. Исследование должно быть выполнено в следующем объеме: оба каротидных бассейна и обе позвоночные артерии. ДСА осуществляют в прямой, боковой, косой, а при необходимости в других атипичных проекциях.
Помимо выявления источника кровоизлияния, необходимо оценить степень выраженности и распространенность сосудистого спазма, особенности кровообращения.
При отсутствии визуализации аневризмы при ДСА у пациентов с типичной клиникой аневризматического САК, при ангиографических признаках сосудистого спазма целесообразно через 3-4 недели после кровоизлияния выполнить повторное ангиографическое исследование, которое позволяет выявить ранее не контрастированные аневризмы приблизительно еще у 3% больных.
Диагностика ангиоспазма.
Сосудистый спазм развивается исключительно при разрывах аневризм и практически не наблюдается при разрывах артериовенозных мальформаций и САК иной этиологии.
Под сосудистым спазмом следует понимать изменения всех слоев артериальной стенки, приводящие к сужению просвета артерии. Они возникают в ответ на кровоизлияние в церебральные цистерны.
Морфологические, изменения в сосудистой стенке следующие: отек и десквамация эндотелия, сокращение гладкомышечных клеток с их последующим некрозом и заместительным склерозом, разрушение эластических волокон наружной и внутренней эластических мембран, коллагеновых волокон адвентиции. Подобные морфологические изменения приводят к сужению просвета артерий, изменению упругоэластических свойств артерии, пристеночному тромбообразованию и иногда полному тромбозу артерий мозга (в 20% случаев). Из вышеописанных морфологических изменений следует, что, во-первых, термин «сосудистый спазм» весьма условен, более уместен термин «констриктивная ангиопатия», во-вторых, более понятным становится, почему терапия артериального спазма спазмолитическими препаратами является неэффективной.
Обычно ангиоспазм при САК развивается с 3-4-х суток от начала заболевания, его пик отмечается на 7-14-е сутки и в последующие дни наблюдается регресс.
Важную роль в оценке выраженности ангиоспазма и характера развивающейся у пациента ишемии мозга играют траскраниальная допплерография — ТКДГ, ЭЭГ и регистрация акустических стволовых вызванных потенциалов. ТКДГ является наиболее чувствительным методом диагностики спазма. При увеличении линейной скорости кровотока до 120 см/с сужение просвета определяется на ангиограммах, а при повышении линейной скорости кровотока более 200 см/с у больных обнаруживаются неврологические расстройства, обусловленные ишемией мозга.
Хирургическое лечение больных с разрывом аневризмы.
Основной целью операции у больных с аневризмами являются выключение аневризмы из кровотока для предотвращения повторных кровотечений и устранение сгустков крови из базальных цистерн для предотвращения сосудистого спазма и ишемии мозга. Учитывая, что и ишемические осложнения, и повторное кровоизлияние возникают через несколько дней после разрыва аневризмы, необходимо стремиться произвести операцию в течение первых 3 суток заболевания. В случаях поздней госпитализации больных с САК и запоздалой диагностики аневризмы, когда развиваются сосудистый спазм и ишемия мозга, операцию приходится откладывать на несколько недель до регресса ишемических осложнений.
В первые 2 недели после разрыва аневризмы повторные кровотечения происходят у 15-20% больных. В первые 6 месяцев после разрыва аневризмы они развиваются у 50% пациентов с летальностью до 60%. В последующем риск повторного кровотечения составляет 3% в год со смертностью 2% в год, что склоняет многих нейрохирургов к тактике ранних оперативных вмешательств.
Показания к проведению открытых хирургических вмешательств.
1) больные с I-II степенью тяжести САК по Hunt-Hess;
2) больные с III степенью тяжести САК по Hunt-Hess при легком или умеренном ангиоспазме (скорость кровотока в сегменте M1 менее 200 см/с);
3) больные с III-IV степенью тяжести САК по Hunt-Hess, ес¬ли тяжесть состояния обусловлена внутримозговой гематомой с развитием дислокационного синдрома.
Показаниями к отсроченному хирургическому лечению являются:
1) III-IV степень тяжести САК по Hunt-Hess при наличии умеренного или выраженного ангиоспазма (скорость кровотока в сегменте M1 менее 200 см/с), III-IV тип изменений ЭЭГ;
2) анатомически сложные аневризмы (гигантские аневриз¬мы, аневризмы базилярной артерии);
3) V степень тяжести САК по Hunt-Hess без внутримозговой гематомы.
Эндоваскулярные методы лечения аневризм.
Абсолютные показания:
1) невозможность клипирования аневризмы в ходе открытой операции.
Приоритетные показания:
1) труднодоступность аневризмы для прямого хирургического вмешательства (аневризмы кавернозного и параклиноидного отделов ВСА, вертебрально-базилярного бассейна);
2) больные старшей возрастной группы (старше 75 лет);
3) тяжелое состояние больных (III-IV степень по Hunt-Hess);
4) фузиформные и расслаивающие аневризмы.
Операции по поводу разрыва аневризм производят под общим обезболиванием, обязательно с использованием операционного микроскопа и микрохирургической техники.
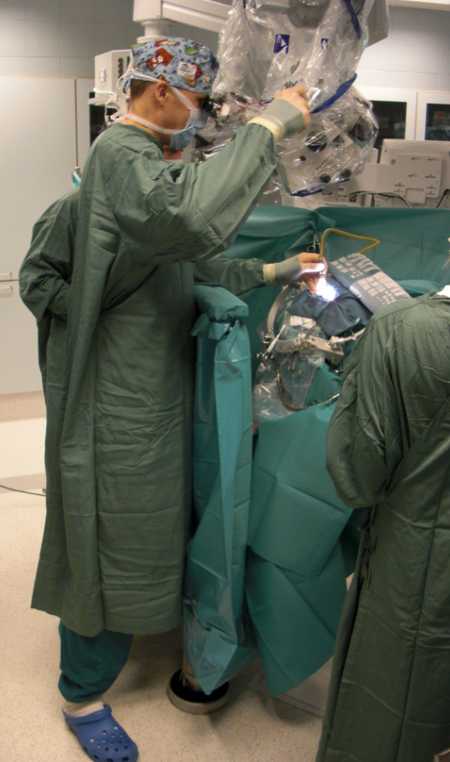
Хирург работает с микроскопом (Хельсинки, Финляндия, проф. Ниемели М.).
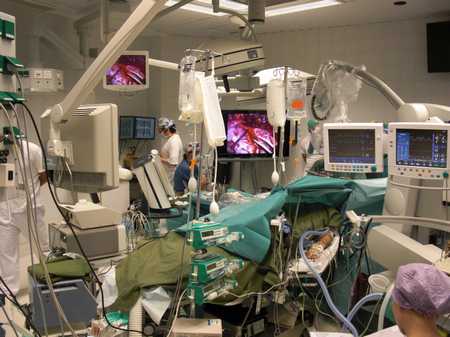
Общий вид нейрохирургической операционной (Хельсинки, Финляндия).
Операция складывается из нескольких этапов: трепанации черепа в лобно- височной области, вскрытия твердой мозговой оболочки, paссeчения арахноидальной оболочки на основании мозга и аспирации СМЖ, выделения магистральных сосудов головного мозга, выделения несущей аневризму артерии, самой аневризмы и выключения ее из кровотока путем клипирования.
Факторами риска в хирургии аневризм в остром периоде кровоизлияния являются:
— тяжелое состояние больного (IV-V степень по Hunt-Hess);
— наличие распространенного спазма и ишемии мозга;
— внутримозговая гематома объемом более 30 мл;
— прорыв крови в желудочки мозга и окклюзионная гидроцефалия;
— смещение срединных структур мозга более 5 мм.
Лечение в послеоперационном периоде.
До настоящего времени каких-либо эффективных методов медикаментозной терапии сосудистого спазма не существует. Поэтому при разрыве аневризмы для профилактики ишемии мозга или ее лечения проводят терапию, направленную на нормализацию перфузии мозга. С этой целью широко используют так называемую ЗН-терапию (hypertensia, hypervolemia, hemodilucia). До настоящего времени не установлено, какой из этих компонентов наиболее важен. Артериальное давление удерживают на уровне 15-20% выше обычного для данного больного давления, используя симпатомиметики. Гиперволемия достигается внутривенным введением альбумина и плазмы, гемодилюция — физиологического раствора. Гематокритное число не должно превышать 38-40. Подобная терапия позволяет значительно снизить риск развития ишемии мозга (до 15%) или уменьшить ее выраженность. Однако подобная терапия не позволяет предотвратить развития повторных кровотечений из аневризмы. Кроме того, при ЗН-терапии увеличивается риск развития сердечно-легочной недостаточности, почечной недостаточности, нарушений водно-электролитного баланса, коагулопатий.
Для профилактики ишемии и в ее лечении необходимо использовать антагонист кальция — нимодипин. Являясь блокатором кальциевых каналов, нимодипин препятствует поступлению ионов кальция через поврежденную мембрану в клетку и предотвращает ее повреждение. Первоначально препарат вводят внутривенно, через инфузомат, доводя скорость инфузии до 5 мл/час, под контролем артериального давления, затем назначают перорально. Иcпoльзовaниe препарата позволяет уменьшить число неврологических расстройств, обусловленных спазмом, на 12%. Необходимо помнить, что при внутривенном введении нимодипина может развиться артериальная гипотония, поэтому параллельно необходимо вводить и симпатомиметики. поддерживая нормальную перфузию мозга.
При написании статьи использованы материалы методических рекомендаций (№ 37) ДЗ Москва 2008.
Учреждение-разработчик: Научно-исследовательский институт скорой помощи им. Н.В. Склифосовского.
Составители: Академик РАМН проф. В.В. Крылов, канд. мед. наук А.Э. Талыпов.
Автор статьи: врач-нейрохирург Воробьев Антон Викторович Рамка вокруг текста
Почему стоит выбрать именно нас:
- мы предложим самый оптимальный способ лечения;
- у нас есть большой опыт лечения основных нейрохирургических заболеваний;
- у нас вежливый и внимательный персонал;
- получите квалифицированную консультацию по вашей проблеме.
Источник