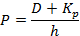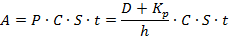Особенность сублингвального пути введения лекарственного средства
Сублингвальное введение препаратов является альтернативным методом системной доставки лекарственных средств, имеющее ряд преимуществ перед пероральным приемом и даже впрыскиванием.
В связи с быстротой действия, достаточной эффективностью, простотой и экономичностью изготовления сублингвальных препаратов, они завоевали особую популярность. В течение последнего десятилетия многие фармацевтические компании пересматривают стратегии производства носителей и средств доставки своих препаратов, чтобы повысить их эффективность, поэтому сублингвальные препараты интенсивно изучаются. Однако, несмотря на огромные усилия, предпринятые в разработке трансмукозальных систем доставки, лишь немногие препараты появились на рынке. Одной из причин этого может быть отсутствие стандартизированной методологии оценки и оптимизации таких систем доставки invitro и invivo до выполнения гораздо более дорогой и трудоемкой клинической оценки.
Таким образом, цель этого обзора – изучить особенности трансмукозальной системы доставки и определить общие закономерности создания сублингвальных препаратов.
Результаты исследования и их обсуждение
Согласно определению Европейской фармакопеи, сублингвальные таблетки и таблетки защечные представляют собой твёрдые дозированные лекарственные препараты, предназначенные для введения под язык или в защечную полость, соответственно, с целью получения системного эффекта [1]. Они изготавливаются путём прессования смеси порошков или гранул в таблетки подходящей для их использования формы.
Преимущества сублингвальных препаратов:
- относительно быстрое начало действия по сравнению с пероральным путем введения;
- вследствие обхода печени, препараты не подвергаются деструкции, а также воздействию пищеварительных ферментов и рН желудочно-кишечного тракта;
- лучшее восприятие пациентами по сравнению с инъекциями из-за отсутствия боли; удобство приема;
- возможность снижения лечебной дозировки из-за высокой биологической доступности таких препаратов и снижения побочных эффектов;
- возможность использования в чрезвычайных ситуациях, например, при болевых, спастических синдромах, приступах стенокардии и астмы;
- отсутствие необходимости в запивании водой или разжевывании.
Недостатки сублингвальных препаратов:
- относительно малая площадь поверхности подъязычной слизистой и, вследствие этого, небольшое количество всосавшегося препарата, чаще для этого подходят препараты с небольшой дозировкой активной субстанции;
- значительные потери препарата из-за неконтролируемого проглатывания слюны;
- сублингвальный прием препаратов препятствует приему пищи, питью, разговору и, как правило, считается не подходящим для длительного применения;
- этот путь приема не подходит для пролонгированных лекарств;
- сублингвальный прием не может быть использован, когда пациент отказывается от сотрудничества или находится в бессознательном состоянии;
- пациент не должен курить во время приема сублингвального лекарства, т.к. курение вызывает сужение кровеносных сосудов, что в свою очередь снижает всасывание.
Детали обобщенной структуры и физиологии слизистой, механизмы проникновения лекарственных средств и пути их переноса, а также системы доставки различных препаратов были обстоятельно рассмотрены в работах авторов [5 — 19].
С точки зрения проницаемости, сублингвальная область полости рта более проницаема, чем щечная, которая в свою очередь превосходит небную область. Различия в проницаемости связаны с относительной толщиной, кровоснабжением и степенью кератинизации этих мембран. Биологическая доступность лекарств при сублингвальном введении зависит также от физико-химических свойств субстанций, поэтому не все лекарства могут быть пригодны для транспорта через слизистую оболочку полости рта из-за особенностей ее строения и физико-химической природы лекарственного средства.
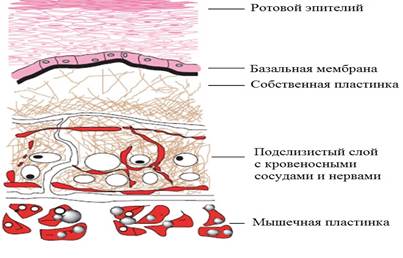
Эффективность сублингвальных препаратов связана со строением сублингвальной зоны, которая высоко васкуляризирована (см. рисунок). Препараты непосредственно попадают в большой круг кровообращения в обход желудочно-кишечного тракта, и минуя метаболизм первого прохода в печени.
Строение слизистой оболочки полости рта
Абсорбция препаратов осуществляется посредством пассивной диффузии через липидные мембраны и в единицу времени превышает пероральный прием в 3–10 раз, уступая только подкожным инъекциям. Динамика подъязычного всасывания подчиняется первому закону Фика. Если для упрощения слизистую оболочку полости рта принять за гидрофобную мембрану, то процесс диффузии лекарственного средства может быть описан следующими уравнениями:
где P – коэффициент проницаемости слизистой оболочки;
A – количество всосавшегося лекарственного средства;
D – коэффициент распространения лекарственного средства в слизистой оболочке полости рта;
Кр– коэффициент распределения лекарственного средства между слюной и слизистой оболочкой полости рта;
h – толщина слизистой оболочки;
C – концентрация лекарственного средства в слюне;
S – площадь поверхности места всасывания на слизистой оболочке полости рта;
t – время контакта со слизистой оболочкой полости рта.
Для большинства составов сублингвальных таблеток малый объем слюны, как правило, достаточен, чтобы привести к их распаду в полости рта. Следовательно, всасывание лекарственного вещества зависит главным образом от его природы, площади контакта таблетки и концентрации вещества в слюне. Эти моменты необходимо учитывать при создании лекарственных средств для сублингвального применения.
Большое значение имеет также коэффициент распределения лекарственного средства между слюной и слизистой оболочкой полости рта. Гидрофобность вещества (его липофильность) оценивается на основании расчета логарифма коэффициента распределения вещества в двухфазной системе н-октанол–вода logP. Отрицательное значение logP означает, что соединение имеет более высокую близость к водной фазе (более гидрофильно); когда logP = 0, то соединение одинаково распределено между липидной и водной фазами; положительное значение logP означает более высокую концентрацию соединения в липидной фазе (более липофильно). Этот параметр характеризует транспорт вещества через мембраны, его взаимодействие с биополимерами.
Гидрофобные препараты с высоким коэффициентом распределения предпочтительно распределяются в гидрофобных местах, например, в билипидном слое клеток, в то время как гидрофильные препараты (низкий коэффициент распределения) предпочтительно могут быть найдены в гидрофильных местах, например, в сыворотке крови [3].
Коэффициент распределения может быть определен экспериментально. Самыми распространенными методами являются метод ShakeFlask и метод ВЭЖХ. Однако использование компьютерных алгоритмов делает результаты исследования более унифицированными, т.к. сравнивать коэффициенты распределения, полученные в различных экспериментальных условиях, на наш взгляд, не вполне корректно [19].
Коэффициент распределения (logP) исследуемых соединений может быть определен с помощью программы ACD/LogP v.12.0 (Advanced Chemistry Development Inc., Toronto, Canada, http://www.acdlabs.com/resources/freeware/), а также с использованием модуля «QSARProperties» академической версии программы HyperChem (http://www.hyper.com/) [16].
Практические исследования систем доставки препаратов позволили установить, что преимуществами всасывания в ротовой полости перед другими обладают препараты, содержащие гидрофильные макромолекулы с многочисленными водородными связями [12]. Адгезии к слизистой способствуют также присутствующие в молекуле препарата гидроксильные, карбоксильные или аминогруппы. Они называются «мокрые» клеи, поскольку способствуют биоадгезии к поверхности слизистых и активируют пассивный транспорт молекул препаратов. Первый шаг трансмукозального транспорта – гидратация молекулы препарата и контакт со слизистой. Шаг второй – этап «консолидация», где происходят различные физико-химические взаимодействия с белками слизистой, способствующими транспорту. Огромная роль здесь принадлежит лектинам. Лектины являются естественными белками, которые играют основополагающую роль в регуляции клеточной адгезии препаратов различной структуры [18].
Наряду с быстротой действия, продолжительность терапевтического эффекта некоторых сублингвальных препаратов относительно невысока. Нитроглицерин, например, является мощным коронарным вазодилататором, используемым более 100 лет для быстрого облегчения симптомов стенокардии. При приеме внутрь он интенсивно метаболизируется (>90 %). При сублингвальном приеме пик его концентрация в плазме крови достигается в течение 1–2 мин, однако из-за его короткого периода полураспада (3–5 мин.), его концентрация в крови становится ниже терапевтической в пределах 10–15 мин [8].
Сублингвальные препараты были разработаны для многочисленных показаний, для которых важно быстрое начало действия, начиная от мигрени, заканчивая психическими заболеваниями, такими как депрессия и шизофрения. Кроме нитроглицерина с большим успехом используются аналгезирующие средства. Примеры этих препаратов включают мощные анальгезирующие средства, такие как сублингвальные формы фентанила цитрата и бупренорфина, ингибиторов AПФ (например, каптоприл, верапамил). Нитроглицерин является одним из наиболее распространенных препаратов, применяющихся путем транспорта через слизистую оболочку полости рта. Исследование других сердечно-сосудистых препаратов, таких как каптоприл, верапамил и пропафенон, также доказало перспективность их использования в сублингвальной форме [14].
Значительный интерес представляет сублингвальное применение анальгезирующих средств. Так, для достижения быстрого анальгезирующего эффекта была разработана оральная форма фентанила, которая удовлетворяет пациентов в первую очередь своей атравматичностью и простотой использования. Нужно отметить, что для анальгезирующих средств, использующихся для симптоматической терапии умеренных болей, быстрое начало действия дает существенное преимущество [18].
Оральные трансмукозальные формы тестостерона и эстрогена также показали свою эффективность. В клинических исследованиях использование подъязычной формы тестостерона приводило к увеличению сухой мышечной массы и мышечной силы, улучшения положительных параметров настроения и увеличения половой реактивности у женщин. Кратковременное назначение эстрогена в период менопаузы женщинам с сердечно-сосудистыми расстройствами улучшало коронарное и периферическое кровообращение [6].
Несмотря на то, что многие препараты были положительно оценены для использования в полости рта, лишь немногие из них коммерчески доступны. Клиническая потребность в оральной доставке лекарственного средства должна быть достаточно высокой, чтобы она могла возместить высокую стоимость процесса разработки лекарственной формы.
Производство и испытания
При производстве таблеток подъязычных и таблеток защечных обеспечивается соответствующая механическая прочность, они не должны крошиться или разламываться при изготовлении и применении. Это может быть подтверждено путем проведения испытаний «Прочность таблеток без оболочки на истирание» и «Прочность таблеток на излом», «Растворение». Если иное обосновано и разрешено уполномоченным компетентным органом, проводят испытание для подтверждения соответствующего высвобождения действующего вещества или веществ [1,2]. Номенклатура сублингвальных таблеток, зарегистрированных в России, представлена следующими торговыми названиями: Апилак, Биотредин®, Валидол, Галавит®, Гипорамин®, Глицин, Исмиген®, Луналдин®, Минирин®, Никоретте®, Нитроглицерин, Оралейр®, Сафрис®, Элтацин® и многие другие [4].
В таблице представлены требования НД к распадаемости и массе некоторых видов сублингвальных таблеток.
Параметры качества для некоторых видов сублингвальных таблеток
Источник
Особенность сублингвального пути введения лекарственного средства
2. Пути введения лекарственных веществ в организм (классификация, сравнительная характеристика). Трансдермальный путь введения. Особенности сублингвального, ректального, интраназального и ингаляционного путей введения лекарственных веществ, их преимущества и недостатки.
Все способы введения лекарств в организм принято разделять на две большие группы — энтеральные, то есть через желудочно-кишечный тракт, и парентеральные, то есть минуя его. Этим самым подчеркивается важнейшая роль ЖКТ как основной системы проникновения лекарств в организм. 1. Выделяют следующие энтеральные способы введения лекарств:
а) пероральное введение — прием лекарства через рот в желудок. Самый удобный и простой, поэтому наиболее часто используемый метод. Эффект препарата, введенного внутрь, развивается через 20-40 минут, в зависимости от содержимого желудка, липофильности лекарства, характера растворителя. Эффект спиртовых растворов препаратов наступает примерно в два раза быстрее, чем водных. Необходимо помнить, что все лекарства, введенные через рот, прежде чем попасть в системный кровоток, проходят через печень, где определенная часть их мегаболизируется и теряет свою активность (пресистемная элиминация). Характеристикой этого процесса является биодоступность — то есть отношение количества лекарства, находящегося в крови, к общему количеству лекарства, введенного в организм.
б) сублингвальное введение — нанесение лекарства под язык. Подъязычная область чрезвычайно интенсивно кровоснабжается, имеет множество поверхностно расположенных капилляров, поэтому обладает высокой всасывательной способностью. Пресистемной элиминации лекарства при этом способе введения не происходит. Этот метод используется при экстренной терапии — например, нитроглицерин, принятый под язык, начинает оказывать свое действие уже через 1-2 минуты.
в) ректальное введение — введение лекарств через прямую кишку в виде лекарственных клизм или свеч. Достоинством этого метода является то, что всасывающиеся лекарства в основном минуют печеночный барьер и сразу поступают в кровоток. То есть биодоступность лекарств при этом пути введения выше, чем при пероральном.
2. Наиболее распространенными парентеральными путями введения лекарственных препаратов являются следующие:
1. Введение под кожу Вводят стерильные, изотонические водные и масляные растворы лекарственных средств в объеме 1 — 2 мл. Растворы имеют физиологические значения рН. Препараты не должны оказывать раздражающего действия (подкожная жировая клетчатка богата болевыми окончаниями) и вызывать спазм сосудов. Фармакологический эффект возникает через 15 — 20 мин после инъекции.
2. Введение в мышцы Вводят стерильные изотонические водные и масляные растворы и взвеси. Максимальный объем внутримышечной инъекции — 10 мл. Эффект большинства лекарственных средств развивается быстрее, чем при инъекции под кожу, — через 10 — 15 мин, так как мышцы имеют обильное кровоснабжение. Медленно всасываются дифенин, бутадион, сибазон, образующие прочную связь с белками мышечной ткани. При введении в мышцы масляных растворов и взвесей получают депо лекарственных средств, обеспечивающее их длительное поступление в кровь и пролонгированное действие (ретаболил, препараты инсулина, бензилпенициллина).
3. Введение в вену Применяют стерильные водные растворы или жировые ультраэмульсии заводского приготовления. Допустимо введение гипертонических растворов и средств со слабыми раздражающими свойствами (во избежание флебита вены промывают физиологическими растворами глюкозы или натрия хлорида). Эффект после вливания в вену в 5 — 10 раз сильнее по сравнению с активностью при приеме препаратов внутрь, наступает быстро. Внутривенные инъекции проводят медленно, чтобы в органах с богатым кровоснабжением (головной мозг, сердце, легкие, почки, печень) не создавались токсические концентрации.
Только 60% детей в возрасте 3 — 12 лет имеют удовлетворительные для инъекций вены (лекарственные средства приходится вводить в вену пальмарного сплетения руки, что увеличивает болевую реакцию).
4. Введение в артерии Для введения в артерии, а также внутрисердечно, в губчатое вещество костей, субарахноидальное и эпидуральное пространства, используют только стерильные изотонические водные растворы лекарственных средств.
В артерии пораженных органов вводят антибиотики и противоопухолевые средства в высоких концентрациях. При эндартериите и отморожении в артерии конечностей вливают сосудорасширяющее средство ацетилхолин. Доступ к артериям хирургический, создают артериовенозный шунт, чтобы исключить попадание токсических лекарственных средств в системный кровоток.
1. Внутрисердечный путь Единственным показанием для этого пути служит остановка здорового сердца при травмах. В полость левого желудочка вводят адреналин.
2. Внутрикостный путь Этот путь введения лекарственных средств обеспечивает такую же скорость наступления эффекта, как и внутривенные инъекции. В губчатое вещество пяточной кости вливают местные анестетики (лидокаин) при операциях на конечностях.
3. Субарахноидальный и эпидуральный пути В субарахноидальное или эпидуральное пространства спинного мозга вводят местные анестетики для спинномозговой анестезии, наркотические анальгетики с целью лечебной анальгезии, антибиотики при менингите. Инъекцию проводят на уровне нижних грудных — верхних поясничных позвонков атравматической иглой диаметром менее 0,4 мм с конусовидным концом. Это необходимо потому, что отверстие в твердой мозговой оболочке плохо затягивается. Через него сочится ликвор, вызывая перепады внутричерепного давления и тяжелую головную боль. При объеме инъекции более 1 мл удаляют соответствующее количество ликвора.
Трансдермальный путь Применяют лекарственные средства в форме мазей, паст, растворов, эмульсий, суспензий, лосьонов для местного воздействия при заболеваниях кожи, ранах, ожогах или с целью получения рефлекторных ответов со стороны внутренних органов. Следует учитывать возможность всасывания липидорастворимых лекарственных средств в кровь, особенно при повреждении кожи, воспалении и у детей. У детей тонкий роговой слой кожи, повышено содержание воды в подкожно-жировой клетчатке, увеличено по сравнению с показателем взрослых отношение площади поверхности к массе тела. У недоношенных детей, кроме того, отсутствуют врожденные барьерные свойства кожи. Пожилой возраст также вносит коррективы в биодоступность лекарственных средств при накожном применении. Старение кожи начинается с 40 лет. К 60 годам все слои кожи истончаются, в ней уменьшается количество капилляров, возникают нарушения микроциркуляции в виде стаза и микротромбозов. В последнее время стали использовать трансдермальные терапевтические системы (ТТ S ) . Они представляют собой форму введения липофильных лекарственных средств в большой круг кровообращения через неповрежденный кожный покров по заданной программе. Лекарственное средство находится в резервуаре в форме суспензии или геля, скорость всасывания регулируется проницаемостью мембраны из микропористого полимера или диффузией из полимерной матрицы. Количество поступающего в организм активного вещества можно регулировать площадью и конструкцией наклеиваемой системы, эффективность действия повышается за счет равномерного поступления дозы в кровоток, побочные эффекты снижаются. После удаления TTS всасывание лекарственного средства прекращается через 20 — 30 с.
В состав TTS вводят препараты для профилактики или длительного лечения хронических заболеваний, средства заместительной терапии. Все лекарственные средства в TTS должны оказывать действие в малых дозах, не вызывать раздражения и воспаления кожи. В настоящее время в медицинской практике применяют TTS, содержащие скополамин (профилактика укачивания), нитроглицерин (курсовое лечение стенокардии), клофелин (при артериальной гипертензии), теофиллин (курсовая терапия бронхиальной астмы), 17-β-эстрадиол (в период менопаузы у женщин
Сублингвальный (рассасывание под языком) и трансбуккальный (рассасывание за щекой) пути
Рассасывание в полости рта обеспечивает быстрое поступление лекарственных средств в систему верхней полой вены, при этом отсутствует действие пищеварительных соков и ферментов печени. Сублингвально принимают только лекарственные средства с высокой растворимостью в липидах — нитроглицерин для купирования приступа стенокардии, антигипертензивные препараты при гипертоническом кризе, стероидные гормоны.
Ректальный путь Ректальный путь используют при невозможности приема лекарственных средств внутрь (рвота, бессознательное состояние). Из прямой кишки 50 % дозы всасывается в систему нижней полой вены, минуя печень, 50 % — поступает в воротную вену и частично инактивируется в печени.
Ограничения ректального введения — высокая чувствительность слизистой оболочки прямой кишки к раздражающим воздействиям (опасность проктита), малая всасывающая поверхность, короткий контакт лекарственных средств со слизистой оболочкой, небольшой объем растворов для лечебных клизм (50 — 100 мл), неудобство проведения процедур на работе, в путешествии.
Ингаляционный путь Ингаляции позволяют получить быстрый резорбтивный эффект лекарственных средств в связи с большой площадью контакта альвеол и капилляров (150 — 200 м 2 ). Ингаляционно вводят наркозные средства — летучие жидкости и газы, а также с целью местного действия применяют аэрозоли бронхолитических средств, глюкокортикоидов, местных анестетиков, антибиотиков, порошок противогистаминного препарата кромолина-натрия (интал). Глубина проникновения аэрозолей в дыхательные пути зависит от размеров частиц. Частицы величиной 60 мкм оседают в глотке и попадают в желудок, частицы величиной 20мкм проникают в терминальные бронхиолы, размером 2мкм — в предальвеолярный жом, 1 мкм — в альвеолы.
Следует учитывать сложность дозирования лекарственных средств для ингаляционного применения, их раздражающее влияние на легкие, опасность воздействия пропеллентов на медицинский персонал, возможность поступления аллергенов. При правильном применении ингалятора в легкие поступает только 10 — 20 % дозы. Аэрозоли с особо мелкодисперсными частицами распыляют с помощью ингалятора-небулайзера (лат. nebula — туман). Он позволяет быстро доставлять терапевтическую дозу препарата в аэрозольной форме, пригоден для применения с первых месяцев жизни ребенка.
Интраназальный путь введения целесообразен в ситуациях, когда желательно совместить экстренность введения препарата с одновременным воздействием его на эпителий верхних дыхательных путей. Доза препарата — не более 1 мл в форме для интраназального введения.
Источник