- Сертификат GMP: подтверждение качества лекарственных средств
- К каким производствам применима эта процедура?
- Нормативная база
- Преимущества обладания сертификатом
- Стандарт GMP в международной практике
- Правила GMP в России
- Процедура получения сертификата в России
- Документы для сертификации
- Сроки сертификации
- Стоимость получения сертификата
- Сертификат соответствия на лекарственный препарат
- Обязательная сертификация лекарственных препаратов в России
- Что потребуется для подтверждения качества и безопасности препаратов
- Процедура оформления документов
- Преимущества работы с нами
Сертификат GMP: подтверждение качества лекарственных средств
Сертификат GMP — это соблюдение изготовителем лекарственных препаратов требований надлежащей производственной практики. В России они сформулированы в национальном стандарте ГОСТ Р 52249-2009, который идентичен правилам, действующим в Европейском Союзе.
К каким производствам применима эта процедура?
В настоящее время в странах, которые контролируют соответствие стандарту GMP на своих территориях, его правила применяются для проверки качества следующих категорий продукции:
- лекарственные препараты;
- медицинские изделия различного назначения, включая те из них, которые применяются в диагностических целях;
- продукты питания и ингредиенты для их производства;
- биологически активные добавки.
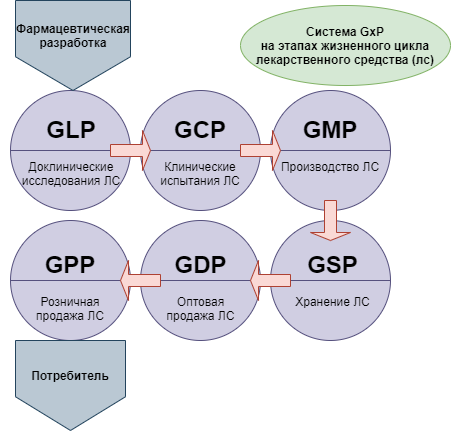
При этом для понимания ситуации следует принимать во внимание, что новая версия сертификации GMP — это не единственная система требований, которые в международной практике применяются в целях стандартизации медицинского обслуживания населения. Кроме них, производителям, работающим в такой сфере как фармация, необходимо соответствовать требованиям комплекса правил, объединенных под общим наименованием GxP:
- GLP — Good Laboratory Practice (надлежащая лабораторная практика);
- GCP — Good Clinical Practice (надлежащая клиническая практика);
- GDP — Good Distributon Practice (надлежащая дистрибьюторская практика);
- GACP — Good Agricultural and Collection Practice (надлежащая практика культивирования и сбора лекарственных растений).
Нормативная база
В Российской Федерации получение сертификата GMP осуществляется на основании действующей нормативной базы, включающей следующие основные правовые акты:
- национальный стандарт РФ ГОСТ Р 52249-2009, устанавливающий правила изготовления и контроля качества лекарственных препаратов;
- постановление Правительства от 5 июня 2008 года N 438 с рядом изменений, внесенных за последние годы, которое утверждает полномочия Министерства промышленности и торговли в этой области;
- постановление Правительства от 3 декабря 2015 года N 1314, устанавливающее порядок оценки соответствия производителей требованиям стандарта надлежащей практики;
- приказ Минпромторга от 14 июня 2013 года N 916, утверждающий правила применения надлежащей производственной практики в соответствии с актуальным стандартом;
- приказ Минпромторга от 26 мая 2016 года N 1714, определяющий административный регламент предоставления государственной услуги по выдаче документации, подтверждающей соответствие изготовителя установленным нормам надлежащей производственной практики;
- приказ Минпромторга России от 17.12.2015 N 4119, утверждающий правила ведения реестра сведений о том, какие лекарства имеют сертификат качества GMP в России.
При этом необходимо принимать во внимание, что в настоящий момент наша страна вместе с другими государствами, входящими в состав Евразийского экономического союза, находится на этапе становления общего рынка, объединяющего фармацевтическое и косметическое производство в границах Союза. Это предполагает в том числе введение в действие единых требований к качеству и безопасности таких продуктов. В соответствии с принятым в мире порядком они реализуются в форме внедрения стандартов надлежащей производственной практики. Применение таких стандартов регулируется следующими нормативными документами:
- Решение Совета ЕЭК от 3 ноября 2016 года N 77, утверждающее правила надлежащей производственной практики в границах ЕАЭС;
- Приказ Минпромторга от 4 сентября 2020 года N 2945, которым введен административный регламент предоставления госуслуги по выдаче документации, подтверждающей соответствие производств установленным правилам.
Обратите внимание!
Для полноценного применения разработанного административного регламента необходимо решение Правительства о порядке реализации некоторых процедур, связанных с проведением фармацевтических инспекций. Приказ № 2945 вступит в силу только после принятия соответствующего постановления: пока этого не произошло.
Преимущества обладания сертификатом
Несмотря на необходимость проведения достаточно сложной и дорогостоящей процедуры, производители знают, что сертификация по стандартам GMP является весьма важной для представителей фармацевтической отрасли. В частности, оно обеспечивает продукции и производству следующие серьезные преимущества:
- стабильное качество продукции, не зависящее от внешних факторов;
- повышение доверия потребителей, включая крупных оптовых покупателей, которые всегда отслеживают, какие производители имеют сертификат соответствия GMP на их продукцию;
- возможность вывода продукции на международные рынки, где ее может купить гораздо больше потребителей;
- возможность привлечения инвесторов для реализации проектов по расширению производства;
- получение преимуществ при участии в конкурсном отборе поставщиков, в том числе для государственных закупок.
КОММЕНТАРИЙ ЭКСПЕРТА АТТЭК
Каков срок действия сертификата?
Срок действия российских сертификатов составляет 3 года. При этом срок действия иностранного сертификата GMP составляет от 1 до 3 лет. По истечении этого периода сертификацию потребуется проходить заново. Кроме того, это означает, что на протяжении всего этого срока компании необходимо обеспечить соответствие своего производства и продукции требованиям комплекса правил GMP.
Кто в России занимается сертификацией по стандартам GMP?
Сейчас сертификация контролируется департаментом развития медицинской и фармацевтической промышленности Министерства промышленности и торговли РФ. Он является организацией, ответственной за обеспечение надлежащего контроля за качеством, безопасностью и эффективностью лекарственных средств. Осуществлением требуемых сертификационных процедур занимается Государственный институт лекарственных средств и надлежащих практик (ФГБУ «ГИЛС и НП»).
Стандарт GMP в международной практике
Процесс сертификации на соответствие лекарственного препарата стандартам GMP в международной практике имеет комплексный характер, а ее основной целью является подтверждение безопасности и действенности продукции. В этой связи для достижения поставленной цели специалисты аккредитованных сертификационных организаций не ограничиваются оценкой ряда выборочных образцов лекарственных препаратов, как это часто предусматривается другими стандартами. В процедуру установления требуемого уровня качества лекарств любой международный центр сертификации лекарственных средств включает оценку предприятия, занимающегося его выпуском. В результате эксперты, занимающиеся проведением сертификации, анализируют конкретный препарат и процесс его выпуска в следующих областях:
- оценка производства на соответствие критериям безопасности, включая проведение его проверки в отношении вероятности попадания в продукт посторонних примесей и веществ;
- оценка производства на соблюдение технических требований к выпуску продукции, включая выполнение условий относительно влажности, температуры и других параметров в производственных помещениях;
- оценка качества, безопасности и действенности лекарственных средств, производимых на конкретном предприятии;
- оценка соответствия параметров производства и характеристик лекарственного средства нормативной документации, принятой в рамках процедуры GMP.
Правила GMP в России
Порядок и сроки проведения всех операций в рамках этой процедуры, список лиц и организаций, ответственных за их осуществление, размер платы за проведение экспертной оценки и другие аспекты выполнения сертификации определены постановлением Правительства № 1314.
Процедура получения сертификата в России
Первым шагом для производителя, который желает пройти сертификацию, является подача соответствующего заявления в Минпромторг. В течение 10 рабочих дней специалисты ведомства проводят проверку корректности представленных в заявлении сведений и определяют возможность проведения сертификации.
В случае необходимости они вправе запросить у заявителя дополнительные документы, которые он обязан предоставить в течение 20 рабочих дней. В случае, если в отношении данного препарата принято положительное решение о проведении процедуры сертификации, необходимые данные направляются в ФГБУ «ГИЛС и НП», который в течение 20 рабочих дней с момента их получения обязан определить дату проведения сертификационных мероприятий и внести ее в график. Такая дата должна наступить не позднее 160 рабочих дней со дня, когда специалисты Минпромторга приняли положительное решение о сертификации, а сама экспертиза и расшифровка ее результатов должны занимать не более 10 рабочих дней.
На подготовку итогового отчета по результатам ее проведения исполнителю отводится 30 рабочих дней, а на его направление заявителю — 3 рабочих дня. Копия такого отчета также направляется в Минпромторг. На основании отчета формируется окончательное заключение, которое в случае положительного характера сопровождается выдачей сертификата производителю лекарственного препарата.
Документы для сертификации
Чтобы получить сертификат GMP в России, производитель обращается в уполномоченный орган с заявлением, к которому прилагает пакет документов, включающий:
- копию документа, подтверждающего наличие у заявителя полномочий по взаимодействию с контролирующей организацией;
- копия основного досье используемого производственного объекта;
- информация о фактах несоответствия препарата действующим требованиям к качеству и безопасности и о фактах отзыва медикамента из оборота за период не менее 2 лет;
- полный список лекарств, который изготавливаются на данном производственном объекте;
- копия лицензии на производство лекарств;
- письмо о согласии на проведение инспекции производства.
Важнейшие документы предоставляются заявителем в копиях, поскольку при утере их восстановить невозможно или очень сложно. Правила регламентируют, что если заявление подает иностранный производитель, и некоторые документы в составе пакета представлены на другом языке, они должны быть переведены на русский язык и заверены в установленном порядке.
Сроки сертификации
Общая продолжительность процедуры сертификации складывается из следующих сроков.
Этап сертификационной процедуры
Максимальная допустимая продолжительность
Проверка полноты пакета документации, представленной с заявлением о сертификации, и правильности ее оформления, назначение инспекции
10 рабочих дней
Направление информации о назначении инспектирования в уполномоченное учреждение, которое проводит проверку
Инспектирование и анализ лекарственного средства
160 рабочих дней
Принятие решения о выдаче заключения по результатам инспекционного отчета
10 рабочих дней
160-дневный период инспектирования включает внесение производителя в график инспекций, ожидание процедуры и проведение самой инспекции. Она должна занимать не более 10 рабочих дней.
Такой порядок действует, если в документации, поданной производителем, не обнаружат ошибок и недочетов, из-за которых ее могут направить на доработку. В этом случае вся процедура займет немногим более 180 рабочих дней, то есть свыше 8 месяцев.
Стоимость получения сертификата
Обязательной для всех производителей лекарственных средств, претендующих на получение сертификата, подтверждающего соответствие их продукции стандартам GMP, является оплата государственной пошлины за рассмотрение соответствующего заявления в Министерстве промышленности и торговли. Ее размер составляет 7500 рублей. Оплатить данную сумму необходимо еще до подачи заявления в ведомство, а ее размер никак не зависит от результатов рассмотрения документа.
Однако данная пошлина — это далеко не единственный и не самый крупный платеж, который потребуется осуществить производителю лекарств. Другой значительной статьей расходов станет плата за проведение экспертной оценки производства и продукции заявителя. Такая процедура выполняется специалистами ФГБУ «ГИЛС и НП»: для каждого из них предварительно проводится аттестация эксперта по GMP в России.
При этом размер платы за проведение оценки не является строго установленным, а определяется в зависимости от объема, характера и сложности необходимых процедур в соответствии с положениями приказа Министерства промышленности и торговли Российской Федерации от 11.01.2016 № 9 «Об утверждении методики определения размера платы за оказание услуги по инспектированию GMP». В случае, если проверка потребует проведения значительного объема работы и привлечения большого количества высококвалифицированных экспертов, размер платы за ее проведение может превышать 2,5 миллиона рублей.
Источник
Сертификат соответствия на лекарственный препарат
Одной из ключевых функций государства является охрана здоровья граждан, которая заключается в обеспечении доступности приобретения лекарственных средств, их качества и безопасности для использования по непосредственному назначению. Благодаря предоставлению сертификата качества на лекарственные препараты производитель или импортер имеют возможность подтвердить полное соответствие требованиям стандартов, действующих на территории РФ или всех стран, входящих в состав Евразийского экономического союза.
Процедура подтверждения качества медицинских изделий и лекарственных средств осуществляется гораздо сложнее, чем в отношении остальных видов продукции, которые могут реализовываться на территории ЕАЭС. Связано это с необходимостью обеспечения должного эффекта от приема лекарственного средства, учета возможных побочных эффектов, негативного влияния на организм человека, совместимости с другими средствами и полного соответствия всем нормативным показателям, которые имеют отношение к нему. Обратившись к нам, вы сможете получить подробную информацию относительно процедуры сертификации медицинских препаратов и делегировать выполнение всех необходимых действий нашим специалистам.
Обязательная сертификация лекарственных препаратов в России
Под товарами, используемыми в медицине понимают:
- все материалы и продукцию, применяемые для медицинских целей – профилактики и лечения различного рода заболеваний и отклонений, диагностики проведения исследований, мониторинга состояния человека, восстановления утраченных функций;
- лекарственные средства и различные фармакологические препараты, спектр применения которых достаточно широк.
В отношении лекарственных препаратов возникает необходимость оформления следующих типов документов:
- регистрационного свидетельства Росздравнадзора. Необходимость прохождения такой процедуры существует в отношении всех медицинских препаратов. Она может длиться достаточно долго – от 8 до 18 месяцев в зависимости от перечня необходимых испытаний, которые нужно провести и времени ожидания результата рассмотрения поданного заявления сотрудникам государственной организации. Только после того, как документ будет получен, допускается направлять заявление на обязательное и добровольное подтверждение качества продукции;
- декларации соответствия нормам национальных стандартов на основании положений Постановления Правительства РФ №982. Точный список тех препаратов, которые должны пройти такую процедуру, вы можете узнать в нашем центре сертификации;
- лицензия на осуществление фармацевтической деятельности;
- сертификация производственного процесса выпуска медицинских препаратов.
Получение полного перечня разрешительной документации, которая необходима для определенного типа продукции даст возможность осуществлять следующие виды деятельности:
- налаживание производственного процесса выпуска лекарственного средства;
- организация сбыта продукции;
- налаживание импорта и экспорта товара.
При намерении реализации на территории других государств в обязательном порядке стоит учитывать те законодательные нормы, которые действуют в определенной стране. Мы можем проконсультировать вас по этому поводу и обозначить перечень необходимых документов, которые можно оформить на территории РФ или обратившись в сертификационные центры других государств ЕАЭС.
В дополнение к перечню обязательных документов мы можем предложить вам оформление и добровольного сертификата соответствия на лекарственный препарат. За счет его предоставления производитель или импортер имеют возможность повысить интерес к своему товару, значительно расширить предполагаемый рынок сбыта, принять участие в тендерах или государственных закупках. Сертификация лекарственных препаратов предполагает проведение необходимых испытаний с последующим оформлением документа, подтверждающего соответствие определенным параметрам ГОСТов.
При возникновении вопросов, обязательно свяжитесь с нашими экспертами – все консультации бесплатны!
Что потребуется для подтверждения качества и безопасности препаратов
При возникновении необходимости оформить сертификаты на лекарственные препараты, свидетельства о регистрации, подтвердить их соответствие требованиям качества и безопасности, необходимо будет предоставить следующий пакет документов:
- свидетельство о регистрации предпринимателя;
- уставная документация;
- банковские реквизиты организации;
- наименование лекарственного средства, его характеристика, инструкция по применению с подробным описанием фармакологических свойств, побочных эффектов, противопоказаний и т.д.;
- данные о производственном процессе;
- сведения о производителе и заключенном с ним контракте при условии, что сертификат соответствия препарата будет оформляться в отношении импортированной продукции;
- другие документы, необходимость в которых может возникнуть.
При условии, что клиент испытывает трудности в предоставлении определенных документов из указанного списка, наши эксперты оказывают помощь на данном этапе, чтобы вся процедура оформления прошла максимально быстро.
Процедура оформления документов
При получении разрешительной документации потребуется пройти следующие этапы:
- Направление обращения в наш Центр и подача необходимой документации.
- Идентификация продукта, определение точного перечня тех документов, которые могут быть оформлены для клиента.
- Организация проведения независимой лабораторной экспертизы, в результате которой проходит оценка соответствия требованиям качества и безопасности.
- Получение результатов исследований, оформление разрешительной документации, проведение регистрации.
- Направление клиенту необходимого пакета документов (при желании мы организуем бесплатную доставку курьером).
Важным моментом сотрудничества с нами является то, что мы стараемся максимально выполнить все процедуры самостоятельно. Фактически заявитель необходим только в процессе предоставления документов, который можно провести в удаленном режиме.
Преимущества работы с нами
Процедура оформления документации у нас выгодна следующим:
- большой перечень сертификатов, деклараций и других документов, которые может с нашей помощью оформить представитель любой сферы бизнеса;
- проведение бесплатных консультаций для всех обратившихся;
- приемлемые цены, установленные на весь перечень оказываемых услуг;
- гарантия полной конфиденциальности для каждого заявителя;
- индивидуальный подход к каждому заказчику и максимальный учет пожеланий клиента.
Поможем быстро оформить необходимую разрешительную документацию для вашего бизнеса!
Свяжитесь с нами – мы следим за изменениями в законодательстве и всегда готовы предложить наиболее оптимальную схему оформления документов!
Узнать условия оформления и стоимость сертификации
Источник