- Орфанные препараты
- Правовое регулирование орфанных заболеваний и орфанных препаратов в РФ
- Преференции для орфанных лекарственных препаратов
- Обеспечение орфанными лекарственными препаратами
- Орфанные препараты — новая категория на фармрынке
- Нередкие редкие (орфанные) заболевания
- Редкие болезни известных людей
- Примеры списка орфанных заболеваний
- Что такое “болезни-сироты” и почему их лечение проблематично
- «Болезни-сироты»
- Орфанные лекарства
- Проблемы орфанных препаратов
- Перспективы орфанных препаратов
- Ситуация с редкими болезнями в Украине
Орфанные препараты
Статья подготовлена 15.11.2016
Младший юрист Юридической фирмы « BRACE »
Впервые термин «орфанные болезни» (редкие заболевания, «болезни-сироты») появился в 1983 г. в США при принятии закона об орфанных болезнях (Orphan Drug Act). Это такие болезни, как: фенилкетонурия, муковисцидоз, множественная миелома, хронический миелолейкоз, болезнь Гоше, глиома и другие. Сегодня понятие орфанных заболеваний закреплено в законодательствах многих стран, к примеру, в Австралии, Японии, Сингапуре. В 1999 г. аналогичный американскому закон был принят Европейским парламентом.
Правовое регулирование орфанных заболеваний и орфанных препаратов в РФ
В России, где орфанными заболеваниями страдают по разным подсчетам от 1,5 до 5 миллионов жителей, нет отдельного федерального закона, регулирующего орфанные заболевания и препараты. Впервые в российском законодательстве определение понятия орфанных заболеваний было дано в 2011 году в Федеральном законеот 21.10.2011 № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» (далее ФЗ — №323) в ст. 44. Согласно указанному закону орфанными заболеваниями признаются заболевания, которые имеют распространенность не более 10 случаев заболевания на 100 тысяч населения. В 2014 г. понятие орфанных лекарственных препаратов было введено в ФЗ от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств».
Для того, чтобы получить статус орфанного препарата, необходимо наличие определенных критериев. Препарат должен быть предназначен для лечения заболеваний, не превышающих 10 случаев такого заболевания на 100 тысяч населения. В ЕС, например, помимо вышеуказанных факторов, также важно, чтобы орфанный препарат предназначался для пациентов с заболеванием, для которого не существует официально признанных удовлетворительных методов диагностики, профилактики и лечения. Если препарат для лечения заболевания существует, то необходимо доказать, что новый продукт имеет преимущества по сравнению с лекарством, которое уже имеет статус орфанного. Более того, в ряде зарубежных стран орфанным лекарственным препаратом может быть признан препарат, расходы на разработку которого превышают потенциальные доходы от выхода на рынок.
Стоит отметить, что российское законодательство рассматривает понятие орфанного препарата гораздо уже, чем зарубежные правопорядки, ограничиваясь лекарственными препаратами для лечения и диагностики редких заболеваний (диагностика, лечение и предотвращение заболевания – например, ЕС). При этом лечение должно быть связано с механизмом развития заболевания, что, по мнению многих врачей, является необоснованным ограничением.
Преференции для орфанных лекарственных препаратов
Российское законодательство содержит ряд льгот для орфанных лекарственных средств. ФЗ № 61 предполагает возможность ускоренной процедуры экспертизы орфанных препаратов в целях последующей государственной регистрации (80 рабочих дней). Сначала происходит экспертиза всех документов, предоставляемых для определения возможности рассматривать препарат в качестве орфанного, на основании копий документов, заверенных в установленном порядке, о регистрации препарата на территории других государств в качестве орфанного лекарственного препарата. Затем, если решение будет положительным, проводятся следующие виды экспертизы, предусмотренные законодательством, — (1) качества и (2) соотношения ожидаемой пользы к риску. Для орфанных препаратов признаются результаты доклинических и клинических исследований, которые были выполнены за пределами РФ в соответствии с правилами надлежащей лабораторной практики и правилами надлежащей клинической практики, что, например, в ЕС является общим правилом, а в России считается исключением.
Одним из главных недостатков существующей системы создания и регистрации орфанных препаратов в РФ является отсутствие налоговых стимулов и льгот, увеличенных сроков эксклюзивности на рынке в отличие от других стран. К примеру, срок эксклюзивности товара в ЕС – 10 лет; в США – 7 лет; в Японии — 5 лет, т.е., после вывода препарата на рынок по этому показанию в течение определенного срока больше не будет зарегистрировано ни одного препарата. Утверждение статуса орфанного для препарата в Японии дает право производителю на возмещение 50% затрат на разработку препарата, снижение налогов на 6% и другие финансовые льготы. Если производитель орфанного препарата в Японии получил прибыль от его реализации, он обязан вернуть часть этих денег в фонды, из которых были выделены деньги на производство препарата и его разработку.
Однако у таких преференций есть и обратный эффект. Так, власти США, стараясь сделать терапию доступнее, в 2013 году снизили цены на определенные препараты, применяемые для борьбы с орфанными заболеваниями. В результате получилось, что эта мера пациентов с редкими заболеваниями так и не коснулась: существует ряд орфанных лекарственных средств, предназначенных для лечения более распространенных заболеваний, и снижение цен затронуло именно этих пациентов. Также одной из проблем в США является то, что фармацевтические компании, используя все преференции для выпуска орфанных лекарственных средств, в дальнейшем продают их как препараты для широкого пользования .
Обеспечение орфанными лекарственными препаратами
В Российской Федерации существует Федеральный регистр граждан, страдающих орфанными заболеваниями.Согласно ч. 9 ст. 83 ФЗ № 323, обеспечение граждан зарегистрированными в установленном порядке на территории России лекарственными препаратами для лечения заболеваний, включенных в перечень жизнеугрожающих и хронических прогрессирующих редких (орфанных) заболеваний, приводящих к сокращению продолжительности жизни гражданина или его инвалидности, осуществляется за счет средств бюджетов субъектов РФ. Такое распределение полномочий с учетом цен на орфанные лекарственные препараты приводит к тому, что зачастую потребность пациентов в лечении не удовлетворяется, как результат, многочисленные судебные споры об обязании обеспечить пациента лекарственными средствами в рамках реализации конституционного права гражданина на охрану здоровья.
В нашей стране нет четких технологий фармакотерапии орфанных больных, а стоимость лечения больного не сопоставима с бюджетом субъектов РФ, на которых и отпущено лекарственное обеспечение таких больных. В 2013 г. была сделана попытка передачи финансирования на уровень федерального бюджета в виде внесения законопроекта о таком изменении в Государственную Думу, однако законопроект так и не был принят.
Таким образом, на сегодняшний день российское законодательство не содержит достаточных гарантий как для разработчиков орфанных лекарственных препаратов, так и для пациентов, страдающих редкими заболеваниями.
Источник
Орфанные препараты — новая категория на фармрынке
Роза Ягудина о росте количества орфанных препаратов и их роли в лечении пациентов
Нередкие редкие (орфанные) заболевания
Редкие болезни известных людей
Примеры списка орфанных заболеваний
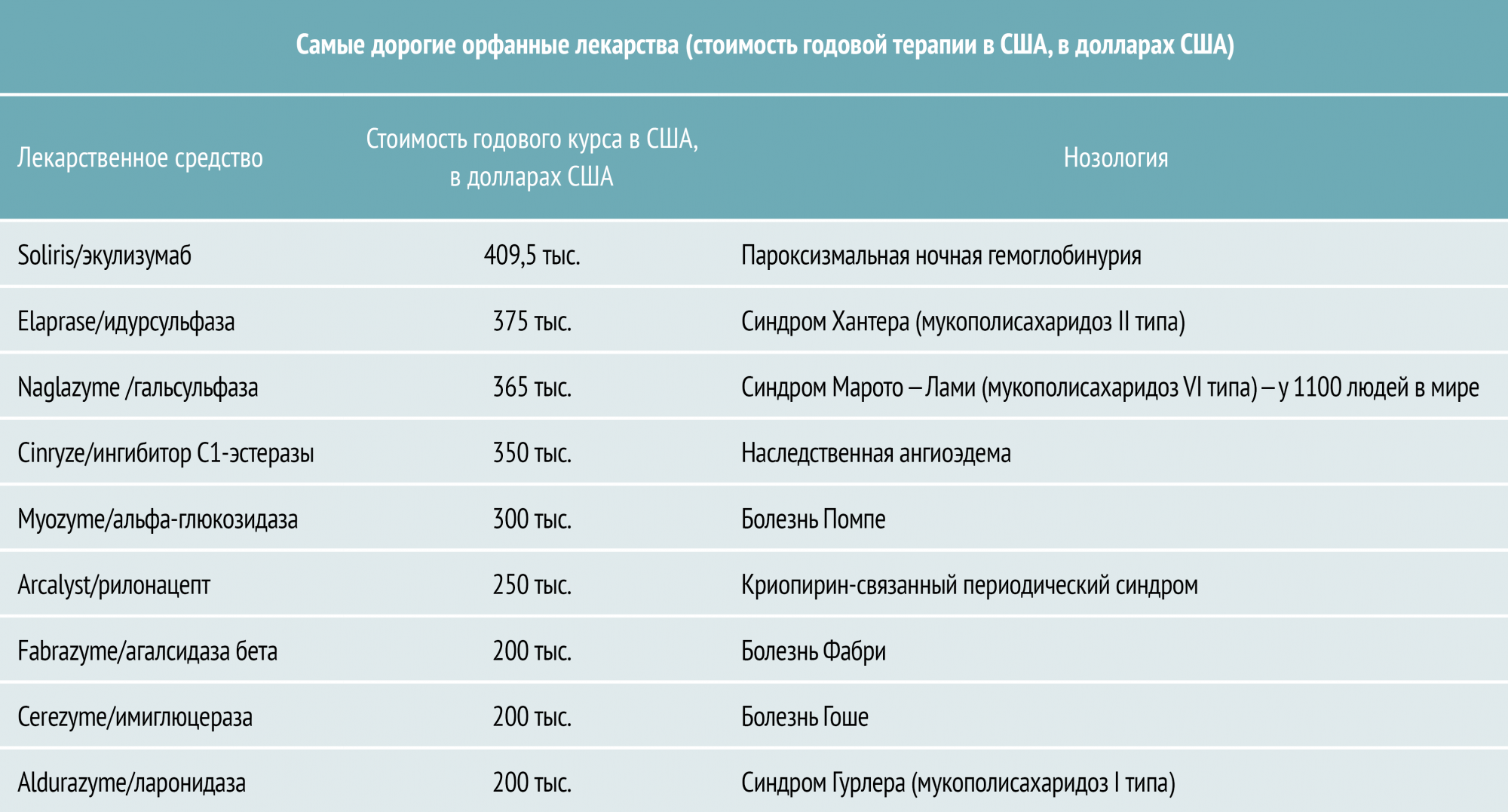
Почему так дорого?
- Всероссийское общество гемофилии
- Общероссийская общественная организация инвалидов — больных рассеянным склерозом
- Межрегиональная общественная организация «Помощь больным муковисцидозом»
- Межрегиональная общественная организация «Содействие инвалидам с детства, страдающим болезнью Гоше, и их семьям»
- Региональная общественная организация помощи больным несовершенным остеогенезом
- «Хрупкие дети»
- Межрегиональная общественная организация «Содействие больным саркомой»
- Ассоциация нервно-мышечных болезней «Надежда»
- Благотворительный фонд «Подари жизнь»
Материалы об орфанных препаратах и заболеваниях:
Системные васкулиты как пример редких, орфанных заболеваний
Первичные системные васкулиты — редкие (орфанные) заболевания, и врачи, работающие в обычных лечебных учреждениях, а не в специализированных центрах, просто не могут накопить необходимого опыта в распознавании и лечении этих болезней.

Новые открытия и актуальные проблемы в мире лекарств
Сегодня орфанным препаратам стали уделять повышенное внимание. Появились препараты для лечения таких редких болезней, как мукополисахаридоз II типа, болезнь Ниманна-Пика и так далее.

Оригинальные лекарственные препараты и дженерики
В «лекарственном портфеле» многих инновационных компаний присутствуют орфанные препараты, которые окупаются долго и не приносят большой прибыли. Их разработка и производство являются следствием осознания ответственности перед каждым пациентом в отдельности.
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.
19 августа 2021
Редакция не несет ответственности за информацию, размещенную в рекламных материалах. Мнение редакции может не совпадать с мнением наших авторов. Все материалы, опубликованные в журнале, охраняются законом «Об авторском праве». Любое воспроизведение статей, перепечатка либо ссылка на них допускаются исключительно с письменного согласия редакции.
Источник
Что такое “болезни-сироты” и почему их лечение проблематично
В настоящее время в мире не существует лечения более чем для 6000 редко отмечающихся заболеваний, две трети которых поражают пациентов детского возраста. В целях привлечения внимания общественности к этой проблеме Европейская организация по редким заболеваниям (European Organization for Rare Diseases — EURORDIS) 29 февраля 2008 г. учредила День редких заболеваний. Последний день февраля в високосном году был выбран отнюдь не случайно — он выпадает только раз в четыре года, поэтому символично отождествляется с редкими болезнями. Общественные акции, проводимые в последний день февраля, получили широкое распространение не только в европейских странах, но и во всем мире
«Болезни-сироты»
Редкие или орфанные (от англ. оrphan — сирота) болезни — это обобщенное название для врожденных либо приобретенных заболеваний, которые крайне редко отмечаются в общей популяции населения, ухудшают качество жизни, хронически прогрессируют и могут приводить к инвалидности или смерти.
Многие орфанные заболевания являются генетически обусловленными и сопровождают человека на протяжении всей жизни, даже если их симптомы проявляются не сразу. Часто болезнь возникает уже в раннем возрасте — около 30% детей с редкими заболеваниями не доживают до 5 лет.
Следует отметить, что не существует сведений о едином уровне распространенности заболевания в популяции, при котором его начинают считать редким. Заболевание может быть редким в одной части мира или среди определенной группы людей, но при этом часто отмечаться в других регионах либо среди других популяционных групп. К примеру, во всем мире выявлено лишь 200 человек с дефицитом N-ацетилглутамат синтетазы — наследственным заболеванием, которое приводит к нарушению обмена веществ. Но поскольку редких заболеваний самих по себе достаточно много, то в целом количество людей с различными их видами также весьма внушительно: например, в США около 30 млн человек (каждый десятый), в Европейском Союзе — более 30 млн человек (от 6 до 8% от общей численности населения).
Вместе с тем существует так называемое социально направленное определение редких болезней, которое отображает границу финансово-экономического обоснования выгоды для разработки лекарственных средств, используемых в лечении соответствующего заболевания. В разных странах критерии «орфанности» болезни определяют на основании частоты распространенности на уровне от 1 случая на 1 тыс. человек до 1 случая на 200 тыс. человек. В частности, в США редким заболеванием считается патология, диагностированная менее чем у 200 тыс. человек, что составляет менее 6,4 пациента на 10 тыс. человек (из расчета, что население США — 314 млн человек), а в России — 10 случаев на 100 тыс. человек. В странах ЕС под определение «редкое заболевание» подпадают состояния, отмечаемые менее чем у 5 пациентов на 10 тыс. человек (1:2000) или менее чем у 250 тыс. больных, при том что население стран ЕС составляет 506 млн человек. Для сравнения: в Японии заболевание считается орфанным, если оно диагностировано менее чем у 50 тыс. человек (т.е. менее 4 на 10 тыс.), из расчета, что население Японии —128 млн человек.
В настоящее время для Украины адекватным является распространенность на уровне 1:2000, как принято в ЕС [1].
Орфанные лекарства
Очевидно, что наряду с редкими заболеваниями существуют и редкие (орфанные) лекарства для их лечения. Орфанные препараты — это лекарственные средства, предназначенные для диагностики, профилактики и лечения редких заболеваний [2]. Препарат получает статус орфанного, если его применяют для терапии редко отмечающегося заболевания, которое угрожает жизни пациента или может привести к тяжелой инвалидности. Это общий принцип, которому следуют во многих странах мира.
Некоторые заболевания отмечаются настолько редко, что затраты на разработку и выведение на рынок препаратов для их диагностики, профилактики или лечения не окупятся ожидаемыми доходами от продаж; фармацевтическая промышленность не готова заниматься их разработкой на стандартных рыночных условиях; такие лекарства называются «орфанными» — именно так описана проблема в Директиве ЕС 141/2000. В результате в настоящее время для 95% редких заболеваний терапии просто не существует.
В настоящее время стоимость лечения одного пациента с орфанным заболеванием составляет от 20 тыс. грн до 6–8 млн грн в год. Финансирование лечения редких заболеваний в Украине в 2015 г. было увеличено на 50% по сравнению с 2014 г., однако в проекте бюджета на 2016 г. оно осталось на уровне 2014 г. (138 млн грн вместо необходимых 500 млн грн)[6].
Тем не менее орфанные лекарства появляются благодаря общим усилиям всех заинтересованных сторон, а также сочетанию рыночных и регуляторных стимулов. При этом очень важным аспектом стимуляции исследований по созданию орфанных препаратов является поддержка со стороны государства.
В конце 1999 г. Европа последовала примеру США и Японии, которые предложили различные меры стимулирования разработки орфанных препаратов. В директиве ЕС был определен порядок отнесения лекарственных препаратов к категории орфанных, а также перечислены меры поддержки исследований, разработки и продвижения на рынок лекарств для терапии редких заболеваний, включая эксклюзивное право на продажу препарата по этим показаниям на срок до 10 лет.
И если на момент принятия Закона об орфанных лекарствах в США в 1983 г. Управлением по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDА) к применению было одобрено лишь 38 орфанных препаратов, то по состоянию на октябрь 2014 г. согласно отчету аналитической компании «Evaluate Pharma» «Orphan Drug Report 2014» в США число одобренных орфанных препаратов составило 373 [3].
Проблемы орфанных препаратов
По мнению EURORDIS, в условиях рыночной экономики фармацевтическая промышленность не заинтересована в разработке и продаже малых партий лекарств, предназначенных только для небольшого количества больных. Это объясняется тем, что ожидаемые поступления от продажи таких лекарственных средств не покрывают чрезвычайно высоких расходов фармацевтических компаний, связанных с их выводом на рынок [2].
Во многом сложность развития этого сектора клинической фармакологии обусловлена отсутствием разработанных подходов к оценке эффективности и безопасности орфанных лекарств, т.к. проведение обычных крупномасштабных клинических исследований в этом случае невозможно.
В настоящее время наибольшее количество «лекарств-сирот» используют для лечения гемобластозов и рака (острые лимфобластные лейкозы, промиелоцитарные лейкемии, хронический миелолейкоз; рак почки, надпочечников, пищевода; неходжкинская лимфома, семейный аденоматоз кишечника и т. д.). На втором месте по применению этих препаратов находится группа наследственных заболеваний — акромегалия, болезнь Фабри, гипераммониемия, болезнь Гоше, мукополисахаридоз I, II, IV типов и др. Третье место занимают тяжелые врожденные и наследственные заболевания центральной нервной системы, прежде всего миоклоническая эпилепсия (синдром Драветса), эпилепсия Леннокса, катаплексия с нарколепсией у взрослых, хронический болевой синдром, резистентный к анальгетикам [4].
Перспективы орфанных препаратов
Преимущество орфанных препаратов заключается в том, что им не грозит конкуренция, поскольку их генерики появляются на рынке крайне редко. Кроме того, если препарату присвоен статус орфанного, то процедура одобрения регуляторными органами проходит намного быстрее, а клинические испытания обходятся компаниям дешевле. Одной из ключевых законодательных инициатив, призванных стимулировать разработку орфанных средств, является продление срока их патентной защиты по сравнению с другими инновационными ЛС.
Кроме того, фармацевтические компании, занимающиеся разработкой орфанных препаратов, могут претендовать на получение целевых грантов в рамках соответствующих программ, осуществляемых на уровне ЕС и отдельных стран, а также инициатив, направленных на проведение исследований в области разработки лекарств для лечения редких заболеваний, включая рамочные программы ЕС в сфере здравоохранения.
Фармацевтическим компаниям, которые занимаются разработками орфанных ЛС в США, также предоставляются различные финансовые льготы для осуществления своих проектов. Таким компаниям полагается 50% налоговый кредит на R&D-расходы. Также правительство США дает гранты на проведение I–III фазы клинических исследований продуктов, предназначенных для лечения редких заболеваний, в объеме $30 млн. Налоговые сборы с потребителей этой продукции отменены, что делает ее более доступной и способствует увеличению объема продаж в натуральном выражении.
Согласно данным аналитического доклада «Thomson Reuters», объем мирового рынка орфанных препаратов к концу 2011 г. превысил $50 млрд, что составило примерно 6% общего объема рынка фармпродукции ($880 млрд). По прогнозам, к 2018 г. рынок орфанных ЛС будет оцениваться в $127 млрд, достигнув 16% рынка рецептурных препаратов.
Термин «орфанные болезни» впервые появился в США в 1983 г. во время принятия закона о препаратах-сиротах («Orphan Drug Act»), предназначенного для поощрения фармацевтических компаний к разработке лекарств для лечения заболеваний, которые занимают небольшой объем рынка
По данным аналитической компании «Evaluate Pharma», объем продаж орфанных препаратов в США, ЕС и Японии будет уверенно увеличиваться до 2020 г. Данная тенденция вызвана снижением затрат на разработку орфанных препаратов по сравнению с инновационными лекарственными средствами, предназначенными для лечения заболеваний в большой популяции, а также повышением продуктивности таких разработок.
По данным отчета «Orphan Drug Report 2014», доля орфанных препаратов в общем объеме продаж рецептурных лекарственных средств (за исключением генериков) к 2020 г. составит 19,1% (около $176 млрд), при этом среднегодовой прирост в период 2014–2020 гг. в денежном выражении достигнет 10,5%. Для сравнения: среднегодовой прирост доли лекарств для лечения заболеваний, часто выявляемых в популяции и не относящихся к орфанным, за данный период составит лишь 4,3%, а рецептурных средств — 5,3%. Таким образом, можно проследить четкую тенденцию к увеличению доли орфанных препаратов в общем объеме продаж рецептурных лекарственных средств (за исключением генериков), начиная с 8,9% в 2006 г. до 19,1% в 2020 г. [3].
Ситуация с редкими болезнями в Украине
В Украине к орфанным заболеваниям отнесены болезнь Гоше, фенилкетонируя, гемофилия типов А или В, болезнь Виллебранда, муковисцидоз, гипофизарный нанизм, тирозинемия, болезнь Помпе, болезнь Нимана — Пика, лейциноз (болезнь кленового сиропа), мышечная дистрофия, первичные (врожденные) иммунодефициты, редкосные онкологические заболевания и др.
Следует отметить, что в 2014 г. Минздрав Украины упорядочило понятие «орфанные заболевания», а также усовершенствовало и привело в соответствие с европейскими нормами реестр орфанных заболеваний. Кроме того, был разработан порядок пожизненного обеспечения больных лекарственными средствами и специальным диетическим питанием, а также принято решение о создании центра орфанных заболеваний на базе Национальной детской специализированной больницы «Охматдет» для взаимодействия с аналогичными центрами в других странах мира и др. [5].
Были внесены изменения в Основы законодательства Украины о здравоохранении относительно обеспечения профилактики и лечения редких (орфанных) заболеваний (Закон Украины № 2461 от 15 апреля 2014 г.). В соответствии со статьей 531 «Профилактика и лечение редких (орфанных) заболеваний» государство обеспечивает меры по профилактике редких (орфанных) заболеваний и организации предоставления гражданам, страдающим такими заболеваниями, соответствующей медицинской помощи. С этой целью центральный орган исполнительной власти, обеспечивающий формирование государственной политики в сфере здравоохранения: определяет и утверждает перечень редких (орфанных) заболеваний и обеспечивает официальную публикацию этого перечня; в порядке, установленном Кабинетом Министров Украины, обеспечивает создание и ведение государственного реестра граждан, страдающих редкими (орфанными) заболеваниями; определяет меры, необходимые для проведения профилактики редких (орфанных) заболеваний, и устанавливает порядок оказания медицинской помощи гражданам с этими заболеваниями.
Законом также предусмотрено, что граждане с редкими заболеваниями бесперебойно и бесплатно обеспечиваются необходимыми для лечения этих заболеваний лекарственных средств и соответствующими пищевыми продуктами для специального диетического потребления.
В настоящее время стоимость лечения одного пациента с орфанным заболеванием составляет от 20 тыс. грн до 6–8 млн грн в год. Финансирование лечения редких заболеваний в Украине в 2015 г. было увеличено на 50% по сравнению с 2014 г., однако в проекте бюджета на 2016 г. оно осталось на уровне 2014 г. (138 млн грн вместо необходимых 500 млн грн)[6].
Подготовила Александра Демецкая, канд. биол. наук
Список литературы находится в редакции
Источник