Разъяснения по «Маркировке»
Специалисты оператора ЦРПТ комментируют вопросы аптек: ФАПы, отпуск лекарственных средств по безналу, работа в личном кабинете ИС «Маркировка», перемещение ЛП внутри аптечной сети и другие практические аспекты
Мы продолжаем серию материалов, в которых представители «Центра развития перспективных технологий» отвечают на вопросы читателей «Катрен-Стиль», посвященные работе с маркированными лекарственными препаратами. Вопросы возникают в ходе специальных бесплатных вебинаров, а также приходят на почту редакции. На этот раз руководитель проекта «Фарма» компании «ЦРПТ» Алексей Косарев и его коллеги решили ответить на самые распространенные вопросы, которые повторяются из раза в раз. Для большей ясности в начале статьи авторы объясняют, где брать информацию самостоятельно — кому из пользователей МДЛП пригодится тот или иной официальный документ.
Вступление: три категории пользователей
Всех пользователей МДЛП можно условно разделить 3 категории. Первая — это участники оборота с объемами более 10 упаковок в день. Они работают с МДЛП через ИТ-интеграторов и ККТ, которые передают данные в МДЛП автоматически. ЦРПТ сотрудничает со всеми крупными ИТ-интеграторами и поставщиками ККТ. Если ваш поставщик ПО есть на сайте «Честный знак» в разделе «Партнеры и Протестированные решения», то интеграция у вас уже есть. Если вы работаете с другим поставщиком, то уточните у него наличие в системе модуля для работы с маркированным товаром. Если у вас «самописная» система, ее надо доработать в соответствии с документами, которые предназначены для ИТ-специалистов (см. ниже). Рекомендуем получить все разъяснения у провайдеров услуг и пройти обучение по работе с новым функционалом в том интерфейсе, в котором вы осуществляете свою ежедневную деятельность.
Вторая категория — это участники оборота с объемами менее 10 упаковок в день. Они могут (но не должны) работать с ИС «Маркировка», внося данные о лекарственных средствах «вручную» через личный кабинет.
Третья категория пользователей — это ИТ-специалисты, которые взаимодействуют с МДЛП на уровне программы.
Для этих трех категорий пользователей подготовлены схемы и инструкции разного уровня погружения в технические детали. Просим обращать внимание на это при изучении ответов на вопросы. Для 1‑й категории основной документ — «Паспорта процессов». Для 3‑й категории (и 2‑й по желанию) основной документ — это «Логическая модель файлов обмена функциональной подсистемы информационной системы маркировки товаров контрольными (идентификационными) знаками лекарственных препаратов для медицинского применения».
Ответы на вопросы
Как будет проходить процесс маркировки товаров в аптечных учреждениях отдаленных населенных пунктов, где работают онлайн-кассы без передачи данных?
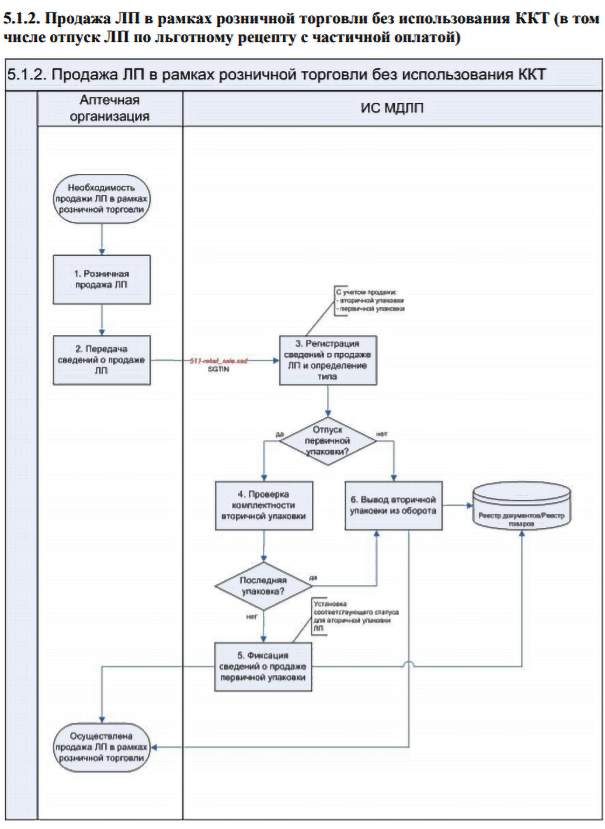
Сведения о розничной продаже маркированных лекарств должны передаваться вручную через личный кабинет или через головную организацию при наличии таковой (в таком случае процесс не меняется).
При наличии у учреждения вышестоящей (головной) организации, сведения о выбытии передает указанная организация. Действия происходят по схеме:
Детальное описание последовательности действий описано в документе «Паспорта процессов» в разделе 5.1.2.
Подскажите, мы планируем осуществлять деятельность в рамках договора комиссии с ФАП, расположенными в сельской местности. Каким образом нам организовать деятельность по маркировке ЛП?
При отпуске лекарственных препаратов через ФАП, сведения о выбытии передаются вышестоящей организацией.
Отпуск препаратов на медпункты, детские сады и детские лагеря при оплате по безналичному расчёту (без ККМ). Как работать с маркированными ЛС?
Если участник оборота, которому осуществляется отпуск ЛП, имеет лицензию на медицинскую деятельность, то он должен быть зарегистрирован в МДЛП. Если не зарегистрирован, тогда выполняется операция отгрузки ЛП под названием «Регистрация в ИС «Маркировка» сведений об отгрузке лекарственных препаратов на незарегистрированное место деятельности».
Как отражать в МДЛП безналичный расчет между организациями, как аптека регистрирует выбытие ЛП, купленных по безналичному расчету другой организацией?
В данном случае осуществляются операции об отгрузке лекарственных препаратов со склада отправителя/приема лекарственных препаратов на склад. Детальное описание последовательности действий описано в документе «Паспорта процессов» в разделах 4.1 и 4.2 соответственно.
Подскажите, какие действия нужно совершать поставщику. Мы небольшая компания, зарегистрированы в «Честном знаке». Дальше непонятно — что нам нужно делать, когда мы получаем товар от производителя и когда мы производим отгрузку в ЛПУ. Где можно найти подробную инструкцию по работе дистрибьютора?
Каждая операция (приемка, перемещение, выбытие лекарственных препаратов) должна фиксироваться в МДЛП. Для каждой из этих операций определен состав передаваемых данных и последовательность действий. Имеется два руководящих документа. Последовательность действий описана в документе «Паспорта процессов».
Первично осуществляется приемка товара от производителя. Для этого необходимо использовать операцию «Регистрация в ИС «Маркировка» подтверждения (акцептования) сведений».
Далее при реализации товара другому участнику оборота (ЛПУ), выполняются следующие операции:
- В случае прямого акцептования — «Регистрация в «ИС «Маркировка» сведений об отгрузке лекарственных препаратов со склада отправителя»
- В случае обратного акцептования — «Регистрация в ИС «Маркировка» подтверждения (акцептования) сведений».
Допустимо ли будет с 01.01.2020 для аптечной сети отражать в ИС МДЛП перемещение отозванной из обращения (забракованной) серии лекарственного препарата между местами осуществления деятельности (из аптеки на аптечный склад) при осуществлении централизованного возврата поставщику с аптечного склада?
Допустимо, если в дальнейшем с отозванной из обращения серией будут выполнены следующие операции:
- Регистрация в ИС «Маркировка» сведений о передаче лекарственных препаратов на уничтожение.
- Регистрация в ИС «Маркировка» сведений о факте уничтожения лекарственных препаратов.
Как будет производиться отпуск лекарственных препаратов в структурные подразделения юридического лица? Как будет осуществляться отпуск в структурных подразделениях, если в них нет программы товарного учета, а только ККТ? Как осуществлять отпуск по договорам, школам и т. д.?
Для выполнения операции перемещения лекарственных средств между местами деятельности в рамках одного ИНН необходимо выполнить операцию — «Регистрация в ИС «Маркировка» сведений о перемещении лекарственных препаратов между различными адресами осуществления деятельности».
При использовании ККТ в аптеке данные о выбытии ЛП будут передаваться в МДЛП в момент осуществления покупки. Данные передаются оператором фискальных данных автоматически, в рамках стандартного пакета.
Учреждения, обладающие лицензией на медицинскую или фармацевтическую деятельность, должны быть зарегистрированы в ИС МДЛП. Реализация ЛП происходит по операциям:
- В случае прямого акцептования — «Регистрация в «ИС «Маркировка» сведений об отгрузке лекарственных препаратов со склада отправителя».
- В случае обратного акцептования — «Регистрация в ИС «Маркировка» подтверждения (акцептования) сведений».
Если препарат в стационаре забракован после списания в отделение регистратором выбытия — как его вернуть поставщику?
Необходимо выполнить операцию повторного ввода ЛП в оборот, а затем осуществить возврат поставщику. Далее выполнить операции:
«Регистрация в ИС «Маркировка» сведений о передаче лекарственных препаратов на уничтожение» и «Регистрация в ИС «Маркировка» сведений о факте уничтожения лекарственных препаратов».
Что будет с остатками в МДЛП, если аптека не смогла принять КиЗы от поставщика при обратном акцептовании (КиЗы, например, на производителе), а продавать уже начала?
В МДЛП рассматривается возможность реализации реестра ожиданий, позволяющего выводить ЛП до момента акцептования. После того как ЛП будет оприходован, он будет выведен из оборота.
Как можно будет осуществлять перемещение товара из одной аптеки в другую в одной сети аптек?
Движение ЛП между местами деятельности в рамках одного ИНН регистрируется операцией — «Регистрация в ИС «Маркировка» сведений о перемещении лекарственных препаратов между различными адресами осуществления деятельности». Данные передаются автоматически через товарно-учетную систему, интегрированную с МДЛП, или вручную посредством функционала личного кабинета МДЛП (последнее целесообразно, если оборот — не более 10 уп./сутки).
Как осуществлять возврат ЛС от структурных подразделений?
Возврат регистрируется операцией — «Регистрация в ИС «Маркировка» сведений о перемещении лекарственных препаратов между различными адресами осуществления деятельности». Данные передаются автоматически.
Если у вас еще остались вопросы по работе с маркированными ЛС, приглашаем вас 11 декабря посетить очередной бесплатный вебинар на тему «АРМ в аптеке: знакомимся с техническими средствами маркировки». Там вы сможете не только услышать официальные рекомендации, но и задать свои вопросы в режиме онлайн. Спешите регистрироваться, количество мест ограниченно.
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.
Источник
Правила мерчендайзинга в аптеке: как выкладывать лекарства на витрину не нарушая закон
Выкладка на витрину призвана обратить внимание пациента на продаваемый товар и способствовать увеличению продаж. Она позволяет ознакомиться с товаром и принять решение о покупке. При размещении лекарств для обозрения в торговом зале надо учитывать требования нормативной документации. Как же сделать так, чтоб все было «правильно» и соответствовало закону? Разберем три наиболее частых вопроса, вызывающих затруднения у фармспециалистов.
Можно ли выкладывать светочувствительные препараты на витрину?
К светочувствительным относятся многие антибиотики, галеновы препараты, лекарственное растительное сырье, органопрепараты, витамины, эфирные масла и др. К особо светочувствительным: нитрат серебра, прозерин, физостигмина салицилат, тимол и некоторые другие. В 646н приказе о надлежащей практике хранения и перевозке ЛП мы находим только рекомендацию защищать светочувствительные препараты от попадания прямых солнечных лучей. Однако согласно 706н приказу по хранению ЛС, на чувствительные к свету препараты не должен попадать естественный и искусственный свет, а лекарства в первичной и вторичной упаковке следует хранить в шкафах или на стеллажах при условии, что на них не будут попадать прямые солнечные лучи или иной яркий направленный свет.
Вторичная заводская упаковка, сделанная из картона, сама по себе защищает лекарственный препарат от света. Другое дело, что она не защитит от нагрева под действием прямых лучей.
Большинство препаратов хранится при температуре до 25-30 градусов, поэтому даже несветочувствительные ЛС не желательно хранить на местах, открытых прямым солнечным лучам. Однако для них мы ограничиваемся измерением температуры в помещении. Но для светочувствительных ЛС этой предосторожностью ограничиться не имеем права , поэтому такое лекарство нуждается в дополнительной защите.
Светозащита может представлять из себя светоотражающую пленку, жалюзи, козырьки и прочие приспособления, создающие затененное место. Таким образом, данную группу ЛС можно размещать на витринах без подсветки, расположенных в затененном месте, вдали от окон в первичной и вторичной упаковке, которая будет защищать препарат от света.
А как на счет пустышки на витрине?
Что касается такого варианта, как выставление пустой вторичной упаковки на витрине, то это решение не лучшее, поскольку встает вопрос о правильном хранении препарата без нее. Выходит, что лекарство лишается защиты в виде вторичной упаковки, а первичная упаковка может не защищать лекарство от света. Директор юридической компании «Юнико-94»
Марат Милушин на сайте отвечает на этот вопрос так: запрета на выставление пустой потребительской упаковки на витрину нет, но в данном случае вынутое лекарственное средство должно храниться в закрытом темном шкафу. Однако дьявол в деталях: если лекарственный препарат хранится в заводской упаковке, это означает, что условия хранения (в части светозащиты) соблюдаются, а извлечение светочувствительного препарата из вторичной упаковки и хранение без нее лишает препарат гарантированной производителем защиты от света — предупреждает Елена Неволина
исполнительный директор некоммерческого партнерства «Аптечная гильдия». Суды в отношении правил хранения светочувствительных лекарственных препаратов принимают разные решения . Поэтому самым разумным решением для светочувствительных препаратов, позволяющим избежать лишних вопросов проверяющих, будет их хранение в упаковке производителя в шкафах с непрозрачными дверцами.
Можно ли выкладывать рецептурные препараты на витрину?
Приказ 647н позволяет хранить рецептурные препараты на витринах и в открытых шкафах, находящихся вне доступа покупателей. Однако Федеральный закон от 13.03.2006 № 38-ФЗ «О рекламе» запрещает рекламу рецептурных лекарственных средств потребителям. Реклама — это информация о товаре, направленная на привлечение внимания, формирования, поддержания интереса и продвижения на рынке. При том, что функции у рекламы и выкладки совпадают, одно лишь расположение препарата на витрине без дополнительной информации не будет рекламой. Некоторые юристы трактуют закон о рекламе в отношении лекарственных препаратов по-другому и считают, что выкладку все же следует относить к рекламе, поскольку это стимулирующая к покупке информация о препарате, выраженная «любым» способом, ссылаясь при этом на п.1 ст. 3 ФЗ-38. Однако, пп.7,8 статьи 2 этого же закона говорят о том, что сведения на упаковке, включающие информацию о товаре, его производителе, любые элементы оформления товара на его упаковке не попадают под действие закона. Поскольку рецептурные препараты требуют определенных показаний, вряд ли человек не имеющий заболевания захочет просто так приобрести рецептурное лекарство. А для хронических больных, принимающих рецептурные препараты регулярно, выкладка позволяет получить информацию о наличии и цене препарата.
На сегодняшний день никаких действующих нормативных документов, запрещающих выкладку рецептурных препаратов на витрину, нет.
Рецептурные препараты выкладывать на витрины можно, но другой вопрос — нужно ли. Это вопрос спорный и решает каждая аптека для себя. Во избежание недоразумений, при необходимости выкладки рецептуры, непосредственно для покупателей лучше разместить на данную витрину надпись «отпуск по рецепту врача», «рецептурные препараты». Всё дело в статье 10 Закона «О защите прав потребителей», которая предписывает предоставлять покупателям необходимую и достоверную информацию о товарах, обеспечивающую возможность их правильного выбора. Для того, чтобы у покупателя не создалось ложного впечатления, что эти препараты можно приобрести без рецепта, а фармработнику не пришлось давать лишние объяснения, эти меры следует предпринять.
Nota Bene! Что еще следует помнить при выкладке ЛС?
Раздельно размещаются:
- лекарственные препараты, БАД и медизделия ( приказ Минздрава № 646н и Закон от 07.02.1992 № 2300–1 «О защите прав потребителей» ) ;
- рецептурные и безрецептурные препараты (Приказ 647н );
- внутренние и наружные (Приказы 646н, 706н).
Кроме этого, лекарственные препараты на витринах группируются по фармакологическому действию. (Приказы 646н, 706н). П ри этом лекарственные препараты на витринах размещаются отдельно.
А в вашей аптеке полностью безопасная или же рискованная выкладка (с рецептурой и светочувствительными ЛС)?
Источник