- НАЦИОНАЛЬНАЯ ЛЕКАРСТВЕННАЯ ПОЛИТИКА РОССИИ НА ПЕРИОД 2020-2030 ГГ.: КАКОЙ ОНА БУДЕТ?
- 11. Понятие Национальной лекарственной политики. Основные составляющие Национальной лекарственной политики.
- 2. Национальная лекарственная политика и ее роль в обеспечении доступности лекарственных средств.
- 12. Национальная лекарственная политика стран Евросоюза и снг.
- Подходы к формированию проекта Национальной лекарственной политики. Часть 2
- Национальная лекарственная политика как документ стратегического планирования
- О Национальной лекарственной политике
- Цели и задачи Национальной лекарственной политики
- Разработка Национальной лекарственной политики
- Основы стратегического планирования в Российской Федерации
- Достижения и проблемы системы лекарственного обеспечения в Российской Федерации сегодня
НАЦИОНАЛЬНАЯ ЛЕКАРСТВЕННАЯ ПОЛИТИКА РОССИИ НА ПЕРИОД 2020-2030 ГГ.: КАКОЙ ОНА БУДЕТ?
В РАН состоялось заседание Межведомственного совета по научному обоснованию и сопровождению национальной лекарственной политики России на ближайшее десятилетие. В ходе заседания академики, представители органов государственной власти и ведущих фармацевтических компаний обсудили вклад фармацевтической отрасли в экономику государства, оценили роль государства в разработке новых лекарств и определили ключевые показатели, которые должны быть включены в национальную лекарственную политику и в соответствии с которыми будет вестись оценка инновационных лекарственных препаратов.
Межведомственный совет по научному обоснованию и сопровождению национальной лекарственной политики России (далее – совет) был создан на базе Российской академии наук в марте 2019 года. На настоящий момент итоговый документ официально еще не представлен, поскольку участникам межведомственного совета ещцце предстоит определить приоритетные направления в разработке новых лекарств, при этом представителями государственного сектора отмечена необходимость включения в документ четких индикаторов по оценке системы здравоохранения и показателей, по которым Россия может и должна выйти на лидирующие позиции в мире. Четкие критерии должны обеспечить эффективное финансирование научных разработок и стимулировать скорейший вывод таких продуктов на отечественный рынок.
В декабре 2019 г. в ходе итогового заседания совета первый заместитель Министра промышленности и торговли Российской Федерации Сергей Цыб отметил активную работу ведомства в части поддержки и развития фармацевтической отрасли: созданы привлекательные условия для инвестирования в экономику, индустриальные зоны и технопарки, промышленные фармацевтические кластеры, государственные и негосударственные фонды развития, а также разработан механизм специальных инвестиционных контрактов (СПИК). На протяжении многих лет основным инструментом поддержки отрасли остается государственная программа Российской Федерации «Развитие фармацевтической и медицинской промышленности». За время ее реализации удалось создать компетенции фактически по всем группам лекарственных препаратов, а объем отечественного производства лекарственных препаратов вырос более чем в 3 раза. Сегодня стоит цель создания конкурентоспособной фармацевтической промышленности, основанной на собственных инновационных разработках. При этом, основными направлениями реализации Стратегии являются:
- развитие собственных продуктов и инноваций, разработка инновационных лекарственных препаратов;
- поддержка экспортного потенциала, в том числе биологических лекарственных препаратов, биоаналогов, дженериков.
Учитывая капиталоемкость инновационных разработок, на которые, по оценкам академиков, требуется не менее $ 2 млрд, необходимо отметить, что их большую часть составляют затраты на маркетинг. Сергей Цыб подчеркнул, что при реализации проектов по разработке новых продуктов имеет большое значение приоритизация направлений разработки, которая и будет обуславливать необходимые объемы финансирования.
Стимулирование разработок собственных инновационных продуктов предполагается обеспечить за счет поддержки их реализации на внутреннем и внешних рынках, при этом, определяющим критерием для решения вопроса об оказании поддержки должны быть качество, эффективность и безопасность лекарственных препаратов.
Все научные центры в России, относящиеся к структуре Российской академии наук, получают государственное задание с соответствующим финансированием из различных ведомств. При этом, детального аудита результатов таких разработок, поддержанных из государственного бюджета, не проводится. Учитывая, что сегодня формируется перечень технологий, которые будут утверждаться Правительством Российской Федерации и финансироваться из бюджета Российской Федерации, очевидна необходимость выстраивания приоритетов к таким технологическим продуктам:
- приоритеты с точки зрения здравоохранения (влияния на показатели смертности, заболеваемости и т.д.);
- приоритеты с точки зрения возможностей компаний;
- приоритеты с точки зрения понимания, где сосредоточены усилия мировых глобальных игроков и компаний, инвестирующих в создание лекарств;
- приоритеты с точки зрения востребованности препаратов, которые будут выведены на рынок к 2030 году, в будущем.
В продолжение выступления Сергея Цыба, директор ФБУ «ГИЛС и НП» Минпромторга России Владислав Шестаков отметил, что национальная политика России с точки зрения ее эффективности должна включать 4 базовых критерия, утвержденных и рекомендованных ВОЗ для таких документов:
- способствовать улучшению медицинского обслуживания населения;
- обеспечивать равный доступ населения к основным лекарственным средствам при их умеренной стоимости;
- гарантировать качество, безопасность и эффективность всех лекарственных средств;
- обеспечивать необходимые условия рационального применения лекарственных средств.
«Важно правильно определить приоритетные направления развития и конкретные области развития инноваций с учетом потребности системы здравоохранения и обеспечения национальной безопасности государства: производить оригинальные препараты, биосимиляры, дженерики массового применения, лекарственные препараты с новыми формами доставки действующего вещества или специализирующиеся на одном конкретном заболевании», – отметил Владислав Шестаков. Говоря о конкретных мерах поддержки инновационной деятельности, которые параллельно обеспечат условия для развития бизнеса и создадут благоприятную для развития инноваций среду, заместитель главы российского государственного GMP-инспектората Владислав Шестаков выделил следующие направления:
- создание единых информационных порталов для всех участников рынка и потенциальных инвесторов, обеспечивающих доступ к передовым разработкам в фармацевтической отрасли. Например, создание площадки (биржи) по продаже инновационных биотехнологических разработок;
- проведение независимой научно-технической экспертизы проектов на разных стадиях их развития: создать независимый экспертный совет, проводящий аудит разработок на «входе» и «выходе». По итогам такого аудита к не исполнившим обязательства могут быть применены различные санкционные меры, вплоть до возврата ранее инвестированных государством средств. Как отметил Владислав Шестаков, научный и экспертный совет ФБУ «ГИЛС и НП» Минпромторга России готов выступить таким независимым аудитором;
- организация эффективного процесса, позволяющего собирать обратную связь у представителей бизнеса и разработчиков;
- совершенствование нормативной правовой базы, относящейся к вопросам регистрации и обращения лекарственных препаратов для медицинского применения, в том числе посредством закрепления понятия «инновационный препарат», ускоренной регистрации таких препаратов и бессрочной регистрации лекарственных препаратов, доказавших клиническую эффективность и безопасность. При этом, целесообразно использовать опыт существующих регуляторных систем, в частности FDA в части присвоения статуса «прорывной» для инновационных препаратов и их регистрация на условиях, не требующих третьей фазы клинических исследований. Немаловажным фактором при этом, является имплементация данных нововведений в нормативное правовое регулирование на наднациональном уровне;
- создание единой системы патентов, синхронизированной с государственными реестрами Минздрава России;
- актуализация перечня жизненно необходимых и важнейших лекарственных препаратов и наполнение перечня наиболее эффективными и современными новыми препаратами, в том числе отечественного производства;
- обеспечение устойчивых долгосрочных правил работы отрасли, касающихся ценообразования, поддержки локализованного производства, включая критерии локализации, в соответствии с которыми производители получают соответствующие преференции, механизмы оценки фармакоэкономической эффективности лекарственных препаратов.
Источник
11. Понятие Национальной лекарственной политики. Основные составляющие Национальной лекарственной политики.
2. Национальная лекарственная политика и ее роль в обеспечении доступности лекарственных средств.
Под термином «национальная лекарственная политика» понимают официальный документ, принимаемый на правительственном уровне, отражающий международно признанные принципы, концепции и управленческие механизмы функционирования и развития фармацевтического сектора, выполняющий стратегическую роль в развитии сферы обращения лекарственных средств.
Первым национальную лекарственную политику разработал Бангладеш в 1982 году, вслед за ним – Индия. В настоящее время национальная лекарственная политика разработана более чем в 140 странах. В их число входят Австралия, Япония, Греция, Чехия, Словакия, Румыния, Китай, страны Латинской Америки и Экваториальной Африки, бывшие республики СССР, за исключением России и Азербайджана.
В развитых странах (США, Великобритания) мира компоненты национальной политики также присутствуют, хотя не носят систематизированного характера.
Глобальными целями национальной лекарственной политики являются:
Доступность– равный доступ населения к основным лекарственным средствам по обоснованным ценам реализации. При формировании НАП этот приоритет является определяющим;
Качество,под котором понимают Государственный контроль за качеством лекарственных средств включающих мероприятия, направленные на соблюдение требований актов законодательства Республики Беларусь, регламентирующих обеспечение качества лекарственных средств;
Рациональное применение– обеспечение условий для назначения врачам и применения пациентами лекарственных средств на основании доказательной медицины, соответствия клинических показателей и экономической целесообразности.
Национальная лекарственная политика включает следующие компоненты:
— совершенствование нормативно-правового регулирования сферы обращения лекарственных средств;
— выбор основных лекарственных средств;
— рациональное использование лекарственных средств;
— экономическая доступность и цены на лекарственные средства;
— финансирование лекарственного обеспечения;
— система фармацевтического снабжения;
— регулирование и обеспечение качества;
— исследования в сфере лекарственных средств;
— контроль и оценка выполнения работы.
12. Национальная лекарственная политика стран Евросоюза и снг.
Фармацевтическая политика в Европейском союзе
Самым острым вопросом при разработке фармацевтической политики в Европейском союзе (ЕС) является конфликт между приоритетами здравоохранения и промышленности.
При проведении Национальной лекарственной политики на первом месте стоит ответственность перед потребителем, который должен иметь гарантию, что на рынок попадут только безопасные, качественные и эффективные лекарственные средства. Следующая задача – составление сбалансированного бюджета здравоохранения, с учетом контроля расходов на лечение и обеспечение лекарственными средствами. Третьей задачей во многих странах является осуществление регулирования, благоприятного для промышленности. Кроме того, у рынка лекарственных средств есть особенности структуры спроса: лекарственные средства назначают врачи, а основную часть расходов, как правило, несут на себе пациенты, обычно через какой–либо вид медицинского страхования. При этом не всегда существует конкуренция: иногда на рынке определенного класса лекарственных средств могут господствовать одна – две ведущие компании. Это делает необходимым еще большее вмешательство государства.
Национальной лекарственной политики в странах СНГ
С начала 90–х годов произошли значительные социально–экономические изменения в государствах СНГ. Эти изменения оказали серьезное влияние как на здравоохранение в целом, так и на систему обращения лекарственных средств в частности. Для определения стратегии развития фармацевтического сектора в странах бывшего Советского Союза Программой по фармацевтическим препаратам Европейского регионального бюро ВОЗ и Программой действий по основным лекарственным средствам, ВОЗ (Женева), при участии представителей всех стран СНГ, был подготовлен документ «Фокус на пациента».
Координация Национальной лекарственной политики стран СНГ осуществляется Межгосударственной комиссией по стандартизации, регистрации и контролю качества лекарственных средств, изделий медицинского назначения и медицинской техники государств–участников СНГ, работающей при Совете по сотрудничеству в области здравоохранения Содружества Независимых Государств.
Источник
Подходы к формированию проекта Национальной лекарственной политики. Часть 2
Национальная лекарственная политика как документ стратегического планирования
О Национальной лекарственной политике
В 1975 г. 28-я Всемирная ассамблея здравоохранения приняла резолюцию, рекомендующую всем странам – членам Всемирной организации здравоохранения (ВОЗ) разработать Национальную лекарственную политику (НЛП).
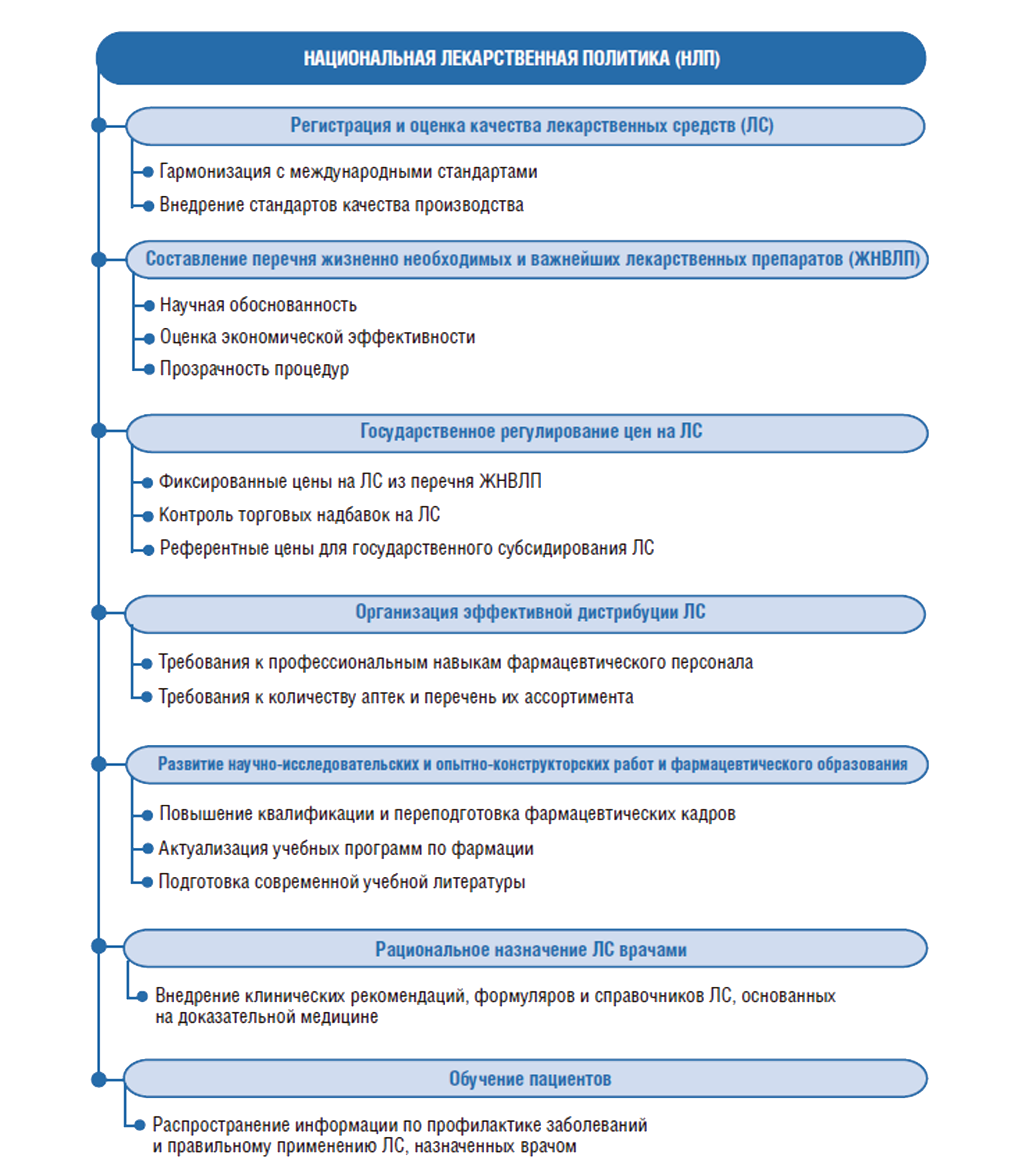
НЛП сегодня принята в 133 странах мира (из 165 исследованных стран [1] ) и есть практически во всех странах Европейского союза (ЕС). НЛП – это стратегический документ, который разрабатывается на долгосрочную перспективу, как правило, 10 лет. Он объединяет и балансирует роли многочисленных участников фармацевтического рынка – от разработки новых лекарств до их рационального потребления. Основные разделы НЛП представлены на рис.1.
Рисунок 1. Составляющие Национальной лекарственной политики 
Цели и задачи Национальной лекарственной политики
Все правила и задачи, которые устанавливает данная политика, должны быть подчинены единым целям государства в этой сфере. Для России цели Национальной лекарственной политики вытекают из указов Президента РФ В.В. Путина – № 204 от 07.05.2018 «О национальных целях и стратегических задачах развития Российской Федерации на период до 2024 года» и № 642 от 01.12.2016 «О Стратегии научно-технологического развития Российской Федерации». Это:
1) увеличение ожидаемой продолжительности жизни (ОПЖ) до 78 лет к 2024 г. и до 80 лет к 2030 г.;
2) обеспечение безопасности (независимости) РФ в сфере лекарственного обращения;
3) восстановление передового научно-технологического потенциала в разработке и производстве новых лекарственных препаратов (ЛП).
Исходя из данных целей НЛП должна ответить на ряд существенных вопросов, которые схематично представлены на рис. 2.
Рисунок 2. Вопросы, на которые должна ответить Национальная лекарственная политика
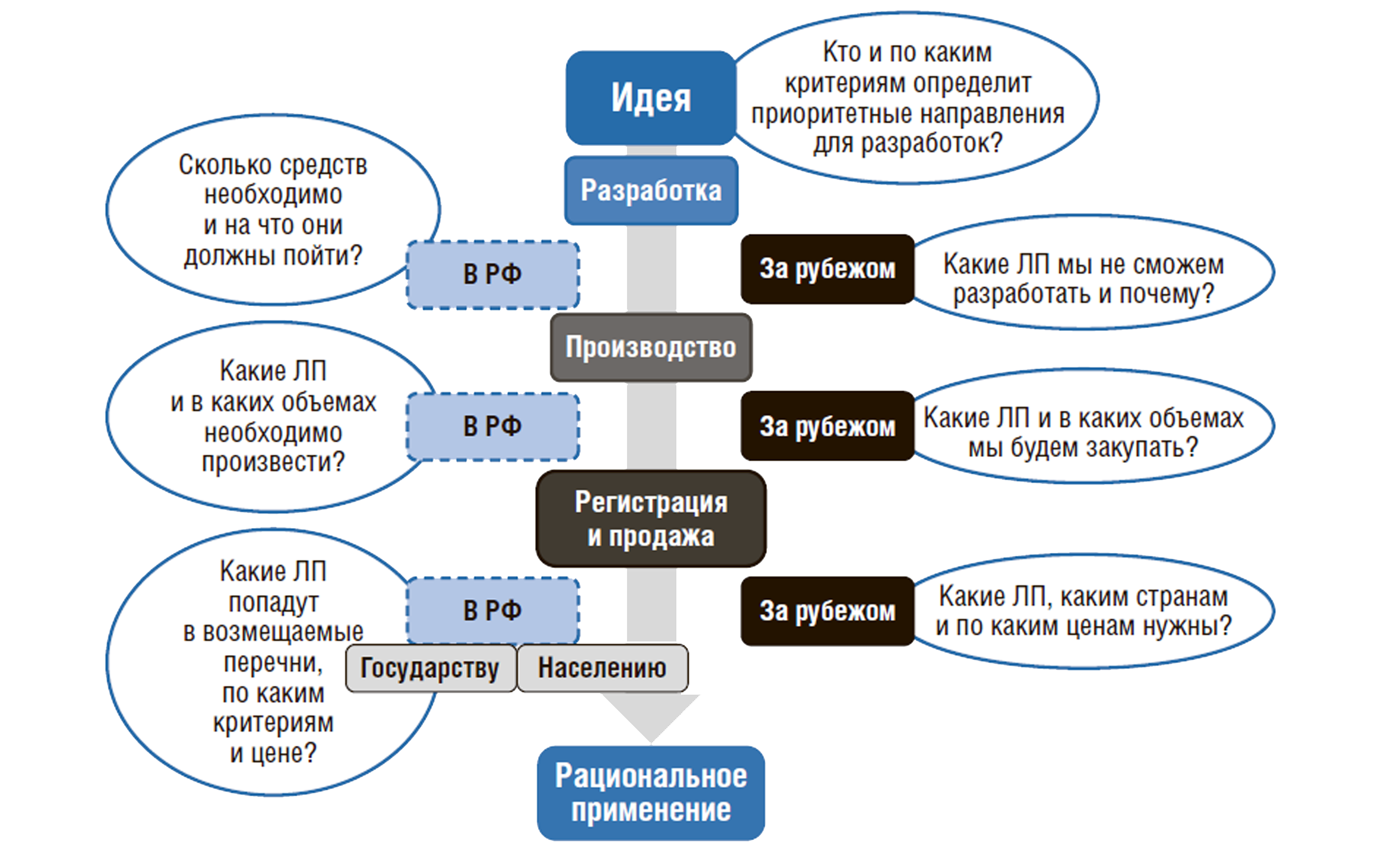
Отметим, что фармацевтический рынок не является саморегулируемым, он требует от государственных органов власти постоянного вмешательства во все процессы лекарственного обращения. Сегодня в России в регулировании этого рынка задействованы Министерство здравоохранения (Минздрав России), которое обеспечивает доступность лекарств для населения и их закупку, Министерство промышленности и торговли (Минпромторг России), отвечающее за развитие отечественного производства лекарств, Министерство науки и высшего образования (Минобрнауки России), которое занимается разработкой новых лекарств, Федеральная служба по надзору в сфере здравоохранения (Росздравнадзор), обеспечивающая качество и безопасность обращающихся на рынке лекарственных препаратов, и Федеральная антимонопольная служба (ФАС), контролирующая вопросы ценообразования на ЛП.
Соответственно принципиально важно, чтобы разработка НЛП носила межведомственный характер, а ведомственные стратегии развития были согласованы с ней и между собой. Система планирования и регулирования должна быть выстроена таким образом, чтобы разработанные и произведенные в России лекарства были действительно востребованы для снижения смертности, заболеваемости и инвалидности наших граждан, а фармацевтические производители знали объем внутреннего рынка на предстоящие годы, чтобы спланировать свои мощности.
При формировании этой политики «регуляторы-ведомства» сталкиваются с двумя непростыми задачами. Первая – необходимость соблюдения оптимального баланса между интересами множества субъектов лекарственного обращения: разными группами пациентов и их объединениями, фармацевтическими компаниями (в том числе отечественными и зарубежными производителями), оптовыми и розничными дистрибьюторами (государственными и частными), врачами и их общественными объединениями. Вторая – финансовые ограничения: общественные средства, направляемые на оказание бесплатной медицинской помощи, ограничены в любой стране.
В этой связи решение такой сложной многофакторной и межведомственной задачи, как разработка НЛП, требует серьезных научных обоснований, правильной расстановки приоритетов и неоднократных обсуждений.
Разработка Национальной лекарственной политики
Научное обоснование НЛП инициировала Российская академия наук (РАН), а головное ведомство в этой сфере – Минздрав России поддержал эту идею. Сегодня в РАН создан межведомственный Совет по научному обоснованию и сопровождению НЛП под руководством академика РАН В.П. Чехонина.В рамках 4 рабочих групп организована подготовка материалов по основным вопросам регулирования:
1. Координация фундаментальных и прикладных исследований в области разработки, создания и производства лекарственных средств (координатор – член-корр. РАН А.Д. Дурнев).
2. Оптимальные механизмы реализации системы всеобщего лекарственного возмещения (обеспечения) (координатор – акад. РАН Р.У. Хабриев).
3. Совершенствование системы формирования перечней ЛП и ценообразования на них (координатор – член-корр. РАН А.Л. Хохлов).
4. Обеспечение рационального и безопасного применения ЛП (координатор – член-корр. РАН Д.А. Сычев).
За общую координацию работ по научному обоснованию отвечает ученый секретарь Совета доктор медицинских наук Г.Э. Улумбекова. Следует отметить, что формировать стратегические документы и программы намного легче, когда поставлены конкретные цели. Мерилом предлагаемых решений в этих программах и стратегиях является время достижения целей и эффективность, т.е. возможность достижения результата за минимальные средства. Это главные принципы стратегического планирования.
Основы стратегического планирования в Российской Федерации
В РФ имеется серьезная база по стратегическому планированию:
- Федеральный закон от 28.06.2014 № 172-ФЗ (ред. от 31.12.2017) «О стратегическом планировании в Российской Федерации»;
- Постановление Правительства РФ от 02.08.2010 № 588 (ред. от 15.11.2017) «Об утверждении Порядка разработки, реализации и оценки эффективности государственных программ Российской Федерации»;
- Постановление Правительства РФ от 26.06.1995 № 594 (ред. от 28.12.2017) «О реализации Федерального закона “О поставках продукции для федеральных государственных нужд” (вместе с “Порядком разработки и реализации федеральных целевых программ и межгосударственных целевых программ, в осуществлении которых участвует Российская Федерация”, “Порядком закупки и поставки продукции для федеральных государственных нужд”, “Порядком подготовки и заключения государственных контрактов на закупку и поставку продукции для федеральных государственных нужд”)».
- Постановление Правительства РФ от 15.10.2016 № 1050 «Об организации проектной деятельности в Правительстве Российской Федерации (вместе с “Положением об организации проектной деятельности в Правительстве Российской Федерации”)».
- Методические рекомендации по подготовке паспорта приоритетного проекта правительства РФ от 20.10.2016 № 7951п-п6;
- Методические указания по разработке национальных проектов (программ), утверждены Правительством РФ 05.05.2018.
Соподчинение названных документов стратегического планирования представлено на рис. 3.
Рисунок 3. Соподчинение главных стратегических документов в части достижения ожидаемой продолжительности жизни 78 лет
НЛП, согласно этим нормативным документам, должна сбалансировать стратегии различных ведомств и роли различных сторон в интересах достижения поставленных целей (рис. 4).
Рис. 4.  Национальная лекарственная политика на стыке отраслевых стратегий и программ
Национальная лекарственная политика на стыке отраслевых стратегий и программ
1. Анализ – оценка состояния соответствующей сферы.
2. Прогнозы развития на долгосрочный период.
3. Приоритеты, задачи и показатели для их измерения.
4. Способы их эффективного достижения.
5. Сроки и этапы проведения мероприятий.
6. Ожидаемые результаты проведения мероприятий.
7. План мероприятий на среднесрочный период.
В соответствии с этими рекомендациями и будут формироваться основные разделы НЛП.
Достижения и проблемы системы лекарственного обеспечения в Российской Федерации сегодня
В РФ за последние годы благодаря государственной политике достигнуты серьезные позитивные сдвиги в сфере лекарственного обращения, а именно: принят основной Федеральный закон от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств», развивается отечественная фармацевтическая промышленность, осуществляется жесткий контроль за ценами на ЛП из списка жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП), существенно повышена прозрачность процессов включения лекарств в этот перечень, внедряется система идентификации ЛП от производителя до конечного потребителя.
Вместе с тем сохраняются проблемы. Главные из них подробно разобраны в части 1 «Анализ рынка лекарственных препаратовв РФ» (см.: ОРГЗДРАВ: новости, мнения, обучение. Вестник ВШОУЗ. 2018. Т. 4, № 4. С. 53–75).
1. Недостаточное лекарственное обеспечение населения ЛП в амбулаторных условиях – сегодня за счет государства на ЛП в РФ тратится в 2,4 раза меньше в доле ВВП, чем в «новых» странах ЕС, имеющих близкий уровень экономического развития (в 2,8 раза меньше по доллару ППС). В РФ эти средства идут только на лекарственное обеспечение тех категорий населения, которые имеют специальные льготы. Всего в РФ получают бесплатные лекарства в амбулаторных условиях за счет государства только 9 млн человек, а в развитых странах – все, кто нуждается. Кстати, в названных странах сегодня продолжительность жизни составляет 78 лет, показатель которого должна достичь РФ к 2024 г.
2. Различия в лекарственном обеспечении в разных субъектах РФ, связанные с отсутствием единых подходов в формировании перечней ЖНВЛП и ценовой политики, в ряде случаев имеет место нерациональное применение лекарств. Все это вызывает недовольство населения. Так, среди опрошенных ВЦИОМ доля граждан, которые не смогли купить необходимое лекарство из-за высокой цены, с 2013 по 2017 г. увеличилась на 20% (с 39 до 47%), также растет число обращений граждан на «горячую линию» Росздравнадзора по поводу доступности ЛП.
При формировании стратегических документов предварительно необходимо определить значения макроиндикаторов и оценить объемы необходимых ресурсов для достижения поставленных целей. В части 3, проведена оценка потребностей в необходимых объемах финансирования лекарственного обеспечения в амбулаторных условиях на ближайшие 2–5 лет и показателей по разработке новых лекарств в РФ на перспективу 10 лет.
1 Улумбекова Г.Э., Калашникова А.В. Подходы к формированию концепции национальной лекарственной политики. Часть 1. Анализ рынка лекарственных препаратов в РФ // ОРГЗДРАВ: новости, мнения, обучение. Вестник ВШОУЗ. 2018. Т. 4, № 4. С. 53–75.
Источник

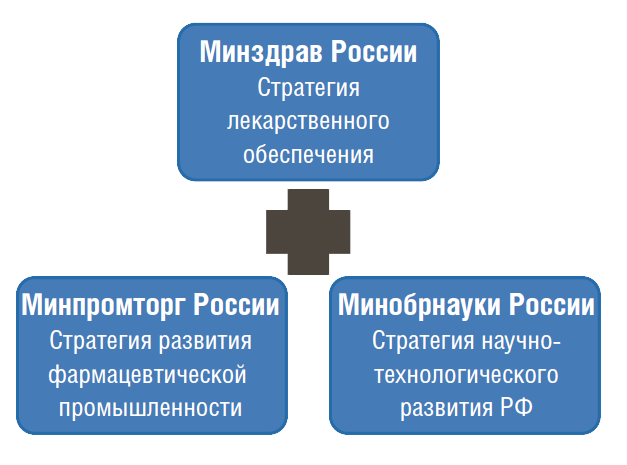 Национальная лекарственная политика на стыке отраслевых стратегий и программ
Национальная лекарственная политика на стыке отраслевых стратегий и программ

