Профилактика возникновения плесени и методы борьбы с плесенью
Плесень сопровождала человечество на протяжении всего его существования, представляя собой почти невидимого, но страшного врага. И всегда человек находился в поисках эффективного метода борьбы с ней. Существует мнение специалистов, сводящееся к тому, что планету Земля постигнет глобальная катастрофа и все животное погибнет, плесень останется живой и невредимой.
Плесень не настолько безобидна, чтобы закрывать глаза на её возникновение в ванной комнате или на зелёный налет, появившийся на стенах подвала, там где хранятся продукты впрок. Существуют так называемые болезни от плесени. Или болезни, которые она спровоцировала. Именно плесень является источником болезней верхних дыхательных путей, аллергии, в некоторых случаях плесень представляет собой причину заболеваний других внутренних органов человека. Особенно опасны споры плесени для детей и младенцев.
Очень маленькие, невидимые невооруженному глазу человека споры плесени есть везде, в домах, в воздухе. Попадая в организм человека, они вызывают такие болезни от плесени, как разного вида аллергии и микозы. У маленьких детей часто причиной диатеза являются именно споры плесени. И в том случае, если иммунитет человека ослаблен (например в случае ВИЧ-инфекции) болезнь, спровоцированная плесенью, заканчивается летальным исходом. Самой смертельно-опасной и распространенной болезнью на сегодняшний день считается аспергиллез-заболевание, спровоцированное плесенью рода Аспергилус.
Иммунологи из Америки пришли к выводу, что в организме человека существует первичная иммунная система, сформированная благодаря особым формам плесневых микрогрибов. Они очень чувствительны к изменениям в организме человека происходящим в зависимости от того, какие именно эмоции в данный момент его наполняют. Такие чувства, как ненависть, страх, злость, раздражение, апатия и депрессия провоцируют изменения микрогрибов, из-за которых и возникают такие страшные и неизлечимые болезни от плесени, как рак и туберкулез.
Несмотря на то, что именно благодаря плесени, из которой делают пенициллин, человечество нашло лекарство от пневмонии, болезни распространяются вместе с самой плесенью в геометрической прогрессии и представляют собой большую опасность для здоровья и даже жизни человека. Плесень вездесуща даже в совершенно чистой комнате в каждом кубометре воздуха при исследовании можно обнаружить до 500 спор. Крупные споры нередко вызывают аллергию, а небольшие- болезни легких.
Плесень— это гриб. Обязательно нужно проводить борьбу с ней, а если плесень ещё не видна- профилактику плесени.
Причины возникновения плесени!
1) Трещины в стенах дома, вокруг оконных коробок, под подоконником способствуют проникновению влаги с улицы, промерзанию стен, а следовательно, образованию конденсата внутри помещения.
2) Нарушение герметичности кровли, панельных стыков – ведет к тем же проблемам, что были описаны выше.
3) Но главная причина – не работает вентиляция в квартире, а значит, вся влажность остается в нем, скапливаясь в местах, где возникли перечисленные выше проблемы.
4) Повышенная влажность.
Сырые помещения больше других подвержены появлению плесени, поскольку повышенное содержание влаги в воздухе является самым благоприятным фактором для закрепления на стенах, обоях и потолке спор грибов, а также для их дальнейшего стремительного размножения.
5) Отсутствие сквозняков, слишком редкие проветривания.
Плесень почти всегда можно встретить в затхлых, душных помещениях, в которые очень редко попадает свежий воздух. В качестве примера можно привести однокомнатные торцевые квартиры, в которых очень сложно организовать качественное проветривание.
6) Постоянная повышенная температура воздуха.
Помимо влажности и отсутствия ветерка, эти простейшие грибы очень уважают тепло. Поэтому в постоянно обогреваемых и мало проветриваемых помещениях плесень встречается почти в 100% случаев.
7) Обилие тропических комнатных растений в квартире.
Как правило, такие растения очень требовательны к теплу и повышенной влажности, поэтому хозяева опрыскивают их достаточно часто для того, чтобы на стенах появился грибок.
8) Самые верхние и самые нижние этажи зданий.
Как показывает наш многолетний опыт, появлению грибка особенно подвержены квартиры на первых и последних этажах многоэтажных домов. Это объясняется тем, что под первым этажом расположен часто затапливаемый подвал – постоянный источник сырости, а в квартиру на последнем этаже влага попадает с крыши, особенно если она находится в плачевном состоянии.
9) Чрезмерное использование увлажнителя воздуха.
Несмотря на то, что увлажнитель помогает избавиться от излишней сухости воздуха, связанной с работой отопительных приборов, одновременно он же становится причиной избыточной влажности. Результат очевиден – создается идеальная среда для появления плесени.
Ни в коем случае нельзя употреблять в пищу продукты, на которых Вы заметили плесень. Нельзя просто срезать ее ( с хлеба), нельзя есть варенье с плесенью, т.к. продукты заражены плесенью.
Эффективным методом с Аспергилус Нигер или попросту чёрной плесени, по результатам исследований российских учёных, является обработка мест пораженных плесенью эфирным маслом монарды.
Профилактика плесени— это не устранение её, а предотвращение её появления.
Антисептическая обработка стен комнат, регулярное проветривание квартиры или дома (причем, не приоткрыв для этого форточку), а раскрыв настежь все окна и двери), гидроизоляция всего помещения, т.к. именно влажность – самая благоприятная среда для образования плесени, а значит и болезней от плесени. Использование именно тех кондиционеров, которые имеют фильтры с фунгицидной «пропиткой», применение очистителей воздуха с нера-фильтрами- прекрасная профилактика плесени и гарантия отсутствия возникновения болезней от плесени.
Для того, чтобы у Вас не возникало болезней от плесени, достаточно избегать плохо проветриваемых и сырых помещений- погребов, чердаков и подвалов. Ни в коем случае нельзя жить в квартире, где есть плесень. Нужно предварительно избавиться от плесени и только потом заселяться в квартиру или дом. Нельзя допускать даже небольшого протекания воды из крана- это повышает влажность- идеальную среду для размножения плесени.
Следует регулярно протирать влажные места на стенах дома или квартиры сухой тряпкой, внимательно следить за землей в цветочных горшках-идеальной средой обитания плесени. Отопление дома, квартиры должно быть высококачественным и постоянным, нельзя выключать отопление даже ночью, активизация роста плесени происходит именно тогда, когда дом или квартира начинают остывать. Нельзя прятать в шкаф влажную, плохо просушенную одежду, это провоцирует появление плесени. Все эти меры борьбы с плесенью являются эффективными методами и способны оградить Вас от болезней.
Помимо того, что плесень портит ремонт и делает квартиру неухоженной, её присутствие в жилом помещении чрезвычайно опасно для здоровья человека. Перечень заболеваний, вызванных плесенью, такие как конъюнктивит, кожный зуд, высыпания, аллергический ринит, стоматит, синусит, ларингит, мигрень, трахеит, отит, бронхит, насморк и ринит, сердечно-сосудистые заболевания, бронхиальная астма, пневмония, микотоксикоз, вызывать головные боли, желудочно-кишечные расстройства, носовые кровотечения, плесневые поражения внутренних органов (преимущественно у людей со сниженным иммунитетом), ослабление иммунитета, также являются болезнями, первопричиной которых стала плесень.
Если никаких мер по уничтожению плесневого грибка не принимается, возможны: серьезное поражение почек, печени, внутренние кровотечения, эмфизема легких.
Самой опасной для жизни человека является жёлтая плесень, поражающая как правило, такие продукты, как рыба, молоко, рис, ливер, земляные орехи. Продукты немедленно надо уничтожать. При попадании плесневых спор так называемой жёлтой плесени (самой опасной для жизни и здоровья человека, вырабатывающей такой яд, как афлатоксин) в желудочно-кишечный тракт, смертельно развивается пищевая аллергия.
Наиболее подверженный плесени является строительный материал-дерево. Борьба с плесенью в домах и квартирах- это биоцидная защита и обработка строительных материалов.
Как же избавиться от плесени навсегда?
Шаг 1. Намочите стены водой и удалите гребок скребком или щеткой, т.е. насколько это возможно соскоблите с потолка, стен, оконных откосов, шкафов. Обои, краску и штукатурку тоже следует снять. Советуем делать это в очках и маске, чтобы не заболеть.
Шаг 2. Очищенные от плесени поверхности просушите.
Шаг 3. Если нарушена теплоизоляция стен, крыши проведите ремонт и утепление. Трещин быть не должно. Если вы этого не сделаете, плесень появится снова. Мы рекомендуем для решения проблем теплоизоляции навсегда — жидкую керамическую теплоизоляцию «БРОНЯ». Почему «БРОНЯ»? Это очень качественное и долговечное теплоизоляционное покрытие.
Вам достаточно обработать только проблемный участок, т.к. достаточно толщины в 3 мм. Все стены помещения, или всю крышу обрабатывать не потребуется, хотя наша практика показывает, что заказав одну банку на небольшую поверхность, клиенты берут потом на весь дом. Вы можете выбрать как слабогорючую, так и негорючую модификацию.
Шаг 4. Подберите антисептическое средство для удаления грибка. Советуем отдать предпочтения химикатам, а не народным средствам. К наиболее популярным средствам относятся: Дали (Dali), Фонгифлюид альпа (Alpa) — активный фунгицид, OLIMP. Стоп-плесень, биоантисептик Биатол-спрей, Mavix-bio + кремнийорганический гидрофобизатор ВВМ-М 7 АС . Выбор зависит от того, какие помещения и поверхности вы будете обрабатывать, от степени их пораженности грибком и ваших финансовых возможностях. Отзывы о них хорошие. Почитайте, узнаете особенности. Советуем выбрать средство, которое можно нанести с помощью распылителя. Заранее подберите себе и средства индивидуальной защиты, в которых будете проводить обработку. Специалисты делают это в маске и специальном костюме. ВНИМАНИЕ! Эта стадия обязательна, т.к. плесень не удаляется водой. Ее споры остаются.
Шаг 5. Проведите антисептическую обработку, согласно инструкциям производителя. Если потребуется, сделайте это несколько раз, пока грибок со стены, потолка или окна не исчезнет совсем. Всем членам семьи, домашним животным советуем на это время квартиру покинуть. Вам после окончания работ тоже следует выйти на свежий воздух.
Шаг 6. Проведите гидроизоляцию стен. Мы рекомендуем жидкую теплоизоляцию «Броня«, которая навсегда «похоронит»плесень за своим сверхтонким слоем. Грибок не будет больше представлять опасности. Наносится как краска, действует как тепловой барьер. Мы рекомендуем выбрать модификацию «БРОНЯ Стена» или «БРОНЯ Лайт».
Шаг 7. Перед тем как проводить окончательный ремонт, установите приточные клапаны. Тогда ваша вытяжная вентиляция начнет работать, влажность будет уходить, и все ваши труды и деньги не пропадут. Если вы удалите плесень, а вопрос с неработающей вентиляцией не решите, то повторное появление грибка на стенах — вопрос времени.
В соответствии с требованиями СанПиН 2.1.2.2645-10 «Санитарно-эпидемиологические требования к условиям проживания в жилых зданиях и помещениях» не регламентируется содержание плесени в жилых помещениях, в связи с чем ФБУЗ «Центр гигиены и эпидемиологии в Республике Мордовия» провести исследования воздуха на наличие плесневого грибка в квартире жилого дома не представляется возможным.
ФБУЗ «Центр гигиены и эпидемиологии в Республике Мордовия» аккредитован на проведение инструментальных замеров параметров микроклимата в жилых помещениях, сделав акцент на исследование относительной влажности воздуха в помещениях.
Источник
КАНДИДОЗ ПИЩЕВОДА
Кандидоз — инфекционное заболевание слизистых оболочек, кожи и внутренних органов, вызванное дрожжеподобными грибами рода Candida . Кандидоз пищевода (КП), являющийся проявлением висцерального кандидоза, занимает видное место среди инфекционных поражени
Кандидоз — инфекционное заболевание слизистых оболочек, кожи и внутренних органов, вызванное дрожжеподобными грибами рода Candida. Кандидоз пищевода (КП), являющийся проявлением висцерального кандидоза, занимает видное место среди инфекционных поражений пищевода. В последние годы прослеживается тенденция нарастания частоты КП, особенно у пациентов с нарушением иммунитета. Рост кандидозной инфекции в значительной степени обусловлен увеличением количества больных с ВИЧ-инфекцией, успехами в трансплантологии и иммуносупрессивной терапии, бесконтрольным использованием антибиотиков. КП встречается у 0,7-1,5% больных гастроэнтерологического профиля [5, 6].
Проблема тяжелых грибковых инфекций, вызываемых оппортунистическими патогенами, состоит в том, что они трудно поддаются лечению и могут приводить к летальному исходу. Было обнаружено, что смертность при инвазивных кандидозных инфекциях составляет 34% [16].
Этиопатогенез. Различные виды Candida представляют собой наиболее часто встречающийся пищеводный патоген, прежде всего это касается Candida albicans, иногда встречаются C. tropicalis, C. parapsilosis, C. glabrata, C. lusitania и C. krusei. Эти микроорганизмы являются нормальными компонентами оральной флоры, и их рост сдерживается бактериальными комменсалами. Заражение грибами типа Candida, которые широко распространены в окружающей среде, происходит эндогенным или экзогенным путем. Эндогенное заражение связано с активированием грибов-сапрофитов; экзогенное инфицирование может произойти при прямом контакте с носителями инфекции или из окружающей среды. Если организм хозяина не ослаблен, многие грибы не проявляют своих патогенных свойств. Исследования последних лет показали, что источником диссеминации грибов служит кишечник, а кандидоз полости рта, гениталий, пищевода является проявлением системного кандидоза. Вероятность развития системного поражения зависит как от свойств самого микроорганизма (их количества, вирулентности, генетической и видовой неоднородности популяции), так и от состояния макроорганизма, особенно его иммунной системы, алиментарного статуса и абдоминального кровотока [3, 17].
Благоприятные условия для развития инфекционного процесса создают различные нарушения физиологических, анатомических и иммунологических механизмов защиты организма. В качестве факторов, провоцирующих возникновение эзофагеального кандидоза, можно назвать использование антибиотиков, ингаляционных или инъекционных кортикостероидов, антацидную терапию или гипохлоргидрическое состояние, сахарный диабет, алкоголизм, последствия интоксикации, недоедание, пожилой возраст, нарушение моторики пищевода или пищеводную обструкцию, трансплантацию органов и костного мозга, энтеральное и особенно парентеральное питание и др. Ослабление иммунной системы может привести к возникновению кандидозной инфекции. При сахарном диабете повышенный уровень глюкозы в крови способствует росту грибов, так как гипергликемия ослабляет функцию гранулоцитов. Гипофункция паращитовидных желез и надпочечников приводит к нарушению кальциево-фосфорного обмена, что вызывает скрытую спазмофилию пищевода, тем самым снижая его местные защитные возможности [9]. Нарушения нутритивного статуса из-за недостатка белка в организме и низкой калорийности пищи влияют на состояние иммунной системы и создают предпосылки для развития кандидоза [3]. К факторам риска заболевания кандидозом относится снижение кислотности желудочного сока (рН 7,4 является оптимальной для роста грибов Candida, а при сдвиге рН до 4,5 рост грибов полностью угнетается) [3, 4, 7].
Патологические проявления КП разнообразны. Сначала пораженные участки пищевода имеют вид отдельных беловатых или желтоватых очажков, приподнятых над слизистой оболочкой. Позднее эти очажки могут сливаться, образуя плотные налеты с внедрением гриба в подслизистую оболочку или псевдомембранозные наложения с проникновением гриба в мышечную оболочку и сосуды [9]. Пленки, образующиеся на слизистой пищевода в особенно тяжелых случаях, могут почти полностью закрывать просвет пищевода. Налет состоит из слущенных эпителиальных клеток, которые смешиваются с грибками, клетками воспаления и бактериями. Микроскопическое исследование позволяет выявить равномерно окрашенные дрожжеподобные клетки и нити мицелия грибов Candida [9]. Истинное язвообразование наблюдается нечасто и в большинстве случаев отмечается у иммуносупрессированных больных с гранулоцитопенией [29]. Иногда возникает некроз стенки пищевода и развивается флегмонозное воспаление пищевода и средостения, что может стать одной из причин смерти больного [1].
Существует морфологическая классификация, согласно которой все случаи КП подразделяются на три группы в зависимости от степени тяжести процесса, то есть в зависимости от глубины поражения его стенки: 1-я группа — отдельные беловатые налеты с внедрением псевдомицелия гриба между эпителиальными клетками; 2-я группа — пленчатые налеты, сливающиеся между собой и образующие обширные поля, при этом нити псевдомицелия прорастают не только слизистую, но и подслизистую оболочку; 3-я группа — псевдомембранозные наложения, сочетающиеся с глубокими изменениями, при которых нити гриба глубоко проникают в толщу мышечной ткани [10].
Клинические проявления и осложнения. Симптомы заболевания практически отсутствуют у 25-30% пациентов, страдающих КП, особенно у иммунокомпетентных лиц. Тем не менее большинство пациентов предъявляют жалобы, связанные с поражением желудочно-кишечного тракта. Наиболее типичные клинические проявления КП — дисфагия и несколько реже одинофагия. Степень выраженности пищеводных симптомов колеблется от умеренного затруднения при глотании до резко выраженной боли, результатом чего являются неспособность принимать пищу и развитие вторичной дегидратации. При тяжелой одинофагии возможно наличие других причин или коинфекции, особенно у больных со СПИДом. Гораздо реже больные могут жаловаться на загрудинные боли, не связанные с глотанием, изжогу, тошноту, иногда рвоту с выделением пленок (псевдомембран), снижение аппетита и веса, появление жидкого стула со слизью (см. рисунок) [4, 9, 29].
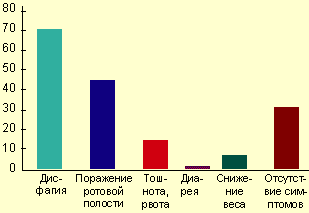 |
| Симптомы кандиозного эзофагита (R. S. Orlando, 1996) |
При КП может быть полезно физикальное исследование. Приблизительно две трети пациентов со
СПИДом и пищеводным кандидозом имеют кандидозный стоматит. КП наблюдается у больных с хроническим слизисто-кожным кандидозом, который относится к тяжелым формам кандидозной инфекции и чаще наблюдается при дисфункции надпочечников и околощитовидных желез [29].
Осложнения пищеводного кандидоза наблюдаются редко. Эзофагеальное кровотечение может наблюдаться при тяжелом течении болезни, сопровождающемся образованием эрозий, язв, и ассоциироваться с коагулопатией; возможно развитие перфорации. Описана вторичная обструкция просвета мицетомой. Редко возникает некроз с развитием флегмонозного воспаления пищевода и средостения [1]. В тяжелых случаях специфический эзофагит может осложниться развитием кандидамикозного сепсиса [6].
Диагностика. Подозрение на пищеводный кандидоз должно возникнуть у любого больного при наличии факторов риска развития пищеводной инфекции и жалоб на дисфагию и одинофагию. Наличие кандидозного стоматита подтверждает этот диагноз, но при его отсутствии поражение пищевода также не исключается.
Рентгенография пищевода с использованием бария обычно применяется для начальной оценки перед проведением эндоскопии. Однако на ранних стадиях кандидозного эзофагита рентгенологическое исследование пищевода не имеет большого диагностического значения, так как оно отражает лишь неспецифические изменения, общие для всех эзофагитов [2]. Классическими рентгенологическими признаками острого эзофагита, вызванного Candida spp., являются линейные или неправильной формы дефекты наполнения с четкими краями. При тяжелом течении кандидозного эзофагита происходит слияние повреждений, из-за чего большие дефекты наполнения иногда образуют скопления в виде гроздьев винограда [2]. Пищевод при этом приобретает «косматый» («ворсистый») вид, симулируя ульцерацию [25]. Наличие больших, хорошо очерченных язв не является признаком кандидозного эзофагита. Могут наблюдаться нарушение моторики и сужение просвета пищевода за счет псевдомембран. Следует помнить о том, что нормальная рентгенограмма пищевода с использованием бария не исключает пищеводного кандидоза. Из-за тяжелой одинофагии больной не сможет выпить барий, что затрудняет рентгеногрфию пищевода [29].
Более информативным для диагностики кандидозного эзофагита считается рентгенологический метод двойного контрастирования, эффективность которого достигает 70% [26].
Цитологическая щетка и баллонный катетер используются для быстрой диагностики пищеводных инфекций без эндоскопии. Эти инструменты могут быть легко введены через носовые ходы или рот сквозь защитный зонд, который предотвращает контаминацию. Материал, полученный на защищенной щетке или баллонном катетере после того, как они будут изъяты из пищевода, оценивается цитологически и культурально. Методика с использованием защищенных щеток имеет чувствительность 88% и специфичность почти 100% [26].
Цитологический метод предполагает окраску мазков-отпечатков или осадка смыва с цитологической щетки в поисках активных форм Candida — почкующихся дрожжевых клеток, псевдомицелия и мицелия. Культуральный метод предполагает помещение исследуемого материала на обогащенную глюкозой среду Сабуро или другие среды, чтобы затем по характеру образующихся колоний судить об этиологии инфекционного процесса в пищеводе.
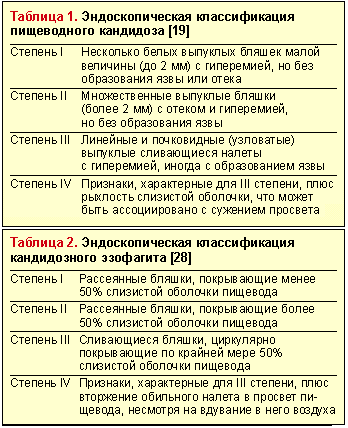
Эндоскопическое исследование пищевода — наиболее чувствительный и специфический метод диагностики пищеводного кандидоза. Эндоскопическая картина КП характеризуется чаще всего наличием легко снимающихся фибринозных рыхлых наложений белого или желтого цвета, под которыми обнаруживается легкоранимая и/или отечная слизистая. Реже наблюдаются катаральный и эрозивно-язвенный эзофагит [19]. Candida spp. редко вызывает истинное язвообразование. Наличие язвы при кандидозном эзофагите нередко служит признаком дополнительного патологического процесса в пищеводе [29]. Существуют различные эндоскопические классификации пищеводного кандидоза (табл. 1 и 2).
В ходе эндоскопии пораженные участки слизистой могут быть подвергнуты щеточной биопсии для цитологического исследования или биопсии для гистологической диагностики. Когда эндоскопически идентифицируются язвы, многократное проведение биопсии помогает исключить наличие сосуществующих патологических процессов. Цитологическое исследование материала, полученного с помощью браш-биопсии, имеет более высокую ступень чувствительности, чем гистологическое исследование образцов биопсии при умеренном поверхностном кандидозе, потому что микроорганизмы могут быть вымыты с поверхности ткани при обработке биопсийного материала [19]. В редких случаях позитивная цитология при наличии отрицательной гистологии указывает на то, что речь идет скорее о колонизации, чем об инфекции. При более тяжелом кандидозном поражении пищевода наибольшее диагностическое значение имеет гистологическое исследование биоптатов слизистой с использованием специальной окраски на нейтральные мукополисахариды по Шиффу PAS (ШИК-реакция) или по Gomori гексаметилентетрамином серебра. Только гистологическое исследование демонстрирует инвазию мицелия или псевдомицелия гриба в глубь ткани пищевода.
Кожное тестирование и серологические тесты малоинформативны для диагностики пищеводного кандидоза.
Лечение. Существует множество пероральных и внутривенных медикаментов, которые используются для лечения кандидозного эзофагита. Несмотря на относительно широкий выбор препаратов, лечение КП является актуальной проблемой, так как некоторые лекарственные средства недостаточно эффективны, другие имеют серьезные побочные эффекты; кроме того, в настоящее время отмечается рост резистентности к антигрибковым препаратам.
При лечении КП первоначально должна быть назначена пероральная терапия, внутривенное введение используется лишь в случае рефрактерного течения заболевания или если имеются противопоказания к пероральному использованию медикаментов. Больным с умеренной степенью тяжести заболевания и минимальным нарушением иммунитета необходим сокращенный курс терапии с использованием системных абсорбируемых лекарственных препаратов типа орального азола. Иммунокомпрометированных больных после трансплантации и больных СПИДом с КП лучше лечить более длинными курсами азола. У пациентов с гранулоцитопенией, когда имеется существенный риск диссеминации Candida инфекции, оправданно использование внутривенных препаратов системного действия (азолов, амфотерицина B) [29].
Арсенал современных противогрибковых средств достаточно широк. Для лечения пищеводного кандидоза используют антигрибковые препараты нескольких групп. Наиболее эффективны препараты из группы азола. Перорально используют невсасывающиеся азолы (клотримазол, миконазол); однако более эффективны препараты системного действия из этой группы (кетоконазол, флуконазол и итраконазол). Эти препараты, подобно другим из группы азола, изменяют проницаемость клеточной мембраны грибов посредством цитохром P450 (CYP)-зависимого вмешательства в биосинтез эргостерола, что приводит к повреждению грибной клетки и ее смерти. Новые триазолы (итраконазол и флуконазол) имеют большее аффинное подобие, чем имидазолы (миконазол и кетоконазол) для грибных CYP-энзимов [14]. Хотя другие средства, такие, как миконазол, клотримазол и нистатин, могут быть использованы для лечения кандидозного стоматита, а также для профилактики пищеводного поражения, эти лекарственные средства менее эффективны в качестве основной группы препаратов для терапии КП [24].
Клотримазол и миконазол — препараты имидазолового ряда. В настоящее время выпускаются клотримазол в таблетках и миконазол для перорального применения. Однако они не всасываются в желудочно-кишечном тракте. Эти препараты могут использоваться при легком кандидозном поражении пищевода у лиц без иммунодефицита.
Кетоконазол (низорал, ороназол) является производным имидазола и при ежедневном приеме в дозе от 200 до 400 мг дает хороший эффект в лечении пищеводного кандидоза. У больных СПИДом, которым обычно требуются более высокие дозы кетоконазола, дневная доза может быть увеличена, если не возникает тошноты, до максимальной (800 мг). Кетоконазол хорошо проникает в различные органы и ткани, но плохо — через гематоэнцефалический барьер. Препарат хорошо всасывается в желудочно-кишечном тракте, но для оптимального всасывания требуется кислая среда. При желудочной гипохлоргидрии и использовании антацидных средств его биодоступность уменьшается. Для улучшения всасывания кетоконазол следует принимать за 2 часа до приема противоязвенных препаратов. Приблизительно у 10-25% больных СПИДом наблюдается снижение желудочной кислотной секреции. Кетоконазол же может вызвать временную блокаду синтеза тестостерона и кортизола [6, 8, 29].
Итраконазол (споранокс) относится к группе триазолов, подобно кетоконазолу, назначается в дозе 200 мг в день. Дальнейшее увеличение дозы удлиняет период полураспада препарата и повышает его эффективность. Всасывание интраконазола уменьшается при снижении pH желудочного сока [23]. Кетоконазол и итраконазол метаболизируются в печени и выделяются с желчью. Период полураспада этих двух препаратов составляет от 7 до 10 часов и от 24 до 42 часов соответственно [14]. Коррекции дозы у больных с почечной недостаточностью не требуется.
Флуконазол (дифлюкан, дифлазон, форкан, флюкостат — отечественный флуконазол) представляет собой водорастворимый триазол и назначается в дозе 100 мг в день. Флуконазол — это препарат, всасывание которого не зависит от pH желудочного сока и который значительно более эффективен при лечении пищеводного кандидоза при СПИДе, чем кетоконазол (200 мг ежедневно) [21]. Флуконазол доступен для перорального и внутривенного применения. Он минимально метаболизируется и выделяется неизмененным с мочой. Флуконазол отличается высоким тканевым тропизмом и не влияет на синтез андрогенов, хорошо проникает через гематоэнцефалический барьер. В отличие от кетоконазола и интраконазола он хорошо растворим в воде и минимально связывается белком. Препарат обладает длительным периодом полураспада (приблизительно 30 часов, если не нарушена функция почек, а наличие пищи или гипохлоргидрия не изменяют всасывание), что позволяет принимать его один раз в сутки. Показано, что введение флуконазола улучшает иммунные показатели по Т- и В-системам [18]. И флуконазол, и итраконазол можно принимать перорально в виде растворов. Эти формы могут быть более эффективны, чем таблетки, потому как усиливают локальный эффект и улучшают всасывание.
Неблагоприятные воздействия кетоконазола, флуконазола и итраконазола прежде всего зависят от дозировки и проявляются в виде тошноты, гепатотоксичности, замедления продукции стероидов и метаболизма циклоспорина [14]. В редких случаях кетоконазол может вызывать фатальный гепатит [12]. Незначительное увеличение аминотрансфераз — общий побочный эффект для всех трех препаратов, однако это не должно служить оправданием для их отмены. Влияние на стероидогенез наиболее выражено у кетоконазола. Обратимое замедление гонадального и надпочечного синтеза стероидов под воздействием кетоконазола может наблюдаться, когда доза превышает 400 мг в сутки [27]. В рекомендуемых дозах флуконазол и итраконазол не влияют на стероидогенез. В результате воздействия на печеночные микросомальные ферменты все три азола ингибируют метаболизм циклоспорина, что приводит к увеличению уровня циклоспорина в крови; этот эффект наиболее ярко выражен у кетоконазола [14].
Другая основная группа противогрибковых средств — антибиотики полиены, представленные амфотерицином и нистатином. Эти препараты необратимо связываются со стеролами в грибковых клеточных мембранах, тем самым изменяя свойства проницаемости мембраны, нарушая ее барьерную функцию и вызывая клеточную смерть. Нистатин (антикандин, микостатин, фунгицидин) практически не всасывается в желудочно-кишечном тракте. Он используется для лечения кандидозного стоматита, но менее эффективен при поражении пищевода. Кроме того, эффективность, безопасность и легкость применения производных азола позволяют рассматривать нистатин в качестве средства терапии второго ряда. Амфотерицин В (амфостат, фунгизон) — единственный полиеновый антибиотик для парентерального введения. Он не всасывается в желудочно-кишечном тракте, применяется внутривенно капельно, хорошо проникает в различные органы и ткани, выделяется из организма почками. Период полувыведения составляет 24-48 часов, однако при систематическом применении может возрастать до 15 дней вследствие кумуляции в тканях [8]. Хотя амфотерицин B является наиболее эффективным препаратом, использующимся для лечения системных микозов, но из-за серьезных побочных эффектов его применение в лечении КП ограничено. Среди побочных эффектов амфотерицина можно выделить нейротоксичность, гематоксичность, нефротоксичность, местно-раздражающее действие (флебиты), аллергические реакции, диспептические расстройства, лихорадку и др. [8]. Наиболее неблагоприятным побочным эффектом, возникающим вследствие длительного использования амфотерицина, является нефротоксичность, которая обычно обратима. Этот препарат теперь доступен в виде раствора для перорального применения и пастилок. У больных с КП, которые резистентны к лечению флуконазолом или другими азолами, эффективными могут быть низкие дозы амфотерицина B, вводимого внутривенно (от 10 до 20 мг в день). Общая доза препарата для лечения пищеводного кандидоза составляет от 100 до 200 мг [29].
Флуцитозин — препарат с узким спектром противогрибковой активности, который действует благодаря вмешательству в трансляцию РНК. Он включается в клетки гриба, где превращается в 5-фторурацил и ингибирует тимидилат-синтетазу. Этот пероральный препарат, который назначается в дозе от 50 до 150 мг/кг в день каждые 6 часов, может быть использован в комбинации с амфотерицином B, но он не должен применяться в качестве монотерапии, потому что грибы быстро становятся к нему резистентными. Кроме того, монотерапия флуцитозином оказывается лишь умеренно эффективной [12].
Новейшим классом противогрибковых препаратов являются кандины, вмешивающиеся в синтез грибковой стенки. Они эффективны в отношении большинства видов Candida, в том числе C. krusei. Первые исследования показали, что капсофунгин, представляющий эту группу препаратов, оказался столь же эффективен при КП, как и амфотерицин В [16].
При лечении больных КП следует учитывать наличие резистентности, которая из-за широкого применения азолов в настоящее время значительно возросла. При развитии резистентности часто бывает полезно увеличить дозу азола. Если этого оказывается недостаточно, переходят на другой препарат из этой группы или используют пероральный раствор итраконазола [13], который нужно назначать в более высоких дозах из-за часто наблюдающейся перекрестной резистентности. Когда высокой дозы (то есть 400 мг ежедневно) флуконазола недостаточно, переходят на внутривенное введение амфотерицина B, при этом результат достигается в 90% случаев. Резистентность к амфотерицину наблюдается редко [29].
В табл. 3 представлено лечение кандидозного эзофагита в зависимости от функции лимфоцитов и гранулоцитов.
При лечении кандидозного эзофагита у больных СПИДом препаратами первого ряда являются кетоконазол и флюконазол, причем предпочтение следует отдавать флюконазолу. Из-за лучшей переносимости он прежде всего показан пациентам, находящимся на поздней стадии болезни, которые имеют много сопутствующих заболеваний. При нарушении глотания могут применяться парентеральные формы флуконазола. При неэффективности препаратов первого ряда используют лекарственные средства из группы резерва (амфотерицин В, итраконазол), которые более токсичные и/или более дорогие. Этиотропная терапия кандидоза пищевода, кроме основного курса лечения, требует проведения поддерживающего лечения, которое может быть пожизненным (табл. 4) [4].
Лечение кандидоза на фоне тяжелого иммунодефицита и лейкопении — задача сложная. Наряду с антигрибковой терапией актуально восстановление пула нейтрофильных лейкоцитов и их функциональной активности, так как нейтрофильные лейкоциты являются одним из основных звеньев механизма защиты от Candida spp. Предлагается в качестве дополнительного средства при лечении кандидозной инфекции на фоне нейтропении использовать гранулоцитарный колониестимулирующий фактор, который сокращает дефицит миелопероксидазы в нейтрофильных лейкоцитах и усиливает их кислородозависимую антикандидозную активность [7]. Получен хороший эффект от эндоскопического введения больным КП концентрата гранулоцитов и высокоинтенсивного импульсного лазерного излучения, что улучшает иммунные функции [5].
Таким образом, для достижения успеха у больных с тяжелыми грибковыми инфекциями, в том числе с кандидозом, целесообразен комплексный подход к диагностике и лечению. Повышению выживаемости будет способствовать оперативная диагностика с последующими подбором эффективной специфической противогрибковой терапии и проведением лечебных мероприятий, направленных на повышение числа гранулоцитов и стимуляцию фагоцитоза [16].
По вопросам литературы обращайтесь в редакцию
Источник