- Эндоскопическое бужирование
- Показания для выполнения бужирования
- Процедура бужирования
- Продолжительность и периодичность лечения
- Наши результаты
- Возможные осложнения
- Подготовка к процедуре
- Рак пищевода
- Филиалы и отделения где лечат рак пищевода
- Рак пищевода
- Статистика (эпидемиология)
- Морфологическая классификация рака пищевода
- Стадии и симптоматика рака пищевода
- Причины возникновения рака пищевода и факторы риска
- Диагностика рака пищевода
- Лечение рака пищевода
- Осложнения противоопухолевого лечения рака пищевода и их коррекция
- Использование уникальных методик/ Новые методы лечения рака пищевода :
- Клинические исследования рака пищевода
- Особенности реабилитации после лечения рака пищевода
- Филиалы и отделения Центра, в которых лечат рак пищевода
Эндоскопическое бужирование
Эндоскопическое бужирование – методика расширения просвета полого органа или анастомоза с целью восстановления его проходимости. Эта манипуляция относится к категории лечебных эндоскопических процедур и осуществляется с помощью специальных инструментов – бужей.
Показания для выполнения бужирования
- Рубцовое сужение пищевода II-IV степени как следствие случайного или умышленного приема агрессивных химических веществ, пептического эзофагита, микотического поражения пищевода, проведенной ранее лучевой терапии, склерозирования варикозно расширенных вен пищевода (при этом диаметр просвета пищевода составляет менее 11 мм).
- Стриктуры пищеводных анастомозов (эзофагогастро-, эзофагоэнтероанастомозов). Пациентам выполняется бужирование на любых сроках формирования стриктуры, но не ранее чем 10 дней после оперативного вмешательства.
- Рубцовые сужения анального канала, прямой кишки или дистальных отделов сигмовидной кишки после перенесенных воспалительных заболеваний (парапроктит, болезнь Крона), оперативных вмешательств (геморроидэктомии), лучевой терапии.
- Стриктуры низкорасположенных межкишечных анастомозов (после операции низкой передней резекции прямой кишки, резекции сигмовидной кишки).
На отделении эндоскопии НИИ онкологии бужирование пищевода применяется и в лечении опухолевых стенозов пищевода, однако не является окончательным методом лечения, а решает задачу кратковременного расширения просвета пищевода в месте циркулярно распространяющейся опухоли перед проведением брахитерапии, установкой самораскрывающегося стента (если диаметр зонда для брахитерапии или доставочного устройства стента превышает диаметр просвета органа).
Процедура бужирования
На отделении эндоскопии НИИ онкологии им. Н.Н.Петрова применяется методика бужирования стриктур по направляющей струне без использования рентгенологической установки.
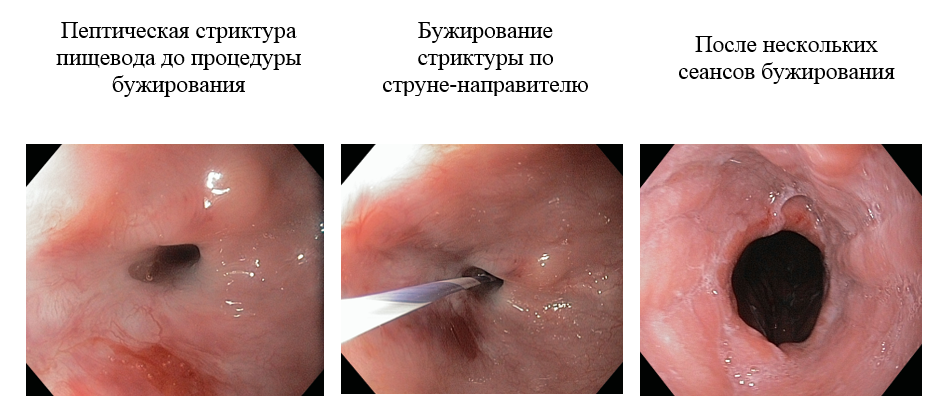
Она заключается в установке гибкой или более ригидной металлической струны по биопсийному каналу эндоскопа за область сужения с последующим проведением по проводнику, как по направителю, пластиковых бужей разного диаметра, начиная от наименьшего. Для процедуры бужирования мы применяем бужи типа Savary с конусообразным дистальным концом и внутренним каналом на всем протяжении бужа.
Эта методика имеет целый ряд преимуществ перед аналогичными вмешательствами, выполняемыми под рентгенологическим контролем. Во-первых, она позволяет выполнять бужирование преимущественно амбулаторно из-за минимальной опасности возникновения осложнений. Во-вторых, наличие проводника позволяет успешно бужировать даже сложные, протяженные стриктуры с извитым ходом, а также стриктуры с эксцентричным расположением входа. В-третьих, полностью отсутствует лучевая нагрузка на больного и врача
Специалист выполняет исследование используя эндоскоп небольшого диаметра. Во время исследования оценивается локализация верхнего края сужения, диаметр суженного участка и его протяженность (по возможности).
Важной задачей для специалиста является проведение эндоскопа через сужение, т.к. это позволит не только установить протяженность стриктуры, но и оценить её ход, направление, убедиться в отсутствии двойных или множественных сужений, свищевых ходов, дивертикулов, что позволит избежать осложнений. Если эндоскоп провести за сужение не удается, то делается попытка проведения струны вслепую, что также является безопасным для пациента, т.к. проведение струны осуществляется её мягким концом. В редких случаях струну не удается провести через сужение, что наблюдается, например, при полном рубцовом сращении, либо при выраженном изгибе и извитости участка сужения, всё это рассматривается как противопоказание для выполнения бужирования и пациенту назначается рентгенологическое исследование с водорастворимым контрастным веществом для установления причины возникших трудностей.
Бужирование начинается с проведения бужа малого диаметра, не превышающего диаметр наиболее суженного участка. Затем буж заменяют на следующий, большего диаметра. За один сеанс применяется от 2 до 3 бужей. При бужировании специалист определяет степень ригидности стриктуры по мануальным ощущениям, что позволяет ему контролировать прилагаемое усилие, ограничивая насильственное преодоление чрезмерного сопротивления рубцовых тканей, и таким образом повышает безопасность вмешательства.
Во время проведения бужирования пациент может испытывать умеренные болевые ощущения.
Продолжительность и периодичность лечения
Длительность и специфика лечения во многом зависит от индивидуальных особенностей пациента и конкретной картины заболевания. Лечение в целом состоит из основного и поддерживающего курсов и завершается динамическим наблюдением.
- Основной курс лечения для достижения просвета полого органа 14-15 мм и анастомозов 19-20 мм, включает в себе не менее 4-5 сеансов, которые проводятся с интервалом 3-4 дня.
- После окончания основного курса лечения бужирование проводится с частотой 1 раз в неделю до стабилизации результата, т.е. когда при очередном визите пациента не будет отмечено повторного сужения просвета более чем на 1-2 мм. Следующий интервал между процедурами составляет 10-14 дней и впоследствии увеличивается до 3 недель, а затем при отсутствии стенозирования – до 1 месяца. Для предупреждения повторного возникновения стеноза поддерживающее лечение обычно длительное и составляет 3-6 месяцев.
- При положительном результате поддерживающего эндоскопического лечения в дальнейшем проводится динамическое наблюдение 1 раз в год. У больных со стриктурами пищевода при необходимости выполняется бужирование 1–2 раза в год. После проведения полноценного курса поддерживающего бужирования повторное лечение при стриктурах пищеводных анастомозов, как правило, не требуется.
Наши результаты
Бужирование является высокоэффективной лечебной процедурой. Специалисты нашего отделения достигают хороших результатов в решении таких сложных задач, как:
- Восстановление самостоятельного перорального питания у пациентов с критическими стенозами пищевода и пищеводных анастомозов IV степени (просвет менее 3 мм), а также у пациентов с высокой локализацией верхнего края сужения (глоточно-пищеводный переход, шейный отдел пищевода).
- Ликвидация угрозы кишечной непроходимости без повторного оперативного вмешательства при стенозах межкишечных анастомозов, ригидных постлучевых стриктурах прямой кишки.
Возможные осложнения
Процедура бужирования, если она выполняется по проводнику, с поэтапным переходом от меньшего бужа к большему без излишнего форсирования, является наименее травматичным и наиболее безопасным методом лечения стриктур полых органов и анастомозов. В процессе выполнения процедуры обычно возникают неглубокие продольные надрывы рубцово измененной слизистой в области анастомоза или на поверхности стенки органах, и которых отмечается кратковременное незначительное подтекание крови, останавливающееся самостоятельно. Однако осложнения все же возможны, и самым серьезным считается перфорация стенки органов, для устранения которой может потребоваться оперативное вмешательство, а также кровотечение из краев глубокого разрыва слизистой, с которым почти всегда удается справиться эндоскопически.
Подготовка к процедуре
Бужирование верхних отделов желудочно-кишечного тракта проводят строго натощак, полностью исключается прием пищи за 12 часов и жидкости за 6 часов до начала процедуры. Если Вы не отмечаете выраженных затруднений при прохождении пищи по пищеводу или задержки пищевых масс в желудке на долгий срок, то последний прием пищи накануне может быть не позднее 18.00. Если вы отмечаете у себя вышеуказанные симптомы, то последний прием пищи в виде легкого обеда должен быть не позднее 13.00 в день накануне процедуры.
Процедура бужирования стриктуры толстой кишки или межкишечного анастомоза проводится только после очищения толстой кишки. Как выполнить подготовку толстой кишки см. «подготовка к колоноскопии» в разделе «колоноскопия». При низко расположенных стриктурах толстой кишки, а также в случае критических стриктур диаметром не более 4-5 мм (особенно если Вы отмечается систематическую длительную задержку отхождения стула и газов) подготовку толстой кишки следует проводить с помощью клизм.
Необходима отмена пероральных антикоагулянтов (препаратов для разжижения крови) накануне исследования, пауза п/к введения гепарина за 4-6 часов до процедуры
Баллонная дилатация стриктур желудочно-кишечного тракта может быть выполнена под внутривенной анестезией. Если исследование будет проводиться под наркозом, прием любого количества жидкости до процедуры строго воспрещен. Управление транспортным средством после окончания исследования является нежелательным и может представлять угрозу для жизни и здоровья.
Источник
Рак пищевода
Вам поставили диагноз: рак пищевода?
Наверняка Вы задаётесь вопросом: что же теперь делать?
Подобный диагноз всегда делит жизнь на «до» и «после». Все эмоциональные ресурсы пациента и его родных брошены на переживания и страх. Но именно в этот момент необходимо изменить вектор «за что» на вектор «что можно сделать».
Очень часто пациенты чувствуют себя безгранично одинокими вначале пути. Но вы должны понимать — вы не одни. Мы поможем вам справиться с болезнью и будем идти с Вами рука об руку через все этапы вашего лечения.
Предлагаем Вашему вниманию краткий, но очень подробный обзор рака пищевода.
Его подготовили высоко квалифицированные специалисты Торакоабдоминального отделения МНИОИ имени П.А. Герцена – филиала ФГБУ «НМИЦ радиологии» Минздрава России.
Филиалы и отделения где лечат рак пищевода
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отделение торакоабдоминальной хирургии
Заведующий отделения – к.м.н. Владимир Михайлович Хомяков.
Контакты: (495) 150 11 22
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отделение лучевого и хирургического лечения заболеваний абдоминальной области
Заведующий отделением — к.м.н. Леонид Олегович Петров
Контакты: (484) 399-31-30
Рак пищевода
Введение – Особенности локализации. Анатомия органа.
Пищевод представляет собой полую, мышечную трубку, по которой пищевой комок перемещается из полости рта и глотки в просвет желудка (Рис.1). Пищевод взрослого человека имеет длину 25—30 см. Является продолжением глотки, начинается в области шеи на уровне VI—VII шейного позвонка, затем проходит через грудную полость в заднем средостении (центральной части грудной полости ближе к позвоночнику) и заканчивается в брюшной полости на уровне X—XI грудных позвонков, впадая в желудок. Соответственно областям залегания в пищеводе различают: шейную, грудную и брюшную части. В зависимости от того, в каком сегменте возникла опухоль, могут развиваться соответствующие симптомы.
Стенка пищевода состоит из нескольких слоев и включает в себя: слизистую оболочку, мышечную оболочку и соединительнотканный наружный слой (адвентиция).
Рак пищевода – злокачественная опухоль, развивающаяся из клеток внутренней оболочки – слизистого слоя органа, и распространяется в толщу стенки, прорастая один слой за другим по мере роста опухоли, но также и вдоль органа. В связи с тем, что ширина просвета пищевода небольшая, рост опухоли постепенно перекрывает ее просвет, вызывая затруднение прохождения пищи по пищеводу. В зависимости от отдела, в котором появилась опухоль, выделяют рак грудного отдела (и его верхней, средней и нижней трети), шейного и абдоминального отделов пищевода.
Рисунок 1. Анатомия органа
Статистика (эпидемиология)
По результатам Global Cancer Statistics от 2012г, среди опухолей ЖКТ рак пищевода по заболеваемости занимает 1-е место и насчитывает до 16000 заболевших ежегодно, и восьмое место в мире среди причин смертности от онкологических заболеваний. Наибольшая заболеваемость отмечается в так называемом «центрально-азиатском поясе рака пищевода», включающем Каспийское побережье, центрально-азиатские республики, Монголию и северо-западный Китай. Низкая заболеваемость наблюдается в странах западной Европы, США и Австралии.
В пределах одного региона заболеваемость существенно варьирует в зависимости от национальности, расовой принадлежности, пола и социально-экономического статуса.
В Российской Федерации заболеваемость раком пищевода неуклонно растет. В 2017 году абсолютное число заболевших составило 8220 случаев, по сравнению с 2010 г. данный показатель возрос в два раза.
Мужчины заболевают в 3,5 раза чаще женщин. Пик заболеваемости приходится на возраст 50-59 лет.
Среди больных с впервые установленным диагнозом почти 70% имеют III-IV стадию заболевания.
Морфологическая классификация рака пищевода
Существуют две основные гистологические формы рака пищевода, который названы по типу клеток, которые становятся злокачественными:
- Плоскоклеточный рак пищевода — образуется в плоских клетках, являющихся тонкой выстилкой просвета пищевода. Этот рак чаще всего встречается в верхней и средней части пищевода.
- Аденокарцинома пищевода — опухоль, которая образуется в железистых (секреторных) клетках стенки пищевода, продуцирующих слизь. Аденокарцинома пищевода как правило образуется в нижней части пищевода, около желудка.
Стадии и симптоматика рака пищевода
Как все злокачественные новообразования, в развитии рака пищевода выделяют 4 стадии, классифицируемые на основании символов T (распространенность опухоли в органе), N (степень поражение регионарных лимфоузлов) и наличие отдаленных метастазов (M), по системе TNM
Символ T варьирует возрастает пропорционально распространенности основной опухоли (Tis — carcinoma in situ, интраэпителиальная опухоль без инвазии в собственную пластинку слизистой оболочки, тяжёлая дисплазия); T1 — опухоль прорастает до подслизистого слоя; Т2 — опухоль прорастает в мышечную оболочку;T3 — опухоль прорастает соединительнотканную оболочку — адвентицию; T4 — опухоль прорастает в прилежащие органы соседние структуры (плевра, перикард, бронх, трахею, диафрагмы и т.д.).
Символ N зависит от количества пораженных метастазами лимфоузлов (N0 — нет метастазов в регионарных лимфатических узлах;
N1 — метастазы в 1-2; N2 —в 3-6, N3 —в 7 и более регионарных лимфатических узла.
M0 — нет отдалённых метастазов; M1 — есть отдалённые метастазы.
Метастазирование рака пищевода обусловлено развитой лимфатической сетью пищевода. Метастазы распространяются на прилежащие лимфатические сосуды, а затем и на отдаленные лимфатические узлы.
Первой стадии процесса соответствует распространенность опухоли в пределах слизисто-подслизистого слоев, без метастазов, в том числе регионарных.
Вторая стадия характеризуется глубиной инвазии до адвентиции, но без метастазов в регионарных лимфоузлах, либо наличие регионарных метастазов с небольшой инвазией опухоли.
Третья стадия определяется глубокой инвазией и наличием метастазов в регионарных лимфоузлах.
Четвертая стадия определяется при прорастании прилежащих органов и структур и наличием не более 6 пораженных регионарных метастазов, либо при любой инвазии поражение 6 и более регионарных лимфоузлов, либо при наличии отдаленных метастазов (М1).
Специфических симптомов развития ранней стадии рака пищевода нет. Как правило, на начальных этапах заболевание диагностируется при плановых профилактических осмотрах.
Наиболее частым проявлением болезни является нарушение прохождения пищи по пищеводу (дисфагия). Выделяют четыре степени выраженности дисфагии.
- I степень — затруднение прохождения твёрдой пищи (хлеб, мясо);
- II степень — затруднение, возникающее при приёме кашицеобразной и полужидкой пищи (каши, пюре);
- III степень — затруднение при глотании жидкостей;
- IV степень — полная непроходимость пищевода.
Частый симптом – это боли, самостоятельные или связанные с приёмом пищи, постоянные или периодические. Боли локализуются за грудиной, в межлопаточной области или в эпигастрии. Нередко боли симулируют стенокардию, проявления остеохондроза и деформирующего спондилёза.
Также у пациентов могут присутствовать следующие симптомы:
- Слабость и снижение работоспособности
- Избыточное отделение слюны
- Нарушения пищеварения (диспепсия, отрыжка, изжога)
- Осиплость голоса (при поражении возвратного нерва метастазами)
- Кашель, поперхивание при еде вследствие либо расширения просвета пищевода выше сужения с периодическим попаданием застреваемой пищи в дыхательные пути, либо при формировании пищеводно-трахеального свища
- Анемия и сопутствующие симптомы – бледность, сонливость, вялость
- Изменение вкусовых пристрастий (отвращение к мясной пище)
- Снижение веса вследствие невозможности полноценного питания;
- Тошнота, рвота;
- Боли в грудной клетке при прохождении пищи, повышенная температура;
Причины возникновения рака пищевода и факторы риска
Факторы риска включают следующее:
2. Злоупотребление крепкими спиртными напитками.
3. Пожилой возраст
4. Погрешности в диете: употребление в пищу горячих блюд и напитков, наличие в рационе острых, консервированных и копченых продуктов.
6. Ожоговая стриктура пищевода
7. Ахалазия кардии
8. Папилломавирусная инфекция
9. Рубцовая стриктура
10. Хронические воспалительные заболевания пищевода
Хронические заболевания пищевода — это заболевания, которые вызывают возникновение и размножение несвойственных для слизистой оболочки клеток.
К таким болезням относятся:
Неопухолевые стриктуры пищевода (в результате перенесенных ожогов) — состояние, при котором происходит сужение пищевода, что затрудняет глотание.
Гастрэзофагельная рефлюксная болезнь (ГЭРБ), приводящая к возникновению опухолей в области соединения пищевода и желудка;
Пищевода Барретта — одно из серьёзных осложнений ГЭРБ, при котором в эпителиальной выстилке слизистой оболочки пищевода обнаруживается нехарактерный цилиндрический эпителий, вместо присутствующего в норме многослойного плоскоклеточного.
Ахалазия пищевода — заболевание, при котором нарушается способность гладкомышечного сфинктера в нижнем отделе пищевода к расслаблению. Результатом становится затруднение попадания пищи и жидкости в желудок, застаивание их в пищеводе и, как следствие, его расширение.
Грыжи пищевода — выпячивание стенки пищевода вызывает затруднение проглатывания пищи.
Диагностика рака пищевода
Для диагностики рака пищевода применяются следующие методы обследования:
- Анамнез и физикальный осмотр во время, которого ваш врач выяснит, когда появились первые признаки заболевания, что способствовало возникновению болезни. Какие имеются симптомы, а также проведет осмотр.
- Рентген грудной клетки и пищевода с контрастным усилением с взвесью бария. При котором, выполняется осмотр легочных полей на предмет наличия патологии, а так же оценивается распространенность опухолевого процесса по пищеводу, и наличие степени сужение просвета пищевода (Рис. 2).
- Эзофагогастродуоденоскопия (ЭГДС) — процедура, выполняемая для визуального осмотра просвета пищевода и нижележащих отделов ЖКТ. Эндоскоп — это тонкий, подобный трубе инструмент с подсветкой и объективом для просмотра. Также при помощи эндоскопа возможно получения образцов ткани опухоли для последующего гистологического исследования (рис. 3).
- Фибробронхоскопия (ФБС) – процедура схожая с выполнением ЭГДС, однако при данном исследовании выполняется осмотр верхних и нижних отделов дыхательных путей, а также оценивают возможное вовлечение последних в опухолевый процесс.
- КТ (компьютерная томография) органов грудной и брюшной полости с контрастным усилением — процедура, при которой на специальной аппаратуре выполняют серию изображений внутренних органов. Данной обследование необходимо для оценки наличия пораженных лимфатических узлов вдоль опухоли, определения связи образования с соседними анатомическими структурами и уточнения распространенности опухолевого процесса.
- ПЭТ-КТ (позитронно-эмиссионная компьютерная томография): процедура позволяющая обнаружить злокачественные опухолевые клетки в организме. Небольшое количество радиоактивной глюкозы (сахара) вводится в вену. Сканер ПЭТ вращается вокруг тела пациента и дает представление о том, где глюкоза используется в организме. Злокачественные опухолевые клетки проявляются ярче на снимке, потому что они более активны и потребляют больше глюкозы, чем нормальные клетки. Сканирование ПЭТ и КТ может выполняться одновременно. Это называется ПЭТ-КТ.
Рисунок 2. Рентген пищевода с контрастным усилением взвесью бария.
Рисунок 3. Эзофагогастродуоденоскопия (ЭГДС).
Лечение рака пищевода
Лечение подбирается индивидуально в зависимости от типа, стадии, общего состояния здоровья пациента.
Цель лечения: удаление первичной опухоли и всех тех органов и тканей, на которые она могла распространиться, а также профилактическое или лечебное воздействие на отсевы опухоли (метастазы).
Варианты лечения в первую очередь определяются той стадией (то есть степенью распространенности опухоли) на которой было выявлено заболевание.
Прогноз при I стадии рака пищевода благоприятный. Операция заключается в удалении пищевода и выполнением пластики. В случае ранних форм, у ряда больных могут быть успешно применены неоперативные методы. Для этого необходимо выполнение дополнительного исследования – эндоскопической сонографии. Дополнительного лечения не требуется.
При II и III стадии прогноз менее благоприятный. Нередко лечение начинается с применения химиотерапии или лучевой терапии, а также возможно комбинация этих методов лечения с последующим хирургическим вмешательством и удалением всего пищевода с пластикой.
При IV стадии заболевания основным методом лечения является паллиативное лечение направленное на уменьшение размеров опухоли или снижение темпов ее роста. Также применяется симптоматическое лечение направленное на устраненные основных симптомов заболевания (стентирование пищевода при критическом опухолевом стеннозе, инфузионная и обезболивающая терапия рис. 4).
Рисунок 4. Стентирование при опухолевом стенозе.
Хирургическое
Операция является основным методом лечения рака желудка. Объем оперативного вмешательства включает удаление пораженного опухолью органа в едином блоке с лимфатическими узлами (параэзофагеальные, паратрахеальные, нижние трахеобронхиальные, парааортальные лимфатические коллекторы) и окружающей клетчаткой. Стандартом хирургического лечения больных раком пищевода является — одномоментная резекция и пластика пищевода с двухзональной лимфаденэктомией (рисунок 5).
Этапы операции включают:
q Субтотальная резекция или экстирпация пищевода
q Расширенная лимфаденэктомия (удаление регионарного лимфатического аппарата)
q Пластика пищевода с применением желудочного или кишечного трансплантата
Хирургическое доступы включают: абдоминальный, при котором выполняется лимфаденэктомия верхнего этажа брюшной полости, и формируется трансплантат из большой кривизны желудка, и второй этап – трансторакальный, при котором удаляется пищевод, производится внутригрудная лимфаденэктомия, и формируется соустье между желудочным стеблем и оставшейся частью пищевода (Рисунок 6).
Рисунок 5. Этапы хирургического вмешательства.
В ряде ситуаций пищевод удается без вскрытия плевральной полости, т.е. через предварительно расширенное пищеводное отверстие диафрагмы (трансхиатально), однако такой доступ не позволяет осуществить полноценную внутригрудную лимфаденэктомию.
Любой из этих этапов (кроме шейного) возможно выполнить и малоинвазивными доступами (лапароскопически, торакоскопически).
Операции по поводу рака пищевода в целом достаточно длительные, относительно травматичные для пациента, требует сочетания высокотехнологичной оснащенности хирургической и анестезиологической составляющих, а также наличие высококвалифицированных врачебных кадров и среднего медицинского персонала.
Лучевая терапия
Лучевая терапия – это использование излучения высокой энергии, для того, чтобы убить раковые клетки.
При раке пищевода лучевая терапия применяется в трех вариантах:
— в качестве самостоятельного радикального лечения как альтернатива хирургическому лечению, при стадиях I-III, преимущественно при плоскоклеточном варианте и обязательно в сочетании с химиотерапией. При этом подводится максимальная доза облучения (60-70Гр) не только на зону опухоли, но и зоны регионарного метастазирования. Лечение проводится длительно (в течение 1,5-2мес).
Лучевая терапия может предшествовать оперативному вмешательству, то есть быть первым этапом комбинированного лечения. В этих случаях облучение, направленное на устранение сопутствующих воспалительных явлений и повреждение наиболее чувствительных элементов опухоли, приводит к уменьшению размеров опухоли и нередко делает ее операбельной. Она также проводится в сочетании с химиотерапией. Хирургическое вмешательство целесообразно проводить через 4-5 недель после окончания лучевой терапии.
Рисунок 6. Лапаротомия+трансторакальный доступ
Паллиативная лучевая терапия при IV стадии процесса с целью уменьшения опухолевого процесса и облегчения симптомов заболевания.
Иногда до лучевой терапии, если больной плохо глотает даже жидкую пищу, приходится накладывать гастростому. Однако спешить с гастростомой не следует, так как после 10—15 сеансов облучения проходимость пищевода почти всегда улучшается, и больные начинают удовлетворительно питаться.
Противопоказания для лучевой терапии рака пищевода: перфорация пищевода или предперфоративное состояние, отдаленные метастазы и выраженная кахексия. Наличие метастазов в регионарных лимфатических узлах первого порядка не препятствует лучевому лечению. Метастазы в лимфатические узлы второго и третьего порядка (система лимфатических узлов средостения, включая и корни легких) также не исключают возможности применения лучевой терапии, но в этих случаях она будет паллиативной.
Побочные эффекты лучевой терапии
Лучевая терапия может вызвать покраснение и сухость кожи на участке, куда направлено излучение. Многие пациенты испытывают усталость во время курса лечения. Также возможно негативное воздействие на показатели крови.
Лекарственное противоопухолевое лечение
Химиотерапия может проводиться при комбинированном лечении в составе предоперационной химиолучевой терапии (либо при химиолучевой терапии по радикальной программе), либо применяться как самостоятельный метод при генерализованном (IVстадии) раке пищевода, а также в ситуациях, когда другое лечение (хирургическое или лучевое) невозможно из-за серьезной сопутствующей болезни пациента. Применяются препараты платины (преимущественно оксалиплатин), таксаны (паклитаксел), фторпиримидины (5-фторурацил, капецитабин), таргетные препараты (гефитиниб, цетуксимаб, бевацизумаб) и другие препараты.
Осложнения противоопухолевого лечения рака пищевода и их коррекция
Наиболее частое осложнение химиотерапии – угнетение миелопоэза — роста и размножения различных фракций лейкоцитов с развитием лейкопении (низкого уровня в крови общего числа лейкоцитов) и нейтропении (снижение уровня относительного и абсолютного числа нейтрофильных лейкоцитов), как наиболее интенсивно делящихся и чувствительных к повреждающему действию цитотоксических препаратов. Использование колониестимулирующих факторов (лейкостим, филграстим и др.) позволяет существенно снизить число опасных для жизни инфекционных осложнений, возникающих при нейтропении. Не менее часто встречается осложнение в виде тошноты и рвоты – субъективно тягостные для больных токсические проявления, связанные с разрушением клеток слизистой тонкой кишки с выбросом серотонина в кровоток, активацией волокон блуждающего нерва и воздействием на особую область в головном мозге, ответственную за рефлексы тошноты и рвоты. Для купирования этих явлений наибольшей эффективностью обладает противорвотные препараты группы антагонистов рецепторов серотонина (трописетрон, ондансетрон и др.).
Диарея достаточно часто сопровождает проведение химиотерапии. Она является следствием повреждения быстро делящихся клеток слизистой оболочки тонкой и толстой кишки, что провоцирует транссудацию жидкости в просвет кишки с последующим многократным водянистым стулом. Потери жидкости восполняются по возможности обильным питьем, при необходимости возможно проведение инфузионной терапии.
Анемия также является частым осложнением химиотерапии, применяются препараты железа, в т.ч. внутривенные формы, а также при рефрактерной анемии целесообразно назначение препаратов – стимуляторов эритропоэза (препараты эритропоэтина альфа- и бетта-).
Ладонно-подошвенный синдром – дерматонейропатия, возникающая на коже дистальных отделов конечностей. Для лечения данного синдрома применяются сложносоставные кремы и мази на основе масел и растительных экстрактов (крем Mapisal, Элима).
Использование уникальных методик/ Новые методы лечения рака пищевода :
В настоящее время в хирургической практике при раке пищевода применяются малоинвазивные методы лечения: эндоскопическое удаление рака пищевода при расположении опухоли в пределах слизистой оболочки пищевода; в полостной хирургии – торакоскопические и лапароскопические доступы при выполнении стандартного объема хирургического лечения.
В лучевой терапии разрабатываются методики гиперфракционирования дозы (HART режим), подводимой к опухоли и на регионарные зоны, для укорочения лечебного периода.
Возможно применение HIFU (Фокусированный ультразвук высокой интенсивности) при единичных метахронных (развившихся через некоторое время после ремиссии) метастазах рака пищевода в паренхиматозные органы.
Клинические исследования рака пищевода
Ежегодно фармацевтические компании разрабатывают новые лекарственные препараты, которые еще не входят в существующие стандарты лечения, в связи с чем проводятся клинические исследования для оценки эффективности и безопасности этих препаратов. Целью такого исследования является улучшение методов лечения рака, внедрение новых более эффективных препаратов и, как следствие, улучшение выживаемости пациентов. Если тот или иной препарат или методика в исследовании продемонстрировали свою эффективность и безопасность, а также улучшили показатели выживаемости по сравнению с предшествующим стандартом лечения, то при ежегодном обновлении рекомендаций их также включают в алгоритмы лечения.
Особенности реабилитации после лечения рака пищевода
Наибольшее значение имеет реабилитация после радикального хирургического лечения, т.к. операции носят обширный характер.
Непосредственно после операции пациент переводится в палату отделения интенсивной терапии и реанимации, где в течение 24-48 часов осуществляется наблюдение, перевязки и реабилитация. С первых суток назначается голод, а питание проводится с помощью внутривенных инфузий.
У некоторых пациентов во время операции устанавливается тонкий зонд, заведенный за зону швов, в послеоперационном периоде питание начинается сразу после операции – вводятся растворы солей, глюкозы, а затем питательные смеси. С разрешения лечащего врача рекомендуется полоскание рта и питье чистой воды небольшими глотками.
Во время операции устанавливается катетер в мочевой пузырь для отвода мочи и контроля диуреза. Мочевой катетер удаляется на вторые-третьи сутки, после чего пациент должен самостоятельно помочиться. Если возникают затруднения, необходимо сообщить об этом врачу.
Необходимо знать, что боли в операционной ране неизбежны, в связи с этим проводится плановое поликомпонентное обезболивание, в том числе посредством эпидуральной анестезии, однако если боль начинает усиливаться, необходимо сразу дать знать об этом врачу, т.к. предупредить сильную боль значительно легче, чем купировать развившийся выраженный болевой синдром.
С целью ранней реабилитации и профилактики нарушений дренажной функции трахеи и бронхов, а также более быстрого и устойчивого появления перистальтики рекомендуются лечебная, в том числе дыхательная гимнастика в постели с первого послеоперационного дня, и ранняя вертикализация: постепенное присаживание, вставание и хождение с поддержкой. Также полезно выполнять движения кистями и стопами, сгибание в локтевых и коленных суставах, нерезкое покашливание.
Дыхательная гимнастика необходима для профилактики развития пневмонии, рекомендуется проводить серии глубоких, но не резких, вдохов и выдохов, иногда с этой целью рекомендуется упражнение с побудительным спирометром. При необходимости проводится респираторная терапия с ингаляциями противовоспалительных, бронхолитических и муколитических средств (рисунок 7).
Рисунок 7. Побудительный спирометр и компрессорный небулайзер для ингаляций
Питание через рот начинается при наличии устойчивой работы кишечника (хорошо выслушиваемая перистальтика и отхождение газов), что происходит в среднем на 4-5-6 сутки после операции, и отсутствии подозрений на развитие хирургических осложнений. Иногда для стимуляции перистальтики используются специальные медикаментозные средства (прозерин, убретид), а также лечебные клизмы с гипертоническим раствором соли. В это время пациент должен быть полностью активизирован, самостоятельно передвигаться и обслуживать себя. Компрессионные чулки необходимо носить постоянно, особенно ночью, допускается снять их в дневное время на 1-2 часа, затем снова надеть в положении лежа.
Спать рекомендуется с приподнятой верхней половиной кровати, особенно в первые 5-7 суток после операции, а при развитии рефлюксных явлений в позднем послеоперационном периоде – постоянно (положение Фаулера) (рисунок 8).
Прогноз заболевания
«Нелеченный» рак пищевода имеет плохой прогноз – средняя продолжительность жизни не превышает 5-8 месяцев с момента появления признаков болезни.
Рисунок 8. Положение в послеоперационном периоде (Фаулера)
При поверхностном раке пищевода (Т1) и отсутствии регионарного метастазирования 5-летняя выживаемость при хирургическом лечении стремится к 100%, при инвазии в подслизистый слой – снижается до 83%, при наличии метастазов в регионарные лимфоузлы – 5-летняя выживаемость снижается до 48%. При аденокарциноме результаты лучше, чем при плоскоклеточном раке (83,4% и 62,9% соответственно).
В среднем во всей популяции больных раком пищевода при хирургическом лечении 5-летний срок переживают 25-35% оперированных, среди перенесших радикальные операции этот показатель достигает 48,8%, при паллиативных не более 5%. Комбинированное лечение несколько улучшает результаты: 5-летняя выживаемость составляет 35-56,6%.
Наличие регионарных метастазов снижает 5-летнюю выживаемость до 20-25% для комбинированного лечения. Прорастание опухолью всех слоев стенки пищевода (Т3-4) общая продолжительность жизни не превышает 5 лет.
При поражении опухолью верхней трети органа (шейного отдела) после хирургического лечения 5-летняя выживаемость равна нулю, при комбинированном лечении – не более 15-20%.
Филиалы и отделения Центра, в которых лечат рак пищевода
ФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, химиотерапевтического и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.
Рак пищевода можно лечить:
В Отделении торакоабдоминальной хирургии МНИОИ имени П.А. Герцена – филиала ФГБУ «НМИЦ радиологии» Минздрава России
Заведующий отделения – к.м.н. Владимир Михайлович Хомяков.
Контакты: (495) 150 11 22
В Отделении лучевого и хирургического лечения заболеваний абдоминальной области МРНЦ имени А.Ф. Цыба — филиала ФГБУ «НМИЦ радиологии» Минздрава России
Заведующий отделением — к.м.н. Леонид Олегович Петров
Контакты: (484) 399-31-30
Источник