- Синдром портальной гипертензии
- Введение
- Причины
- Симптоматика
- Диагностика
- Лечение
- Сплено-ренальный анастомоз
- Кратко о методе лечения
- Показания и противопоказания к методу лечения
- Подготовка к лечению
- Как проходит метод лечения
- Возможные осложнения при лечении
- Прогноз после метода лечения
- Признаки синдрома портальной гипертензии и методы его лечения
- Автор:
- Рецензент:
- Синдром портальной гипертензии: признаки, методы лечения
- Симптомы портальной гипертензии
- Лечение портальной гипертензии
- Жировой гепатоз, неалкогольная жировая болезнь печени (НАЖБП) — симптомы и лечение
- Определение болезни. Причины заболевания
- Симптомы жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
- Патогенез жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
- Классификация и стадии развития жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
- Осложнения жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
- Диагностика жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
- Лечение жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
- Прогноз. Профилактика
Синдром портальной гипертензии
Введение
Кровь, питающая ряд органов брюшной полости, отводится по единому венозному руслу. Эта вена называется (учитывая ее расположение) воротной или портальной веной печени; она имеет множество ответвлений и является наиболее крупной веной в организме человека, достигая в диаметре 8-12 мм. Как и в любом ином магистральном кровеносном сосуде, в воротной вене должно постоянно поддерживаться определенное кровяное давление – здесь оно в норме составляет от 5-7 до 10-12 мм рт. ст. Хроническое превышение этого уровня приводит к общим нарушениям гемо- и гидродинамики брюшной полости, дегенеративным изменениям в тканях и другим тяжелым последствиям, которые в совокупности образуют синдром портальной гипертензии.
По определению, синдром не является самостоятельным заболеванием; это устойчивое, повторяющееся сочетание взаимосвязанных клинических симптомов, которое может формироваться в силу разных причин, но обладает собственными специфическими закономерностями развития и протекания. Это в полной мере касается и синдрома портальной гипертензии.
Причины
Выделяют две основные группы причин развития портальной гипертензии: внепеченочные и внутрипеченочные. На этих же критериях (конкретная локализация блока воротной вены) построены общепринятые ее классификации, обычно включающие под- или предпеченочную форму, внутрипеченочную (с несколькими подтипами), надпеченочную и смешанную.
Согласно доступной медицинской статистике, наиболее распространенной (85-90%) является внутрипеченочная локализация нарушений портально-венозного оттока. В этиологическом плане внутрипеченочная портальная гипертензия чаще всего обусловлена циррозом печени или иным процессом дегенеративного замещения паренхиматозных клеток соединительной тканью.
Предпеченочная форма составляет 10-12% в общем объеме портальной гипертензии и, как правило, развивается вследствие механического давления (например, злокачественной опухолью), врожденных или приобретенных аномалий анатомического строения вены, воспалительного процесса в миокарде, обструктивного тромбоза Бадда-Киари и пр.
Частота надпеченочной (постпеченочной) формы не превышает 3-4%; причинами обычно становятся прорастание опухоли, тромбоз, эндофлебит печеночных вен.
В целом, к перечню этиопатогенетических факторов портальной гипертензии следует добавить все разновидности гепатитов, онкозаболевания, патологию билиарной (желчевыводящей) и сердечнососудистой систем, последствия травм и некоторых хирургических вмешательств, отравления (медикаментами, грибами, соединениями меди и пр.), ожоги. Кроме того, портальная гипертензия нередко развивается на фоне жизнеугрожающих состояний в ходе реанимационных мероприятий.
Симптоматика
Классическая триада симптомов включает варикозное расширение вен пищевода и верхних отделов желудка (в 85% случаев), спленомегалию (селезенка в той или иной степени увеличена практически всегда) и асцит (массивное скопление жидкости в брюшной полости).
Ранние проявления синдрома портальной гипертензии могут быть неспецифическими: признаки диспепсии (абдоминальные боли и тяжесть в животе, тошнота, различные проблемы с дефекацией, метеоризм и т.д.). Кроме того, по мере нарастания выраженности нарушений кровоснабжения печени снижается ее способность к выполнению дезинтоксикационных функций, что отражается и на функционировании мозга, – развивается т.н. печеночная энцефалопатия с присущей ей психоневрологической симптоматикой. При тяжелой печеночной недостаточности наблюдается желтуха. Прямую угрозу жизни несут (и нередко приводят к летальному исходу) внутренние кровотечения из растянутых и истонченных венозных стенок.
Выраженность, стадийность и скорость появления симптомов в значительной мере различаются при разных типах портальной гипертензии. Так, «водянка живота» (асцит) в одних случаях развивается постепенно, в других остро, и т.д.
Диагностика
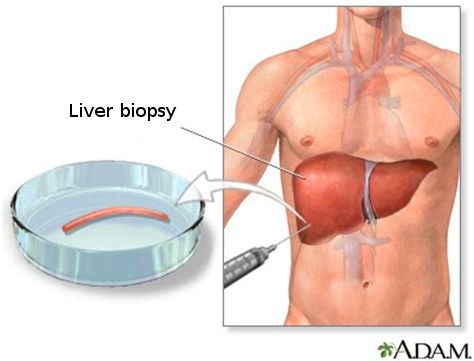
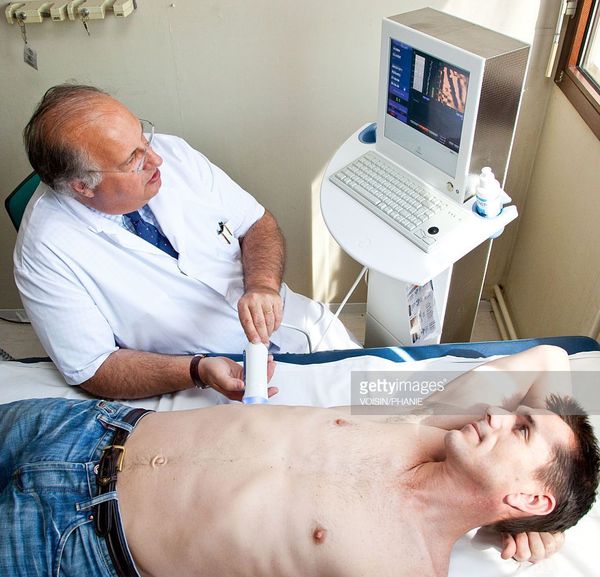
Диагноз устанавливается путем сопоставления жалоб, анамнестических данных, результатов клинического осмотра и инструментального обследования. В частности, необходимой и обязательной является ФГДС (фиброгастродуоденоскопия), в ходе которой визуализируются вены пищевода и желудка, оценивается их статус и собирается другая клинически значимая информация. Назначают УЗИ в дуплекс-режиме, рентгенографию, по необходимости – дополнительные методы исследования селезенки и гепатобилиарной системы (сканирование печени, спленоманометрия, спленопортография, КТ, МРТ и т.д.).
Лечение
Синдром портальной гипертензии, в целом, весьма проблематичен в терапевтическом плане. Амбулаторное консервативное лечение и курсы поддерживающей терапии могут занимать несколько лет; назначаются «прицельные» гипотензивные средства для снижения давления в воротной, нижней полой и печеночных венах, вазо- и гепатопротекторы. Однако с усугублением ситуации амбулаторное лечение становится все менее эффективным, и пациента приходится госпитализировать, – сроки стационарного лечения варьируют от двух недель до месяца и более.
Масштабы и цели хирургического вмешательства, – если оно целесообразно и необходимо, – определяются особенностями конкретного случая: в различных ситуациях основной задачей может быть восстановление венозной проходимости, коррекция путей отвода крови, удаление из брюшной полости избыточной жидкости при асците, склерозирование расширенных и кровоточащих вен пищевода, и т.д. Однако относительными или абсолютными противопоказаниями к операции могут становиться сопутствующие хронические заболевания, беременность, пожилой возраст, тяжелое общее состояние пациента (обусловленное, например, выраженной печеночной недостаточностью).
Отдаленный прогноз при некоторых формах синдрома портальной гипертензии (внутрипеченочная, надпеченочная) неблагоприятен, особенно при пищеводно-желудочных геморрагиях у больных циррозом печени. В других случаях оперативное вмешательство может значительно улучшить ситуацию. Однако единственным радикальным лечением в настоящее время остается трансплантация печени.
Источник
Сплено-ренальный анастомоз
О сплено-ренальном аностомозе
Кратко о методе лечения
Термин «спленоренальный шунт» обозначает анастомоз (соединение двух полых органов) между селезеночной и почечной венами, применяемый в основном для лечения портальной гипертензии.
Пока ещё мало используются возможности селезеночной артерии как источника артериального кровоснабжения других внутрибрюшных внутренних органов. Эта большая артерия продемонстрировала адекватную замену для печеночной, верхней брыжеечной или левой почечных артерий.
Сплено-ренальный аностомоз (спленоренальное шунтирование) — сосудистая реконструктивная операция. Показания к ней ограничены. Обычно в качестве «донора» для кровоснабжения почки через почечную артерию используют аорту. Однако в некоторых случаях сделать это не возможно. И тогда применяется сплено-ренальный анстомоз.
Данная процедура выполняется только с левой почечной артерией. В качестве доступа используется лапаротомия или левостроннюю торакофренолюмботомию (разновидность хирургического доступа).
Показания и противопоказания к методу лечения
Потенциальные показания к сплено-ренальному артериальному анастомозу:
1) портальная гипертензия;
2) тромбоз аорты;
3) обструкция почечной артерии;
4) повреждение почек;
5) аневризма почечной артерии;
6) аномальная почечная артерия.
Противопоказанием к процедуре является патология в системе чревного ствола, асцит и тромбоз селезеночной вены.
Подготовка к лечению
Перед проведением процедуры проводиться лечение для нормализации функционального состояния печени.
Как проходит метод лечения

Операция проходит в несколько этапов:
1/ Создается доступ к селезенке и левой почке, это достигается с помощью специальных (торакоабдоминального или абдоминодиафрагмального) разрезов.
2/ Мобилизация селезенки (селезенка отделяется от желудка и ободочной кишки). Это нужно для того, чтобы обнажить её сосудистую ножку.
3/ Удаление селезенки.
4/ Выделение селезеночной вены и перевязывание её притоков. Процедура требует осторожности, чтобы не травмировать стенку сосуда. Для сплено-ренального аностомоза необходимо выделить не менее 5 сантиметров вены.
5/ Выделение почечной вены.
6/ Наложение аностомоза. Конец селезеночной вены сшивают с почечной.
Операция длится около 3-х часов.
Возможные осложнения при лечении
Наиболее опасным осложнением анастомоза является тромбоз портальной системы. Очень редко развивается энцефалопатия и послеоперационный панкреатит.
Прогноз после метода лечения
Несомненным плюсом операции является то, что не требуется выделение аорты и использование пластического материала.
После операции снижается риск кровотечения и асцита. Это наиболее эффективный метод лечения варикоза вен пищевода.
Источник
Признаки синдрома портальной гипертензии и методы его лечения
Автор:
Терапевт, ревматолог, кардиолог
Рецензент:
Терапевт, кардиолог, гастроэнтеролог, врач функциональной диагностики
Синдром портальной гипертензии: признаки, методы лечения
Синдром портальной гипертензии – это состояние, чаще всего возникающее вследствие цирроза печени (ЦП). Из-за того, что в печени вместо нормальных клеток начинает развиваться соединительная ткань, из внутрипеченочного кровотока выключаются самые мелкие элементы кровеносной системы — капилляры, которые в печени называются синусоидами. Кровь начинает сбрасываться по обходным путям, в воротной вене, которая несет ее к печени, возрастает давление, и это проявляется определенными признаками.
Симптомы портальной гипертензии
Врачи различают несколько признаков этой патологии:
- варикозно расширенные вены особых локализаций;
- асцит;
- увеличение селезенки — спленомегалия;
- гастропатия.
Первый признак чаще всего выявляется лишь тогда, когда одна из расширенных вен лопается и начинается кровотечение. Расположены варикозные узлы обычно в области нижней трети пищевода, и гораздо реже — в желудке и вокруг прямой кишки. Кровотечение может быть очень обильным, сопровождаться большой кровопотерей вплоть до геморрагического шока.
Асцит связан с тем, что поверхность печени, пораженной циррозом, перестает быть плотной. Напоминая губку, она начинает пропускать сквозь поры в себе жидкость, богатую белком. Из-за этого, кстати, больные циррозом печени интенсивно худеют.
Спленомегалия и сопутствующий ей гиперспленизм проявляется снижением выработки некоторых клеточных элементов крови – эритроцитов, тромбоцитов. В результате возникают анемия и тромбоцитопения, из-за чего на коже больных появляются мелкие и крупные кровоизлияния. Это – плохой прогностический признак, знак того, что неблагоприятный исход близок.
Гастропатия чаще всего возникает после манипуляций на венах пищевода, носящих название «склеротерапия» (введение в вены особых растворов, после чего сосуды полностью закрываются).
Лечение портальной гипертензии
Из-за того, что цирроз печени — это необратимое состояние, идеальным его лечением является трансплантация печени. К сожалению, далеко не каждому больному «везет» успеть получить донорский орган, поэтому пока человек находится на очереди, его лечат медикаментозно, применяя два принципа: обеспечение печени функционального покоя и коррекция сосудистой сети в ней.
Для достижения первой цели пациенту назначают щадящую диету, известную под номером 5, с исключением жирных, жареных, острых блюд, растительных горечей, алкоголя, кофе, чая, маринадов и копченостей, свежего хлеба.
Для уменьшения выработки и всасывания токсических продуктов переваривания пищи из кишечника назначаются препараты лактулозы — дюфалак, лактовит, нормазе. Для улучшения микробного состава кишечника и перекладывания на него части задач по правильному усвоению пищи, рекомендован прием про- и пребиотиков. Эта группа лекарств помогает организму синтезировать витамины и аминокислоты, которые поврежденная печень выработать не в состоянии. Кроме того, микробные препараты обладают детоксикационными свойствами.
Препараты урсодезоксихолевой кислоты способствуют снижению нагрузки на клетки печени за счет улучшения обмена желчи. Также при портальной гипертензии рекомендовано введение глюкозы, аминокислотных и жировых смесей, адаптированных к нуждам больных печеночными заболеваниями, витаминов.
Для улучшения внутрипеченочной микроциркуляции используются препараты группы статинов, вызывающие расширение внутрипеченочных сосудов — синусоидов. Тем же эффектом обладают и нитраты (нитропруссид натрия), правда, при длительном приеме они могу дать обратное действие.
Пентоксифиллин и антиоксиданты в целом улучшают жизнеспособность печеночных клеток, снижают частоту серьезных осложнений цирроза.
Основой лечения портальной гипертензии является применение препаратов, сужающих сосуды печени и тем самым снижающих давление в воротной вене. К таким лекарствам относятся терлипрессин, мидодрин, норэпинефрин, пропранолол, карведилол. Также показано введение альбумина, который способствует сохранению жидкости в кровяном русле, препятствуя асциту, и нормализует давление в системе воротной вены.
Источник
Жировой гепатоз, неалкогольная жировая болезнь печени (НАЖБП) — симптомы и лечение
Что такое жировой гепатоз, неалкогольная жировая болезнь печени (НАЖБП)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, врача общей практики со стажем в 14 лет.
Определение болезни. Причины заболевания
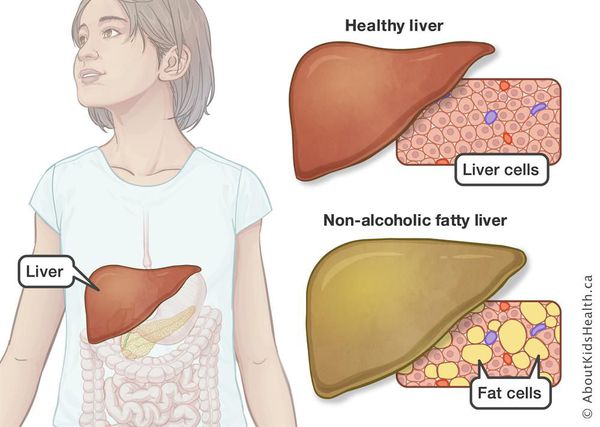
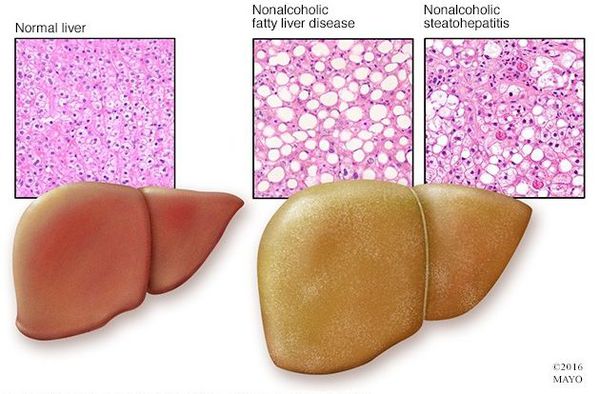
Неалкогольная жировая болезнь печени / НАЖБП (стеатоз печении или жировой гепатоз, неалкогольный стеатогепатит) — это неинфекционное структурное заболевание печени, характеризующееся изменением ткани паренхимы печени вследствие заполнения клеток печени (гепатоцитов) жиром (стеатоз печени), которое развивается из-за нарушения структуры мембран гепатоцитов, замедления и нарушения обменных и окислительных процессов внутри клетки печени.
Все эти изменения неуклонно приводят к:
- разрушению клеток печени (неалкогольный стеатогепатит);
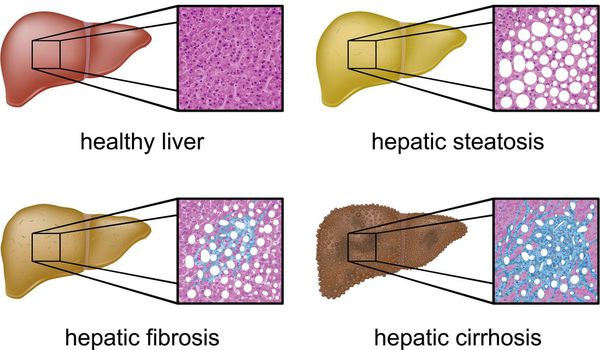
- накоплению жировой и формированию фиброзной ткани, что вызывает уже необратимые, структурные (морфологические) изменения паренхимы печени;
- изменению биохимического состава крови;
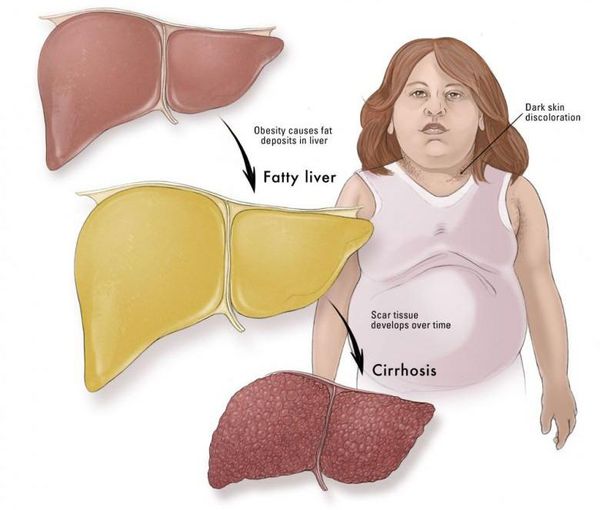
- развитию метаболического синдрома (гипертоническая болезнь, ожирение, сахарный диабет);
- в конечном итоге, циррозу.
Метаболический синдром — широко распространённое состояние, характеризующееся снижением биологического действия инсулина (инсулинорезистентность), нарушением углеводного обмена (сахарный диабет II типа), ожирением центрального типа с дисбалансом фракций жира (липопротеинов плазмы и триглицеридов) и артериальной гипертензией. [2] [3] [4]
В большинстве случаев НАЖБП развивается после 30 лет. [7]
Факторами риска данного заболевания являются:
- малоподвижный образ жизни (гиподинамия);
- неправильное питание, переедание;
- длительный приём лекарственных препаратов;
- избыточная масса тела и висцеральное ожирение;
- вредные привычки.
Основными причинам развития НАЖБП являются: [11]
- гормональные нарушения;
- нарушение жирового обмена (дисбаланс липопротеидов плазмы);
- нарушение углеводного обмена (сахарный диабет);
- артериальная гипертензия;
- ночная гипоксемия (синдром обструктивного апноэ сна).
При наличии гипертонической болезни, ожирения, сахарного диабета, регулярном приёме лекарств или в случае присутствия двух состояний из вышеперечисленных вероятность наличия НАЖБП достигает 90 %. [3]
Ожирение определяется по формуле вычисления индекса массы тела (ИМТ): ИМТ = вес (кг) : (рост (м)) 2 . Если человек, например, весит 90 кг, а его рост — 167 см, то его ИМТ = 90 : (1,67х1,67) = 32,3. Этот результат говорит об ожирении I степени.
- 16 и менее — выраженный дефицит массы;
- 16-17,9 — недостаточная масса тела;
- 18-24,9 — нормальный вес;
- 25-29,9 — избыточная масса тела (предожирение);
- 30-34,9 — ожирение I степени;
- 35-39,9 — ожирение II степени;
- 40 и более — ожирение III степени (морбидное).
Симптомы жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
У большинства больных данное заболевание на ранних стадиях протекает бессимптомно — в этом и заключается большая опасность.
У 50-75% больных могут появляться симптомы общей (хронической) усталости, снижение работоспособности, недомогание, слабость, тяжесть в области правого подреберья, набор веса, длительное повышение температуры тела без всякой причины, красные точки на коже в области груди и живота. Печень часто увеличена. Возникают расстройства пищеварения, повышенное газообразование, кожный зуд, редко — желтуха, «печёночные знаки».
Часто НАЖБП сопутствуют заболевания желчного пузыря: хронический холецистит, желчнокаменная болезнь. Реже, в запущенных случаях, возникают признаки портальной гипертензии: увеличение селезёнки, варикозное расширение вен пищевода и асцит (скопление жидкости в брюшной полости). Как правило, данные симптомы наблюдаются на стадии цирроза печени. [7]
Патогенез жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
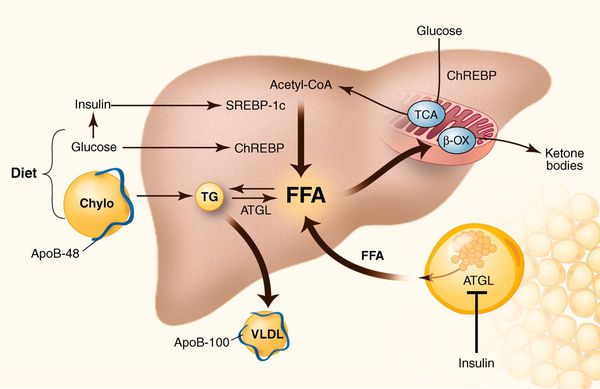
К накоплению холестерина, а именно липидов (жироподобных органических соединений) в печени, приводят, прежде всего, следующие факторы:
- избыточное поступление свободных жирных кислот (FFA) в печень;
- усиленный синтез свободных жирных кислот печени;
- пониженный уровень бета-окисления свободных жирных кислот;
- снижение синтеза или секреции липопротеинов очень высокой плотности. [7]
У пациентов с ожирением в ткани печени повышенно содержание свободных жирных кислот, что и может быть причиной нарушения функций печени, так как жирные кислоты химически активны и могут привести к повреждению биологических мембран гепатоцитов, образуя в них ворота для поступления в клетку эндогенного жира, в частности липидов (преимущественно низкой и очень низкой плотности), а транспортом является сложный эфир — триглицерид. [2]
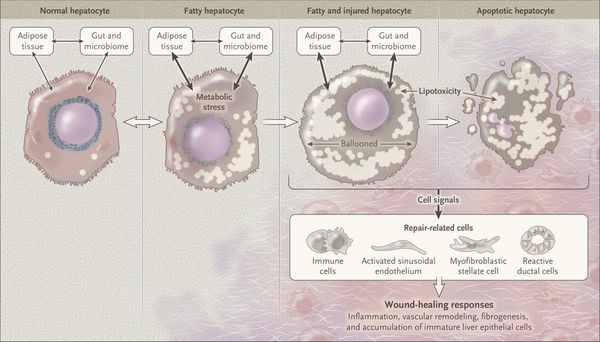
Таким образом, гепатоциты заполняться жиром, и клетка становиться функционально неактивной, раздувается и увеличивается в размерах. При поражении более миллиона клеток макроскопически печень увеличивается в размерах, в участках жировой инфильтрации ткань печени становиться плотнее, и данные участки печени не выполняют своих функций либо выполняют их с существенными дефектами.
Перекисное окисление липидов в печени приводит к синтезу токсичных промежуточных продуктов, которые могут запускать процесс апоптоза (запрограммированной гибели) клетки, что может вызывать воспалительные процессы в печени и сформировать фиброз. [2]
Также важное патогенетическое значение в формировании НАЖБП имеет индукция цитохрома P-450 2E1 (CYP2E1), который может индуцироваться как кетонами, так и диетой с высоким содержанием жиров и низким содержанием углеводов. [7] CYP2E1 генерирует токсические свободные радикалы, приводящие к повреждению печени и последующему фиброзу.
Кроме того, патогенетическое значение в формировании НАЖБП имеет эндотоксин-опосредованное повреждение, которое, в свою очередь, усиливает выработку провоспалительных цитокинов (ФНО-α, ИЛ-6 и ИЛ-8), приводящих к нарушению целостности мембран гепатоцитов и даже к их некрозу [9] , а также к развитию воспалительной клеточной инфильтрации как в портальных трактах, так и в дольках печени, что приводит к стеатогепатиту.
Продукты перекисного окисления липидов, некрозы гепатоцитов, ФНО и ИЛ-6 активируют стеллатные (Ito) клетки, вызывающие повреждение гепатоцитов и формирование фиброзных изменений.
Классификация и стадии развития жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В настоящий момент общепринятой классификации НАЖБП не существует, однако ряд авторов выделяет стадии течения заболевания и степени неалкогольного стеатогепатита (НАСГ).
Оценка стеатоза печени и гистологической активности НАЖБП по системе E.M. Brunt: [9] [10] [11]
- I степень (мягкий НАСГ) — стеатоз крупнокапельный, не более 33-66% поражённых гепацитов;
- II степень (умеренный НАСГ) — крупно- и мелкокапельный, от 33% до 66% поражённых гепацитов;
- III степень (тяжелый НАСГ) — крупно- и мелкокапельный, больше 60% поражённых гепацитов.
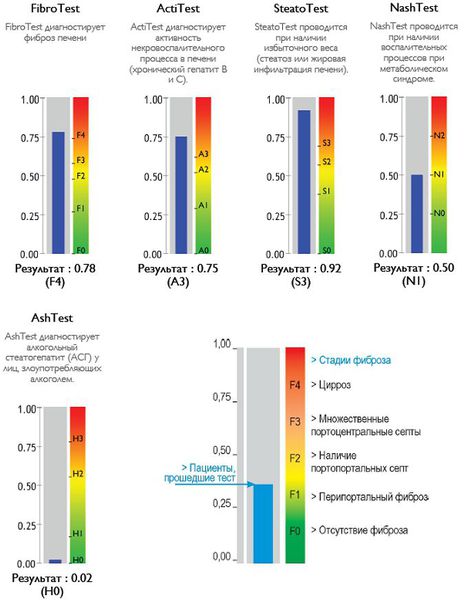
Также можно условно разделить степени стеатоза, фиброза и некроза по результату теста ФиброМакс — степени выраженности жировой инфильтрации:
- S1 (до 33% жировой инфильтрации);
- S2 ( 33-60% жировой инфильтрации)
- S3 (более 60% жировой инфильтрации)
- F1,F2, F3, цирроз.
Осложнения жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
Наиболее частые осложнения НАЖБП — это гепатит, замещение нормальной паренхиматозной ткани печени фиброзной — функционально нерабочей тканью с формированием в конечном итоге цирроза печени.
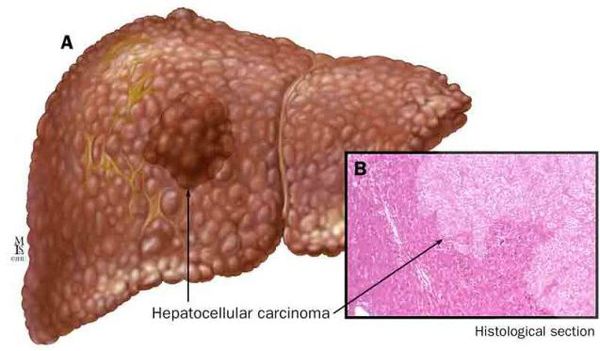
К более редкому осложнению, но всё же встречающемуся, можно отнести рак печени — гепатоцеллюлярную карциному. [9] Чаще всего она встречается на этапе цирроза печени и, как правило, ассоциируется с вирусными гепатитами.
Диагностика жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В диагностике НАЖБП используются лабораторные и инструментальные методы исследования.
В первую очередь оценивается состояние печени на предмет воспалительных изменений, инфекционных, аутоиммунных и генетических заболеваний (в том числе болезней накопления) с помощью общеклинических, биохимических и специальных тестов. [7]
Далее проводится оценка выполняемых печенью функций (метаболическая/обменная, пищеварительная, детоксикационная) по способности выработки определённых белков, характеристикам жиров и углеводов. Детоксикационная функция печени оценивается преимущественно при помощи С13-метацетинового теста и некоторых биохимических тестов.
Кода первые два этапа завершены, исследуется структурное состояние печени при помощи УЗИ [4] , МСКТ, МРТ и эластометрии (FibroScan), при необходимости исследуется морфологическое состояние — биопсия печени. [3]
С помощью эластометрии исследуется эластичность мягких тканей. Злокачественные опухоли отличаются от доброкачетсвенных повышенной плотностью, неэластичностью, они с трудом поддаются компрессии. На мониторе FibroScan более плотные ткани окрашены в голубой и синий цвет, жировая ткань — жёлто-красный, а соединительная ткань — зелёный. Высокая специфичность метода позволяет избежать необоснованных биопсий.
После проведённой диагностики, устанавливается окончательный диагноз и проводится соответствующее лечение.
Лечение жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
С учётом механизма развития заболевания разработаны схемы курсового лечения НАЖБП, направленные на восстановление структуры клеточных мембран, обменных и окислительных процессов внутри клеток печени на молекулярном уровне, очистку печени от внутриклеточного и висцерального жира, который затрудняет её работу.
В процессе лечения производится:
- коррекция углеводного, жирового (липидного) обмена веществ;
- нормализация процессов окисления в клетке;
- влияние на основные факторы риска;
- снижение массы тела;
- улучшение структуры печени на обратимых стадиях.
После лечения наступает заметное улучшение дезинтоксикационной (защитной), пищеварительной и метаболической функции печени, пациенты теряют в весе, улучшается общее самочувствие, повышается умственная и физическая работоспособность.
Курсовые программы лечения занимают от трёх до шести месяцев и подбираются в зависимости от степени выраженности метаболических нарушений. К ним относятся:
- программа «Лайт»;
- программа «Медиум»;
- программа «Премиум»;
- индивидуальная программа лечения — разрабатывается на основании сопутствующих заболеваний, текущего состояния пациента и необходимой интенсивности лечения.
Программы включают в себя предварительное обследование, постановку диагноза и медикаментозное лечение, которое состоит из двух этапов:
- инфузионная терапия с пролонгацией приёма препаратов внутрь, подбор диеты и физической активности;
- сдача контрольных анализов и оценка результатов.
Прогноз. Профилактика
На ранних стадиях заболевания прогноз благоприятный.
Профилактика НАЖБП предполагает правильное питание, активный образ жизни и регулярную календарную диспансеризацию.
К правильному питанию можно отнести включение в свой рацион питания омега-3 полиненасыщенных жирных кислот, коротких углеводов, ограничение потребления приправ, очень жирной и жаренной пищи. Разнообразие рациона питания также является ключевым моментом полноценного питания. Показано потребление продуктов, богатых растительной клетчаткой.
Для активного образа жизни достаточно ходить пешком от 8 000 до 15 000 шагов в сутки и уделять три часа в неделю физическим упражнениям.
В отношении календарной диспансеризации следует ежегодно выполнять УЗИ органов брюшной полости и оценивать уровень своих печёночных ферментов (АЛТ, АСТ, общий билирубин), особенно при приёме каких-либо лекарственных препаратов на постоянной основе.
Источник