- Абляция очагов при пищеводе Барретта
- Лечение пациентов с пищеводом Барретта
- Аргоноплазменная абляция очагов метаплазии
- Подготовка к процедуре
- Хронический гастрит и рак желудка
- Врачи
- Хронический гастрит – маленький шаг на пути к раку желудка
- Причины хронического гастрита
- Факторы риска развития аденокарциномы (рака) желудка
- Рекомендации по профилактике развития аденокарциномы (рака) желудка
- Заключение
Абляция очагов при пищеводе Барретта
Пищевод Барретта – это патологическое состояние, при котором плоский эпителий нижней трети пищевода замещен метапластическим цилиндрическим эпителием. Пищевод Барретта является серьезным осложнением гастроэзофагеальной рефлюксной болезни (ГЭРБ), официально доказанным предраковым состоянием, которое может приводить к развитию злокачественной опухоли пищевода.
Диагностировать данное заболевание можно при эндоскопическом исследовании с проведением биопсии.
Специалисты отделения эндоскопии НИИ онкологии им. Н.Н.Петрова придерживаются позиции, согласно которой для постановки диагноза «пищевод Барретта» необходимо обнаружение кишечной метаплазии в биоптатах, т.к. только неполная кишечная метаплазия в дистальном отделе пищевода предрасполагает к развитию дисплазии и повышает риск возникновения рака пищевода в 30-125 раз.
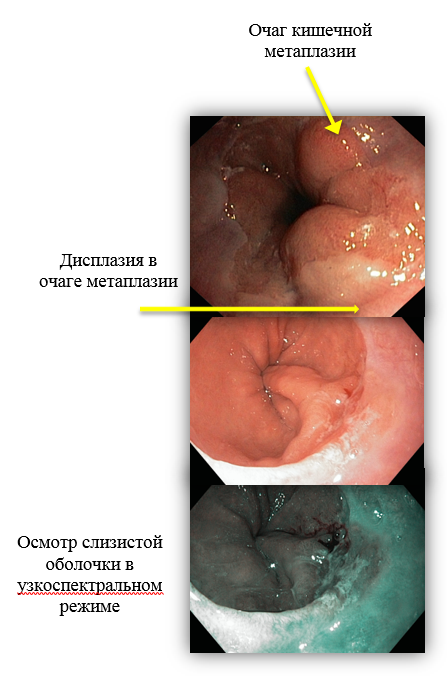
При обнаружении очагов метаплазии перед врачами-эндоскопистами ставится важная диагностическая задача – выполнить тщательный прицельный осмотр слизистой для выявления участков с нерегулярным рельефом и сосудистым рисунком, которые свидетельствуют о возникновении дисплазии различной степени тяжести или аденокарциномы. Такой подход позволяет произвести забор биоптатов прицельно, а не случайным образом, что повышает диагностическую ценность и снижает вероятность ошибки в обнаружении рака.
Для решения этих задач требуется оснащение эндоскопического отделения современным оборудованием и применение современных уточняющих методик осмотра слизистой оболочки.
- На отделении эндоскопии НИИ онкологии им. Н.Н.Петрова обследование пациентов выполняется с использованием эндоскопических стоек Olympus Evis Exera серии II и III, эндоскопов Olympus H-180AL и HJ-180AL.
- В качестве уточняющих методик осмотра слизистой мы используем хромоскопию (прижизненное окрашивание слизистой) с 1,5% р-м уксусной кислоты, а также виртуальную хромоскопию, которая заключается в осмотре слизистой в особом узкополосном световом режиме (NBI). Это позволяет детализировать структуру слизистой и увидеть изменения рельефа размером менее 1 мм.
- Мы используем общепринятый стандартизованный международный протокол описания этого патологического состояния, используя Пражские критерии. Забор биоптатов мы проводим в соответствии с официально принятым Сиетловским протоколом: слепая 4-х-квадрантная биопсия через каждый 1 см поверхности цилиндроклеточной метаплазии, а также прицельная биопсия из всех видимых патологически измененных участков слизистой.
Лечение пациентов с пищеводом Барретта
Принятая в НИИ онкологии им. Н.Н.Петрова тактика лечения и последующего динамического наблюдения пациентов с цилиндроклеточной метаплазией основана на рекомендациях Британского общества гастроэнтерологов по диагностике и лечению пищевода Барретта (2014 г) и Американской Гастроэнтерологической Ассоциации.
Все пациенты с метаплазией в нижней трети пищевода получают курс комплексной антирефлюксной терапии длительностью 4-8 недель, включающий в себя:
- регламентацию образа жизни (исключение физических перегрузок, последний прием пищи не позднее, чем за 3 часа до сна, частое дробное питание)
- диету (исключение острой, солёной, жареной пищи, газированных напитков и т.д.)
- медикаментозную антисекреторную терапию (ингибиторы протоновой помпы по 20 мг 2 раза в день), прокинетики и обволакивающие препараты.
Тактика лечения зависит прежде всего от результатов гистологического исследования материала, взятого из участков метаплазии, а также от протяженности сегмента метаплазии:
- Пациентам с цилиндроклеточной метаплазией протяженностью менее 3 см, без кишечной метаплазии и дисплазии рекомендуется курсовое медикаментозное лечение для коррекции причины заболевания – желудочно-пищеводного рефлюкса. Наблюдение не требуется. ЭГДС проводится с периодичностью 1 раза в 2-3 года.
- Пациентам с цилиндроклеточной метаплазией (без кишечной метаплазии) протяженностью сегмента 3 см и более, а также пациентам с доказанным пищеводом Барретта (без дисплазии по результатам двухкратной биопсии) вне зависимости от протяженности сегмента, мы рекомендуем выполнить аргоноплазменную абляцию очагов метаплазии.
- В отношении пациентов с пищеводом Барретта и выявленной дисплазией низкой степени тяжести мы применяем активную тактику лечения, которая заключается в эндоскопической резекции метаплазированного участка слизистой. Это позволяет снизить риск развития дисплазии высокой степени и аденокарциномы пищевода на 25% по сравнению с эндоскопическим наблюдением за 3-летний период.
- Пациенты с пищеводом Барретта и дисплазией высокой степени рассматриваются как пациенты с подтвержденным ранним раком кардиоэзофагеального перехода и подлежат оперативному лечению методом эндоскопической диссекции в подслизистом слое.
Аргоноплазменная абляция очагов метаплазии
Это метод разрушения участков изменённой слизистой оболочки с помощью тока высокой частоты, который передается на слизистую бесконтактным способом — через ионизированный электропроводящий газ аргон, а точнее, аргоновую плазму.
Аргоноплазменная абляция может осуществляться 2-мя способами:
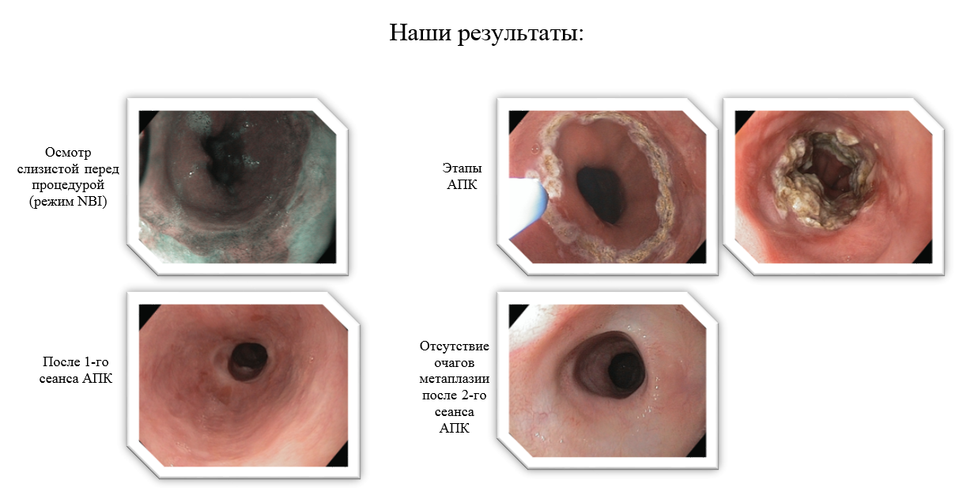
- Традиционным способом является аргоноплазменная коагуляция очагов метаплазии слизистой с помощью стандартного АПК-зонда. Выходящая из отверстия зонда струя плазмы образует на дистальном конце аргоновое облако, которое ионизируется подаваемым высокочастотным напряжением в несколько тысяч вольт до возникновения между наконечником зонда и поверхностью ткани аргоноплазменной дуги. По этой дуге энергия тока высокой частоты бесконтактно передается на подлежащий коагуляции участок ткани. Контролируемая глубина проникновения тепловой энергии составляет не более 3 мм, что исключает риск повреждения глубоких слоев стенки пищевода. При необходимости данная процедура выполняется несколько раз до достижения полной абляции очагов метаплазии.
- В европейских клиниках всё более распространённым становится гибридный метод аргоноплазменной коагуляции. С 2015 года он успехом стал применяться и на отделении эндоскопии НИИ онкологии им. Н.Н.Петрова.
С помощью гибридного водоструйного зонда (HybridAPC, «ERBE», Германия) выполняется инъекция физиологического раствора в подслизистый слой, далее этим же инструментом выполняется абляция метаплазированного эпителия. С помощью пластикового колпачка, предварительно монтированного на дистальном конце эндоскопа, выполняется очищение поверхности от образовавшегося струпа. При этом более отчетливо выявляются участки метаплазии, не подвергшиеся абляции. После чего производится дополнительная абляция этих очагов. Преимущество комбинированного метода перед стандартным в том, что вводимая в подслизистый слой жидкость защищает мышечный слой от термического воздействия. Это позволяет проводить аргоноплазменную коагуляцию на достаточно глубоком уровне и при большей мощности. Дальнейшее повреждение мышечной ткани, а также риск стриктуры будут исключены. Процедура может выполняться несколько раз, пока не будет достигнуто полное удаление очагов метаплазии.

Эндоскопическое лечение сопровождается антисекреторной терапией с помощью ингибиторов протоновой помпы для эффективного и быстрого заживления дефектов слизистой оболочки и создания условий для появления в этих зонах многослойного плоского эпителия пищевода.
Подготовка к процедуре
Процедура аргоноплазменной абляции очагов метаплазии проводится строго натощак, полностью исключается прием пищи за 12 часов и жидкости за 6 часов до начала процедуры
Необходима отмена пероральных антикоагулянтов (препаратов для разжижения крови) накануне исследования, пауза п/к введения гепарина за 4-6 часов до процедуры
Процедура абляции может быть выполнена под внутривенной анестезией. Если исследование будет проводиться под наркозом, прием любого количества жидкости до процедуры строго воспрещен. Управление транспортным средством после окончания исследования является нежелательным и может представлять угрозу для жизни и здоровья.
Источник
Хронический гастрит и рак желудка
Врачи
Рак желудка – одно из самых распространенных злокачественных заболеваний в мире, где оно занимает 5 место в структуре онкологических болезней и 2 место в структуре смертности от онкопатологии. В России рак желудка занимает пятое место в структуре заболеваемости злокачественными новообразованиями у мужчин и шестое место – у женщин.
Широкая распространенность этой болезни и низкий процент пятилетней выживаемости (в среднем по миру 10-20%) заставляет специалистов по всему миру активно искать алгоритмы своевременной диагностики не столько рака желудка, сколько предраковых заболеваний.
С учетом локализации поражения принято выделять два основных типа рака желудка: кардиальный (поражение кардиального отдела) и некардиальный рак (тело и/или выходной отдел желудка).
Хронический гастрит – маленький шаг на пути к раку желудка
Такое пугающее название подзаголовка достаточно точно отражает текущее понимание этапов развития рака желудка. Само заболевание «хронический гастрит» обычно не вызывает явных симптомов. А вот наличие типичных проявлений болезни, таких как боли в животе, чувство тяжести, переполнения после еды, тошнота – это симптомы функциональной диспепсии, до сих пор неверно определяемой не только пациентами, но даже врачами-гастроэнтерологами как хронический гастрит.
Итак, хронический гастрит – заболевание, которое не проявляется симптомами, а диагноз подтверждается только на основании гистологического исследования биоптатов желудка. Врач-морфолог, выполняющий исследование, может выявить воспаление в слизистой оболочке различной степени выраженности. Это и есть хронический гастрит.
У определенной части лиц длительное воспаление в слизистой желудка (хронический неатрофический гастрит) может привести к развитию атрофических изменений, а иногда клетки желудка могут замещаться нетипичными кишечными клетками (так называемая кишечная метаплазия).
Кишечная метаплазия повышает риск развития дисплазии – предракового заболевания, которое со временем может трансформироваться в аденокарциному (рак) желудка.
Эти этапы, сменяющие друг друга, – хронический гастрит без атрофии, атрофический гастрит, кишечная метаплазия, дисплазия, рак желудка – получили название «каскад Корреа» по имени автора, который описал данную последовательность.
Причины хронического гастрита
Поскольку воспалительные изменения в слизистой желудка, т.е. гастрит – начальные этапы развития рака желудка, попробуем разобраться, откуда же возникает это заболевание. Давно уже доказано, что нерегулярное питание, еда всухомятку и другие нарушения режима приема пищи не вызывают гастрит. Скорее, эти факторы могут способствовать обострению функциональной диспепсии. Тогда что же, образно выражаясь, подкидывает дрова в топку воспаления в слизистой оболочке желудка?
На сегодняшний день выделено несколько факторов, которые доказано вызывают развитие воспаления в желудке:
- инфекция, прежде всего инфекция Helicobacter pylori (H.pylori);
- аутоиммунное воспаление;
- воспаление в ответ на химическое повреждение (например, желчью при дуодено-гастральном рефлюксе).
Конечно, существуют и другие причины, но их вклад в развитие воспаления в желудке можно считать незначительным.
Инфекция H.pylori в настоящее время рассматривается как основной фактор, вызывающий развитие хронического гастрита. Около 44% населения земного шара инфицированы этим возбудителем. Известно, что распространенность атрофического гастрита на фоне инфекции H.pylori риска варьирует от 8% в Западных странах до 84% в Японии и Китае. H.pylori считается наиболее значимым фактором риска развития некардиального рака желудка.
Аутоиммунное воспаление встречается намного реже, однако также приводит к развитию хронического гастрита, нередко с атрофией, и ассоциировано с повышенным риском развития рака желудка.
Факторы риска развития аденокарциномы (рака) желудка
1) Наследственная предрасположенность.
Известно, что риск развития рака желудка у родственников первой степени родства (родители, дети) повышен в 2,3-3,5 раза. При указании на 2 и более случаев рака желудка у ближайших родственников этот риск возрастает в 5-12 раз. Риск выше в тех случаях, когда онкопатология желудка была выявлена у родственников в возрасте менее 50 лет.
2) Аутоиммунное поражение желудка с развитием пернициозной (В12-дефицитной) анемии.
Для аутоиммунного поражения желудка помимо развития атрофии характерно также разрушение внутреннего фактора (фактора Кастла), который обеспечивает нормальное всасывание витамина В12 в тонкой кишке. Установлено, что аутоиммунный гастрит повышает риск развития аденокарциномы (рака) желудка в 2-6,8 раз.
3) Этнические факторы.
Установлено, что риск развития рака желудка выше у азиатов по сравнению с белыми (в 2,1 раза) и лицами негроидной расы (в 1,7 раза). Среди лиц азиатской расы наибольший риск отмечен у китайцев (4,77) и корейцев (7,39). Нельзя исключить, что такое различие обусловлено в том числе высокой частотой инфекции H.pylori у этих лиц и генетическими особенностями.
4) Старший возраст.
Существуют доказательства того, что в разных возрастных группах риск развития рака желудка различается. «Пограничным» считается возраст старше 45 лет, после которого риск развития заболевания повышается в 1,92-3,1 раза. Вероятнее всего, такая взаимосвязь обусловлена длительностью инфицирования H.pylori и возникшего на этом фоне хронического воспаления
5) Мужской пол.
По данным исследований мужчины имеют больший риск развития аденокарциномы (рака) желудка по равнению с женщинами, при этом риск повышен в 1,3-3 раза.
6) Табакокурение.
Курильщики имеют повышенный риск развития рака желудка, локализованного в кардиальном отделе. Вероятность развития заболевания увеличивается в 1,45-2 раза по данным разных исследований.
7) Инфекция H.pylori.
По всей видимости, это наиболее «весомый» фактор риска развития рака желудка, учитывая широкую распространенность этой инфекции по всему миру. Исследования показали, что риск развития некардиального рака желудка у инфицированных лиц увеличен в 12 раз. Примерно у 1% из них в течение жизни развивается аденокарцинома желудка. Риск развития рака кардиального отдела желудка не повышается.
8) Полипы желудка.
Полипы желудка делятся на 3 вида: полипы фундальных желез, гиперпластические полипы и аденоматозные полипы. В полипах фундальных желез размерами более 1 см редко, но выявляет дисплазия и рак (с частотой по 1,9%, соответственно). Для гиперпластических полипов больших (>1 см) размеров характерно нередкое выявление дисплазии (1,9-19%) и, реже злокачественное перерождение (0,6-2,1%). Аденоматозные полипы значительно повышают риск развития аденокарциномы желудка, а при размерах полипов >2 см частота выявления в них аденокарцином достигает по некоторым данным 50%.
9) Атрофический гастрит.
Поскольку атрофический гастрит является одним из этапов в «каскаде Корреа» (см.выше), проводилась оценка риска его трансформации в рак желудка. Согласно современным данным, ежегодный риск перехода атрофического гастрита в рак желудка составляет 0,1-1,2%. Частота выявления рака желудка у пациентов с атрофией в течение 5 лет варьирует от 0,7% (для слабо выраженной атрофии) до 10% (тяжелая атрофия).
10) Кишечная метаплазия.
Как и атрофический гастрит, кишечная метаплазия является одним из этапов «каскада Корреа» на пути к развитию рака желудка. Ежегодный риск перехода кишечной метаплазии в рак желудка составляет 0,25-0,4%. Частота выявления рака желудка у пациентов с кишечной метаплазией в течение 5 лет составляет 5,3-9,8%.
11) Дисплазия.
Дисплазия (предраковое состояние) делится на два типа: низкой и высокой степени. Дисплазия низкой степени имеет ежегодный риск трансформации в рак желудка 0,6%, в то время как для высокой степени – 6%.
Частота выявления рака желудка у пациентов с дисплазией низкой степени в течение 5 лет составляет 0-23%, высокой степени – 60-85%.
Рекомендации по профилактике развития аденокарциномы (рака) желудка
В течение 2019 года были опубликованы рекомендации по диагностике и лечению пациентов с высоким риском аденокарциномы (рака) желудка сразу двумя группами авторов: Британским обществом гастроэнтерологов и коллегией ученых, представленных членами Европейского общества гастроинтестинальной эндоскопии, Европейской группы по изучению Helicobacter pylori и микробиоты, Европейского общества патологов и Португальского общества гастроинтестинальной эндоскопии (т.н. международные рекомендации по лечению предраковых состояний и изменений желудка второго пересмотра (MAPS II). Были даны рекомендации по недопущению развития и своевременному выявлению грозной болезни – рака желудка.
Итак, каковы же рекомендации в отношении профилактики развития рака желудка?
1) Пациенты с хроническим атрофическим гастритом или кишечной метаплазией подвержены риску развития рака желудка.
Комментарий: Наибольший риск отмечается при выявлении атрофии/кишечной метаплазии одновременно в антральном отделе и теле желудка.
2) Лица, проживающие в регионах с высокой частотой рака желудка должны быть тестированы на инфекцию H.pylori.
Комментарий: следует использовать достоверные методы диагностики, включающие дыхательный тест с С13 меченой мочевиной, определение антигена H.pylori в кале или антител к H.pylori класса IgG в крови. Россия относится к регионам с высокой распространенностью рака желудка.
3) Лицам без симптомов в возрасте ≥50 лет с множественными факторами риска (мужской пол, курение табака, наследственность по раку желудка и т.д.) следует проводить скрининговую гастроскопию.
Примечание: скрининг в медицине – это комплекс мероприятий, направленных на выявление заболевания, которое себя никак не проявляет. В данном случае речь идет о проведении гастроскопии лицам без симптомов рака желудка.
Очень важно! Существует несколько видов наследственного рака желудка, для которого характерно более раннее появление (в возрасте до 40 лет).
4) Лицам с высоким риском развития рака желудка (включая гастрит с атрофией и кишечной метаплазией) необходимо проведение регулярной гастроскопии с фотофиксацией и гистологическим исследованием.
Комментарий: согласно данным зарубежных исследований, рак желудка оказывается невыявленным при проведении гастроскопии в 6-11% случаев. Очень важной является медленный осмотр слизистой оболочки желудка и фиксация изображений (фотографии, видеозапись), что позволяет увеличить выявление раннего рака желудка. В клинике «Эксперт» ведется видеозапись всех эндоскопических исследований желудочно-кишечного тракта на обязательной основе.
5) Пациентам с распространенной атрофией и кишечной метаплазией (вовлечение антрального отдела и тела желудка) показана регулярная гастроскопия с биопсией.
Комментарий: частота гастроскопий зависит от многих факторов, включая случаи рака желудка в семье, сохранение инфекции H.pylori, несмотря на адекватное лечение, и т.д.
6) Лицам, имеющим хронический гастрит или гастрит с атрофией на фоне H.pylori, должна быть проведена эрадикационная терапия инфекции.
Комментарий: профилактика развития рака желудка наиболее эффективна в тех случаях, когда пациента начинали лечить от инфекции H.pylori на этапе выявления неатрофического гастрита или гастрита с атрофией.
7) Лечение инфекции H.pylori может быть эффективной мерой в отношении профилактики развития рака желудка у части пациентов, которые уже имеют кишечную метаплазию, дисплазию или рак желудка.
Комментарий: лечение инфекции H.pylori у пациентов с кишечной метаплазией и дисплазией, а также у лиц с удаленной эндоскопическим методом аденокарциномой желудка снижает риск развития/повторного развития рака желудка. Однако профилактический эффект от лечения на этих этапах меньший, чем при хроническом неатрофическом или атрофическом гастрите.
Заключение
Своевременная и адекватная по объему диагностика на этапе «простого гастрита», т.е. до развития атрофии/метаплазии/дисплазии позволяет определиться с рисками развития онкопатологии желудка, подобрать верную тактику, позволяющую избежать развития грозного заболевания.
Источник