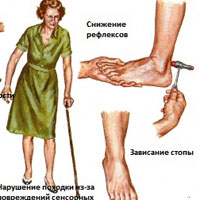
Полинейропатия
Периферическая нервная система передает информацию от головного и спинного мозга (центральной нервной системы) к остальным частям тела. Периферическая нейропатия может быть результатом травматических повреждений, инфекций, нарушения обмена веществ, наследственных причин и воздействия токсинов. Одной из наиболее распространенных причин полинейропатии является сахарный диабет.
Пациенты с периферической нейропатией обычно описывают боли, как ощущения покалывания или жжения. Во многих случаях, симптомы снижаются, если возникает компенсация основного заболевания.
Каждый нерв в периферической нервной системе имеет определенную функцию, так что симптомы зависят от типа нервов, которые оказались повреждены. Нервы подразделяются на:
- Чувствительные нервы, которые получают ощущения от кожи, такие как температура, боли, вибрации или давление
- Двигательные (моторные) нервы, которые контролируют движения мышц
- Вегетативные нервы, которые контролируют такие функции, как кровяное давление, частота сердечных сокращений, пищеварение и функцию мочевого пузыря
Симптомы
Симптомы полинейропатии, могут включать:
- Постепенное появление онемения и покалывание в ногах или руках, которые могут распространяться вверх по рукам и ногам
- Острая колющая или жгучая боль
- Повышенная чувствительность к прикосновениям
- Отсутствие координации и падения
- Мышечная слабость или паралич, если повреждены двигательные нервы
Если задействованы вегетативные нервы, симптомы могут включать:
- Непереносимость жары, а также изменение потоотделения
- Проблемы с пищеварением, мочевым пузырем или кишечником
- Изменения артериального давления, в результате чего могут появиться головокружение
Причины
Ряд факторов может привести к развитию невропатии, в том числе:
- Алкоголизм. Скудная диета может привести к дефициту витаминов.
- Аутоиммунные заболевания. Они включают такие заболевания как синдром Шегрена, системная красная волчанка, ревматоидный артрит, синдром Гийена-Барре, хроническая воспалительная демиелинизирующая полинейропатия и некротический васкулит.
- Диабет. Более чем у половины пациентов с диабетом развиваются некоторые типы нейропатии.
- Воздействие ядов. Токсичные вещества включают в себя тяжелые металлы или химикаты.
- Лекарства. Некоторые лекарства, особенно те, что используются для лечения рака (химиотерапия), могут привести к развитию периферической невропатии.
- Инфекции. К ним относятся некоторые вирусные или бактериальные инфекции, в том числе болезнь Лайма, опоясывающий лишай, вирус Эпштейна-Барр, гепатит С, проказа, дифтерия и ВИЧ.
- Наследственные заболевания. Например такое заболевание как болезнь Шарко-Мари-является наследственным типом нейропатии.
- Травма или компрессия на нерв. Травмы, такие как дорожно-транспортные происшествия, падения или спортивные травмы, могут повредить или даже привести к разрыву периферических нервов. Компрессия нерва может возникать при постоянном воздействии на периферические нервы.
- Опухоли. Злокачественные и доброкачественные опухоли могут повреждать нервы или оказывать давление на них.
- Дефицит витаминов. Витамины группы В, в том числе B-1, B-6 и B-12, витамин Е и ниацин имеют большое значение для нервов.
- Заболевания костного мозга. Они включают в себя наличие аномального белка в крови (моноклональные гаммопатии), миеломная болезнь, лимфома и амилоидоз.
- Другие заболевания. К ним относятся заболевания почек, заболевания печени, заболевания соединительной ткани и щитовидной железы (гипотиреоз).
Осложнения полинейропатии могут включать
- Ожоги и травмы кожи. Если есть онемение частей тела пациент не может чувствовать изменения температуры или боль.
- Инфекции. Ноги и другие области тела со сниженной чувствительностью могут незаметно повреждаться. Необходимо следить за целостностью кожных покровов, особенно если есть сахарный диабет так как даже незначительные повреждения кожи могут приводить к инфицированию тканей.
Диагностика
Врача при диагностике полинейропатии, в первую очередь, могут интересовать ответы на следующие вопросы
- Есть ли у пациента соматические заболевания, такие как диабет или заболевания почек?
- Когда появились симптомы?
- Были ли симптомы были постоянными или возникали эпизодически?
- Насколько выражены симптомы?
- Что приводит к увеличению или снижению симптомов?
- Были ли аналогичные симптомы у кого – то в семье пациента?
- Врачу необходима полная медицинская история болезни. Врач рассмотрит историю болезни, в том числе симптомы, образ жизни пациента, воздействие токсинов, наличие вредных привычек и семейную историю неврологических заболеваний.
- При неврологическом обследовании врач может проверить сухожильные рефлексы, силу и тонус мышц, способность чувствовать определенные ощущения, и координацию.
Врач может назначить обследование
- Методы визуализации КТ или МРТ могут выявить различные заболевания (в том числе опухоли).
- Нейрофизиология. Электромиография записывает электрическую активность в мышцах, что позволяет определить, вызваны ли симптомы, в том числе слабость, повреждением мышечной ткани или повреждением нерва. ЭНМГ проверяет проведения импульса по нервам и позволяет определить степень повреждения нервных волокон. Могут быть также проведены нейрофизиологические исследования вегетативной нервной системы — сенсорные тесты, которые регистрируют, как пациент чувствует касание, вибрацию, холод и тепло.
- Биопсия нерва. Врач может рекомендовать удаление небольшой части нерва, обычно чувствительного нерва, чтобы изучить морфологические изменения в нерве для того, чтобы определить причину повреждения нерва.
- Биопсия кожи. При этом исследовании удаляется небольшая часть кожи для исследования количества нервных окончаний. Снижение количества нервных окончаний свидетельствует о невропатии.
- Лабораторные методы исследования необходимы для исключения различных заболеваний, таких как сахарный диабет, аутоиммунные заболевания болезни почек и Т.Д.
Лечение
Целью лечения полинейропатии является лечение основного заболевания и минимизация симптомов. Если лабораторные тесты и другие методы обследования указывают на отсутствие основного заболевания, врач может рекомендовать выжидательную тактику, для того чтобы увидеть, есть самостоятельное уменьшение симптомов нейропатии. Если есть воздействие токсинов или алкоголя, врач будет рекомендовать избегать этих веществ.
Медикаментозное лечение
Лекарства, используемые для облегчения болей при полинейропатии включают в себя:
- Обезболивающие, такие как парацетамол или из группы НПВС снижают болевые проявления
- Лекарства, содержащие опиоиды, такие как трамадол (Conzip, Ultram ER и другие) или оксикодон (Oxycontin, Roxicodone и другие), могут привести к развитию зависимости и наркомании, так что эти препараты, как правило, назначают только тогда, когда другие методы лечения не оказывают эффекта.
- Противосудорожные. Медикаменты, такие как габапентин (Gralise, Neurontin) и прегабалин (Лирика), синтезированные для лечения эпилепсии, могут значительно снижать боль при нейропатии. Побочные эффекты этих препаратов могут включать сонливость и головокружение.
- Капсаицин. Крем, содержащий это вещество (в природе встречается в остром перце) может применяться для некоторого облегчения симптомов нейропатии. Но учитывая раздражающее действие капсаицина на кожу не все пациенты могут терпеть действие кремов с капсаицином.
- Антидепрессанты. Некоторые трициклические антидепрессанты, такие как амитриптилин, доксепин и нортриптилин (Pamelor), могут применяться для уменьшения болей при нейропатии через воздействия на центральную нервную систему.
- Ингибитор серотонина и обратного захвата норадреналина дулоксетин (Cymbalta) и антидепрессант венлафаксин (Effexor XR), также могут облегчить боль при периферической нейропатии, вызванной диабетом. Побочные эффекты могут включать сухость во рту, тошноту, сонливость, головокружение, снижение аппетита и запор.
- Внутривенное введение иммуноглобулина является основой лечения хронической воспалительной демиелинизирующей полинейропатии и других воспалительных нейропатий.
- Альфа-липоевая кислота. Используется для лечения периферической невропатии в Европе в течение многих лет. Этот антиоксидант помогает уменьшить симптомы. Прием альфа-липоевой кислота необходимо обсудить с врачом, потому он может повлиять на уровень сахара в крови. Другие побочные эффекты могут включать желудочные расстройства и сыпь на коже.
- Травы. Некоторые травы, такие как масла энотеры, может помочь уменьшить нейропатическую боль у пациентов с диабетом.
- Аминокислоты. Аминокислоты, такие как ацетил-L-карнитин, может помочь улучшить симптоматику периферической нейропатии у пациентов, перенесших химиотерапию и у пациентов с сахарным диабетом. Побочные эффекты могут включать тошноту и рвоту.
Кроме медикаментозного лечения могут применяться и другие методы лечения.
- Миостимуляция позволяет в определенной степени восстановить проведение нервно импульса по мышцам.
- Плазмаферез и внутривенное введение иммуноглобулина.
- ЛФК. При наличии мышечной слабости физические нагрузки позволяет улучшить силу и тонус мышц. Регулярные физические упражнения, такие как ходьба три раза в неделю, могут уменьшить боль при нейропатии, улучшить мышечную силу и помогают контролировать уровень сахара в крови. Гимнастики, такие как йога и тай-чи также могут быть достаточно эффективны.
- Акупунктура. Воздействие на биологически активные точки позволяет улучшить чувствительность нервных рецепторов и снизить болевые проявления.
Источник
Нейропатическая боль
В статье описаны клинические подходы к диагностике нейропатической боли, приведены Британские рекомендации по лечению нейропатической боли в общесоматической практике и возможности повышения эффективности терапии, в частности рациональное использование комплекса витаминов В в комбинации с габапептиноидами.
Причиной центральной нейропатической боли может являться инсульт, спинальная травма, рассеянный склероз. Нейропатические боли часто ассоциированны с сахарным диабетом, хроническим приемом алкоголя, дефицитом витаминов, хронической болью в спине, радикулярной болью, онкологическими заболеваниями.
Но зачастую конкретная причина нейропатической боли может быть не установлена даже после обследования в специализированном центре.
Поэтому нейропатическая боль может быть разделена на две категории: 1) Хроническое болевое расстройство с нейропатическими характеристиками. 2) Нейропатическая боль, связанная с определенным состоянием.
Нейропатическая боль — это особо тяжёлый вариант хронической боли, проявляющийся интенсивными жгучими или простреливающими болями, продолжающимися в течение длительного времени, до нескольких месяцев. Боль может усиливаться ночью в покое. Пациенты описывают боль как, как жжет, горит, ноет, скребет, дергает, бьет током.
Эти боли возникать спонтанно, т. е. не связанно с обычными провоцирующими факторами (движение, прикосновение к болевой зоне), болевых или других неприятных ощущений (дизестезия). Боль может сопровождается набором чувствительных расстройств, таких как парестезии (покалывание, ползание мурашек), гипералгезия (избыточный ответ на обычный болевой стимул) и аллодиния. Аллодиния – это когда пациент испытывает болевые ощущения в ответ на неболевые раздражения, когда простое легкое прикосновение, холод или тепло приводят к появлению или усилению боли. Аллодиния может быть настолько выражена, что даже прикосновение одежды является очень мучительным для пациента. Даже малейшего ветерка достаточно, чтобы вызвать боль.
У пациентов в зоне болевых ощущений или рядом могут располагаться участки пониженной чувствительности (гипостезия). Эти симптомы свидетельствуют о повреждении и/или гибели отдельных нервных волокон. Гипостезия является частым, но не обязательным симптомом нейропатической боли. При осмотре в зоне болевых ощущений можно выявить трофические изменения: истончение кожи, подкожной клетчатки, нарушение роста волос, ногтей, сухость кожных покровов, изменения дермографизма, цвета и температуры кожи, что свидетельствует о вовлечении в процесс вегетативных волокон.
Боль всегда сопровождается негативными эмоциями. Психопатологические последствия нейропатической боли включают симптомы нарушения настроения, тревоги [2]. Распространенность депрессивных и тревожных расстройств у пациентов с нейропатической болью как минимум в два раза превосходит этот показатель в общей популяции.
Боль вызывает негативные эмоции, которые приводят к изменению порога болевой чувствительности. Это в свою очередь ведет к персистированию болевых симптомов. Депрессия и тревога воздействуют на механизмы формирования и поддержания боли, являются важными модуляторами боли, усиливают интенсивность боли, увеличивают поверхность распространения болевых ощущений. И, наконец, депрессия является независимым фактором нарушения трудоспособности и социальной адаптации у лиц, страдающих хроническим болевым расстройством. У пациентов с нейропатической болью и депрессией качество жизни ниже, а интенсивность боли выше. Около 50%–80% пациентов, страдающих нейропатической болью, имеют нарушения сна с дневными последствиями: усталость, сонливость, нарушение концентрации внимания. Снижается общая эффективность сна. Бессонница также может быть дополнительным фактором риска для развития депрессии и других психопатологических состояний. Таким образом, нейропатическая боль сопряжена с инсомнией и тревожно-депрессивными расстройствами, которые утяжеляют картину боли.
Ученые признают базисные универсальные механизмы, лежащие в основе нейропатической боли, независимо от природы повреждения. Поврежденные нервные волокна претерпевают функциональные изменения, вследствие чего непрерывно посылают неправильные сигналы в другие болевые центры. Изменения, обусловливающие развитие нейрогенного болевого синдрома, происходят как на периферическом уровне, так и в ЦНС.
Лечение нейропатической боли
В начале терапии болевого синдрома, сначала по возможности возможности следует устраненить этиологический фактор. Однако лечение основного заболевания и даже его полное купирование не всегда приводят к исчезновению болевого синдрома. Поэтому собственно боль рассматривается врачом как целевая мишень для терапии, не зависящая от природы повреждения. Перед началом терапии проводится разъяснительная беседа с больным и его родственниками суть которой заключается в том, что лечение может быть длительным, и уменьшение боли будет происходить постепенно. Даже при правильной программе лечения редко удается достичь полного обезболивания. Хорошим результатом считается снижение интенсивности боли на 30%–50% от исходного уровня. Этот параметр следует иметь в виду при оценке эффективности проводимого лечения и решении вопросов о переходе на другой препарат или присоединении нового лекарства к уже принимаемому препарату.
Британские рекомендации по лечению нейропатической боли в общеврачебной практике 2013 г, модернизированные в 2017 г., предлагают в качестве начальной терапии для нейропатической боли любого происхождения, за исключением тригеминальной невралгии, выбор из следующих препаратов: амитриптилин, дулоксетин, габапентин или прегабалин [9]. Из перечисленных препаратов наилучшей переносимостью обладают габапептиноиды (прегабалин, габапентин). Эти препараты характеризуются практически полным отсутствием лекарственных взаимодействий и сравнительно невысокой частотой развития нежелательных явлений. Пациентом с локализованной нейропатической болью на начальном этапе лечения альтернативно можно рекомендовать средства для наружного применения, содержащие капсаицин. Если первоначальное лечение не является эффективным или плохо переносится пациентом, нужно перевести пациента на альтернативную монотерапию препаратом первого ряда или предложить пациенту комбинацию из двух препаратов разных классов. Неэффективное первоначальное лечение требует консультации со специалистом (невролог, альголог) для обсуждения вопроса о назначении препаратов второй линии (лакосамид, ламотриджин, леветирацетам, окскарбазепин, топирамат, венлафаксин, трамадол).
Комбинированная терапия обычно считаются более эффективной, чем монотерапия, но неясно, какие комбинации лучше. Очень мало рандомизированных исследований, посвященных комбинированной терапии нейропатической боли. Но по факту комбинированная терапия используется чрезвычайно широко. К самым часто используемым дополнительным средствам относят Acetyl-L-carnitine, витамины группы В, альфа-липоевая кислота, магнезия [10]. Витамины B1, B6 и B12 действуют в основном как коферменты различных реакций, участвуя в метаболизме углеводов, белков и липидов. Они также играют важную роль в формировании новых клеток, ДНК, РНК и миелина. Абсолютным показанием для их назначения являются состояния, вызванные дефицитом этих витаминов. Дефицит витамина B12 часто наблюдается у пациентов, принимающих метформин, что требует назначения витамина B12 в ежедневной дозе 1000 мкг. Бенфотиамин (жирорастворимая форма тиамина- вит. В1) считается наилучшим вариантом, потому что он лучше проникает через мембраны клетки.
Учет международного и Российского опыта позволяет рекомендовать в качестве инициальной терапии нейропатической боли габапентин (Габагамма) в комбинации с нейротропной терапией Мильгамма в/м №10, с последующим переходом на Мильгамму композитум по 1 драже 3 раза в день шесть недель. Целевая доза габапентина составляет 900 мг/сут., разделенная на 3 приема. При необходимости через 2–4 недели дозу увеличивают.
Лечение нейропатической боли на сегодняшний день продолжает оставаться сложной задачей. Представленные выше принципы и схемы лечения помогают врачу проводить наиболее эффективное и безопасное лечение пациентов с нейропатическим болевым синдромом. Однако, при недостаточной эффективности первоначальной терапии, они не могут заменить индивидуальные консультации со специалистами в конкретных случаях.
Причиной центральной нейропатической боли может являться инсульт, спинальная травма, рассеянный склероз. Нейропатические боли часто ассоциированны с сахарным диабетом, хроническим приемом алкоголя, дефицитом витаминов, хронической болью в спине, радикулярной болью, онкологическими заболеваниями.
Но зачастую конкретная причина нейропатической боли может быть не установлена даже после обследования в специализированном центре.
Поэтому нейропатическая боль может быть разделена на две категории: 1) Хроническое болевое расстройство с нейропатическими характеристиками. 2) Нейропатическая боль, связанная с определенным состоянием.
Нейропатическая боль — это особо тяжёлый вариант хронической боли, проявляющийся интенсивными жгучими или простреливающими болями, продолжающимися в течение длительного времени, до нескольких месяцев. Боль может усиливаться ночью в покое. Пациенты описывают боль как, как жжет, горит, ноет, скребет, дергает, бьет током.
Эти боли возникать спонтанно, т. е. не связанно с обычными провоцирующими факторами (движение, прикосновение к болевой зоне), болевых или других неприятных ощущений (дизестезия). Боль может сопровождается набором чувствительных расстройств, таких как парестезии (покалывание, ползание мурашек), гипералгезия (избыточный ответ на обычный болевой стимул) и аллодиния. Аллодиния – это когда пациент испытывает болевые ощущения в ответ на неболевые раздражения, когда простое легкое прикосновение, холод или тепло приводят к появлению или усилению боли. Аллодиния может быть настолько выражена, что даже прикосновение одежды является очень мучительным для пациента. Даже малейшего ветерка достаточно, чтобы вызвать боль.
У пациентов в зоне болевых ощущений или рядом могут располагаться участки пониженной чувствительности (гипостезия). Эти симптомы свидетельствуют о повреждении и/или гибели отдельных нервных волокон. Гипостезия является частым, но не обязательным симптомом нейропатической боли. При осмотре в зоне болевых ощущений можно выявить трофические изменения: истончение кожи, подкожной клетчатки, нарушение роста волос, ногтей, сухость кожных покровов, изменения дермографизма, цвета и температуры кожи, что свидетельствует о вовлечении в процесс вегетативных волокон.
Боль всегда сопровождается негативными эмоциями. Психопатологические последствия нейропатической боли включают симптомы нарушения настроения, тревоги [2]. Распространенность депрессивных и тревожных расстройств у пациентов с нейропатической болью как минимум в два раза превосходит этот показатель в общей популяции.
Боль вызывает негативные эмоции, которые приводят к изменению порога болевой чувствительности. Это в свою очередь ведет к персистированию болевых симптомов. Депрессия и тревога воздействуют на механизмы формирования и поддержания боли, являются важными модуляторами боли, усиливают интенсивность боли, увеличивают поверхность распространения болевых ощущений. И, наконец, депрессия является независимым фактором нарушения трудоспособности и социальной адаптации у лиц, страдающих хроническим болевым расстройством. У пациентов с нейропатической болью и депрессией качество жизни ниже, а интенсивность боли выше. Около 50%–80% пациентов, страдающих нейропатической болью, имеют нарушения сна с дневными последствиями: усталость, сонливость, нарушение концентрации внимания. Снижается общая эффективность сна. Бессонница также может быть дополнительным фактором риска для развития депрессии и других психопатологических состояний. Таким образом, нейропатическая боль сопряжена с инсомнией и тревожно-депрессивными расстройствами, которые утяжеляют картину боли.
Ученые признают базисные универсальные механизмы, лежащие в основе нейропатической боли, независимо от природы повреждения. Поврежденные нервные волокна претерпевают функциональные изменения, вследствие чего непрерывно посылают неправильные сигналы в другие болевые центры. Изменения, обусловливающие развитие нейрогенного болевого синдрома, происходят как на периферическом уровне, так и в ЦНС.
Лечение нейропатической боли
В начале терапии болевого синдрома, сначала по возможности возможности следует устраненить этиологический фактор. Однако лечение основного заболевания и даже его полное купирование не всегда приводят к исчезновению болевого синдрома. Поэтому собственно боль рассматривается врачом как целевая мишень для терапии, не зависящая от природы повреждения. Перед началом терапии проводится разъяснительная беседа с больным и его родственниками суть которой заключается в том, что лечение может быть длительным, и уменьшение боли будет происходить постепенно. Даже при правильной программе лечения редко удается достичь полного обезболивания. Хорошим результатом считается снижение интенсивности боли на 30%–50% от исходного уровня. Этот параметр следует иметь в виду при оценке эффективности проводимого лечения и решении вопросов о переходе на другой препарат или присоединении нового лекарства к уже принимаемому препарату.
Британские рекомендации по лечению нейропатической боли в общеврачебной практике 2013 г, модернизированные в 2017 г., предлагают в качестве начальной терапии для нейропатической боли любого происхождения, за исключением тригеминальной невралгии, выбор из следующих препаратов: амитриптилин, дулоксетин, габапентин или прегабалин [9]. Из перечисленных препаратов наилучшей переносимостью обладают габапептиноиды (прегабалин, габапентин). Эти препараты характеризуются практически полным отсутствием лекарственных взаимодействий и сравнительно невысокой частотой развития нежелательных явлений. Пациентом с локализованной нейропатической болью на начальном этапе лечения альтернативно можно рекомендовать средства для наружного применения, содержащие капсаицин. Если первоначальное лечение не является эффективным или плохо переносится пациентом, нужно перевести пациента на альтернативную монотерапию препаратом первого ряда или предложить пациенту комбинацию из двух препаратов разных классов. Неэффективное первоначальное лечение требует консультации со специалистом (невролог, альголог) для обсуждения вопроса о назначении препаратов второй линии (лакосамид, ламотриджин, леветирацетам, окскарбазепин, топирамат, венлафаксин, трамадол).
Комбинированная терапия обычно считаются более эффективной, чем монотерапия, но неясно, какие комбинации лучше. Очень мало рандомизированных исследований, посвященных комбинированной терапии нейропатической боли. Но по факту комбинированная терапия используется чрезвычайно широко. К самым часто используемым дополнительным средствам относят Acetyl-L-carnitine, витамины группы В, альфа-липоевая кислота, магнезия [10]. Витамины B1, B6 и B12 действуют в основном как коферменты различных реакций, участвуя в метаболизме углеводов, белков и липидов. Они также играют важную роль в формировании новых клеток, ДНК, РНК и миелина. Абсолютным показанием для их назначения являются состояния, вызванные дефицитом этих витаминов. Дефицит витамина B12 часто наблюдается у пациентов, принимающих метформин, что требует назначения витамина B12 в ежедневной дозе 1000 мкг. Бенфотиамин (жирорастворимая форма тиамина- вит. В1) считается наилучшим вариантом, потому что он лучше проникает через мембраны клетки.
Учет международного и Российского опыта позволяет рекомендовать в качестве инициальной терапии нейропатической боли габапентин (Габагамма) в комбинации с нейротропной терапией Мильгамма в/м №10, с последующим переходом на Мильгамму композитум по 1 драже 3 раза в день шесть недель. Целевая доза габапентина составляет 900 мг/сут., разделенная на 3 приема. При необходимости через 2–4 недели дозу увеличивают.
Лечение нейропатической боли на сегодняшний день продолжает оставаться сложной задачей. Представленные выше принципы и схемы лечения помогают врачу проводить наиболее эффективное и безопасное лечение пациентов с нейропатическим болевым синдромом. Однако, при недостаточной эффективности первоначальной терапии, они не могут заменить индивидуальные консультации со специалистами в конкретных случаях.
Источник