- Инновационный подход к лечению хеликобактерной инфекции желудка детей и взрослых
- Неэффективность традиционного лечения
- Почему при лечении хеликобактера отказываются от антибиотиков
- Лечение хеликобактер пилори по-новому
- Как выбрать пробиотик для лечения хеликобактера
- Кому показано лечение пробиотиками
- Хелинорм – инновационное антихеликобактерное средство из группы метаболиков
- Принцип действия
- Схема лечения
- Советы Британского общества гастроэнтерологов в отношении Helicobacter pylori
- Общая информация о Helicobacter pylori
- Медицинские советы
- Helicobacter pylori и грибы рода Candida: что их объединяет у гастроэнтерологического больного
Инновационный подход к лечению хеликобактерной инфекции желудка детей и взрослых
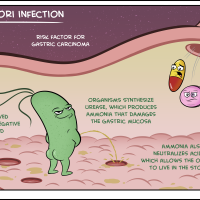
Лечение хеликобактер пилори — одна из наиболее частых забот врача-гастроэнтеролога, а Хеликобактер пилори — один из наиболее «популярных» микроорганизмов, широко изучаемых во многих странах с 1983 года. Заражение, бывает, происходит в детском возрасте и многие годы он может никак не проявлять себя. Установлено, что хеликобактер выявляется у 30-35% детей и у 50-85% взрослого населения. Хеликобактер пилори считается причиной заболеваний желудка, таких как, гастрит, язвенная болезнь, онкология желудка.
Неэффективность традиционного лечения
- нечувствительность хеликобактера к антибиотикам,
- большое количество побочных эффектов на прием ИПП и антибиотиков,
- активное нежелание пациентов принимать антибиотики.
Стандарты лечения регламентируются международными и российскими соглашениями, в основе которых лежит курс лечения с назначением препаратов, снижающих кислотность желудочного сока (антисекреторные препараты – ИПП, например, Омез, Париет и др.), двух антибиотиков (например, Клацид и Амоксициллин).
Лечение хеликобактерной инфекции в любой возрастной категории сопровождается большим количеством побочных, нежелательных реакций на применяемые препараты и то, что их применение не исключает повторения инфекции или повторного заражения препараты-ИПП).
Почему при лечении хеликобактера отказываются от антибиотиков
Нечувствительность хеликобактера к антибиотикам приводит к уменьшению эффективности лечения – отмечено снижение эффективности с 80-90% до 30-60%, что является характерным для многих стран, для различных регионов в России.
Сегодня стоит еще раз напомнить о побочных эффектах применения антисекреторных препаратов и антибиотиков.
Так, при приеме антисекреторных препаратов (ИПП) нарушаются процессы переваривания пищи и всасывания кальция, железа, цинка, лекарственных препаратов при приеме внутрь. При длительном применении ИПП существует риск развития инфекций желудочно-кишечного тракта и легких, т. к. в желудок попадают микроорганизмы из ротовой полости, носоглотки, кишечника. Если они не инактивируются в условиях сниженной желудочной секреции, то некоторые из них могут вырабатывать вещества (канцерогены), которые могут вызывать онкологические заболевания. Длительный прием препаратов, снижающих желудочную секрецию, может привести к
- поносам, вызванным микроорганизмом клостридией,
- грибковому поражению желудочно-кишечного тракта,
- воспалению легких,
- перелому шейки бедра.
Применение антибиотиков в лечении различных заболеваний и, в том числе, хеликобактериозе, несколько ограничено при наличии заболеваний печени, почек, нарушений микрофлоры кишечника, аллергии на антибиотики
Лечение антибиотиками может привести к развитию антибиотико-ассоциированного поноса, ухудшению пищеварения, вызвать дисепсические жалобы – тошноту, рвоту, изменение вкуса, нередко головную боль. Особенно это характерно для пожилых людей. Кроме того, могут развиваться аллергические реакции, вплоть до формирования поливалентной аллергии. Эти побочные эффекты, знакомые нашим пациентам, заставляют многих отказаться от приема антибиотиков из-за риска их развития.
К сожалению, официальные стандарты-IV Маастрихтского соглашения продолжают рекомендовать применение этих схем, однако…
Лечение хеликобактер пилори по-новому
В последние годы официальные стандарты-IV Маастрихтского соглашения пополнились применением препаратов висмута (Денол), пробиотиком Saccharomyces boulardii (препарат Энтерол) – тропического штамма дрожжевых грибов, выделенных из сока личи и манго.
Наиболее перспективным направлением оптимизации лечения хеликобактериоза желудка являлось использование пробиотиков, в первую очередь, лактобацилл в виде монотерапии. Исследования, проведенные российскими, зарубежными учеными и собственные данные подтверждают эффективность пробиотиков для эрадикации хеликобактер пилори. Опыт показал, что применение молочно-кислых бактерий, лактобацилл ацидофилюс, сочетание нескольких штаммов лактобацилл (Трилакт), позволило получить достаточно высокий процент положительных результатов, (39 — 54%) у детей и взрослых. При таком подходе к лечению встает вопрос, какой пробиотик выбрать, при каких заболеваниях желудка и других ситуациях применить, в каком возрасте, какова продолжительность курса.
Как выбрать пробиотик для лечения хеликобактера
Важным условием применения пробиотика является кислотоустойчивость штамма живых микроорганизмов, которая доказана в отношении группы лактобацилл (L.rbamnosus, L.reuteri, L.plantarum, L.acidophilus, способных оказывать прямое действие на хеликобактер пилори. Эти штаммы лактобацилл вырабатывают вещества (метаболиты), которые подавляют рост, обладают антибактериальным действием, снижают активность ферментов хеликобактерий и других микроорганизмов, уменьшают воспаление слизистой оболочки желудка.
Кому показано лечение пробиотиками
Лечение хеликобактерной инфекции с применением только пробиотиков показано:
- лицам, у кого в анамнезе аллергия к антибиотикам,
- при категорическом отказе пациента от приема антибиотиков,
- лицам при выявленном хеликобактериозе без клинических проявлений и жалоб,
- членам семьи пациентов, инфицированных хеликобактером,
- пациентам с хроническим гастродуоденитом, язвенной болезнью вне обострения,
- пожилым людям,
- детям,
- лицам, имеющим поражения печени и почек.
Дальнейшие исследования показали, что положительно действуют не только пробиотики на основе живых микроорганизмов, но и продукты их метаболизма (обмена). На основе этого открытия был разработан в 2014 году в России новый препарат с уникальным антихеликобактерным действием.
Хелинорм – инновационное антихеликобактерное средство из группы метаболиков
Принцип действия

Связывание снижает подвижность хеликобактерий — бактерии перестают связываться со слизистой оболочкой желудка и вымываются из желудка, что приводит к уменьшению бактерий в слизистой оболочке и снижают риск развития гастрита, язвенной болезни.
Хелинорм – разумная альтернатива антибиотикотерапии при хеликобактериозе.
Схема лечения
Курс лечения Хелинормом составляет 4 недели, по 1 капсуле во время еды 1 раз в день.

С профилактической целью в дальнейшем возможно использовать закваски Эвиталия или Нарине, которые позволяют готовить лечебный кисломолочный продукт в домашних условиях, в котором оптимальное сочетание и живых бактерий – лактобацилл, и продуктов их жизнедеятельности. Использовать его в натуральном виде, с добавлением растительных компонентов (овощи, фрукты, отруби), заправлять им разнообразные салаты.
Источник
Советы Британского общества гастроэнтерологов в отношении Helicobacter pylori
На сайте GastroScan.ru в разделе Литература имеется подраздел «Популярная гастроэнтерология», содержащий публикации для пациентов по различным аспектам гастроэнтерологии.
Рекомендации Британского общества гастроэнтерологов пациентам в отношении Helicobacter pylori
Британское общество гастроэнтерологов (BSG) с участием Core (the Digestive Disorders Foundation) и Primary Care Society for Gastroenterology (PCSG) подготовило ряд советов и рекомендаций для пациентов.
Ниже приводятся рекомендации BSG в отношении Helicobacter pylori.
Общая информация о Helicobacter pylori
Что такое Helicobacter pylori (Хеликобактер пилори)?
Как люди заражаются и как передается H. pylori?
Какие проблемы может вызвать H. pylori?
Может ли Helicobacter pylori вызывают рак?
Может ли Helicobacter pylori приносить нам пользу?
Полезно ли лечение H. pylori?
Если у вас язва
До открытия H. pylori было известно, что язва излечивалась лекарствами, снижающими кислотность желудка, но по окончанию лечения она появлялась снова. Уничтожение H. pylori не только помогает вылечить язвенную болезнь, но, что более важно, значительно снижает риск появления язвы в будущем. Хотя H. pylori является причиной большинства язв, также существуют язвы, вызванные аспирином и аналогичными препаратами, используемыми для лечения суставов и мышц. Тем не менее, существует общее мнение, что если пациенты больны или болели в прошлом язвенной болезнью и если они инфицированы H. pylori, то эта инфекция должна быть подвергнута лечению.
Если у вас нет язвы
Меньше, чем один человек из 10 с диспепсией и инфекцией H. pylori и не имеющий язвы, в результате лечения будет чувствовать себя лучше. Многие врачи считают, что из-за возможных проблем, которые могут проявиться в результате антибиотикотерапии, проводить последнюю не имеет смысла, хотя и имеется небольшой шанс, что лечение поможет. Было бы справедливо сказать, что имеются врачи, которые рекомендовали бы лечения H. pylori даже в отсутствии язвы. Они делают это в надежде, что небольшое число из таких пациентов будет чувствовать себя лучше.
Если у вас проблемы с органами пищеварения, но ни вам, ни врачу, не известно, если у вас язва
До недавнего времени большинство людей с проблемами с пищеварением (диспепсией) направляли на эндоскопию (визуальное исследование желудка с помощью вводимой небольшой трубки и камеры), чтобы зрительно определить наличие язвы. В настоящее время люди с проблемами пищеварения, имеющие, кроме того, такие тревожные симптомы, как потеря веса, постоянная рвота или затруднения при глотании, по-прежнему должны выполнять эндоскопию. Пациентам, не имеющим таких симптомов может быть назначено лечение без необходимости прохождения эндоскопии, вместо которой врач может направить пациента на исследование H. pylori и, при положительном тесте, назначить лечение инфекции. Однако, без эндоскопия, врач не может определить, имеется ли язва. Если у пациент действительно язва, по нашему мнению лечение H. pylori, скорее всего, окажется успешным. В других случаях, когда H. pylori не была причиной болезни, вполне вероятно, что никаких улучшений не будет.
Медицинские советы
Как врачи обнаруживают H. pylori?
Самый простой способ — анализ крови. Это полезно для выяснения, есть ли у человека H. pylori, но тест остается положительным даже после уничтожения H. pylori. Это означает, что с его помощью нельзя определить, был ли эффективен курс лечения этой инфекции.
Другой простой метод определения H. pylori — дыхательный тест. Для этого вам будет предложен напиток, содержащий вещество, называемое мочевиной. Наличиие H. pylori в желудке может быть определено на основе анализа выдыхаемого воздуха через короткое время после приема напитка. Это тест применяют для определения, насколько успешным было лечение и он должен быть выполнен по крайней мере в течение одного месяца после окончания курса лечения. В настоящее время также широко используется анализ кала на антигены H. pylori.
Если у пациенту выполняется эндоскопия, то во время ее может быть взят и направлен в лабораторию очень маленький кусочек слизистой оболочки желудка (биопсия), где с помощью ряда различных тестов определяют, присутствует ли H. pylori в желудке. Все тесты для H. pylori, кроме крови могут быть весьма неточными, если пациенты только что выполнили курс антибиотиков или если он принимали некоторые другие противоязвенные препараты. Ваш врач, несомненно, примет решение о направлении Вас на тест на H. pylori с учетом того, какие лекарства Вы принимали в последнее время и могут ли они повлиять на результаты теста.
Каким образом лечится инфекция H. pylori и каковы шансы на успех?
Существует ли согласие среди врачей в отношении лечения Helicobacter pylori?
Какие научные исследования необходимы в отношении H. pylori?
H. pylori был открыт только в 1983 году. Хотя мы провели массу исследований и многое поняли, многое еще мы не знаем. Например, не ясно, как именно H. pylori передается от одного человека к другому и почему только некоторые из инфицированых заболевают язвой. Мы не знаем, насколько H. pylori увеличивает риск рака желудка. Лучшее понимание этого поможет понять, как этот рак возникает и даст больше информации о раковых новообразованиях в целом. Лечение инфекции H. pylori в настоящее время очень эффективно, но H. pylori может становиться резистентным к обычным антибиотикам и поэтому необходимо разработать стратегии, чтобы остановить этот процесс, а также найти альтернативные методы лечения для случаев, когда все-таки резистентность развивается. Также необходима разработка вакцины для профилактики инфекции H. pylori в странах, где большое число носителей Helicobacter pylori и где имеется связь инфекции Helicobacter pylori с раком желудка. В Великобритании инфицированных H. pylori постепенно становится все меньше, но исследования необходимы для того, чтобы понять, как бороться с этой инфекцией в развивающихся странах, где она все еще очень распространена.
Источник
Helicobacter pylori и грибы рода Candida: что их объединяет у гастроэнтерологического больного
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– Сейчас мы передаем слово профессору Юрию Павловичу Успенскому. Юрий Павлович расскажет о хеликобактер пилори и о грибах рода Candida, что их объединяет у гастроэнтерологического больного.
Юрий Павлович Успенский, профессор, доктор медицинских наук:
– Дорогие коллеги, мы с вами прекрасно знаем, что благодаря эпохальному открытию колоссальной роли пилорического хеликобактера в развитии хронического гастрита, язвенной болезни, рака желудка, уже к концу 90-х годов стало очевидным, что количество вновь выявленных случаев язвенной болезни уменьшается, что даже дало возможность гастроэнтерологам заявить о том, что XX век – это век уходящей язвенной болезни, а XXI – это век рождающейся гастроэзофагеальной рефлюксной болезни.
Однако, к сожалению, тенденции последнего времени оказались не столь оптимистичны и основные проблемы связаны все-таки с уменьшающейся эффективностью эрадикационной терапии. Причины этого лежат в плоскости возрастающей резистентности хеликобактер пилори к антибактериальным препаратам, которые входят в состав схем традиционной эрадикационной терапии.
Так один из патриархов, профессор Мегро (F.Megraud), отметил, что резистентность к кларитромицину, согласно молекулярно-генетическим методам, в Европе достигает 46%. Что же происходит при этом? При этом происходит драматическое снижение эффективности эрадикационной терапии, которая не превышает 18%. Что касается Российской Федерации, то диапазон вариаций резистентности к кларитромицину весьма широк. Почему-то в нашем северо-западном регионе наиболее высока резистентность к кларитромицину в Санкт-Петербурге. Причем это были абсолютно независимые исследования: педиатрический анклав профессора Корниенко Е.А., наши исследования доктора Барышниковой Н.В., исследования института Пастера. Причем были разные методы, и все они дали крайне высокие (более 30%) цифры резистентности к кларитромицину.
Коллеги, говоря о новых антибактериальных препаратах как варианте преодоления резистентности к антибиотикам, повышения эффективности эрадикационной терапии, хотелось бы сказать, что все-таки этот путь достаточно опасный, а может быть, даже и тупиковый, потому что тем самым мы способствуем воспитанию полирезистентных штаммов к антибиотикам хеликобактер пилори.
И на самом деле неконтролируемое потребление антибиотиков, это глобальная проблема человечества. Не столь давно, 18 ноября 2012 года, состоялся Европейский день осведомленности о проблеме резистентности и потребления антибиотиков, когда была предложена мировая стратегия борьбы с распространением резистентных форм микроорганизмов.
Что же делать в этих условиях? В этих условиях надо руководствоваться теми соображениями, что, как писал великий испанский драматург Лопе де Вега: «Прогресс – это лучшее, а не только новое». Татьяна Львовна сегодня уже упоминала о том, что имеет место определенный ренессанс ныне схем эрадикации на основе препаратов висмута как в терапии первой, так и второй линий эрадикации пилорического хеликобактера. Действительно, препараты висмута обладают рядом преимуществ, связанных как с собственным антихеликобактерным действием, так и с цитопротективным эффектом, положительным влиянием на качество формированного послеязвенного рубца. К висмуту отсутствует первичная и не формируется вторичная резистентность, он не оказывает отрицательного воздействия на состав кишечной микрофлоры. А по данным профессора А.И. Парфенова в ряде случаев действует как кишечный антисептик, подавляя рост условно патогенных организмов, и он не вызывает развития антибиотико-ассоциированной диареи.
Непосредственное влияние препаратов висмута на хеликобактер пилори было продемонстрировано в виде целого ряда грамотно организованных исследований, и связаны были эти действия с блокированием адгезии хеликобактера с прямым ингибированием энзимов и уреазы этого микроорганизма.
Кроме того, в последние годы утвердилась концепция активно разрабатываемой школы профессора Кононова в Омске о том, что даже в случае успешно проведенной эрадикационной терапии формируется воспалительный инфильтрат (из-за продукции цитокинов, из-за продукции активных форм кислорода), и он сохраняется достаточно долго – от 1 до 12 месяцев. Поэтому и в этой связи включение препаратов висмута в комплекс эрадикационной терапии является оправданным с клинической точки зрения, потому что при этом происходит подавление ассоциированного воспаления из-за уменьшения продукции цитокинов, увеличения продукции цитопротективных простагландинов, и, соответственно, увеличение эпидермального фактора роста.
Такой классик хеликобактериологии как Питер Мальфертейнер (P. Malfertheiner) в одной из своих работ заявил, что добавление висмута к терапии первой линии может сохранять высокую эффективность эрадикации даже при резистентных штаммах. При этом не требуется мониторинг растущей резистентности к «Кларитромицину».
Какая же висмутсодержащая схема эрадикации является предпочтительной? Право на существование имеет и та схема, о которой мы сейчас говорили, когда висмут добавляется к стандартной терапии, и 10-дневная схема, о которой говорила Татьяна Львовна (висмут, метронидазол, тетрациклин и ингибитор протонного насоса). Все они обеспечивают достаточно высокий и эффективный уровень эрадикации.
А какая же связь между пилорическим хеликобактером и грибами рода Candida? Согласно нашим исследованиям, оказалось, что у одних и тех же больных экспрессируются гены, которые кодируют как факторы патогенности хеликобактер пилори, так и факторы адгезии и инвазии грибов рода Candida. А грибы рода Candida albicans действительно обладают факторами вирулентности, факторами адгезии, инвазии. Связь между концентрацией грибов рода Candida в толстой кишке и степенью обсемененности хеликобактер пилори антрального отдела желудка достаточно четко выражена и была продемонстрирована еще 10 лет назад в работах М.М. Захарченко.
Что происходит под влиянием антибактериальной терапии с грибами рода Candida? Их популяция неуклонно растет как следствие прямого стимулирующего действия (есть данные, что больные с кандидемией, то есть с кандидосепсисом, получали 4 и более антибиотиков), а также вследствие ингибирующего влияния на бактерии-антагонисты грибов рода Candida.
Что же такое грибы рода Candida? Посмотрите, вот эти данные показывают, что, оказывается, это транзиторные микроорганизмы, они обнаруживаются и в мороженом, и в других кисломолочных и молочных продуктах. То есть, на первый взгляд, нет ничего страшного в их присутствии, они транзитом проходят через организм человека. Но так происходит лишь тогда, когда иммунологическая реактивность макроорганизма достаточно высока. А если она низка, если это человек, страдающий иммунодефицитом, получающий гормональную терапию, если это ослабленный больной, тогда реален риск инвазии грибов рода Candida в слизистой оболочке, развития кандидоза пищевода, толстой кишки, транслокации микроба через кишечную стенку вплоть до развития кандидемии и кандидосепсиса.
В ряде случаев при пониженной иммунной резистентности макроорганизма инвазивный кандидоз не развивается, но возможно развитие неинвазивного кандидоза, когда увеличивается концентрация грибов рода Candida в просвете кишечника. Но и при этом ситуация далека от благополучной, потому что в этих условиях имеет место сенсибилизация, интоксикация организма, формирование вторичного иммунодефицита и присоединение микст-инфекции. Потому что грибы рода Candida обладают целым рядом ферментных, полисахаридных и иных факторов агрессии и патогенности.
Критерием диагностики неинвазивного кандидоза кишечника и повышенной пролиферации грибов рода Candida является снижение числа нормобиоты ниже 100 миллионов колониеобразующих единиц на грамм фекалий и рост грибов рода Candida ssp. при посеве кала выше 1000 колониеобразующих единиц на грамм фекалий.
Наличие тесной патогенетической взаимосвязи между грибами и хеликобактером подтверждает то, что в 98% образцов грибов рода Candida, выделенных из слизистой, детектируется хеликобактер пилори. И в большинстве образцов содержится ген острова патогенности cag A.
В другой работе показано, что также из грибов, выделенных из ротовой полости, идентифицируется присутствие генов хеликобактер пилори и почти в 100% случаев наблюдается гомологичность между генами грибов и генами контрольной популяции хеликобактера.
Согласно отечественной работе у детей с HP-ассоциированным гастродуоденитом с возрастом увеличивается число высокопатогенных штаммов микроорганизма хеликобактер пилори. Но при этом имеется сопряженность роста таких штаммов с увеличением гена sap2. Это ген, который кодирует синтез фактора вирулентности грибов рода Candida с 41,2% до 100% у детей, достигших 17-18 лет.
Таким образом, в последние годы сформировалась концепция, что дрожжеподобные микромицеты являются естественным биологическим резервуаром для грибов рода Candida. То есть что же при этом происходит? Татьяна Львовна уже говорила сегодня о стратегиях выживания пилорического хеликобактера. Но они не ограничиваются одной лишь уреазной активностью. Дело в том, что хеликобактер – это вообще весьма уязвимый организм, крайне чувствительный и к температурным условиям, и к пищевым, и желчным детергентам. Поэтому для своего выживания он способен пенетрировать капсулу и клеточную стенку гриба рода Candida, адгезировать плазменную мембрану гриба с образованием вакуоли и располагаться внутри этого организма, приобретая устойчивость к изменяющимся условиям среды, в том числе температурным, пищевым и желчным детергентам.
Вот и очень интересная работа, которая была выполнена 10 лет назад. Она показывает, что взаимоотношения между грибами и хеликобактером являются, по сути, эквипотенциальными. Их такая комбинация увеличивает и вирулентность грибов рода Candida. А проведенная эрадикационная терапия, даже в случае своей успешности, достоверно уменьшает частоту выявления хеликобактера в желудке, но увеличивает частоту выявления грибов рода Candida.
Что же делать в этой ситуации? По всей видимости, необходим поиск инновационных подходов к диагностике коррекции кандидозы такого рода пациентов. И сложность заключается в том, что среди традиционно принятого в гастроэнтерологии методов лечения, методы, направленные на предотвращение экспансии Candida spp., по сути, отсутствуют. Равно как и отсутствует антикандидозная активность у всех антибактериальных средств, входящих в состав классической эрадикационной терапии. А между тем такие пути необходимо искать, потому что грибы, как мы уже с вами говорили, способны помимо кишечника заселять другие анатомические и экологические ниши организма и в полной мере проявлять свои патогенные свойства.
К путям минимизации риска развития и прогрессирования кандидоза органов пищеварения при использовании эрадикационной терапии можно отнести исключение из эрадикационного комплекса антибиотика с потенциально высокой резистентностью к ним и включение в терапию первой линии препаратов висмута. Кроме того, у ряда пациентов требуется дополнительное назначение нерезорбцируемых антимикотических препаратов.
К старым препаратам такой генерации относился и относится, например, «Нистатин». Однако этот препарат все-таки нельзя в современных условиях считать средством выбора, потому что он обладает широким спектром побочных эффектов, у него целый ряд противопоказаний, в том числе язвенная болезнь, панкреатиты, беременность и лактация.
И достойной альтернативой, которая обладает всеми преимуществами и лишена всех недостатков препаратов этой группы, является «Пимафуцин» («Натамицин») – противомикробный полиеновый антимикотик, который действует только внутри просвета кишечной стенки. В отличие от «Нистатина», к «Натамицину» не приобретается резистентность даже при длительном применении. Этот препарат выпускается в кишечнорастворимой оболочке, следовательно, он защищен от разрушения в кислой желудочной среде. Как уже говорилось, его можно применять в период беременности, детям в любом возрасте по одной таблетке (100 мг) 4 раза в день, как правило, в течение 5-10 дней.
Гинекологи хорошо знают этот препарат, «Пимафуцин», активно применяют его в своей клинической практике. Но поскольку экологические ниши и эндобиоценозы человека, по сути, как сообщающиеся сосуды, то имеется необходимость при наличии кандидоза, например, той же молочницы, в обязательном порядке выявлять наличие кандидоза органов пищеварения и применять соответствующие усилия для исправления этой ситуации.
Каковы же категории пациентов, которым показаны дополнительные включения в состав комплекса эрадикационной терапии антимикотика «Пимафуцина» или его назначения в течение 7-10 дней после проведения эрадикации? Это больные, у которых определяются клинико-лабораторные критерии кандидоза; это больные, которым уже проводилась эрадикационная терапия; которым проводилась курсовая антибактериальная терапия по разным поводам; иммунодефицитные пациенты, больные, получающие лучевую или гормональную терапию; больные, у которых выявляются признаки кандидоза других органов пищеварения.
Конечно же, «Пимафуцин» («Натамицин») отсутствует как в международных, так и в российских рекомендациях, но наша медицина не догматична, она развивается соответственно клиническим потребностям наших пациентов. Совсем недавно еще мы не говорили о том, что пробиотики могут использоваться в хеликобактериологии, а согласно IV Маастрихтскому соглашению пробиотики могут использоваться в качестве адъювантной терапии, для повышения безопасности терапии.
Пока же позвольте сделать заключение о том, что кандидоз органов пищеварения – это междисциплинарная проблема и для ее решения нужна интеграция усилий гастроэнтерологической и микологической службы. Высокое представительство грибов рода Candida в составе желудочно-кишечной микрофлоры связано с плотностью бактериального обсеменения и вирулентностью микроорганизма в хеликобактер пилори. Перспективным же путем повышения эффективности и безопасности эрадикационной терапии, а также элиминации грибов рода Candida и профилактики прогрессирования кандидоза органов пищеварения является дополнительное включение в схемы эрадикационной терапии тем контингентам пациентов, о которых мы с вами выше говорили, препаратов висмута и нерезорбцируемых антимикотиков.
Источник


