- Почечная недостаточность: симптомы, стадии, лечение
- Причины
- Симптомы почечной недостаточности
- Осложнения
- Диагностика
- Лечение почечной недостаточности
- Грыжа пищеводного отверстия диафрагмы — симптомы диагностика и методы лечения
- О грыже пищевода и рефлюкс-эзофагите
- Распространенность заболевания
- Классификация грыж пищеводного отверстия диафрагмы
- Классификация рефлюкс-эзофагита
- Симптомы, признаки и клиническая картина грыжи пищеводного отверстия диафрагмы и рефлюкс-эзофагита
- Методы диагностики
- Лечение грыжи пищеводного отверстия диафрагмы
- Народные средства и методы лечения народной медицины при грыже пищевода
- Хирургические методы лечения грыжи пищеводного отверстия диафрагмы (грыжи пищевода)
Почечная недостаточность: симптомы, стадии, лечение
Почечная недостаточность – острое или хроническое заболевание, при котором нарушаются фильтрационная, выделительная и другие функции почек с развитием многочисленных сбоев в работе всего организма. При этом происходит отравление собственными токсичными продуктами обмена веществ, попавшими в кровь – уремия. Патология, особенно при стремительном развитии, может угрожать жизни больного и требует скорейшего лечения.
Распространенность хронической болезни почек во всем мире в среднем составляет 13,4%. В России почечная недостаточность встречается у 36% лиц старше 60 лет и у 16% граждан трудоспособного возраста.
Причины
Хроническая форма заболевания чаще всего развивается как осложнение других патологий. Ранее основной причиной почечной недостаточности считался гломерулонефрит. В настоящее же время ведущее место занимают гипертоническая болезнь и сахарный диабет, приводящие к поражению мелких сосудов, питающих почки, и стойкому нарушению кровообращения в них.
Острая почечная недостаточность (ОПН) более чем в половине случаев связана с травмой или перенесенными операциями на органах малого таза. Развивается она также при неправильном приеме лекарственных препаратов, нарушении работы сердца, кровотечениях и шоке, генерализованной аллергической реакции, обезвоживании, циррозе, отравлении, аутоиммунных и инфекционных болезнях, онкологии, переливании несовместимой крови.
Предрасполагают к нарушению работы почек следующие факторы:
- плохая экология;
- особенности питания;
- мужской пол;
- возраст старше 60 лет;
- избыточный вес;
- вредные привычки – табакокурение, злоупотребление алкоголем;
- генетическая предрасположенность;
- прием некоторых медикаментов;
- инфекционные и паразитарные поражения;
- хронические заболевания сердечно-сосудистой (в том числе – повышенное артериальное давление), мочевыделительной и эндокринной систем;
- нарушение жирового обмена, дислипидемия, гиперхолестеринемия, метаболический синдром.
Симптомы почечной недостаточности
Почки не только очищают кровь от токсинов и выводят их из организма, но также регулируют водно-солевой баланс, контролируют уровень артериального давления, тонус сосудов, концентрацию гемоглобина, помогают в сохранении здоровья опорно-двигательного аппарата и сердца. Учитывая такое многообразие функций органа, почечная недостаточность проявляется многочисленными симптомами, выраженность которых зависит от стадии и формы заболевания.
При остром повреждении почек на начальной стадии имеются лишь проявления основного заболевания. Далее следует самая тяжелая, олигурическая стадия, продолжительностью до 3-х недель, со снижением суточного объема мочи менее 500 мл. Первым признаком болезни становится резкое уменьшение или прекращение мочеиспускания.
Состояние часто обратимо (если обратимо основное заболевание или состояние, приведшее к ОПН) и при правильном лечении переходит в полиурическую стадию почечной недостаточности с восстановлением объема мочи. При этом самочувствие пациента нормализуется, но может развиваться обезвоживание организма и присоединиться инфекция. Стадия полного восстановления продолжается от шести месяцев до года. При выраженных нарушениях состояние переходит в хроническую форму.
Хроническая почечная недостаточность (ХПН) развивается медленно, в течение нескольких месяцев и даже лет, и приводит к стойким изменениям в органе. На начальном этапе специфических симптомов обычно не бывает, но иногда человек может заметить снижение объема выделяемой мочи. Либо единственным проявлением патологии может быть никтурия – частое ночное мочеиспускание.
По мере прогрессирования заболевания и присоединения уремии появляются и другие симптомы:
- апатия, общая слабость;
- жажда;
- неприятный вкус во рту;
- расстройство сна;
- ухудшение памяти;
- тошнота.
При отсутствии эффективного лечения присоединяются неврологические расстройства – непроизвольные подергивания мышц, снижение скорости реакций, а также обильная рвота, диарея, одышка, раздражение кожи и слизистых оболочек.
Осложнения
Болезнь осложняется появлением артериальной гипертензии, анемии, перикардита, аритмии и сердечной недостаточности, остеопороза, подагры, энцефалопатии, язвенной болезни желудка и двенадцатиперстной кишки, атеросклероза сосудов с развитием инфаркта и инсульта, синдрома беспокойных ног.
У детей почечная недостаточность приводит к задержке роста костной ткани.
Развитие почечной недостаточности у женщин во время беременности сопряжено с невынашиванием плода или формированием у него врожденных пороков.
Без лечения ХПН может закончиться смертью пациента от сердечно-сосудистых осложнений или уремической комы.
Диагностика
При первичном обследовании врач собирает анамнез заболевания, уточняя жалобы и давность симптомов. Далее проводятся осмотр кожных покровов, пальпация и поколачивание пальцами поясничной области.
Диагноз почечной недостаточности выставляется на основании следующих лабораторных и инструментальных исследований:
- Общий анализ мочи. Метод позволяет установить причину заболевания. Примесь крови, наличие эритроцитов в биоматериале свидетельствуют о мочекаменной болезни, гломерулонефрите, инфекции, новообразовании или травме. Лейкоциты указывают на инфекционный либо аутоиммунный процесс. Также может снижаться плотность мочи, присутствовать белок и восковидные цилиндры в ней.
- Клинический анализ крови. Повышение лейкоцитов и СОЭ говорит об инфекционном процессе, а уменьшение количества эритроцитов и гемоглобина в крови свидетельствует о сопутствующей почечной недостаточности анемии.
- Биохимический анализ крови. Увеличение в сывороточной крови мочевины и креатинина служит основным признаком почечной недостаточности. Эти вещества образуются в процессе распада белков и могут выводиться из организма исключительно с мочой. Прогрессирующий рост концентрации креатинина является главным диагностическим критерием тяжести заболевания. Сахарный диабет – одна из наиболее частых причин ХПН, однако и без эндокринных заболеваний при дисфункции почек есть склонность к умеренному повышению глюкозы в крови. Значительное увеличение уровня калия сопровождает выраженное нарушение функции почек, а высокая концентрация мочевой кислоты характерна для подагры и может привести к развитию мочекаменной болезни. Также в анализах крови при почечной недостаточности часто снижены альбумин, кальций, повышены триглицериды, щелочная фосфатаза, фосфор и холестерин.
- Биопсия почек. В сложных диагностических случаях может осуществляться забор небольшой части почечной ткани, которая подвергается последующему осмотру через микроскоп. Метод позволяет обнаружить характерные гистологические признаки ХПН – замещение клубочков почек рубцовой тканью.
- Ультразвуковое исследование органов малого таза. Важное место в диагностике почечной недостаточности занимает УЗИ почек. При ХПН отмечается их уменьшение (сморщивание) вместе с истончением наружного слоя. Также метод применяется для обнаружения новообразований, камней или кист.
- Компьютерная и магнитно-резонансная томография брюшной полости. Более точный способ визуализации опухолей, кист и конкрементов размером даже менее 5 мм.
Лечение почечной недостаточности
Обязательно проводятся диагностика и лечение патологии, послужившей причиной почечной недостаточности, а также устранение факторов риска.
Важную роль в терапии заболевания играют общие мероприятия, направленные на сохранение функции пораженного органа:
- Ограничение потребления жидкости.
- Отказ от приема ряда медикаментов.
- Коррекция питания. Диета при почечной недостаточности предполагает ограничение продуктов и напитков с повышенным содержанием натрия, фосфора, калия. Это поваренная соль, молочные продукты, печень, бобовые, орехи. Количество потребляемого белка также строго дозируется.
Консервативное лечение почечной недостаточности назначается врачом по результатам анализов. Для восстановления водно-солевого баланса внутривенно через капельницу вводятся специальные растворы. При задержке жидкости могут применяться мочегонные препараты. Также проводится терапия средствами, улучшающими кровообращение в органах малого таза, препаратами эритропоэтина, витамином D.
При выраженном или длительном нарушении фильтрационной функции почек пациенту показано аппаратное очищение крови – гемодиализ. Процедура проводится регулярно и позволяет убрать из организма токсичные вещества. Альтернативой выступает перитонеальный диализ, при котором в брюшную полость вводится с последующим удалением специальный раствор, забирающий на себя вредные вещества.
В случае тяжелого течения хронической почечной недостаточности выполняется операция по трансплантации почки. После пересадки проводится курс терапии препаратами, подавляющими иммунитет, чтобы не произошло отторжения донорской ткани.
Источник
Грыжа пищеводного отверстия диафрагмы — симптомы диагностика и методы лечения
Лечение грыжи пищеводного отверстия диафрагмы. Видео прямого эфира
О грыже пищевода и рефлюкс-эзофагите
Грыжа пищеводного отверстия диафрагмы (ГПОД) и рефлюкс-эзофагит — это заболевание пищевода и связочного аппарата диафрагмы, при котором возникает расширение пищеводного отверстия диафрагмы и растягиваются связки, фиксирующие пищевод и желудок. В результате растяжения верхняя часть желудка выходит в грудную полость и нарушается работа нижнего пищеводного сфинктера.
Изменение угла Гиса и нарушение работы нижнего пищеводного сфинктера приводит к забросу кислого желудочного содержимого или желчи из двенадцатиперстной кишки в пищевод с развитием воспаления и перестройки слизистой оболочки, вплоть до возникновения рака пищевода. По данным Европейской и Американской гастроэнтерологических ассоциаций, если ГПОД существует в течение 5–12 лет без лечения, то риск развития рака пищевода возрастает на 270% через 5 лет и на 350–490%, в зависимости от возраста — через 12 лет.
Видео из операционной. Лапароскопическая операция по поводу ГПОД
Под рефлюкс-эзофагитом понимают воспалительный процесс в пищеводе, возникающий вследствие заброса желудочного или кишечного содержимого в пищевод и воздействия его на слизистую оболочку пищевода.
Грыжа пищеводного отверстия диафрагмы, как правило, сочетается с ГЭРБ. Гастроэзофагеальная рефлюксная болезнь характеризуется комплексом диспептических, пульмонологических и кардиологических расстройств, возникающих, как правило, вследствие ГПОД и патологического желудочно-пищеводного рефлюкса.
Распространенность заболевания
В настоящее время по мнению многих авторов ГПОД считается одним из наиболее распространенных заболеваний ЖКТ и по своей частоте среди прочей гастроэнтерологической патологии занимают 2–3 место, конкурируя со столь распространенными заболеваниями, как язвенная болезнь и холецистит.
Классификация грыж пищеводного отверстия диафрагмы
Выделяют три основных типа ГПОД.
- Скользящая (аксиальная) грыжа. Встречается почти у 90% больных. В этом случае кардия лежит выше пищеводного отверстия диафрагмы, в связи с чем изменяются соотношения между пищеводом и желудком, резко нарушается замыкательная функция кардии.
- Параэзофагеальная грыжа. Отмечается приблизительно у 5% больных. Характеризуется тем, что кардия не изменяет своего положения, а через расширенное отверстие выходят дно и большая кривизна желудка.
- Короткий пищевод. Как самостоятельное заболевание встречается редко и представляет аномалию развития. Обычно встречается в сочетании со скользящей грыжей и является следствием спазма, воспалительных изменений и рубцовых процессов в стенке пищевода.
Классификация рефлюкс-эзофагита
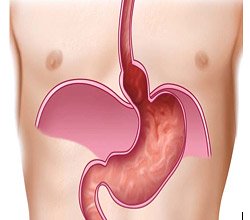
Рис. 1. Нормальное положение желудка и угла Гиса (схема).
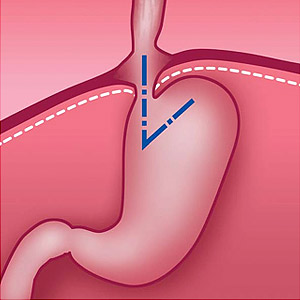
Рис. 2. Перемещение части желудка в грудную полость и изменение угла Гиса при грыже пищеводного отверстия диафрагмы (схема).
Для унификации и оценки данных гастроскопического исследования используют классификацию степени выраженности эзофагита по Savary-Miller, при этом различают четыре стадии заболевания:
- I стадия — округлые и продольные поражения, которые не сливаются и распространяются от Z-линии к слизистой оболочке пищевода;
- II стадия — сливающиеся транзиторные поражения в зоне Z-линии, не захватывающие всю поверхность слизистой оболочки;
- III стадия — язвенные поражения, сливающиеся в нижней части пищевода и охватывающие всю поверхность слизистой оболочки;
- IV стадия — хронические язвенные поражения пищевода, фиброзный стеноз, укорочение пищевода (пищевод Барретта).
Симптомы, признаки и клиническая картина грыжи пищеводного отверстия диафрагмы и рефлюкс-эзофагита
Наиболее частыми симптомами являются изжога, часто упорная, мучительная, возникающая как после еды, так и натощак, особенно при наклоне туловища и в положении лежа, а также отрыжка воздухом, кислым, горьким или срыгивание пищи. Характерным симптом грыжи пищеводного отверстия диафрагмы является боль, обычно жгучего характера, которая возникает в подложечной области, за грудиной, в левом подреберье, усиливается при физической нагрузке, при наклонах. Часто бывает ощущение комка в горле и появление боли при проглатывании пищи. В этой ситуации человек ощущает дискомфорт за грудиной вплоть до сильной распирающей боли, распространяющейся в левое плечо и лопатку (совсем как при стенокардии), жжение, чувство нехватки воздуха или неудовлетворенность вдохом. У некоторых пациентов часто происходит внезапное, без видимых причин, повышение артериального давления. Ночью отмечается повышенное слюноотделение, приступы кашля и удушья, к утру появляется осиплость голоса.
Методы диагностики
Диагностика основывается на клинической картине, описанной выше, и инструментальных методах обследования. Инструментальные методы обследования, используемые для диагностики ГПОД и РЭ, включают:
- фиброгастроскопию — во время которой оценивается состояние слизистой пищевода, желудка и двенадцатиперстной кишки, а также выявляется пролабирование слизистой желудка в пищевод,
- рентгенологическое исследование пищевода и желудка, во время которого выявляется собственно ГПОД, ее размеры, фиксация, а также оценивается моторика пищевода и желудка и наличие рефлюкса бариевой взвеси в пищевод,
- третьим исследованием, помогающим хирургу в определении показаний к операции и выбору метода оперативной коррекции, является суточная рН-метрия пищевода и желудка, во время которой определяется уровень желудочной секреции и наличие патологических рефлюксов из желудка в пищевод. Наиболее важным критерием наличия и тяжести рефлюкс-эзофагита считается общее время, при котором рН составляет менее 4 ед. Увеличение числа рефлюксов продолжительностью более 5 мин. и повышение длительности наиболее продолжительного рефлюкса свидетельствует о снижении пищеводного клиренса и позволяет предположить наличие гипомоторной дискинезии пищевода.
Для выявления ГПОД и определения степени поражения пищевода, а также выбора правильной тактики хирургического лечения, необходимо прислать мне на личный электронный адрес puchkovkv@mail.ru puchkovkv@mail.ru копировать 
Лечение грыжи пищеводного отверстия диафрагмы
Лечение ГПОД на 99% соответствует лечению ее осложнений — рефлюкс-эзофагита и, к сожалению, терапевтическое лечение ГПОД является чисто симптоматическим: пока пациент принимает лекарственные препараты, ограничивает себя в питании, и строго выполняет все предписания и назначения врача, его состояние относительно удовлетворительное. Как только курс лечения прекращен, то все симптомы ГПОД (постоянная отрыжка, мучительная изжога) возвращаются. Консервативному (терапевтическому) лечению у врача-гастроэнтеролога подлежат больные с небольшими нефиксированными грыжами пищеводного отверстия диафрагмы, без выраженной клинической картины и только в том случае, если пациент готов пожизненно принимать препараты, препятствующие возникновению рефлюкс-эзофагита или уменьшающие симптомы заболевания. Но стоит отметить, что при систематическом применении препаратов, снижающих кислотность желудочного сока, например, омеза, кваматела, ранетидина и других, через 5 лет риск развития рака желудка увеличивается на 350%, а через 12 лет — увеличивается на 560% по сравнению с лицами без ГПОД того же возраста. В то же время, отсутствие в желудке кислоты препятствует нормальному перевариванию пищи, в результате чего ее остатки попадают в толстую кишку, вызывая гнилостные процессы и развитие тяжелого дисбактериоза кишечника.
Народные средства и методы лечения народной медицины при грыже пищевода
Хотелось бы особо отметить народные средства и методы народной медицины, применяемые при лечении грыжи пищеводного отверстия диафрагмы. Рекомендуемые различными травниками, сборниками советов для пациентов и другой популярной литературой народные или псевдонародные средства и методы лечения ГПОД, приводят к временному улучшению состояния пациента и снятию симптомов рефлюкс-эзофагита, которые воспринимаются пациентами как излечение. Все народные средства лечения ГПОД по своему механизму действия сопоставимы с лекарственными препаратами — они либо уменьшают кислотность желудочного сока, либо меняют кислотность (нейтрализуют) сам желудочный сок. Но как правило, эффективность народных средств при грыже пищевода ниже на 50–70% по сравнению с лекарственными препаратами.
Рис. 3. Грыжа пищеводного отверстия диафрагмы до оперативного вмешательства (схема).
Хирургические методы лечения грыжи пищеводного отверстия диафрагмы (грыжи пищевода)
При отсутствии эффекта от медикаментозной терапии ГПОД показано оперативное лечение, суть которого заключается в восстановлении нормальных анатомических отношений в области пищевода и желудка.
Показания к хирургическому лечению грыжи пищеводного отверстия диафрагмы:
- неэффективность консервативного лечения;
- наличие осложнений ГПОД (эзофагит, эрозии и язвы пищевода, анемия, кровотечения);
- большие размеры грыжи, ее фиксация в грыжевых воротах;
- параэзофагеальная (около пищеводная) скользящая грыжа (высокий риск ущемления грыжи);
- дисплазия слизистой пищевода (слизистая пищевода приобретает строение слизистой тонкого кишечника).
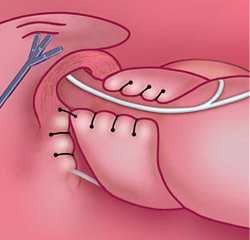
Виды хирургического лечения при грыже пищеводного отверстия диафрагмы: все существующие на сегодняшний день хирургические методики лечения ГПОД направлены на устранение грыжи (ушивание пищеводного отверстия диафрагмы до нормального размера 4 см путем крурорафии) и хирургическое создание арефлюксного механизма, препятствующего забросу желудочного содержимого в пищевод. В большинстве отечественных клиник используются операции фундопликации по Ниссену, которая состоит в хирургическом обороте дна желудка вокруг пищевода на 360 градусов, что позволяет создать манжетку, препятствующую забросу желудочного содержимого в пищевод и, следовательно, развитию эзофагита.
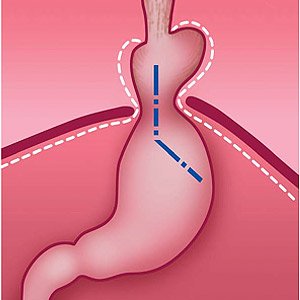
Рис. 4. Окончательный вид операционного поля после крурорафии и физиологической фундопликации по Тоупе (270 град)
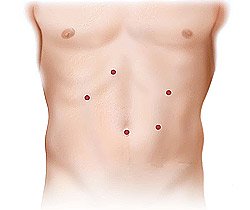
Рис. 5. Места проколов брюшной стенки при лапароскопической операции для ликвидации ГПОД
Операция фундопликации по Ниссену может выполняться открытым или лапароскопическим доступом, но при этом в своей основе она не лишена существенных недостатков. Первое — классическая фундопластика у пациентов с фиксированной, длительно существующей грыжей пищеводного отверстия диафрагмы может приводить к существенному ухудшению качества жизни пациента. В результате этого вида фундопликации формируется абсолютный клапан в области кардии, и пациент утрачивает полностью возможность использовать такой естественный защитный механизм желудка, как срыгивание или рвота. При приеме любых газированных напитков, от шампанского до газированной воды, газы жидкости не могут покинуть желудок через кардию и раздувают его. Чувство тяжести, боли в желудке также возникают при приеме большого количества пищи. Второе — классическая фундопластика не предусматривает фиксации сформированной манжетки, что ведет спустя некоторый срок к соскальзыванию манжеты и рецидиву заболевания. После фундопластики по Ниссену рецидив заболевания возникает всего спустя 1–2 года после операции.
Поэтому большинство европейских хирургов в своей практической работе используют парциальную фундопликацию по Тоупе на 270 градусов, которая позволяет гарантировать пациентам физиологическую работу сфинктера в послеоперационном периоде, а также сохранить естественные защитные механизмы — отрыжку и рвотный рефлекс, о важности которых для поддержания качества жизни пациентов говорилось выше.
С начала 90-х годов, для коррекции грыжи пищеводного отверстия диафрагмы, стали использоваться лапароскопический доступ, который позволяет хирургу выполнить любой вид фундопликации и надежно ушить грыжевой дефект в диафрагме. Формирование физиологической фундопликации по Тоупе требует от хирурга виртуозного владения эндоскопическим швом, поэтому прежде чем приступить к выполнению подобных операций, следует пройти длительную подготовку на специальных тренажерах.
Стоит отметить, что грыжа пищеводного отверстия диафрагмы часто сочетается с желчнокаменной болезнью и язвенной болезнью двенадцатиперстной кишки, которые также требуют оперативного лечения. В данной ситуации лапароскопический доступ представляется идеальным и позволяет одновременно выполнить симультанные (сочетанные) операции на разных органах брюшной полости, например, на желчном пузыре, на сфинктере фатерова соска, и собственно на диафрагме и желудке. При соответствующей квалификации хирурга длительность операции возрастает всего на 30–40 минут, а количество осложнений остается на низком уровне. При проведении симультанной операции лапароскопическим доступом через проколы для ГПОД одновременно проводится холецистэктомия (хронический калькулезный холецистит) и селективная проксимальная ваготомия (хроническая язвенная болезнь двенадцатиперстной кишки).
После лапароскопической операции по поводу коррекции грыжи пищеводного отверстия диафрагмы на коже живота остаются 3–4 разреза длиной по 5–10 мм. Пациенты с первого дня начинают вставать с постели, пить, а на следующие сутки принимать жидкую теплую пищу. Выписка из стационара проводится на 1–3 день в зависимости от тяжести заболевания. К работе пациент может приступить через 2–3 недели. Строгую диету следует соблюдать в течение полутора-двух месяцев, более мягкую — на протяжении полугода. Далее, как правило, пациент ведет обычный образ жизни — без медикаментов и соблюдения диеты. Лапароскопическая операция при ГПОД — самый лучший способ мгновенно скорректировать имеющуюся проблему и вернуть качество жизни пациентам.
Посмотреть видео операций в исполнении профессора Пучкова К.В. Вы можете на сайте «Видео операций лучших хирургов мира».
Источник