- Народная медицина при онкологии легкого
- 2. Какие факторы риска считаются важными для развития рака легкого?
- 3. Какую роль при раке легкого играют гены и наследственность?
- 4. Назовите основные гистологические типы рака легкого и их сравнительную частоту.
- 5. Имеет ли смысл скрининг рака легкого?
- 6. Как проявляется рак легкого?
- 7. Что такое паранеопластический синдром?
- 8. Важна ли классификация рака легкого для определения прогноза и тактики лечения?
- 9. Опишите тактику, если у больного на рентгенограмме грудной клетки обнаружена очаговая тень?
- 10. При каких наименьших показателях функции дыхания можно еще выполнить операцию при раке легкого?
- 11. Как лечат рак легкого?
- 12. Какую роль в лечении рака легкого играет лучевая терапия?
- 13. Какова выживаемость больных раком легкого?
- 14. Что такое медиастиноскопия?
- 15. Перечислите показания к медиастиноскопии.
- «Триумф онкологии». Какие лекарства успешно побеждают рак
- Долгий путь из лаборатории к пациенту
- Как заставить работать иммунитет
- Каждый шестой умирает от рака
Народная медицина при онкологии легкого
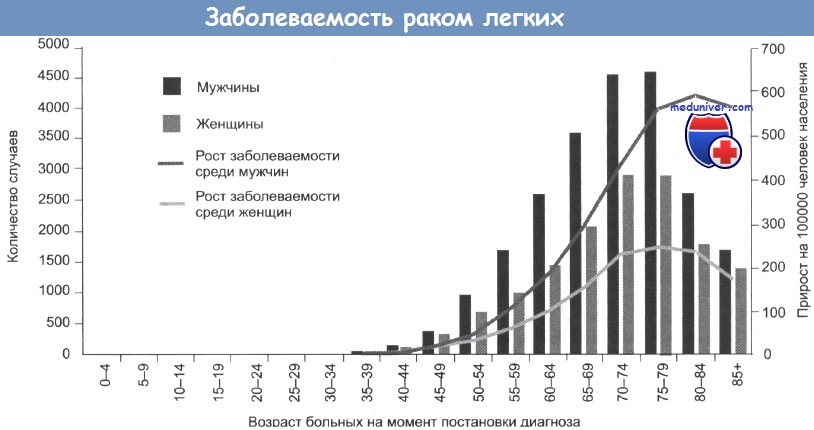
Ежегодно отмечают приблизительно 180 000 новых случаев рака легкого. В 1980 году соотношение мужчин и женщин было 8:1, однако заболеваемость у женщин выросла настолько, что отношение сейчас менее 2:1. Смертность от рака легкого не снизилась. Общая 5-летняя выживаемость составляет 10%.
Из-за связи заболевания с курением беспокоит увеличение числа курящих среди подростков. Более того, заболеваемость раком легкого растет также и у некурящих.
2. Какие факторы риска считаются важными для развития рака легкого?
Важными факторами риска являются курение и возраст; в анамнезе 90% больных есть сведения о курении. Ранее считали, что курение связано лишь с плоскоклеточным раком легкого, однако в последнее время наблюдают тревожное увеличение заболеваемости аденокарциномой, особенно у некурящих. К другим потенциально канцерогенным агентам относят химические вещества (ароматические углеводороды, винилхлорид), радиацию (радон и уран), асбест и металлы (хром, никель, свинец и мышьяк), а также факторы окружающей среды (загрязнение воздуха, угольная смола, нефтепродукты).
3. Какую роль при раке легкого играют гены и наследственность?
Случаи заболевания раком легкого в семье, вероятно, увеличивают вероятность его развития у человека. Более того, в клетках рака легкого и ткани рака легкого обнаружен большой ряд биомаркеров. Примером является геи К-ros, который кодирует белок под названием р21, принимающий участие в росте клеток и в передаче сигнала.
Мутации гена К-ras, которые ведут к его активации, связываются с уменьшением 5-летней выживаемости у больных резектабельным раком легкого. Другие важные биомаркеры рака легкого включают ген опухолевой супрессии р53, ген эпидермального фактора роста c-erb-2, ингибитор апоптоза bcl-2, маркеры ангиогенеза и маркеры клеточной пролиферации.
С увеличением количества образцов раковой ткани, исследуемых на эти маркеры, по ним судят о прогнозе для больных. До сих нор ни но одному маркеру отдельно нельзя точно сделать заключение о прогнозе или результате лечения данного больного.
4. Назовите основные гистологические типы рака легкого и их сравнительную частоту.
а) Немелкоклеточный рак 80%:
— Аденокарцинома 45%. Заболеваемость данным зловещим типом рака легкого резко увеличивается у некурящих.
— Плоскоклеточный рак 40%. Этот тип рака, также называемый эпидермоидным, характеризуется наличием гранул кератина и вызывается курением и вдыханием других раздражителей.
— Крупноклеточный рак 15%. Бронхоальвеолярный рак характеризуется пенистой бронхореей при многократных исследованиях. Он представляет собой подтип аденокарциномы. Злокачественный рост клеток, секретирующих сурфактант, проявляется появлением пенистой мокроты. Хотя клинически этот симптом наблюдают редко, его часто обнаруживают при обследовании.
б) Мелкоклеточный рак 20%. Наиболее важно деление рака легкого на мелкоклеточный и немелкоклеточный, поскольку биология опухоли и клиническое течение этих разновидностей рака существенно различаются. В свою очередь, мелкоклеточный рак подразделяют на ограниченный и распространенный. При ограниченном раке все опухолевые очаги находятся в одной половине грудной клетки и лимфатических узлах, включая медиастинальные, контралатеральные узлы ворот и ипсилатеральные надключичные узлы.
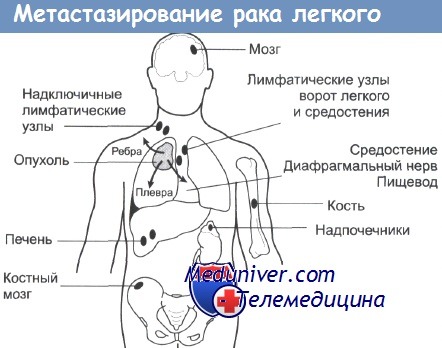
При распространенном раке болезнь выходит за эти пределы; возможно поражение мозга, костного мозга и органов брюшной полости.
5. Имеет ли смысл скрининг рака легкого?
К сожалению, пет. Даже выполнение рентгенологического исследования грудной клетки у 40-60-летних курящих мужчин не увеличивает выживаемость больных, у которых выявляется рак легкого. Разработаны другие методы ранней диагностики рака легкого, такие как использование биомаркеров и позитронной эмиссионной томографии, однако ни один из них в настоящее время не подходит для массового скрининга.
6. Как проявляется рак легкого?
Первичный рак легкого все более часто выявляют при обычном рентгенологическом исследовании грудной клетки. Иногда у больных отмечают кашель, прожилки крови в мокроте или повторные пневмонии. У 10% больных жалобы связаны с проявлениями паранеопластического синдрома.
7. Что такое паранеопластический синдром?
При паранеопластическом синдроме рака легкого наблюдают метаболические (гиперкальциемия, синдром Кушинга), неврологические (периферическая нейропатия, полимиозит или синдром Ламберта-Итона (Lambert-Eaton), протекающий наподобие генерализованной миастении), костные (пальцы в виде «барабанных палочек», гипертрофическая остеопатия), гематологические (анемия, тромбоцитоз, диссеминированное внутрисосудистое свертывание крови) или кожные (гиперкератоз, acanthosis nigricans, дерматомиозит) проявления. Интересно, что наличие паранеопластического синдрома не отражается на прогнозе рака легкого.
8. Важна ли классификация рака легкого для определения прогноза и тактики лечения?
Да. Классификация основывается на клинических и патологических данных для немелкоклеточного рака. Больным часто определяют стадию клинически в соответствии с результатами КТ.
— I стадия. Интрапаренхиматозная опухоль с распространением на висцеральную плевру или без него, отстоящая не менее чем па 2 см от карины, без поражения лимфатических узлов и отдаленных метастазов.
— II стадия. Первичная опухоль соответствует I стадии с поражением перибронхиальных лимфатических узлов (N1) или опухоль распространяется на грудную стенку без поражения лимфатических узлов.
— IIIа стадия. Поражение лимфатических узлов ворог или средостения (N2) или распространение опухоли на грудную стейку с поражением узлов N1. — IIIb стадия. Все элементы IIIа стадии в сочетании с распространением на структуры средостения (сердце или крупные сосуды) и/или поражением контралатеральных лимфатических узлов ворот, паратрахеальпых или надключичных (N3).
— IV стадия. Злокачественный плевральный выпот или отдаленные метастазы.

9. Опишите тактику, если у больного на рентгенограмме грудной клетки обнаружена очаговая тень?
Операция остается наиболее эффективным лечением рака легкого. Таким образом, ранняя диагностика учитывает вероятность торакотомии и направлена па выявление опухоли легкого и определение ее стадии. Только в 60% случаев диагноз можно установить при цитологическом исследовании мокроты; менее чем в 85% — при бронхоскопии с биопсией, и только в 80-90% — при пункционной биопсии под контролем КТ.
Поэтому основным средством диагностики является клиновидная резекция участка легкого с очагом. В стандартное обследование входит КТ грудной клетки (позволяет выявить возможное поражение лимфатических узлов средостения) и живота (позволяет обнаружить метастазы в надпочечники). От других исследований, таких как КТ костей скелета или головного мозга, воздерживаются, если пег специфических жалоб или симптомов.
Для определения возможности торакотомии у больного необходимо оценить функцию сердца (инфаркты в анамнезе, застойная сердечная недостаточность, стенокардия) и легочный резерв (определение ФОВ] при спирометрии у постели больного).
10. При каких наименьших показателях функции дыхания можно еще выполнить операцию при раке легкого?
а) Форсированный объем выдоха за секунду (ФОВ]) должен быть более 1 л/с; парциальное давление кислорода (РO2) и парциальное давление углекислого газа (РСO2) в крови (при комнатном воздухе) должны находиться по соответствующую сторону от 50 (РO2 выше 50, а РСO2 ниже 50).
б) Больной должен быть в состоянии подняться на один пролет лестницы.
в) В пограничных случаях можно применить исследование вентиляции-перфузии, чтобы узнать, какая часть легкого будет функционировать после операции.
11. Как лечат рак легкого?
Наиболее эффективным видом лечения при раке легкого является операция. К сожалению, у 50% больных опухоль уже к моменту выявления носит распространенный характер, а кандидатами на операцию являются только 25% больных. Число больных с III стадией — кандидатов на операцию — можно увеличить, проведя в предоперационном периоде химиотерапию по схеме, включающей цисплатин. Возможно, что эта недавно разработанная методика позволит улучшить выживаемость.
Несколько клинических исследований показали, что проведение при III стадии рака легкого дооперационной химиотерапии и облучения, известных как неоадъювантная терапия, дает лучшие результаты, чем просто операция. Новейшие схемы химиотерапии позволяют повысить эффективность лечения и ранних стадий болезни, и опухолей с высоким риском рецидива.
12. Какую роль в лечении рака легкого играет лучевая терапия?
Лучевая терапия — эффективное паллиативное лечение рака легкого, однако она не излечивает больных. Лучевая терапия часто позволяет устранить синдром верхней полой вены или обструкцию бронха вследствие пневмонии. Ее также с успехом применяют в качестве паллиативной терапии при болях в костях, вызванных опухолевым процессом. Некоторые, но не все клинические исследования показали, что некоторый эффект приносит проведение до операции химиолучевого лечения.
13. Какова выживаемость больных раком легкого?
При полном удалении немелкоклеточного рака I стадии 5 лет живут 60-80% больных. Для II, IIIа и IIIb стадий 5-летпяя выживаемость соответственно составляет 50%, 15% и 5%. При мелкоклеточном раке выживаемость остается низкой: 5 лет живут 7% больных с ограниченным заболеванием и только 1% — с распространенным.
14. Что такое медиастиноскопия?
Медиастиноскопия — диагностическая процедура (позволяющая установить стадию болезни), при которой через небольшой разрез в яремной ямке оценивают паратрахеальные, бифуркационные и проксимальные перибронхиальные лимфатические узлы.
15. Перечислите показания к медиастиноскопии.
Исследование средостения показано больным, имеющим клинически очевидный или подтвержденный исследованиями рак легкого, у которых есть:
а) Подтвержденный рак легкого с увеличением лимфатических узлов средостения > 1 см (по данным КТ), которые можно осмотреть при медиастиноскопии через разрез на шее.
б) Аденокарцинома легкого и множественные лимфоузлы в средостении 5 см) рак легкого с лимфатическими узлами в средостении
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
«Триумф онкологии». Какие лекарства успешно побеждают рак
«Ученые обещают лечить рак одним уколом», «Открыто новое лекарство от рака», «Найдено универсальное средство от злокачественных новообразований» — подобные заголовки появляются в СМИ едва ли не каждую неделю. Однако врачи полагаются на давно опробованные методы: хирургическое удаление опухоли, химио- и лучевую терапию. Практически все онкологические заболевания неизлечимы. РИА Новости разбирается, куда пропадают сенсационные разработки и когда наука победит рак.
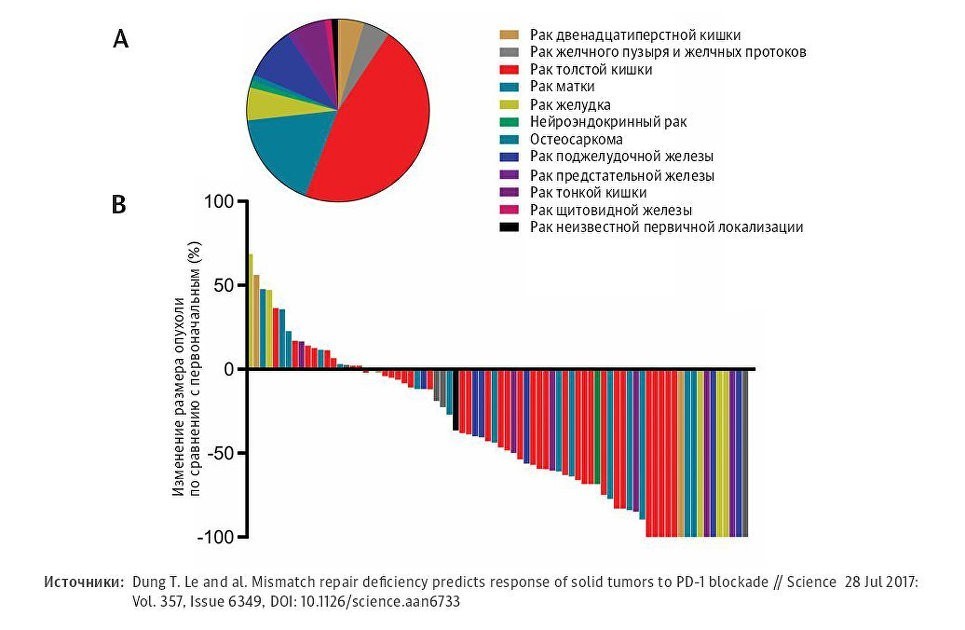
В июле прошлого года в журнале Science вышла статья, наделавшая много шума в научном мире: в результате испытаний нового противоракового препарата от онкологических заболеваний полностью вылечились два десятка человек. У всех были поражены разные органы — матка, желудок, простата, щитовидная железа.
Единственное, что объединяло пациентов, — их опухоли не отвечали на стандартное лечение из-за редких мутаций в геноме. После приема нового лекарства — моноклональных антител, помогающих иммунной системе атаковать болезнь, — 66 из 86 участников исследования почувствовали себя лучше. Их опухоли значительно уменьшились в размерах и стабилизировались, прекратив рост. Восемнадцати пациентам повезло еще больше: рак покинул их навсегда.
И хотя тестирование проходило в урезанном виде, без обязательной в таких случаях контрольной группы, принимающей плацебо, уже через год FDA, главный регулятор лекарственных средств в США, рекомендовал его для лечения сразу нескольких видов рака у детей и взрослых. По мнению специалистов, скорость, с которой была дана рекомендация, — беспрецедентная, и государство могло пойти на такие уступки только в том случае, если разработка действительно оказалась прорывной.
(А) — типы раковых опухолей, обнаруженные у участников исследования; (В) — ответ раковых опухолей на терапию пембролизумабом (результат после первых 20 недель лечения)
На самом деле этой истории почти 11 лет, ведь пембролизумаб (так назывался новый препарат) Грегори Карвен, Ханс ван Эненнаам и Джон Дулос создали в 2007 году. К испытаниям приступили только в 2013-м, а с 2018-го пациенты, страдающие агрессивными видами рака, не отвечающими на стандартную терапию, могли рассчитывать на лечение. Конечно, это состоятельные люди: один курс стоит около 150 тысяч долларов.
Долгий путь из лаборатории к пациенту
«Это долгий и сложный путь: от идеи до пациента. Все перспективные молекулы сначала тестируются на животных, потом проходят исследования с участием 10-20 пациентов, затем их число растет, счет идет на тысячи. На каждый следующий этап препарат переходит, только если продемонстрирует эффективность и безопасность на предыдущем. Это занимает годы, но защищает больных от неприятных последствий», — рассказывает Марина Секачева, руководитель Центра персонализированной онкологии, профессор кафедры онкологии Первого МГМУ им. И. М. Сеченова.
На каждом из этих этапов лекарство может быть выбраковано из-за нулевой эффективности или — еще хуже — негативного воздействия на организм пациентов. Например, в 2017 году во время клинических испытаний препарата CAR-T один из участников исследования умер. Несмотря на доказанную несколькими месяцами ранее эффективность терапии при лечении множественной миеломы и лейкемии, эксперимент был немедленно прекращен.
Похожая история произошла и с инновационным методом лечения рака ROCKET. В ходе клинических испытаний второй фазы проверяли эффективность и безопасность биопрепарата JCAR015, предназначенного для лечения рецидивирующего или устойчивого к терапии В-клеточного острого лимфобластного лейкоза. В июле 2016 года тестирование приостановили на два месяца из-за смерти трех пациентов. Спустя год от исследований лекарства и вовсе отказались, так как еще двое участников исследования скончались по одной и той же причине — отек головного мозга.
Как заставить работать иммунитет
Технология CAR предусматривает введение пациенту его собственных генно-модифицированных Т-лимфоцитов. Таким способом к лечению подключают иммунитет больного. Иммунные клетки распознают опухоль и атакуют ее. Несмотря на первые отрицательные результаты, исследования в этом направлении одобрены в некоторых странах.
«Последние пять лет в онкологии — это триумф иммуноонкологических препаратов, которые делают опухоль доступной для собственной иммунной системы пациента. И мы еще в процессе активного изучения этих лекарств: подбираем оптимальное сочетание, время назначения, последовательность; смотрим, как они влияют на хирургические результаты», — уточняет Марина Секачева.
Каждый шестой умирает от рака
Несмотря на идущую уже четыре десятилетия войну с раком, эта болезнь уносит сегодня жизнь каждого шестого обитателя планеты. По данным Всемирной организации здравоохранения, чаще всего люди погибают от рака легких (один миллион 690 тысяч смертей в год), печени (788 тысяч), толстой и прямой кишок (774 тысячи), желудка (754 тысячи) и молочной железы (571 тысяча).
Как отмечают специалисты, помимо физических канцерогенов (например, ультрафиолетового излучения) и вредных химических веществ (табак, асбест) риск заболевания повышают генетические особенности. В последние годы открыли гены, у носителей которых больше вероятность возникновения рака. С другой стороны, злокачественная опухоль часто образуется у тех, кто когда-то перенес инфекции, вызываемые некоторыми вирусами, бактериями или паразитами. Четверть онкологических заболеваний в развивающихся странах вызваны гепатитом и вирусом папилломы человека.
Ежегодный экономический ущерб от рака, по некоторым оценкам, достигает триллиона долларов. На разработку препаратов из года в год тратятся миллиарды. Однако, несмотря на все усилия, говорить о том, что в ближайшем будущем рак будет побежден, не приходится.
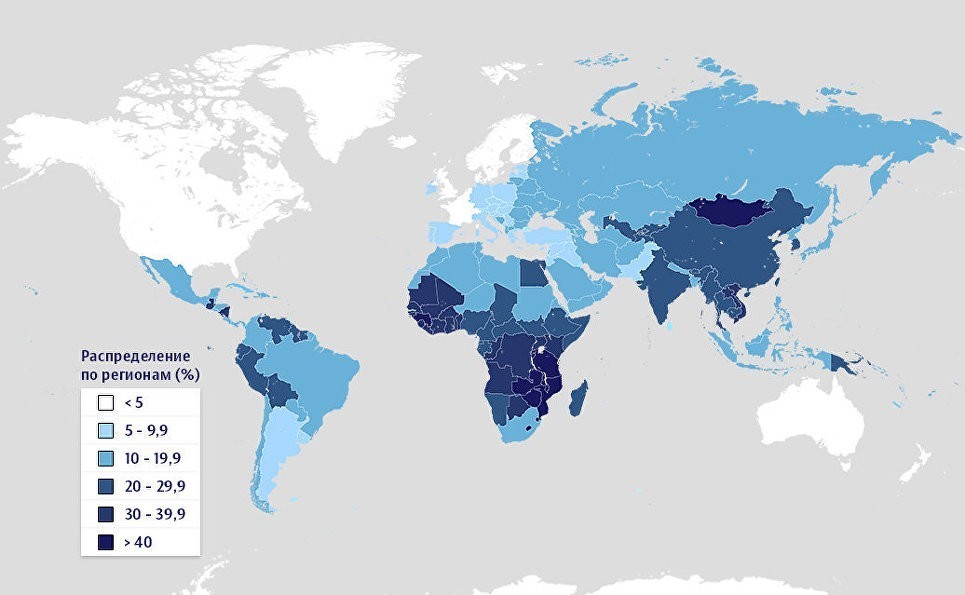
© Pathogen-Associated Malignancies Integrated Research Center, Fred Hutch
Доля онкологических больных, чья опухоль связана с перенесенными ранее инфекциями. Распределение по странам мира.
«К сожалению, человечество изобрело пока не так много лекарственных препаратов, позволяющих добиться полного излечения от того или иного недуга — главным образом, это касается инфекций. В большинстве случаев нам удается лишь перевести заболевание из смертельного или мучительного в хроническое и без выраженных симптомов. Эта тенденция прослеживается и в онкологии. В редчайших случаях лекарственная противоопухолевая терапия приводит к полному излечению, но примеров, когда удается перевести рак в длительный вялотекущий процесс, все больше. Скажем, хронический лимфолейкоз, рак молочной или предстательной железы. Мы каждый день (без преувеличения) открываем молекулярные особенности злокачественных новообразований, и это позволяет нам найти новые пути их лечения», — резюмирует онколог.
Источник