- Как проверить регистрационные удостоверения на медизделия: пошаговая инструкция
- Планируемые изменения
- Что такое регистрационные удостоверения на медизделия
- Когда необходимо требовать регистрационные удостоверения
- Как проверять регистрационные удостоверения
- Форма регистрационных удостоверений в 2020 году
- Расширен перечень медизделий, которым не нужна регистрация, а также иные существенные изменения
- Упрощенная регистрация мед. изделий для предупреждения распространения инфекционных заболеваний
- Упрощенная регистрация медицинских изделий
- Итого была упрощена процедура получения регистрационного удостоверения на:
- Процесс упрощенной регистрации
- Какие документы необходимы для оформления РУ
- При регистрации медицинского изделия потребуется доверенность
Как проверить регистрационные удостоверения на медизделия: пошаговая инструкция
Регистрационное удостоверение — это документ, закрепляющий соответствие той или иной единицы продукции законодательно установленным характеристикам. Планируют, что старые регудостоверения будут действовать и в 2021 году, но не на все медизделия.
Статья доработана экспертом Эллой Залужной
Планируемые изменения
Минпромторг на сайте проектов нормативных актов опубликовал проект постановления правительства, предложив изменить перечень иностранных медизделий одноразового применения (использования) из поливинилхлоридных пластиков, для которых устанавливаются ограничения в рамках госзакупок. Подробнее: «Особенности закупок медоборудования, медизделий и расходных материалов».
Это изменение связано с тем, что с 01.01.2021 код ОКПД2 32.50.50.000 исключается из классификатора. Этот код есть в перечне иностранных одноразовых медизделий из ПВХ, которые закупают с ограничениями в рамках национального режима.
Поэтому Минпромторг предложил, чтобы участники закупок таких медизделий использовали регудостоверения со старым кодом по ОКПД2 с 01.01.2021.
Дополнительно планируют расширить перечень, добавив в него новые позиции. В него, например, войдут:
- 32.50.50.180 — медицинские сумки-холодильники;
- 32.50.13.160 — инфузионные насосы.
| Скачать проект постановления правительства об изменении постановления правительства №102 от 05.02.2015 |
Что такое регистрационные удостоверения на медизделия
В настоящее время продажа медицинских изделий, не прошедших процедуру государственной регистрации, на территории Российской Федерации запрещена, то есть в России фактически невозможна реализация медизделий, не зарегистрированных в соответствии с законом (ст. 38 323-ФЗ от 21.11.2011).
Порядок фиксации закреплен в правилах госрегистрации медизделий (утверждены ПП РФ №1416 от 27.12.2012). Если организация закупает изделия медицинского назначения, заказчик сможет проверить, зарегистрирован товар или нет, только с помощью специального удостоверения.
Удостоверение на медизделие — это официальное подтверждение того, что медицинское изделие является зарегистрированным в соответствии с действующим законодательством.
Таким образом, подтверждение госрегистрации того или иного медизделия демонстрирует только официальное РУ, которое легализует возможность реализации и обращения конкретных товаров в Российской Федерации.
Эксперты КонсультантПлюс разобрали, как получить регудостоверение. Используйте эти инструкции бесплатно.
Чтобы прочитать, понадобится доступ в систему: ПОЛУЧИТЬ БЕСПЛАТНО НА 2 ДНЯ .
Когда необходимо требовать регистрационные удостоверения
Чтобы все закупаемые медицинские изделия были надлежащего качества и соответствовали установленным требованиям, заказчику необходимо указать в закупочной документации условие о предоставлении соответствующего свидетельства. Действующая редакция 44-ФЗ позволяет заказчику воспользоваться таким правом и включить это требование в документацию о закупке.
При этом специалисты организации-заказчика должны помнить, что требовать РУ как составную часть котировочной заявки запрещено согласно ст. 73 44-ФЗ.
Медизделия входят в аукционный перечень в соответствии с РП РФ №471-р от 21.03.2016, следовательно, их надлежит закупать путем электронного аукциона.
В п. 3 ч. 5 ст. 66 44-ФЗ указано, что если законодательно установлены определенные требования к закупаемым товарам, то такое условие допустимо включать в закупочную документацию. Когда в документации к заказу, проводимому путем электронного аукциона, установлен пункт о предоставлении подтверждения, то в составе второй части заявки необходимо предоставить копии документов, подтверждающих соответствие товара законодательному регламенту.
Таким образом, организация-заказчик вправе требовать предоставления копии соответствующего свидетельства во второй части заявки.
Более того, по нормативам ФАС предусмотреть наличие в документации о закупке медизделий требования о предоставлении копии РУ в составе второй части заявки — это обязанность заказчика, а отсутствие такого условия — нарушение ст. 66 44-ФЗ и ст. 38 323-ФЗ (письмо №АД/43043/14 от 23.10.2014).
При этом закупочной комиссии надлежит внимательно изучить факт соответствия товаров, приведенных в первой части заявки, и предоставляемых участниками закупки в составе второй части заявки копий регистрационных удостоверений на закупаемые товары. Если все данные совпадают, то заявка признается соответствующей требованиям закупочной документации. Если нет, то такой запрос необходимо отклонить.
Члены закупочной комиссии должны внимательно изучать копию РУ на предмет сложной части, то есть проверить, входит ли конкретное закупаемое медицинское изделие в совокупность предметов, зарегистрированных в составе удостоверения. Участник госзакупки вправе реализовывать только те медизделия, которые зарегистрированы в совокупности указанных в РУ. Закупаемый товар в обязательном порядке отдельно указывается в приложении к свидетельству (решение Свердловского УФАС по делу №8444-З от 22.06.2015).
Обязательством поставщика является передача заказчику товара вместе со всей относящейся к нему документацией (сертификат соответствия на медицинские изделия, техпаспорт, инструкция, свидетельство о регистрации (п. 2 ст. 456 ГК РФ). Таким образом, организация-заказчик вправе требовать копии РУ как в составе второй части заявки, так и в дальнейшем, при поставке и приемке товара.
Как проверять регистрационные удостоверения
Закупочная комиссия вправе провести проверку регистрационного удостоверения Росздравнадзора, так как рассматривает только те РУ, которые действительны на момент проведения закупки.
Если поставщик предоставляет РУ в составе второй части заявки, то оно должно быть действительным, даже если в такое свидетельство ранее вносились изменения (п. 50 ПП РФ №1416 от 27.12.2012).
Также участник закупки не вправе предоставлять РУ с истекшим сроком действия, так как оно признается недействительным.
Если потенциальный поставщик предоставляет во второй части заявки недействительное свидетельство, то такую заявку надлежит отклонить (решение Свердловского УФАС России по жалобе №145-З от 02.02.2017).
Для проверки того или иного РУ используйте официальный сайт Росздравнадзора. Ведомство ответственно за ведение ГРМИ — реестра регистрационных удостоверений медицинских изделий Минздрава РФ — и организаций, их производящих (ч. 10 ст. 38 323-ФЗ). В этом реестре проверяют как само наличие документа, так и его реквизиты и срок действия.
Инструкция, как проверить регистрационное удостоверение на медицинское изделие с помощью сайта Росздравнадзора:
- перейти по ссылке;
- открыть расширенный поиск;
- ввести в поисковую строку реестра медицинских изделий Росздравнадзора наименование медицинского изделия;
- просмотреть результат.
Форма регистрационных удостоверений в 2020 году
РУ — это официальный документ, имеющий законодательно закрепленную форму.
Формальный вид регистрационного удостоверения на медицинское оборудование, действующего в 2020 году, утвержден приказом Росздравнадзора №40-Пр/13от 16.01.2013. Все необходимые приложения являются его неотъемлемой частью.
Все заявки на участие в закупке на приобретение медицинских изделий должны содержать как копию самого регистрационного свидетельства, так и приложения к нему (при наличии).
Образец регистрационного удостоверения Росздравнадзора на медицинское изделие, которое выдает ведомство:
В 2009 году закончила бакалавриат экономического факультета ЮФУ по специальности экономическая теория. В 2011 — магистратуру по направлению «Экономическая теория», защитила магистерскую диссертацию.
Источник
Расширен перечень медизделий, которым не нужна регистрация, а также иные существенные изменения
 |
| Fahroni / Depositphotos.com |
Поправки к Закону об основах охраны здоровья граждан (частично уже вступили в силу, часть норм вступит в силу с 1 января 2022 г.) внесли значительные изменения в правила оборота медизделий:
- уточнено определение недоброкачественного медизделия (такое изделие не соответствует требованиям безопасности и эффективности медизделий, требованиям к их маркировке, нормативной, технической и эксплуатационной документации и не может быть безопасно использовано по назначению, установленному производителем), а также введено понятие «неблагоприятного события» (сюда входят побочные действия, не указанные в инструкции / руководстве, нежелательные реакции при применении медизделия, особенности взаимодействия медизделий между собой, факты и обстоятельства, создающие угрозу жизни и здоровью при применении и эксплуатации медизделий);
- разрешены применение (а также транспортировка, монтаж, наладка, настройка, калибровка, техобслуживание, ремонт) медизделия, на которое истек срок регистрационного удостоверения, но не истек срок службы/годности;
- более того, если в регдосье на медизделие внесены изменения, то еще полгода после этой даты разрешено производить медизделия в соответствии с информацией, содержащейся в регдосье до изменений, а также разрешено обращение таких медизделий до истечения срока их службы/годности;
- перечень медизделий, которые могут использоваться без их госрегистрации (или регистрации в ЕврАзЭС), дополнен новыми позициями, в частности, это зарубежные медизделия, ввезенные по разрешению Росздравнадзора для оказания медпомощи конкретному пациенту по жизненным показаниям, а также — укладки, наборы, комплекты и аптечки, состоящие из зарегистрированных медизделий и (или) промаркированных лекарств, в общей упаковке и при сохранении вторичной упаковки препаратов (с 2022 г. также медизделия для in vitro диагностики, которые применяются только в той медорганизации, которая их изготовила. Однако для этого нужно разрешение Росздравнадзора);
- с 2022 г. лицензирование деятельности по производству медтехники отменено, но сохранено лицензирование техобслуживания медизделий (владельцы лицензий техники, в части технического обслуживания обязаны переоформить их до 1 января 2024 г. на лицензии на деятельность по техническому обслуживанию медицинских изделий, кроме случаев обслуживания собственных нужд или обслуживания медизделий с низкой степенью потенциального риска их применения);
- с 2022 года вводится инспектирование производства медизделий на соответствие требованиям к внедрению, поддержанию и оценке системы менеджмента качества (для производства зарегистрированных медизделий и отдельных видов медизделий, изготавливаемых по индивидуальным заказам пациентов) (Федеральный закон от 30 апреля 2021 г. № 128-ФЗ «О внесении изменений в Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» и статьи 12 и 22 Федерального закона «О лицензировании отдельных видов деятельности»).
Все важные документы и новости о коронавирусе COVID-19 – в ежедневной рассылке Подписаться
Источник
Упрощенная регистрация мед. изделий для предупреждения распространения инфекционных заболеваний
Упрощенная регистрация медицинских изделий
19 марта 2020 года был введен особый порядок регистрации некоторых видов медицинских изделий, необходимых для предупреждения распространения инфекционных заболеваний. Упрощение процедуры регламентировано Постановлением Правительства № 299 от 18 марта 2020 г.
Правительство Российской Федерации упростило процедуру регистрации для 36 наименований медизделий – респираторов, медицинских масок, изолирующих халатов и костюмов, а также перчаток и бахил. Итоговый документ, регистрационное удостоверение, на данную продукцию ранее оформлялось в течении 3-5 месяцев. Теперь же, Росздравнадзор будет принимать решение о регистрации медицинских изделий, включенных в перечень, в течение трех-пяти рабочих дней дней после поступления первичного пакета документов. Далее уже потребуется в течении 150 дней довезти полный комплект документов.
Росздравнадзор опубликовал методические рекомендации по регистрации медицинских изделий с низкой степенью потенциального риска их применения.
Этим постановлением введен еще один вариант упрощенной регистрации (для продукции указанной в перечне приложенном к постановлению). В случае применения данного способа Регистрационное удостоверение действует до 1 января 2020 года, присутствует возможность регистрации партии медицинских изделий, признании иностранных протоколов испытаний.
Также допускается ввоз незарегистрированных медицинских изделий для проведения испытаний без получения разрешения на временной ввоз (единичные экземпляры).
Допускается реализация не зарегистрированных в Российской Федерации медицинских изделий одноразового использования по перечню, предусмотренному приложением к настоящему документу, без получения разрешения Федеральной службы по надзору в сфере здравоохранения, если указанные изделия зарегистрированы в установленном порядке в стране-производителе.
В перечень к ПП 430 вошли аппараты искусственной вентиляции лёгких (аппарат ИВЛ) разных видов, оксигенаторы, перчатки, костюмы изолюрующие, халаты медицинские, маски разных видов, термометры и т.д. (рекомендуем ознакомиться с полным перечнем отраженным в постановлении).
Однако вместе с упрощением, введенным указанным выше постановление, введены ограничительные меры Постановлением Правительства № 433 от 03 апреля 2020 года по продаже изделий для предотвращения заражения и производных (маски, респираторы, перчатки медицинские, марля) на 90 дней.
Пояснения к ПП 430 и 433
Итого была упрощена процедура получения регистрационного удостоверения на:
1. Костюм изолирующий
2. Перчатки смотровые/процедурные из латекса гевеи,
неопудренные, нестерильные
3. Перчатки смотровые/процедурные из латекса гевеи,
опудренные
4. Халат операционный одноразового использования
5. Халат операционный многоразового использования
6. Халат изолирующий многоразового использования
7. Халат изолирующий одноразового использования
8. Маска лицевая для защиты дыхательных путей
многоразового использования
9. Перчатки смотровые/процедурные из полихлоропрена,
неопудренные
10. Перчатки смотровые/процедурные из полихлоропрена,
опудренные
11. Бахилы токонепроводящие, нестерильные
12. Халат для пациента одноразового использования
13. Халат для пациента многоразового использования
14. Халат процедурный одноразового использования
15. Халат процедурный многоразового использования
16. Респиратор общего применения
17. Костюм хирургический изолирующий
18. Маска хирургическая многоразового использования
22. Перчатки смотровые/процедурные нитриловые,
опудренные
23. Костюм хирургический на манжетах
24. Перчатки смотровые/процедурные виниловые,
неопудренные
25. Перчатки смотровые/процедурные виниловые,
опудренные
26. Костюм хирургический одноразового использования,
нестерильный
27. Бахилы водонепроницаемые
28. Бахилы токопроводящие, нестерильные
29. Перчатки смотровые/процедурные из гваюлового
латекса, неопудренные
30. Перчатки смотровые/процедурные из
этиленвинилацетата, неопудренные, нестерильные
31. Перчатки смотровые/процедурные нитриловые,
неопудренные, антибактериальные
32. Перчатки смотровые/процедурные полиизопреновые,
неопудренные
33. Набор одежды хирургический/смотровой
34. Перчатки смотровые/процедурные полиизопреновые,
опудренные
35. Перчатки смотровые/процедурные из латекса гевеи,
неопудренные, нестерильные, антибактериальные
36. Маска лицевая для защиты дыхательных путей
одноразового использования
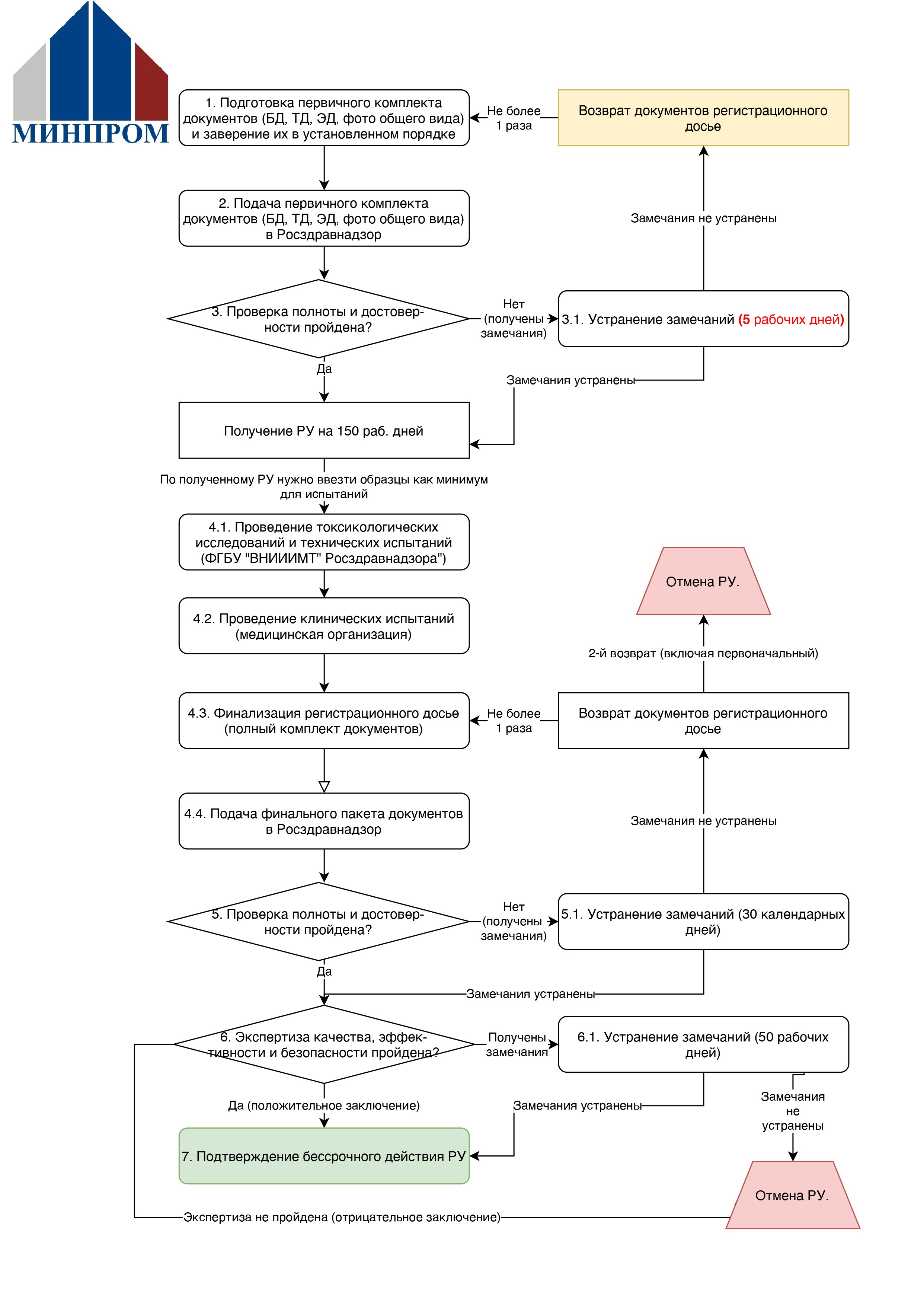
Процесс упрощенной регистрации
1) Подготавливается комплект базовых (юридических) документов, техническая и эксплуатационная документация, фото общего вида.
2) Данный пакет документов подается в Росздравнадзор.
3) Производится проверка полноты и достоверности, по результатам которой может выйти уведомление об устранении нарушений (необходимо устранить в течение 5 рабочих дней) или РУ.
4) В течение 150 рабочих дней во избежание аннулирования РУ необходимо провести токсикологические исследования, технические испытания, клинические испытания, доработать, при необходимости, техническую и эксплуатационную документацию, и подать пакет документов в Росздравнадзор.
5) Росздравнадзор проводит проверку полноты и достоверности, по результатам которой может выйти уведомление об устранении нарушений (необходимо устранить в течение 30 календарных дней) или направление в экспертное учреждение.
6) Экспертное учреждение проводит экспертизу в стандартном порядке (аналогично процедуре экспертизы при обычной регистрации медицинских изделий 1-го класса риска), по результатам которой выходит положительное заключение, замечания (необходимо устранить в течение 50 раб. дней) или отрицательное заключение (влечет отмену государственной регистрации и необходимость регистрации по стандартной процедуре.
7) После положительного заключения РУ продолжает действовать бессрочно.
Какие документы необходимы для оформления РУ
При регистрации медицинского изделия потребуется доверенность
Итого минимальный комплект документов требуемый для оформления составляет:
а) копия документа, подтверждающего полномочия
уполномоченного представителя производителя (изготовителя) (для иностранного изготовителя);
б) техническая документация производителя (изготовителя)
на медицинское изделие (для российского изготовителя разрабатываются Технические условия в соответствии с ГОСТ Р 1.3-2018 Технические условия на продукцию (общие требования к содержанию, оформлению, обозначению и обновлению));
в) эксплуатационная документация производителя (изготовителя)
на медицинское изделие, в том числе инструкция по применению
или руководство по эксплуатации медицинского изделия; (должны соответствовать требованиям Приказа Министерства здравоохранения РФ от 19 января 2017 г. N 11н «Об утверждении требований к содержанию технической и эксплуатационной документации производителя (изготовителя) медицинского изделия»)
г) фотографические изображения общего вида медицинского
изделия вместе с принадлежностями, необходимыми для применения
медицинского изделия по назначению (размером не менее
18 на 24 сантиметра);
д) опись документов.
В дальнейшем потребуется довезти (в течении 150 дней):
а) копия документа, подтверждающего полномочия
уполномоченного представителя производителя (изготовителя);
б) сведения о нормативной документации на медицинское изделие;
в) документы, указанные в подпунктах «б», «в» и «г» пункта 572
настоящих Правил (в случае внесения в них изменения
по результатам проведенных испытаний (исследований) медицинского
изделия);
г) документы, подтверждающие результаты технических испытаний
медицинского изделия, выданные федеральным государственным
бюджетным учреждением «Всероссийский научно-исследовательский
и испытательный институт медицинской техники» Федеральной службы
по надзору в сфере здравоохранения (далее — учреждение);
д) документы, подтверждающие результаты токсикологических
исследований медицинского изделия, использование которого
предполагает наличие контакта с организмом человека, выданные
учреждением;
е) документы, подтверждающие результаты испытаний
медицинского изделия в целях утверждения типа средств измерений
(в отношении медицинских изделий, относящихся к средствам измерений,
в сфере государственного регулирования обеспечения единства
измерений, перечень которых утверждается Министерством
здравоохранения Российской Федерации), выданные учреждением;
ж) документы, подтверждающие результаты клинических испытаний
медицинского изделия, проведенных в медицинской организации
государственной системы здравоохранения, отвечающей требованиям,
утвержденным Министерством здравоохранения Российской Федерации;
з) копии документов, подтверждающих качество лекарственного
препарата, фармацевтической субстанции, биологического материала
и иного вещества, с использованием которых произведено медицинское
изделие или которые входят в его состав и предназначены для применения
только с учетом назначения медицинского изделия, определенного
производителем, и выданных в соответствии с законодательством страны
происхождения лекарственного препарата, фармацевтической субстанции,
биологического материала и иного вещества;
и) оригинал регистрационного удостоверения;
Источник