- Мониторинг движения лекарственных препаратов (маркировка лекарств)
- Человеческий ресурс
- Места хранения
- Финансовый ресурс
- Время
- Прямой порядок
- Обратный порядок
- Подключаемся к системе мониторинга оборота лекарственных препаратов
- Обязанность участия в системе мониторинга.
- Ответственность субъектов обращения лекарственных средств.
- Алгоритм подключения к ИС МДЛП.
Мониторинг движения лекарственных препаратов (маркировка лекарств)
Правительством Российской Федерации в числе основных направлений определена работа по модернизации процесса движения лекарственных препаратов в соответствии с лучшими международными практиками, в том числе по унификации и упрощению процедур вывода лекарств на рынок без ущерба качеству, проведению мониторинга ассортиментной политики и цен на лекарственные препараты, совершенствованию методики регистрации предельных отпускных цен производителей на жизненно необходимые лекарственные препараты, мониторингу движения лекарственных препаратов для медицинского применения от производителя до конечного потребителя с использованием средств идентификации.
25 октября 2016 г. президиумом Совета при Президенте Российской Федерации по стратегическому развитию и приоритетным проектам утвержден паспорт приоритетного проекта «Внедрение автоматизированной системы мониторинга движения лекарственных препаратов от производителя до конечного потребителя для защиты населения от фальсифицированных лекарственных препаратов и оперативного выведения из оборота контрафактных и недоброкачественных препаратов». Краткое наименование — «Лекарства. Качество и безопасность».
Ключевые участники приоритетного проекта:
- Минздрав России;
- Росздравнадзор;
- ФНС России;
- Минпромторг России;
- Минфин России;
- Минкомсвязи России.
Субъекты обращения лекарственных препаратов:
- российские производители;
- российские и иностранные держатели регистрационных удостоверений и их представительства;
- организации оптовой и розничной торговли лекарствами;
- медицинские организации.
Цель приоритетного проекта:
- Защита населения от фальсифицированных, недоброкачественных и контрафактных лекарственных препаратов и предоставление неограниченному кругу потребителей (граждан) возможности проверки легальности зарегистрированных лекарственных препаратов, находящихся в гражданском обороте. Обеспечение прозрачности и развития справедливой конкуренции на фармацевтическом рынке.
Основными ресурсами, освещающими реализацию проекта МДЛП, являются официальные сайты Минздрава России, Росздравнадзора, Национальной системы цифровой маркировки «Честный знак». Информации в соответствующих разделах много, но в сегменте вопросов, касающихся медицинских организаций, она крайне дозированная и отвечает далеко не на все вопросы. При этом важно разобраться, что находится в силах и компетенции самой медицинской организации, и к чему придется тщательно готовиться, особенно к тем аспектам процесса лекарственного обеспечения, на которые система МДЛП влияет опосредованно, без регуляторного или технического воздействия.
Система мониторинга движения лекарственных препаратов будет внедряться с 01.07.2020 одномоментно по всей стране, вовлекая огромное число субъектов обращения лекарственных препаратов. По официальным оценкам в системе будут зарегистрированы около тысячи производителей и держателей регистрационных удостоверений на лекарственные препараты, порядка 2,5 тысяч оптовых фармацевтических организаций и 350 тысяч медицинских и аптечных организаций, не говоря о том, что эта система коснется всех без исключения конечных потребителей — пациентов, а это, без преувеличения, всё население Российской Федерации.
Эксперимент по внедрению системы маркировки лекарств в соответствии с Постановлением Правительства РФ от 24.01.2017 № 62 «О проведении эксперимента по маркировке контрольными (идентификационными) знаками и мониторингу за оборотом отдельных видов лекарственных препаратов для медицинского применения» (вместе с «Положением о проведении эксперимента по маркировке контрольными (идентификационными) знаками и мониторингу за оборотом отдельных видов лекарственных препаратов для медицинского применения») стартовал в начале 2017 года и закончится непосредственно перед переходом к промышленной эксплуатации в конце 2019 года. Промежуточные результаты и опыт добровольных участников эксперимента уже сегодня объективно показывают, что задачи, стоящие перед субъектами оборота лекарственных препаратов, далеко не простые и требуют серьезной подготовки, как организационной, так и финансовой.
При подготовке к внедрению системы МДЛП руководству медицинской организации необходимо самым тщательным образом подойти к оценке готовности и достаточности всех видов её ресурсов.
Человеческий ресурс
Трудоёмкость приемки товара при внедрении системы маркировки неизбежно возрастает, особенно, если мест приемки и выбытия лекарств из гражданского оборота в организации несколько. Частично решить этот вопрос можно при применении автоматизированных средств оптимизации считывания кодов с упаковок, но на рынке пока нет доступных решений, которые бы подходили для данных целей.
Места хранения
С 29.11.2019 ст. 67 Федерального закона от 12.04.2010 № «Об обращении лекарственных средств» дополняется ч. 7.1 в следующей редакции «Лекарственные препараты для медицинского применения, введенные в гражданский оборот до 1 января 2020 года, подлежат хранению, перевозке, отпуску, реализации, передаче, применению без нанесения средств идентификации до истечения срока их годности.». Это значит, что с 1 января 2020 года поток медикаментов разделится на маркированный подтвержденный, маркированный неподтвержденный и немаркированный, что потребует увеличения площадей и мест хранения препаратов, так как совместное хранение этих групп товаров может привести к нарушению требований системы мониторинга движения.
С учетом вышеописанных возможных проблем с увеличением длительности проведения закупочных процедур необходимо пересмотреть в сторону увеличения нормативы складских запасов лекарств, которые смогут обеспечить непрерывность лечебно-диагностического процесса в случае непредвиденных обстоятельств.
Финансовый ресурс
Вышеуказанный прирост численности работников требует увеличения фонда оплаты труда. Потребуются затраты на организацию новых рабочих мест, оснащенным специальным оборудованием, оптимизацию систем хранения, увеличение объемов складских запасов, а также на закупку или развитие информационных систем. Это существенные затраты для любой организации, их надо планировать и своевременно изыскивать.
Время
Временные затраты на администрирование всех этапов движения лекарственных препаратов также вырастут, этот фактор крайне важно заложить в систему управления производственными процессами.
Одним из важнейших аспектов внедрения системы МДЛП для медицинского учреждения является необходимость перенастройки порядка взаимодействия с поставщиками лекарственных препаратов. В соответствии с п. 44 Положения о системе мониторинга движения лекарственных препаратов для медицинского применения, утвержденного Постановлением Правительства Российской Федерации от 14.12.2018 № 1556 «Об утверждении Положения о системе мониторинга движения лекарственных препаратов для медицинского применения» (далее — Положение) при передаче лекарственных препаратов между субъектами обращения внесение информации в ФГИС МДЛП может происходить двумя способами:
При этом решение о выборе типа порядка предоставления сведений принимается субъектами обращения лекарственных препаратов, предоставляющими данные сведения, самостоятельно. Это решение необходимо закрепить в контракте на поставку лекарственных препаратов.
Прямой порядок
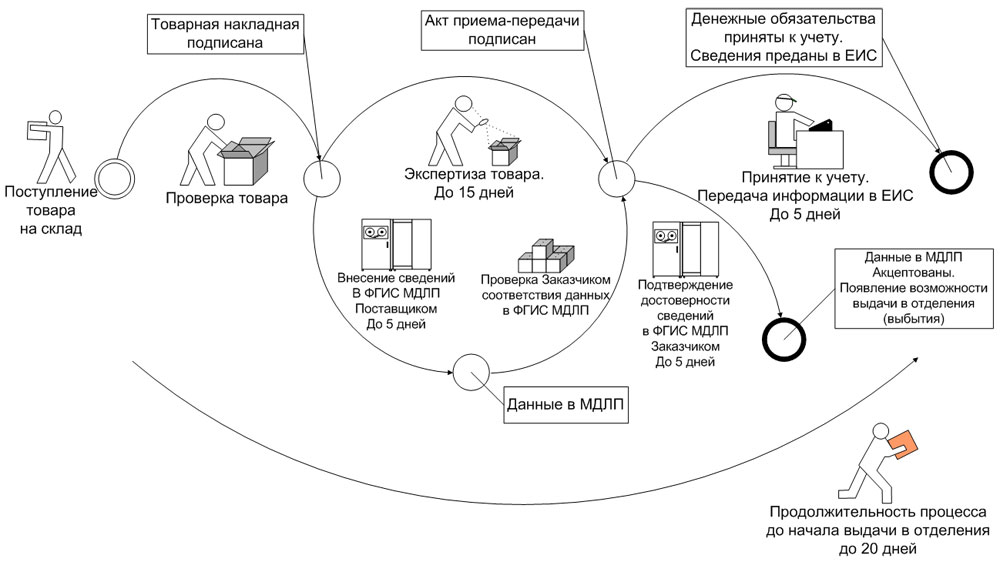
В случае выбора прямого порядка предоставления сведений субъект обращения, осуществляющий передачу лекарственных препаратов другому субъекту обращения в рамках гражданско-правовых отношений (поставщик), предусматривающих переход права собственности на данные лекарственные препараты, или в рамках посреднических отношений (агентский или комиссионный договор), в течение 5 рабочих дней* с даты отгрузки лекарственных препаратов предоставляет об этом в ФГИС МДЛП сведения, предусмотренные пунктом 2 приложения № 6 к Положению.
При этом субъект обращения, осуществляющий приемку лекарственных препаратов от другого субъекта обращения ЛП в рамках гражданско-правовых отношений (заказчик, медицинская организация), предусматривающих переход права собственности на данные лекарственные препараты, или в рамках посреднических отношений (агентский или комиссионный договор), в течение 5 рабочих дней* с даты приемки лекарственных препаратов и регистрации в ФГИС МДЛП сведений об отгруженных медикаментах, но до предоставления сведений о дальнейших операциях с данными препаратами, подтверждает достоверность сведений, содержащихся в ФГИС МДЛП о принимаемых лекарственных препаратах, предоставляя об этом сведения в ФГИС МДЛП, предусмотренных пунктом 4 приложения № 6 к Положению (рис. 1).
Рис. 1. Прямой способ внесения информации в ФГИС МДЛП
Обратный порядок
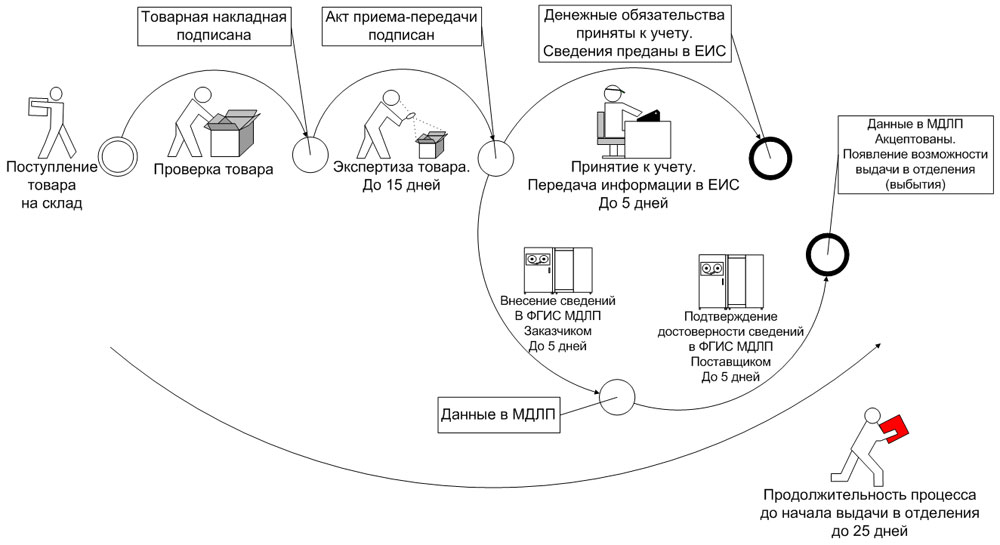
В случае выбора обратного порядка предоставления сведений субъект обращения, осуществляющий приемку медикамента от другого субъекта обращения в рамках гражданско-правовых отношений, предусматривающих переход права собственности на ЛП, или в рамках посреднических отношений (агентский или комиссионный договор), в течение 5 рабочих дней* с даты приемки ЛП предоставляет в ФГИС МДЛП сведения о принятых ЛП, предусмотренные пунктом 3 приложения № 6 к Положению.
При этом субъект обращения, осуществивший передачу лекарства другому субъекту обращения в рамках гражданско-правовых отношений, предусматривающих переход права собственности на данные лекарственные препараты, или в рамках посреднических отношений (агентский или комиссионный договор), в течение 5 рабочих дней* с даты регистрации в ФГИС МДЛП сведений о принятом товаре, но до предоставления сведений о дальнейших операциях с данными препаратами, подтверждает достоверность сведений, содержащихся в ФГИС МДЛП о переданных лекарственных препаратов, предоставляя об этом сведения в ФГИС МДЛП, предусмотренные пунктом 4 приложения № 6 к Положению (рис. 2).
Рис. 2. Обратный способ внесения информации в ФГИС МДЛП
В ходе подготовки к работе в новых условиях системы МДЛП важно учесть особенности медицинской организации в части её системы финансирования, организационной структуры, наличию удаленных (обособленных) подразделений, организации закупок лекарственных препаратов, в том числе участие в централизованных поставках и иные аспекты деятельности, обусловливающие многочисленные внутренние и внешние взаимосвязи, необходимые для бесперебойной работы системы лекарственного снабжения, и проводить внедрение новой системы в контексте данных качественного анализа деятельности организации.
* На заседании рабочей группы Росздравнадзора было принято решение о внесении изменений в Положение, предусматривающих сокращение сроков регистрации операций в ИС МДЛП по передаче лекарственных препаратов всеми участниками до 1 рабочего дня, в целях соблюдения приоритета интересов пациента и предоставления медицинской организации возможности выполнения требований законодательства в сфере охраны здоровья, обращения лекарственных препаратов и закупок (контрактной системы) без нарушений.
Источник
Подключаемся к системе мониторинга оборота лекарственных препаратов
Автор: Тарасова Е. А., эксперт журнала
О системе мониторинга движения лекарственных препаратов для медицинского применения и необходимости подключения к ней участников оборота этих препаратов, а также о принимаемых мерах по созданию данной системы мы неоднократно писали на страницах нашего журнала. Теперь пора переходить от теории к практике. И поможет в этом аптекам и аптечным сетям Инструкция по подключению к ИС МДЛП, опубликованная Росздравнадзором в Письме от 20.05.2019 № 01и-1269/19.
Обязанность участия в системе мониторинга.
Юридические лица и ИП, осуществляющие производство, хранение, ввоз в РФ, отпуск, реализацию, передачу, применение и уничтожение лекарственных препаратов для медицинского применения, должны обеспечить внесение информации о лекарственных препаратах для медицинского применения в информационную систему движения мониторинг лекарственных препаратов (ИС МДЛП) с 1 января 2020 года. Напомним: эта обязанность обусловлена положениями Федерального закона от 28.12.2017 № 425-ФЗ[1] и ч. 7 ст. 67 Закона № 61-ФЗ[2].
Организации и ИП, не подключившиеся к ИС МДЛП, с 1 января 2020 года не смогут осуществлять обращение лекарственных препаратов, имеющих маркировку контрольными (идентификационными) знаками DataMatrix.
Порядок внесения информации о лекарственных препаратах в ИС МДЛП субъектами обращения лекарственных средств и ее состав регламентирован Положением о ИС МДЛП (утверждено Постановлением Правительства РФ от 14.12.2018 № 1556)[3]. А инструкция, определяющая порядок действий субъектов обращения лекарственных средств при подключении к ИС МДЛП, приведена в вышеупомянутом Письме Росздравнадзора № 01и-1269/19.
Итак, организации и ИП, имеющие намерение осуществлять оборот лекарственных препаратов для медицинского применения, до 1 января 2020 года обязаны (Письмо Росздравнадзора № 01и-1269/19)[4]:
пройти регистрацию в ИС МДЛП для медицинского применения;
иметь личный кабинет субъекта обращения лекарственных средств с целью внесения информации о лекарственных препаратах в систему мониторинга.
Ответственность субъектов обращения лекарственных средств.
За производство или продажу лекарственных препаратов для медицинского применения без нанесения средств идентификации, с нарушением установленного порядка их нанесения, а также за несвоевременное внесение данных в ИС МДЛП для медицинского применения или внесение в нее недостоверных данных организации и ИП несут ответственность в соответствии с действующим законодательством.
Так, несвоевременное внесение данных в ИС МДЛП для медицинского применения либо внесение в нее недостоверных данных согласно ст. 6.34 КоАП РФ (действует с 1 января 2020 года[5]) влечет штраф:
для должностных лиц – в размере от 5 до 10 тыс. руб.;
для юридических лиц (и ИП) – в размере от 50 до 100 тыс. руб.
Кроме того, согласно ч. 2 ст. 15.12 КоАП РФ продажа товаров и продукции без маркировки и (или) нанесения информации, предусмотренной законодательством РФ, в случае если такая маркировка и (или) нанесение такой информации обязательны, а также хранение, перевозка либо приобретение таких товаров и продукции в целях сбыта, за исключением продукции, указанной в ч. 4 названной статьи, влечет наложение штрафа:
на должностных лиц – в размере от 5 до 10 тыс. руб. с конфискацией предметов административного правонарушения;
на юридических лиц – в размере от 50 до 300 тыс. руб. с конфискацией предметов административного правонарушения.
Алгоритм подключения к ИС МДЛП.
Для начала работы с ИС МДЛП аптекам и аптечным сетям необходимо выполнить следующие действия (причем некоторые из них могут выполняться параллельно – для ускорения процесса подключения к системе).
Этап
Описание
Определите круг лиц (пользователей), которые будут регистрировать те или иные действия с лекарственными препаратами в ИС МДЛП, а также то, как они будут это делать и в какой момент
Справка. Какие именно действия должны регистрироваться в ИС МДЛП, описано в документе «Паспорта процессов». Он размещен в разделе «Маркировка лекарств» на сайте https://честныйзнак.рф в подразделе «Документы», блок «Основные действия участников МДЛП»
Получите для руководителя организации и каждого пользователя усиленную квалифицированную электронную подпись (УКЭП) в аккредитованном Минкомсвязи удостоверяющем центре (УЦ).
При получении УКЭП руководителя необходимо обратить внимание на точное соответствие данных сертификата данным ЕГРЮЛ. В случае их несоответствия доступ в ИС МДЛП с использованием такого сертификата будет невозможен
Справка. Список центров размещен по адресу https://digital.gov.ru/ru/activity/govservices/2
Установите средство криптографической защиты информации (СКЗИ), содержащее криптопровайдер (CSP), с поддержкой ГОСТ Р 34.10-2012** на компьютер, с которого предполагается регистрировать ответственных пользователей, работающих с ИС МДЛП
Справка. Процесс установки СКЗИ и сертификата УКЭП детально описан в «Руководстве пользователя личного кабинета субъекта обращения лекарственных препаратов» в разд. 2.1 «Установка ПО и сертификатов» и приложении Б «Инструкции по установке криптографического ПО». Документ расположен в разделе «Маркировка лекарств» на сайте https://честныйзнак.рф в подразделе «Документы», блок «Основные действия участников МДЛП».
При возникновении сложностей с выполнением этого и последующих шагов можно обратиться в службу технической поддержки оператора системы по адресу support@crpt.ru или через форму обратной связи на сайте https://честныйзнак.рф
С этого компьютера, используя полученную УКЭП руководителя, зарегистрируйте субъект обращения мониторинг лекарственных препаратов в ИС МДЛП.
О факте регистрации субъекта в ИС МДЛП необходимо проинформировать территориальный орган Росздравнадзора, орган управления здравоохранением субъекта РФ и центр компетенции в соответствующем субъекте РФ
Справка. Для этого нужно воспользоваться ссылкой https://mdlp.crpt.ru или кнопкой «Вход в систему» в разделе «Маркировка лекарств» на сайте https://честныйзнак.рф. Данный шаг подробно описан в «Руководстве пользователя личного кабинета…» в разд. 2.2 «Регистрация Личного кабинета Участника в ИС «Маркировка»
Получите УКЭП пользователей (определенных на шаге 1), если они не были получены на шаге 2, а затем зарегистрируйте этих пользователей в ИС МДЛП (используя средства личного кабинета ИС МДЛП, УКЭП руководителя и установленное СКЗИ). Установите СКЗИ и сертификаты УКЭП данных пользователей на их рабочие места
Справка. Подробно данный шаг описан в разд. 4.11 «Добавить запись пользователя в ЛК Участника (Администрирование)» «Руководства пользователя личного кабинета…»
Закрепите (при необходимости) определенный на шаге 1 порядок действий сотрудников по регистрации действий с лекарственными препаратами во внутренних организационно-распорядительных документах организации
Закажите (при необходимости) доработку используемых информационных систем для автоматизации разработанных бизнес-процессов в соответствии с порядком действий, определенном на шаге 1.
Кроме того, необходимо зарегистрировать в ИС МДЛП используемую субъектом обращения информационную систему, с помощью которой предполагается выполнять обмен данными с ИС МДЛП
Справка. Список разработчиков информационных систем, активно сотрудничающих с Оператором системы, можно найти в подразд. «Партнеры» по ссылке https://честныйзнак.рф/business/projects/21/#87.
Порядок регистрации информационной системы подробно описан в разд. 4.12 «Добавить, удалить учетную систему в ЛК Участника (Администрирование)» «Руководства пользователя личного кабинета…»
– порядок отзыва (при увольнении и изменении должностных обязанностей) ключей электронной подписи пользователей и закрепите его (при необходимости) во внутренних организационно-распорядительных документах;
– иные действия, необходимые для снижения риска компрометации ключей электронной подписи
Составьте перечень мест хранения лекарственных препаратов и мест их выбытия, проверьте его соответствие лицензиям. Опишите в личном кабинете список мест осуществления деятельности в соответствии с составленным перечнем
Справка. Эти действия подробнее описаны в разд. 4.5 «Добавить место деятельности Участника в ЛК Участника» «Руководства пользователя личного кабинета…»
При наличии у субъекта договорных отношений с другими участниками оборота, в соответствии с которыми субъект выполняет действия с лекарственными препаратам в местах осуществления деятельности другими участниками, эти места необходимо указать в соответствии с разд. 4.6 «Добавить место ответственного хранения в ЛК Участника» «Руководства пользователя личного кабинета…»***
Определите порядок действий пользователей при отказе ИС МДЛП зарегистрировать действие с лекарственным препаратом
Справка. Перечень возможных причин отказа приведен в документе «Описание XSD» для каждой регистрируемой в ИС МДЛП операции
В «песочнице» ИС МДЛП (https://sb.mdlp.crpt.ru) с помощью технической поддержки оператора системы (support@crpt.ru) зарегистрируйте тестовые коды маркировки лекарственных препаратов и уведомление об их отгрузке в адрес субъекта-получателя
Справка. Максимальное количество выдаваемых службой технической поддержки в рамках одного обращения кодов маркировки вторичных упаковок для использования в «песочнице» составляет не более 5 штук
Проверьте работоспособность разработанных бизнес-процессов и обученность пользователей (их готовность к реализации этих процессов), используя в качестве исходных данных для прохождения контрольных примеров зарегистрированные на предыдущем шаге в «песочнице» МДЛП коды маркировки лекарственных препаратов
Проверьте (при необходимости) подключение к рабочему контуру ИС МДЛП и работоспособность заказанных доработок информационных систем (шаг 7) во взаимодействии с организацией, обслуживающей данные информационные системы
* Шаги 1 и 2 – 5 могут выполняться параллельно.
** Список сертифицированных на соответствие указанному ГОСТу СКЗИ доступен на сайте ФСБ по ссылке http://clsz.fsb.ru/certification.htm.
***Следует учесть, что реализацию и вывод из оборота для медицинского применения в местах ответственного хранения зарегистрировать невозможно.
[1] «О внесении изменений в Федеральный закон «Об обращении лекарственных средств».
[2] Федеральный закон от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств».
[3] Утверждено Постановлением Правительства РФ от 14.12.2018 № 1556.
[4] Дополнительно информацию по данному вопросу можно получить на официальном сайте Росздравнадзора (http://roszdravnadzor.ru) в разделе «Система маркировки лекарственных препаратов (пилотный проект)» и на официальном сайте оператора системы ООО «Оператор-ЦРПТ» по ссылке https://честныйзнак.рф/business/projects/21.
[5] Федеральный закон от 15.04.2019 № 58-ФЗ «О внесении изменений в Кодекс Российской Федерации об административных правонарушениях».
Источник