Источники и методы получения лекарственных веществ
Источники лекарственных веществ (лекарственное сырье):
из растительного сырья: резерпин, морфин, пилокарпин;
из ткани животных: кортикотропин;
из продуктов жизнедеятельности микроорганизмов: антибиотики;
из минерального сырья.
Пути получения лекарственных веществ:
метод простой обработки: высушивание и измельчение лекарственного сырья. Получаемые препараты называли простыми;
извлечение биологически активных компонентов с частичным освобождением их от примесей (балластных веществ). Препараты, полученные таким образом, называют сложными, или галеновыми. К ним относятся настойки, экстракты. Недостаток: имеющиеся примеси (красящие вещества, белки, слизь) могут ослабить действие лекарственных веществ и препятствовать их парентеральному применению;
извлечение биологически активных компонентов в химико-фармацевтической промышленности с практически полным удалением балластных веществ, что позволило применять эти препараты парентерально. Такие препараты называют новогаленовыми (например, адонизид, лантозид и др.). Они содержат комплекс химических веществ, от которых зависит биологическая активность сырья и изготовленных из него препаратов.
синтез биогенных веществ: адреналин, норадреналин, простагландины;
синтез антиметаболитов, т.е. веществ, близких по структуре к естественным метаболитам, но их функций не выполняющих: сульфаниламиды, азатиоприн;
химическая модификация известных лекарственных веществ: барбитураты, глюкокортикоиды;
синтез метаболитов самого лекарственного вещества. Фенацетин в организме превращается в парацетамол. Данное вещество в настоящее время синтезируется и используется как самостоятельный препарат, обладает более высокой активностью и вызывает меньше побочных эффектов.
метод генной и клеточной инженерии: инсулин, соматостатин.
Этапы создания лекарств изложены в кафедральном учебно-методическом пособии «Общая фармакология».
Фармакопея
Фармакопея (от греч. pharmacon — лекарство, poieo — делаю) — сборник нормативных документов, регламентирующий требования к качеству лекарств, способы аптечного изготовления лекарственных форм, высшие разовые и суточные дозы ядовитых и сильнодействующих препаратов и ряд других стандартов и положений. Носит законодательный характер. Не является учебным пособием, а предназначена для работы контрольно-аналитических служб фармацевтических предприятий и аптечных учреждений.
Кроме Государственной фармакопеи существует Международная фармакопея, которая присваивает единые международные непатентованные наименования лекарственным веществам, осуществляет унификацию терминологии, методов анализа и требований к лекарственным препаратам.
Каждое лекарство имеет три названия: полное химическое, международное непатентованное и патентованное.
Полное химическое название слишком сложное и не употребляется во врачебной практике. Оно соответствует химической формуле и приводится в справочниках и аннотациях к лекарствам.
Международное непатентованное название (генерическое) — это единое официально принятое в фармакопеях различных стран название. Непатентованные названия должны иметь близость в названии к другим препаратам той же группы.
Патентованные названия — это коммерческие названия препаратов, выпускаемые различными фирмами. У каждого лекарства может быть несколько или даже много патентованных названий.
Пример: аспирин – международное название; ацетилсалициловая кислота – химическое; аспинат, ацилпирин, микристин, плидол и т.д. – патентованные, фирменные.
Аптека (от греч. ─ apotheke, от лат. ─ officina ─ склад) ─ учреждение здравоохранения, основные функции которого заключаются в приготовлении, хранении и отпуске лекарственных средств по рецептам врачей и без рецептов. В задачи аптеки входят также снабжение лекарственными средствами лечебно-профилактических учреждений, заготовка лекарственного растительного сырья, оказание неотложной первой медицинской помощи, распространение санитарно-гигиенических знаний среди населения.
хозрасчетные: осуществляют весь комплекс задач, стоящих перед аптеками, для обеспечения медикаментами и медицинскими товарами населения;
больничные: обеспечивают медикаментами и медицинскими товарами стационарных больных лечебных учреждений;
Рецепт (от лат. receptum ─ взятое) — это письменное обращение врача в аптеку об отпуске больному лекарственного средства в определенной лекарственной форме и дозировке с указанием способа его употребления. Является врачебным и юридическим документом. Правила выписывания рецептов для амбулаторных больных и отпуска по ним лекарств установлены соответствующим приказом Министерства здравоохранения.
штамп лечебного учреждения
число, месяц, год
b) Nomen aegroti
фамилия и инициалы больного, его возраст
фамилия и инициалы врача
Praepositio s. Invocatio
перечисление входящих в рецепт лекарственных средств
Praescriptio s. Subscriptio
предписание врача фармацевту о приготовлении определенной лекарственной формы и отпуске ее в определенном количестве
предписание врача больному о способе приема лекарства (количества, кратности приема, связь с приемом пищи)
подпись врача, его личная печать, печать лечебного учреждения
Правила выписывания рецептов:
Рецепт пишут по специальной форме на латинском языке, предписание же больному — на русском или на национальном языках. Писать рецепт принято четким, ясным почерком, чернилами или шариковой ручкой на форменном бланке. Исправления в рецепте не допускаются.
Возраст больного указывается в тех случаях, когда рецепт выписывают ребенку до 18 лет или больному старше 60 лет, а также при выписке лекарственных препаратов на льготных основаниях.
Состав лекарственного средства, обозначение лекарственной формы и обращение врача к фармацевту об изготовлении и выдаче лекарственного препарата выписываются на латинском языке.
Латинский текст начинается с обращения к фармацевту — «Recipe:», что значит «Возьми:». На рецептурном бланке оно сокращенно обозначается Rp. Затем перечисляют входящие в данный рецепт названия веществ в родительном падеже с указанием их количеств.
Существуют сокращенные и развернутые прописи. При выписывании лекарственных средств сокращенно в рецепте сначала указывают лекарственную форму (Solutionis. (Раствора. ); Suspensionis. (Суспензии. ); Unguenti. (Мази. ) и т. д.), затем ─ название лекарственного средства, концентрацию (если это необходимо), количество. В развернутой форме перечисляют все входящие в лекарственный препарат ингредиенты и их количества. В том случае, если в пропись входит несколько компонентов, сначала выписывают основное лекарственное вещество — Basis, затем следуют вспомогательные вещества—Adjuvans. Иногда выписывают вещества, улучшающие вкус, запах лекарственного препарата, которые называют исправляющими— Corrigens. Лекарственная форма определяется в ряде случаев самим лекарственным средством. Однако может возникнуть необходимость в Constituens — веществе, придающем лекарству определенную консистенцию. В этом случае Constituens приводится в рецепте после основных и вспомогательных веществ. Далее с помощью принятых обозначений отмечают ту лекарственную форму, которая должна быть изготовлена, например М. f. unguentum (Misce ut fiat unguentum — Смешай, чтобы образовалась мазь).
Дозы лекарственных веществ указывают в десятичной системе измерения. Единицей массы является 1,0 ─ один грамм. При дозировании лекарств пользуются и величинами менее 1,0: 0,1 ─ один дециграмм, 0,01 ─ один сантиграмм. 0,001 — один миллиграмм, 0,0001 — один децимиллиграмм, 0,00001 — один сантимиллиграмм и т. д. Количество жидких веществ дают в миллилитрах (ml), граммах или каплях. Количество капель обозначают римской цифрой, перед которой пишут gtts (сокращенное обозначение слова guttas—капель — в винительном падеже множественного числа), например gtts. V (капель пять). При выписывании лекарственных средств, дозируемых в единицах действия (ЕД), в рецепте вместо весовых или объемных количеств указывают число ЕД.
Иногда врач не приводит количество Constituens (например, в суппозиториях), предоставляя фармацевту право взять его, сколько нужно; в этом случае пишут q. s. (quantum satis), т. е. сколько потребуется, но это относится только к индифферентным веществам. Если несколько лекарственных веществ выписывают в одной и той же дозе, то ее цифровую величину обозначают только один раз после названия последнего вещества. Для обозначения того, что отмеченное количество относится и ко всем перечисленным выше наименованиям, ставят знак аа, что значит ana ─ поровну.
Количества веществ, входящих в пропись, указывают на правой стороне рецептурного бланка рядом с наименованием вещества (или на одну строку ниже). В тех случаях, когда максимальную дозу ядовитых или сильнодействующих веществ превышают, необходимо указать их количество прописью с добавлением восклицательного знака и подписи в подтверждение того, что большая доза выписана не случайно. Если правильность выписанной дозы не подтверждена, фармацевт снижает дозу вещества (до 50% от высшей разовой дозы, указанной в Фармакопее).
В конце рецепта после обозначения S. (Signa. Signetur.— Обозначь. Пусть будет обозначено) дают предписание больному или медицинскому персоналу о способе употребления лекарственного средства. В этой части рецепта, называемой сигнатурой (Signatura), коротко и исчерпывающе указывают:
1) дозировку (по 1 порошку, по 1 таблетке, по 1 столовой ложке, по 20 капель и т. д.);
2) время и частоту приема лекарственного средства (сколько раз в день, до еды или после еды, на ночь и т. д.);
3) способ применения препарата (внутривенно, подкожно, вводить медленно и т. д.).
Выдавая больным рецепт, врач должен подписать рецепт и поставить личную печать.
Если состояние больного требует немедленного отпуска лекарственного средства из аптеки, то на рецепте слева вверху пишут Cito (Скоро) или Statim (Тотчас). В этом случае лекарственное средство должно быть изготовлено и отпущено вне очереди.
Когда врач выписывает лекарство для себя, на рецепте пишут Pro autore—Для автора или Pro me — Для меня.
Источник
Методы получения лекарственного вещества
Разработка лекарственного средства начинается с синтеза новых химических соединений. Вещества со сложной структурой можно получить из различных иа очников, например растений (сердечные гликозиды), тканей животных (гепарин), микробных культур (бензилпенициллин), культур человеческих клеток (урокиназа), или посредством генно-инженерных технологий (человеческий инсулин).
Чем больше ясности во взаимоотношениях структуры и активности, тем более направленным оказывается поиск новых веществ.
а) Доклинические испытания дают информацию о биологических эффектах новых веществ. Начальный скрининг может включать биохимические и фармакологические исследования (анализ связывания с рецептором) или эксперименты на культурах клеток, изолированных клетках и изолированных органах.
Поскольку эти модели не способны воспроизвести сложные биологические процессы, происходящие в интактных организмах, любое потенциальное лекарственное средство необходимо проверить на животных. Только эксперименты на животных позволяют выяснить, возникаютли желаемые эффекты при дозах, не вызывающих токсичности или сопровождающихся слабой токсичностью. Цель токсикологических исследований заключается в том, чтобы оценить:
1) токсичность, обусловленную кратковременным или длительным приемом;
2) генетические повреждения (генотоксичность, мутагенез);
3) развитие опухолей (канцерогенность);
4) возникновение врожденных дефектов (тератогенность).
В экспериментах на животных также оценивают всасывание, распределение, метаболизм и элиминацию (фармакокинетика) изучаемых веществ. На уровне доклинического изучение лишь у малой части новых веществ обнаруживается потенциал для применения у человека.
Фармацевтическиетехнологии предлагают методы изготовления лекарственных форм.
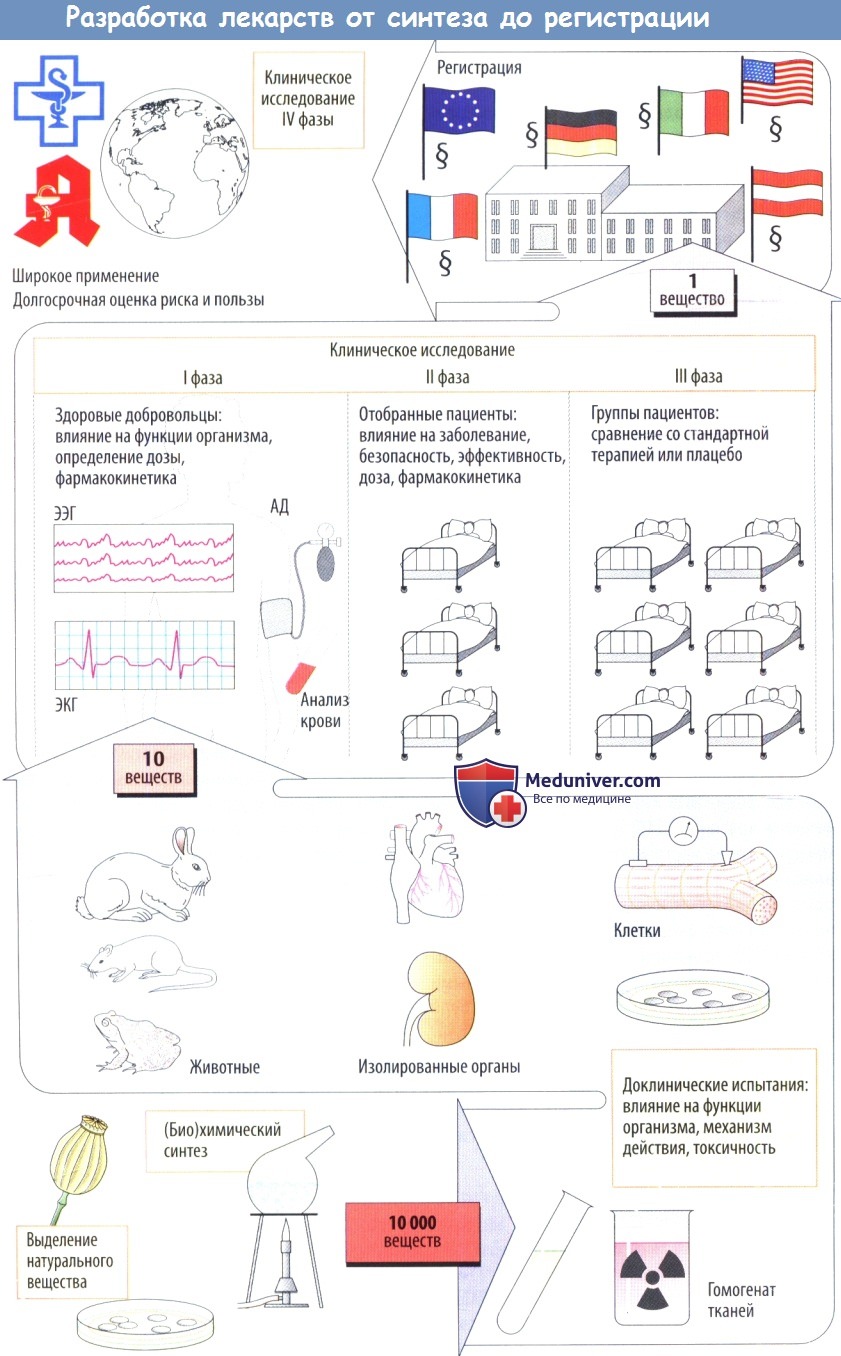
б) Клинические испытания начинаются с исследований I фазы, в которых участвуют здоровые лица; цель этих исследований — определить, будут ли эффекты, наблюдаемые у животных, также возникать у людей. Кроме того, на данном этапе определяется дозозависимость клинических эффектов.
Во II фазе потенциальные лекарственные средства сначала проверяют на отобранных пациентах на терапевтическую эффективность при заболевании, для лечения которого эти препараты предназначались. Если полезное действие очевидно, а частота побочных эффектов приемлема, начинается III фаза, в которой участвует более крупная группа пациентов, у которых новое средство сравнивают с традиционными методами лечения сточки зрения терапевтического результата.
Как форма экспериментов на людях, эти клинические исследования подвергаются анализу и одобрению этическими комитетами медицинских учреждений в соответствии с международными правилами проведения (Хельсинкской, Токийской и Венецианской декларациями). Во время клинических исследований выясняется, что многие вещества нельзя использовать. Как правило, в конце концов примерно из 10 000 вновь синтезированных веществ остается только одно.
в) Решение зарегистрировать новое лекарственное средство выносится национальным регуляторным органом (Food and Drug Administration в США, Health Protection Branch Drugs Directorate в Канаде, комиссией ЕС вместе с European Medicines Agency в Великобритании), которому производители должны подавать регистрационные документы.
Заявители должны документально подтвердить результатами соответствующих испытаний (доклинических и клинических), что критерии эффективности и безопасности удовлетворены и что лекарственные формы продукта (таблетки, капсулы и т. д.) соответствуют всем стандартам контроля качества.
После регистрации новое лекарственное средство может продаваться под торговым названием, оно должно быть доступным, выписываться врачами и отпускаться фармацевтами. В это время наблюдение продолжается в форме постмаркетинговых исследований (IV фаза клинических исследований)
г) Фармакологический надзор — действия, направленные на то, чтобы выявлять и устранять связанные с препаратом риски во время проведения клинических исследований и последующего его выхода на рынок. Фармаконадзор включает отчеты о предполагаемых случаях нежелательных реакций, направляемые в национальные регуляторные органы.
На основе длительного опыта применения можно правильно оценить соотношение риска и пользы и, следовательно, терапевтическую ценность нового лекарственного средства. Если новый препарат имеет небольшое преимущество перед существующими, необходимо принимать во внимание соотношение затрат и пользы от применения лекарственного средства.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник


