Метаболизм лекарственного средства что это
Большинство лекарств метаболизируется до их выведения из организма. Метаболические реакции разделяют на две большие группы — реакции фазы 1 и фазы 2:
• реакции фазы 1: окисление, восстановление и гидролиз, в результате которых к молекуле лекарственного вещества присоединяется химическая группа, снижающая активность образованного соединения и повышающая его полярность (и обычно его водорастворимость);
• реакции фазы 2: конъюгирование или синтетические реакции с присоединением крупной химической группы. Этот процесс обычно также повышает водорастворимость и облегчает экскрецию препарата из организма.
Природа, функции и количество ферментов, метаболизирующих лекарства, у разных индивидов неодинаковы, следствием чего является неодинаковая скорость метаболизма лекарства и его выведения. Ферменты, метаболизирующие лекарства, обладают широкой специфичностью по отношению к субстратам, однако специфичность ферментов носит относительный, а не абсолютный характер. Это означает, что один фермент может катализировать метаболизм многих различных лекарств и что в метаболизме одного и того же лекарства может участвовать несколько изоформ фермента. Обычной метаболической реакцией является окисление.
При окислении к молекуле вещества присоединяется гидроксильная группа или удаляется алкильная, или метильная группа. Примером такой реакции может служить деметилирование теофиллина с образованием 1-метилксантина. Первичным ответственным ферментом служит CYP1A2, однако реакцию катализируют также изоформы CYP1A1 и CYP2D6.
Метаболизирующие лекарства ферменты представлены множеством форм, и индивидуальные различия их генетической экспрессии определяют индивидуальные различия метаболизма лекарств. Ферменты классифицируют на семейства, подсемейства и продукты специфических генов. Степень экспрессии таких ферментов регулируется на разных уровнях. Некоторые ферменты экспрессируются конститутивно, т.е. они всегда присутствуют и всегда активны. Другие первично экспрессируются лишь вследствие индуцирующего влияния экзогенных химических веществ (лекарств, токсинов и/или пищевых факторов).
В результате мутации генов может возникать недостаточность или отсутствие определенной изоформы фермента, поэтому при введении обычно безвредной дозы может неожиданно проявиться токсичность лекарства. И наоборот, избыточность генетического кода способна обусловить присутствие множества копий фермента, метаболизирующего лекарство. Такая ситуация может привести к формированию резистентности к обычным дозам лекарства вследствие ускоренного метаболизма.
Активность ферментов, метаболизирующих лекарства, иногда повышается (индукция) или подавляется (ингибирование). Многие диетические факторы способны влиять на активность ферментов, метаболизирующих лекарства. К числу таких факторов относятся соотношение в пище белков и углеводов, растительные продукты, содержащие флавоноиды (например, крестоцветные растения — капуста, горчица, кресс-салат), и жареная пища с высоким содержанием полициклических ароматических углеводородов, источником которых является горящий древесный уголь.
Повышенный синтез ферментов как результат действия экзогенных химических веществ называют индукцией ферментов. Индукция может быть обусловлена сочетанием изменений транскрипции нуклеиновых кислот, а также трансляционной и посттрансляционной регуляцией. Индукцию способны вызывать некоторые лекарства, компоненты пищи, алкоголь и курение. При длительном приеме внутрь некоторые лекарства (например, барбитураты, рифампицин) индуцируют свой собственный метаболизм, а также метаболизм других лекарств и эндогенных веществ. Локализация ткани, где происходит индукция, может быть определена по природе индуцирующего химического агента.
Так, курение индуцирует экспрессию особой изоформы цитохрома Р-450 главным образом в легких и верхних отделах тонкой кишки.
Иногда два лекарства конкурируют за метаболизм, осуществляемый одним и тем же ферментом. В результате снижается скорость метаболизма одного или обоих лекарств. Этот процесс получил название «ингибирование ферментов». Клинически значимым примером такого ингибирующего взаимодействия могут служить сердечные аритмии или судорожная активность ЦНС, вызываемые теофиллином при его одновременном введении с антибиотиками-макролидами, например эритромицином.
Источник
Метаболизм препаратов и лекарств
Содержание
Лекарственный метаболизм [ править | править код ]
Большинство лекарств метаболизируется до их выведения из организма. Метаболические реакции разделяют на две большие группы — реакции фазы 1 и фазы 2:
- реакции фазы 1: окисление, восстановление и гидролиз, в результате которых к молекуле лекарственного вещества присоединяется химическая группа, снижающая активность образованного соединения и повышающая его полярность (и обычно его водорастворимость);
- реакции фазы 2: конъюгирование или синтетические реакции с присоединением крупной химической группы. Этот процесс обычно также повышает водорастворимость и облегчает экскрецию препарата из организма.
Природа, функции и количество ферментов, метаболизирующих лекарства, у разных индивидов неодинаковы, следствием чего является неодинаковая скорость метаболизма лекарства и его выведения
Ферменты, метаболизирующие лекарства, обладают широкой специфичностью по отношению к субстратам, однако специфичность ферментов носит относительный, а не абсолютный характер. Это означает, что один фермент может катализировать метаболизм многих различных лекарств и что в метаболизме одного и того же лекарства может участвовать несколько изоформ фермента. Обычной метаболической реакцией является окисление. При окислении к молекуле вещества присоединяется гидроксильная группа или удаляется алкильная, или метильная группа. Примером такой реакции может служить деметилирование теофиллина с образованием 1-метилксантина. Первичным ответственным ферментом служит CYP1A2, однако реакцию катализируют также изоформы CYP1A1 и CYP2D6 (см. далее и табл. 4.4).
Метаболизирующие лекарства ферменты представлены множеством форм, и индивидуальные различия их генетической экспрессии определяют индивидуальные различия метаболизма лекарств. Ферменты классифицируют на семейства, подсемейства и продукты специфических генов. Степень экспрессии таких ферментов регулируется на разных уровнях. Некоторые ферменты экспрессируются конститутивно, т.е. они всегда присутствуют и всегда активны. Другие первично экспрессируются лишь вследствие индуцирующего влияния экзогенных химических веществ (лекарств, токсинов и/или пищевых факторов).
В результате мутации генов может возникать недостаточность или отсутствие определенной изоформы фермента, поэтому при введении обычно безвредной дозы может неожиданно проявиться токсичность лекарства. И наоборот, избыточность генетического кода способна обусловить присутствие множества копий фермента, метаболизирующего лекарство. Такая ситуация может привести к формированию резистентности к обычным дозам лекарства вследствие ускоренного метаболизма.
Активность ферментов, метаболизирующих лекарства, иногда повышается (индукция) или подавляется (ингибирование)
Многие диетические факторы способны влиять на активность ферментов, метаболизирующих лекарства. К числу таких факторов относятся соотношение в пище белков и углеводов, растительные продукты, содержащие флавоноиды (например, крестоцветные растения — капуста, горчица, кресс-салат), и жареная пища с высоким содержанием полициклических ароматических углеводородов, источником которых является горящий древесный уголь.
Повышенный синтез ферментов как результат действия экзогенных химических веществ называют индукцией ферментов (табл. 4.3). Индукция может быть обусловлена сочетанием изменений транскрипции нуклеиновых кислот, а также трансляционной и посттрансляционной регуляцией. Индукцию способны вызывать некоторые лекарства, компоненты пищи, алкоголь и курение. При длительном приеме внутрь некоторые лекарства (например, барбитураты, рифампицин) индуцируют свой собственный метаболизм, а также метаболизм других лекарств и эндогенных веществ. Локализация ткани, где происходит индукция, может быть определена по природе индуцирующего химического агента. Так, курение индуцирует экспрессию особой изоформы цитохрома Р-450 главным образом в легких и верхних отделах тонкой кишки.
Иногда два лекарства конкурируют за метаболизм, осуществляемый одним и тем же ферментом. В результате снижается скорость метаболизма одного или обоих лекарств. Этот процесс получил название «ингибирование ферментов» (см. табл. 4.3). Клинически значимым примером такого ингибирующего взаимодействия могут служить сердечные аритмии или судорожная активность ЦНС, вызываемые теофиллином при его одновременном введении с антибиотиками-макролидами, например эритромицином.
Большинство тканей обладает способностью метаболизировать специфические лекарства
Печень — главное место метаболизма лекарств, но большинство тканей также способно метаболизировать специфические лекарства. Тканеспецифичность метаболизма зависит от генетической регуляции и экспрессии ферментов, метаболизирующих лекарство в соответствующей ткани. Таким образом, избирательные тканевые эффекты могут возникать в результате уникальной реакции фермента, метаболизирующего лекарство, в участке ткани, где оно действует. Например, почки окисляют метаболит сулиндак сульфид, активный ингибитор циклооксигеназы, снова в сулиндак, исходное (родительское) пролекарство, тем самым защищая почки от повреждения вследствие ингибиции циклооксигеназы, которое способен вызвать сулиндак сульфид.
Таблица 4.3 Примеры индукторов и ингибиторов ферментов
Выведение лекарства из плазмы (элиминация) может следовать кинетике нулевого порядка, кинетике первого порядка или носить промежуточный характер
В целом лекарства покидают организм посредством одного или комбинации двух кинетических процессов. Один из этих процессов, известный как кинетика нулевого порядка, отличается тем, что скорость выведения лекарства из организма (обычно из плазмы) является постоянной, независимо от количества содержащегося в плазме лекарства. Это происходит, если процессы элиминации являются насыщенными.
Кинетика нулевого порядка не типична для элиминации лекарств. Ее можно сравнить с удалением воды из ведра чашкой, вычерпывая воду раз за разом. Однако в большинстве случаев концентрация лекарства существенно ниже, чем это необходимо для насыщения процессов элиминации, поэтому скорость выведения вещества пропорциональна его концентрации в плазме (кинетика первого порядка).
Обычным параметром, описывающим этот процесс, служит период полувыведения (Т1/2) из плазмы. Кинетику первого порядка можно сравнить с опустошением ведра с водой через открытый кран на дне. В этом случае ток воды из крана будет пропорционален высоте столба воды в ведре. Лекарство с кинетикой выведения первого порядка, в сущности, удаляется из кровотока в течение пяти Т1/2. На протяжении двух Т1/2 выводится 75% лекарства (50% + половина оставшихся 50% = 75%), трех Т1/2 — 87,5%, четырех Т1/2 — 93,75% и т.д.
Однако концепция периода полувыведения неприемлема для веществ с кинетикой нулевого порядка (например, этанола), т.к. скорость их элиминации не зависит от концентрации в плазме, если только концентрация вещества не является очень низкой (обычно фармакологически неэффективной). Процессы элиминации этанола эффективно насыщены при низкой концентрации, поэтому элиминацию этанола лучше всего описывать на основе выведения постоянного количества этанола в единицу времени (элиминация нулевого порядка). Средняя скорость элиминации этанола составляет около 120 мг/кг/час для умеренно пьющего человека. Эта скорость элиминации эквивалентна 150 мг/л плазмы в час — скорости, равной выведению примерно 50% 350 мл бутылки пива (5% алкоголя по объему) за 1 час у мужчины массой 70 кг.
Характеристики элиминации некоторых веществ (например, аспирина, фенитоина) являются промежуточными, свойственными кинетике как нулевого, так и первого порядка. Как только насыщается процесс первого порядка, элиминация приближается к нулевому порядку. Соответственно этому концентрация в плазме повышается непропорционально увеличению дозы, т.к. элиминация не возрастает с повышением дозы, что свойственно процессам нулевого порядка. При использовании таких лекарств целесообразно проводить мониторинг концентрации лекарства в плазме, когда меняется режим дозировки, поскольку небольшие изменения дозы могут привести к непропорционально высокому увеличению концентрации и возможной токсичности.
Фаза 1 метаболизма [ править | править код ]
Наиболее распространенным метаболическим путем фазы 1 является окисление. Восстановление и гидролиз также играют важную роль, но они встречаются реже.
Окисление [ править | править код ]
Цитохромы Р-450 (табл. 4.4) представляют собой суперсемейство, включающее изоформы гемопротеиновых ферментов, катализирующих окислительный метаболизм многих ксенобиотиков (лекарств и других экзогенных химических веществ).
В процесс окисления вещества входят этапы окисления и восстановления (рис. 4.8). Участки окисления значительно варьируют, их общее физическое свойство — высокая растворимость в липидах.
В большинстве случаев окисление лекарств катализируют цитохромы Р-450, хотя в этом процессе, но в меньшей степени, участвуют и другие ферменты. Существует несколько сотен изоформ цитохромов Р-450. Некоторые из них являются конститутивными (т.е. присутствуют всегда), другие начинают синтезироваться лишь в ответ на соответствующие стимулы — обычно экзогенные химические вещества. Специфичность по отношению к субстрату — это функция изоформы цитохрома Р-450, и она обычно не абсолютная, а относительная, поэтому отсутствие какой-либо определенной изоформы цитохрома Р-450 не останавливает данную метаболическую реакцию. Гены суперсемейства цитохрома Р-450 картируются в нескольких хромосомах.
Таблица 4.4 Примеры семейств и изоформ цитохрома Р-450, играющих важную роль в окислительном метаболизме
Источник
Метаболизм лекарственных веществ в организме
ЛС, поступившие в организм, являются для него ксенобиотиками, т. е. чужеродными агентами, следовательно, они подлежат выведению. Комплекс физико-химических и (или) биохимических реакций, в результате которых ЛС превращается в более полярное (водорастворимое) соединение, т. е. продукт, который легче выводится из организма, называется биотрансформацией.
Как правило, химические соединения, образовавшиеся в результате биотрансформации ЛС, менее активны и менее токсичны, однако возможно образование как более токсичных, так и более фармакологически активных соединений (в результате биотрансформации кортизола образуется фармакологически более активный гормон — гидрокортизон, а в результате биотрансформации противокашлевого препарата кодеина образуется наркотический анальгетик морфин).
Биотрансформация лекарств почти исключительно (на 90–95%) протекает в печени. Остальные количества инактивируются в тканях ЖКТ, легких, коже и плазме крови. Некоторое количество ЛС выводится из организма в неизмененном виде.
Выделяют 2 основных вида превращения лекарственных препаратов :
Метаболическая трансформация (реакции I фазы, несинтетические реакции метаболизма).
Конъюгация (реакции II фазы, синтетические реакции метаболизма).
Метаболическая трансформация— это превращение лекарственных веществ за счет окисления, восстановления, гидролиза и др.
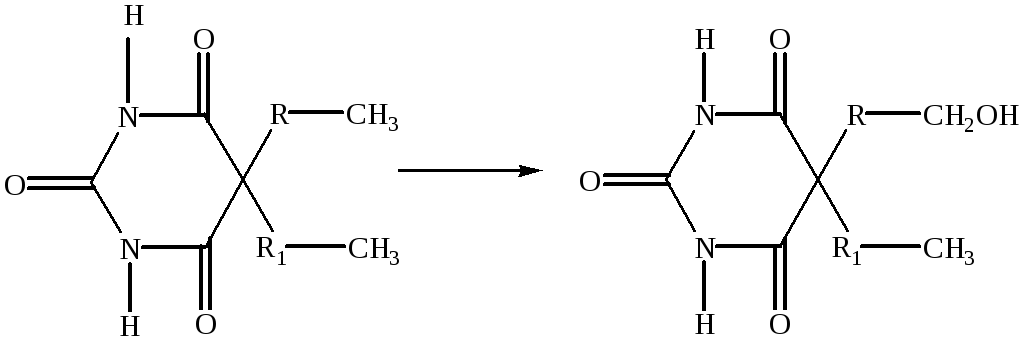
Окисление— один из наиболее характерных и частых путей инактивации препаратов. Осуществляется в гепатоцитах системой микросомальных ферментов оксидаз (основной представитель — цитохром Р-450).
барбитурат Окисление заместителей
Восстановление— сравнительно редкий путь превращения. Он характерен, в частности, для гормонов стероидной структуры и их аналогов.
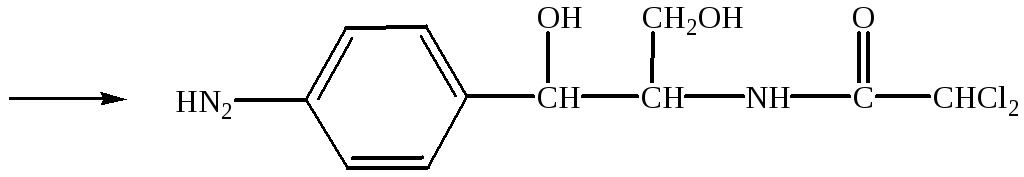
восстановление нитрогруппы в аминогруппу
Гидролиз — очень важный путь инактивации сложных эфиров и амидов, к которым относятся многие ЛС. В процессе гидролиза происходит расщепление сложной эфирной или амидной связи с присоединением воды.
парааминобензойная кислота диэтиламиноэтанол
Конъюгация— это биосинтетический процесс, сопровождающийся присоединением к лекарственному веществу или его метаболитам ряда химических группировок или молекул эндогенных соединений (метилирование, ацетилирование, взаимодействие с глюкуроновой кислотой, сульфатами, глутатионом).
На биотрансформацию ЛС оказывает непосредственное влияние достаточно большое количество факторов:
Возраст (у новорожденных система микросомальных ферментов печени очень несовершенна).
Пол (в опытах на крысах показано, что самцы быстрее метаболизируют лекарственные вещества, что связывают со стимулирующим действием мужских половых гормонов на синтез микросомальных ферментов).
Генетические факторы (генетически обусловленный уровень активности псевдохолинэстеразы).
Вредные привычки (никотин и алкоголь повышает активность микросомальных ферментов и, следовательно, скорость метаболизма одновременно применяемых веществ).
Функциональное состояние печени (при патологии печени нарушается метаболизм лекарственных веществ).
Источник