- Транспорт лекарственных средств через клеточную мембрану и биологические барьеры
- Содержание
- Транспорт лекарственных средств через клеточную мембрану и другие биологические барьеры [ править | править код ]
- Клеточная мембрана [ править | править код ]
- Проникновение лекарственных средств через биологические барьеры [ править | править код ]
- Простая диффузия [ править | править код ]
- Влияние pH на диффузию слабых электролитов [ править | править код ]
- Облегченная диффузия и активный транспорт [ править | править код ]
- Механизм транспорта лекарственных веществ через мембрану
- 6.Виды транспорта лекарственных средств через мембраны. Биологическая доступность
Транспорт лекарственных средств через клеточную мембрану и биологические барьеры
Содержание
Транспорт лекарственных средств через клеточную мембрану и другие биологические барьеры [ править | править код ]
На всех этапах своего пребывания в организме — всасывания, распределения, метаболизма, экскреции — лекарственные средства проникают через клеточные мембраны. Поэтому очень важно понимать механизм мембранного транспорта, знать физико-химические свойства препарата и самой мембраны, от которых этот транспорт зависит. Так, решающее значение имеют размеры и форма молекулы лекарственного средства, степень ионизации, растворимость в жирах и связывание с белками тканей.
Клеточная мембрана — наиболее универсальный биологический барьер, который приходится преодолевать лекарственным средствам. Он входит в состав других биологических барьеров, таких, как слизистая кишечника, состоящая из одного слоя клеток, или кожа, состоящая из нескольких таких слоев. В большинстве случаев лекарственные средства переносятся через клетки, а не между ними, поэтому механизм проникновения через столь разные по строению барьеры во многом сходен.
Клеточная мембрана [ править | править код ]
Клеточная мембрана представляет собой двойной слой амфифильных липидов, гидрофобные углеводородные хвосты которых обращены внутрь, а гидрофильные головки — наружу. Мембраны разных клеток различаются по липидному составу. Перемещаясь вдоль поверхности, липидные молекулы придают мембране текучесть и эластичность. Кроме того, мембраны обладают высоким электрическим сопротивлением и плохо проницаемы для полярных молекул. Встроенные в двойной липидный слой мембранные белки выполняют функции рецепторов, ионных каналов и переносчиков, участвуя в восприятии и передаче химических и электрических сигналов. Эти белки служат мишенями для лекарственных средств.
Проникновение лекарственных средств через биологические барьеры [ править | править код ]
При преодолении биологических барьеров лекарственные средства могут проходить как сквозь клетки, так и между ними. Между эндотелиальными клетками большинства капилляров препараты транспортируются с током воды, происходящим путем фильтрации по градиенту гидростатического давления. Такой вид транспорта доступен только свободным лекарственным средствам, так как молекулы белков, с которыми они связаны, слишком велики. Транспорт веществ через межклеточные контакты осуществляется довольно легко. В капиллярах он зависит только от интенсивности кровотока (см. ниже). Этот вид транспорта играет важную роль в проникновении веществ через почечный фильтрационный барьер. В некоторых органах и тканях (капилляры ЦНС, многие эпителиальные ткани) клетки связаны плотными контактами, транспорт через которые ограничен (см. ниже). При прохождении сквозь клетки лекарственные средства должны переноситься через клеточную мембрану. Последняя хорошо проницаема для воды, которая проникает через мембрану путем диффузии по градиенту осмотического давления. Вместе с водой через мембрану могут проходить небольшие (молекулярная масса не более 100—200), растворимые в воде молекулы лекарственных средств. Большинство липофильных препаратов с высоким молекулярным весом транспортируются путем активного или пассивного транспорта.
Простая диффузия [ править | править код ]
Многие липофильные лекарственные средства проходят через клеточную мембрану посредством простой диффузии (разновидность пассивного транспорта) по градиенту концентрации. Скорость простой диффузии прямо пропорциональна величине трансмембранного концентрационного градиента, коэффициенту распределения препарата между липидной и водной фазами и площади диффузионной поверхности. Чем больше коэффициент распределения, тем выше концентрация препарата в мембране и тем выше скорость диффузии. В случае неионизированных веществ по достижении стационарного состояния концентрации свободного вещества по обе стороны мембраны выравниваются. Трансмембранное распределение ионизированных веществ зависит от электрохимических градиентов для ионов и от градиента pH между внутри- и внеклеточным пространством, так как величина pH влияет на степень ионизации.
Влияние pH на диффузию слабых электролитов [ править | править код ]
Большинство лекарственных средств представляют собой слабые кислоты или слабые основания, которые могут находиться в водном растворе как в ионизированной, так и в неионизированной форме. Неионизированные молекулы обычно липофильны и легко проходят через мембрану (неионная диффузия), в отличие от плохо растворимых в жирах ионизированных молекул.
Трансмембранное распределение слабых электролитов зависит от показателя кислотной диссоциации pКа (рКа соответствует pH, при котором половина всех молекул слабой кислоты или слабого основания ионизирована) и градиента pH. На рис. 1.2 представлено распределение слабой кислоты (рКа 4,4) между плазмой (pH 7,4) и желудочным соком (pH 1,4). Слизистая желудка выполняет функцию липидного барьера, проницаемого только для неионизированных, липофильных молекул. Соотношение неионизированной и ионизированной форм препарата легко вычислить с помощью уравнения Гендерсона—Гассельбальха. В плазме это соотношение равно 1:1000, а в желудочном соке — 1:0,001 (на рисунке эти данные приведены в квадратных скобках, а смещение равновесия в сторону ионизированной или неионизированной Формы указано толстыми горизонтальными стпелками). Таким образом, в стационарном состоянии соотношение концентраций препарата в плазме и желудочном соке составит 1000:1. Для слабого основания с рКа 4,4 указанные соотношения обратные, и равновесие между ионизированной и неионизированной формами также смещено в обратную сторону. Итак, в стационарном состоянии слабая кислота накапливается преимущественно с той стороны мембраны, где среда более щелочная, а слабое основание — с той стороны, где среда более кислая (так называемая ионная ловушка). Эти закономерности во многом определяют всасывание и экскрецию лекарственных средств (см. ниже). Разность концентраций слабого электролита по обе стороны биологических барьеров устанавливается без затрат энергии, за счет избирательной проницаемости мембраны для неионизированных молекул и трансмембранного градиента pH. Последний, впрочем, создается активным транспортом ионов.
Облегченная диффузия и активный транспорт [ править | править код ]
Хотя наиболее распространенный механизм мембранного транспорта лекарственных средств — простая диффузия, препараты могут проходить через клеточную мембрану с участием белков-переносчиков — путем облегченной диффузии или активного транспорта. Облегченная диффузия (разновидность пассивного транспорта) идет по концентрационному или электрохимическому градиенту без затрат энергии, но, в отличие от простой диффузии, осуществляется с помощью белка-переносчика. Активный транспорт идет против концентрационного либо электрохимического градиента и требует затрат энергии. Облегченная диффузия и активный транспорт характеризуются насыщением, специфичностью и конкурентным ингибированием. Белки-переносчики участвуют в переносе через мембрану эндогенных веществ, скорость простой диффузии которых слишком мала, и могут обладать высокой специфичностью к определенной конформации молекулы лекарственного вещества. Кроме того, с помощью белков-переносчиков из клетки выводятся токсичные вещества.
От локализации переносчика в той или иной части клетки часто зависит направление переноса (в клетку или из нее), что во многих случаях обеспечивает направленный транспорт лекарственных средств через клеточные слои. Так, переносчики в базолатеральной мембране гепатоцитов транспортируют желчные кислоты и амфифильные органические ионы в клетку, а системы активного транспорта в апикальной мембране — из клетки в желчь. Сходные механизмы действуют в кишечнике и почечных канальцах. Во всех этих органах, а также в эндотелии капилляров головного мозга присутствует Р-гликопротеид — мембранный белок-переносчик, отвечающий за выведение лекарственных средств из клетки. Этот белок кодируется геном ABCВ1 (старое название MDR- 1) и обусловливает устойчивость опухолевых клеток к химиотерапии (гл. 52). В кишечнике Р-гликопротеид транспортирует лекарственные средства из энтеропита обратно в просвет кишечника, уменьшая их всасывание.
Источник
Механизм транспорта лекарственных веществ через мембрану
Способность проникать сквозь двойные липидные слои является условием для всасывания лекарственных средств, проникновения в клетки или в клеточные органеллы и прохождения через ГЭБ и плацентарный барьер. Благодаря амфифильной природе фосфолипиды образуют двойные слои, характеризующиеся гидрофильной поверхностью и гидрофобной внутренней частью. Вещества могут проникать через такую мембрану тремя разными способами.
а) Диффузия. В зависимости от степени липофильности вещества могут диффундировать непосредственно через двойной липидный слой по градиенту концентрации через мембрану (красные точки). В то же время мембрана практически непроницаема для высокогидрофильных веществ (норадреналина).
б) Пассивный транспорт. Во многих тканях есть транспортные системы для переноса через мембрану веществ, которые самостоятельно не могут через нее пройти. Проникая сквозь мембраны, вещества попадают внутрь клеток и в клеточные отделы, где имеется потребность в них. Эти транспортные системы расположены в мембранах и являются более или менее специфичными для определенной группы веществ.
Пассивный транспорт через мембрану не требует энергии. Каналы или белки-переносчики обеспечивают возможность гидрофильным веществам проникать через мембраны. Примерами являются потенциал- или лиганд-контролируемые ионные каналы (потенциалзависимые Na + -каналы, Са 2+ -каналы) и аквапорины.
Аквапорины — специальные транспортные белки, которые обеспечивают прохождение воды через гидрофобную клеточную мембрану во многих тканях организма.
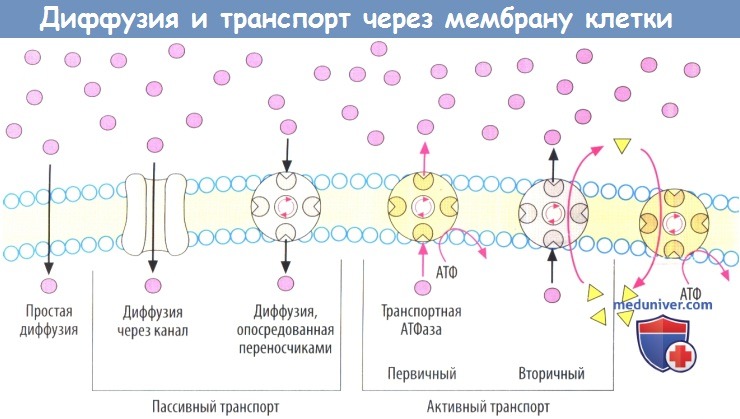
в) Активный транспорт. Многие транспортные процессы в организме осуществляются с прямым или непрямым использованием энергии аденозинтрифосфата (АТФ). Энергия АТФ особенно необходима, когда транспорт веществ через клеточную мембрану осуществляется против градиента концентрации, т. е. с затратой энергии.
В первичном активном транспорте участвуют белки, которые самостоятельно расщепляют АТФ (АТФазы) и таким образом обеспечивают транспорт веществ. Примерами являются Na + /K + -АТФаза или H + /K + -АТФаза.
Некоторые белки первичного активного транспорта выступают в роли мишеней для лекарственных средств; так, гликозиды наперстянки ингибируют Na + /K + -АТФазы] Ингибиторы протонной помпы снижают продукцию кислоты в желудке за счет ингибирования действия H + /K + -АТФазы.
г) При вторичном активном транспорте необходимо функциональное взаимодействие котранспортера с первичным АТФ-зависимым транспортером, В таком случае источником энергии, необходимой для транспорта вещества, служит движение ионов по градиенту концентрации. Градиент Na + обычно служит донором энергии. За поддержание градиента данного иона отвечает, в свою очередь, Na + /К + -АТФаза.
Многие нейромедиаторы и анионные или катионные переносчики используют клеточные градиенты Na + в качестве источника энергии.
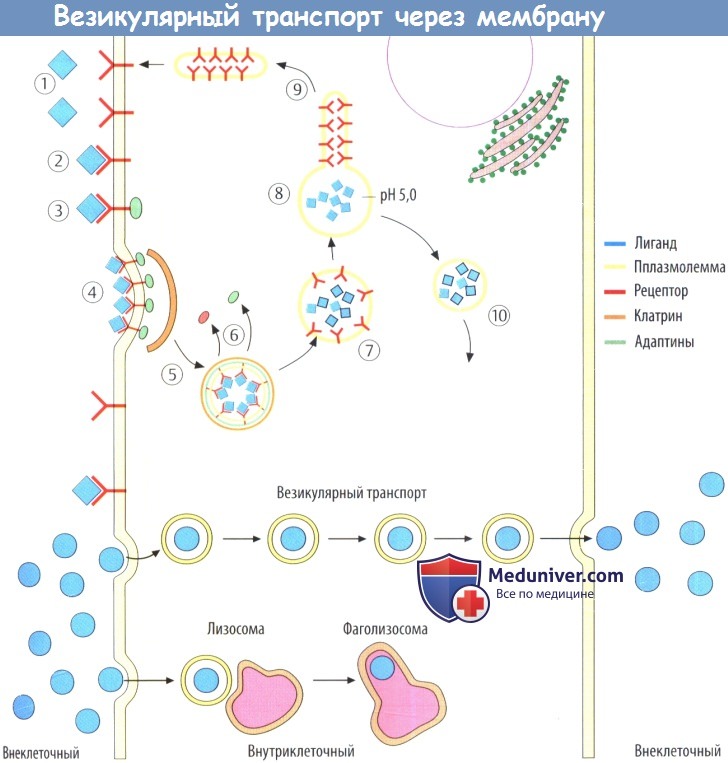
д) Трансцитоз (везикулярный транспорт). Вновь образованные везикулы захватывают растворенные во внеклеточной жидкости вещества и затем переносят их через цитоплазму. В некоторых случаях везикулы (фагосомы) сливаются с лизосомами дообразования фаголизосом, а переносимые вещества метаболизируются.
е) Эндоцитоз, опосредованный рецепторами. Лекарственное средство связывается в первую очередь с рецепторами на поверхности мембраны, а цитозольные участки рецепторов взаимодействуют со специальными белками (адаптины). Комплексы лекарственного вещества с рецептором мигрируют вдоль мембраны и соединяются с другими комплексами на основе клатринзависимого процесс. Область поврежденной мембраны инвагинирует и в конце концов отслаивается до образования обособленной везикулы.
Везикула охватывает клатрин и адаптин, что приводит к образованию ранней эндосомы. Внутри нее повышается концентрация протонов, вызывая диссоциацию комплекса «лекарственное средство-рецептор». Далее участки несущей рецептор мембраны отделяются от эндосомы. Они возвращаются обратно в плазмолемму в то время как эндосома направляется в органеллы мишени.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
6.Виды транспорта лекарственных средств через мембраны. Биологическая доступность
Пассивная диффузия происходит по градиенту концентрации лекарств — из зоны с большей концентрацией в зону с меньшей концентрацией, не требует затрат энергии макроэргов. Простая диффузия
Простая диффузия осуществляется путем растворения лекарств в липидном бислое мембран. Липидорастворимостью независимо от условий среды обладают лишь немногие вещества — ингаляционные наркозные средства, этиловый алкоголь. Большинство же препаратов являются слабыми кислотами или слабыми основаниями и образуют как липидорастворимые нейтральные молекулы, так и водорастворимые ионы. Соотношение нейтральных молекул и ионов зависит от физико-химических свойств лекарств и водородного показателя (рН) среды, из которой происходит всасывание.
У слабой кислоты с рКа*=4,4 содержание нейтральных молекул в желудочном соке (рН =1,4) в 1000 раз больше, чем в крови (рН=7,4), напротив, количество ионов в 1000 раз больше в крови, чем в желудочном соке. У слабого основания с таким же рКа соотношение нейтральных молекул и ионов составляет в крови 1000:1, в желудочном соке — 1:1000.
Условия всасывания лекарств-слабых кислот и оснований различ ные. Противовоспалительное средство ацетилсалициловая кислота имеет рК а=3,6. В кислой среде желудочного сока она присутствует в виде липидорастворимых нейтральных молекул, в щелочной среде кишечника (рН=6,8-7,2) — в виде водорастворимых ионов. В крови при рН=7,4 ацетилсалициловая кислота находится в ионизированной форме, поэтому плохо проникает в ткани. В очаге воспаления в условиях ацидоза преобладают нейтральные молекулы.
Другими представителями лекарств-слабых кислот являются проти-восудорожные средства фенобарбитал, дифенин; нестероидные противовоспалительные вещества бутадион, индометацин, ортофен; мочегонный препарат фуросемид; непрямые антикоагулянты; гипогликеми-ческий препарат бутамид; противомикробные средства — сульфаниламиды, тетрациклин.
Слабые основания — алкалоиды (морфин, кодеин, папаверин, кофеин, атропин и многие другие) и синтетические азотсодержащие вещества (анальгин, димедрол) образуют нейтральные молекулы в кишечнике, крови и клетках.
Знание особенностей всасывания лекарств с различными физико-химическими свойствами имеет большое медицинское значение.
При отравлении производными барбитуровой кислоты для ускорения их элиминации из организма проводят форсированный диурез — вливают в вену мочегонные средства и изотонические растворы глюкозы и натрия хлорида с добавлением натрия гидрокарбоната. Последний создает в первичной моче щелочную среду, в которой ускоряется диссоциация барбитуратов на ионы, не подвергающиеся реабсорбции в почечных канальцах.
При отравлении морфином и некоторыми другими алкалоидами, введенными парентерально, необходимо проводить промывание желудка растворами слабых кислот — уксусной или лимонной, так как около 10% молекул алкалоидов простой диффузией по градиенту концентрации проникает из крови в просвет желудка, где в условиях кислой среды диссоциирует на ионы. Ионы могут поступать в кишечник и вновь образовывать нейтральные молекулы, всасывающиеся в кровь. Промывание желудка направлено на повышение диссоциации и удаление нейтральных молекул алкалоидов.
Нейтральные молекулы лекарств отличаются по растворимости в липидах в зависимости от присутствия в их структуре полярных групп. Полярные вещества плохо растворяются в липидах и менее способны к всасыванию простой диффузией. Фильтрация через поры
Фильтрация лекарств через поры клеточной мембраны происходит с током воды в зависимости от гидростатического и осмотического давлений и возможна только для нейтральных молекул, имеющих молекулярную массу не более 100-200 Да. Это обусловлено размером пор, равным 0,35-0,4 нм, и присутствием в них фиксированных зарядов. Фильтрации подвергаются мочевина, тиомочевина, глюкоза.
Активный транспорт лекарств происходит против градиента концентрации (в сторону большей концентрации) с затратой энергии макроэргов и при участии белков-переносчиков.
Активным транспортом переносятся лекарства-эндобиотики — аналоги метаболитов организма, использующие естественные системы переноса. Известно, что йод поступает в фолликулы щитовидной железы против пятидесятикратного градиента концентрации. Норадреналин подвергается нейрональному захвату нервными окончаниями против двухсоткратного градиента. Активным транспортом при участии естественных систем переноса кислот и оснований происходит секреция веществ в почечных канальцах.
Возможна конкуренция лекарств за связь с белками-переносчиками в процессе активного транспорта. Например, пробенецид используют для пролонгирования действия бензилпенициллина. Этот антибиотик подвергается секреции в почечных канальцах при участии белка-переносчика, высоким сродством к которому обладает пробенецид.
Многие лекарства нарушают функцию ферментов активного транспорта (сердечные гликозиды блокируют мембранную Na+, К+-АТФ-азу).
Пиноцитоз характерен для высокомолекулярных лекарств — полипептидов и осуществляется путем инвагинации клеточной мембраны с образованием вакуоли, содержащей лекарство. Эта вакуоль мигрирует к противоположной стороне мембраны. Пиноцитозом происходит всасывание в тонком кишечнике витамина В12 в комплексе с гликопротеи-ном — внутренним фактором Касла.
Важнейшей характеристикой всасывания является биодоступность -часть дозы лекарств, поступающая в кровь и биофазу циторецепторов. Биодоступность зависит от физико-химических особенностей лекарств, лекарственной формы и технологии ее приготовления, пути введения, интенсивности кровотока, площади всасывающей поверхности (наибольшая — в альвеолах легких и слизистой оболочке кишечника). При внутривенной инъекции транспорт веществ в ткани происходит по широким межклеточным щелям между эндотелием, поэтому биодоступность достигает 100%. При других путях введения она меньше. В случае приема лекарств внутрь большое значение для биодоступности имеют лекарственные формы (лекарства лучше всасываются из растворов, мелкодисперсных взвесей, микрогранул, хуже — из таблеток, драже, капсул), а также присутствие пищи, состояние пищеварительного тракта и сердечно-сосудистой системы, интенсивность метаболизма в печени.
Биодоступность лекарств зависит от возраста больного. В педиатрической практике необходимо считаться с особенностями всасывания лекарств у детей: •Желудочный сок имеет нейтральную реакцию (сразу после рождения рН = 6-8) и
приобретает такую же, как у взрослых, кислотность только ко 2-му году жизни
*8-19% новорожденных страдают гипохлоргидрией; «Эвакуаторная деятельность желудка нерегулярна в течение первых 6 месяцев
жизни (материнское молоко усиливает моторную деятельность желудка); • Кишечник характеризуется низкой микробной обсемененностью с высокой
активностью р-глюкуронидазы микробов;
*Уменьшены синтез и выделение желчных кислот, что нарушает всасывание жирорастворимых веществ, например, витаминов.
Изменение биодоступности лекарств у пожилых людей обусловлено физиологическим старением органов и тканей и наличием заболеваний. В пожилом возрасте увеличивается кислотность желудочного сока, нарушаются эвакуаторная функ-
ция желудка и всасывание лекарств в кишечнике (например, сердечного гликозида дигоксина).
7.БИОБАРЬЕРЫ ИХ ПРОНИЦАЕМОСТЬ ДЛЯ ЛЕКАРСТВ
Из крови лекарства поступают в органы, преодолевая гистогемати-ческие барьеры — капиллярную стенку, гематоэнцефалический, гемато-офтальмический и плацентарный барьеры.
Капилляры легко проницаемы для лекарств. Липидорастворимые вещества диффундируют через эндотелий и базальную мембрану, водорастворимые — через цементирующее вещество (гиалуроновая кислота) или широкие поры, занимающие 0,2% поверхности капиллярной стенки. Транспорт по капиллярным порам возможен для соединений с молекулярной массой, не больше массы инсулина (5-6 кДа). При лучевой болезни и воспалении происходит активация гиалуронидазы с ростом проницаемости капилляров.
Гематоэнцефалический и гематоофтальмический барьеры
Гематоэнцефалический барьер (ГЭБ) представлен капиллярной стенкой с плотными контактами между эндотелием, а также основным межуточным веществом и астроглией головного и спинного мозга. Глиальные клетки выстилают примерно 85% поверхности капилляров. Через ГЭБ простой диффузией проникают только липидорастворимые вещества (наркозное средство тиопентал-натрий, противопаразитарный препарат мет-ронидазол), меньшую роль играет активный транспорт. Для полярных соединений (пенициллины, миорелаксанты) ГЭБ не проницаем. Осмотически активные средства (маннит) могут вызыватьповреждение ГЭБ (особенно у детей) с последующим усилением отека мозга и поступлением в него эндогенных токсических веществ (билирубин).
ГЭБ гипоталамуса, гипофиза, эпифиза отличается повышенной проницаемостью для лекарств.
При менингите, арахноидите, гипоксии, черепномозговых травмах, шоке проницаемость ГЭБ возрастает. У больных тяжелым менингококко-вым менингитом проникновение антибиотика рифампицина в головной
мозг составляет 26% от дозы, при менингите средней тяжести — 14,3%, при легком менингите — 5,2%. При менингите концентрация антибиотика канамицина в головном мозге в 2-8 раз выше, чем в плазме крови.
Удаление лекарств из мозга происходит при участии сосудистого сплетения желудочков по типу секреции веществ в почечных канальцах или с током спинномозговой жидкости через ворсинки паутинной оболочки.
Гематоофтальмический барьер разделяет кровь капилляров и внутриглазную жидкость в камерах глаза. В среды глаза хорошо проникают липидорастворимые лекарства.
Плацентарный барьер разделяет кровообращение матери и плода. Проникновение через этот барьер зависит от физико-химических характеристик лекарств, их концентрации в крови, морфо-функционального состояния плаценты в разные сроки беременности, плацентарного кровотока. К плоду поступают несвязанные с белками и липидорастворимые лекарства с молекулярной массой менее 1 кДа, не проникают четвертичные азотистые соединения и высокомолекулярные вещества (плазмозаменители, гепарин, белки). Основными типами транспорта через плаценту являются простая диффузия, активный перенос и пиноцитоз.
Проницаемость плацентарного барьера значительно повышается с 32-35-й недели беременности в результате истончения плаценты (с 25 до 2 мкм), увеличения количества ворсин, расширения спиральных артерий с ростом перфузионного давления в межворсинчатом пространстве.
Особенности кровообращения у плода увеличивают опасность повреждения его лекарственными средствами. После прохождения через плаценту лекарства попадают в пупочную вену, затем 60-80% крови направляется в печень через воротную вену, а остальные 20-40% пуповинного кровотока через шунт поступает в нижнюю полую вену и системный кровоток без детоксикации в печени.
Некоторые лекарства — сердечный гликозид дигитоксин, противотуберкулезный препарат фтивазид — концентрируются в тканях плода, создавая концентрации в 1,5-2 раза большие, чем в крови матери. Другие лекарства — антибиотики, кофеин, витамин Е — обнаруживаются в крови плода в меньших (на 50-70%) количествах, чем у матери.
В связи с опасностью эмбриолетального, эмбриотоксического, тератогенного и фетотоксического действия многие лекарства противопоказаны при беременности. Известно, что частота врожденных уродств в популяции равна 2-3%, при этом в 25% случаев они объясняются наследственными причинами, в 10% — отрицательным влиянием факторов внешней среды, в 65% — нежелательными эффектами лекарств.
Источник


