- Моноклональные антитела для лечения мигрени
- Достижения фармацевтики: моноклональные антитела
- Чудо генной инженерии — человеческие моноклональные антитела
- История открытия
- Первый шаг — иммунизация антителами животных (XIX в. – начало XX в.)
- Второй шаг — расшифровка структуры моноклональных антител (30–70-е гг. XX в.)
- Третий шаг — разработка первой технологии синтеза антител (70–80-е гг. XX в.)
- Четвертый шаг — применение искусственно синтезированных антител для лечения заболеваний (80-е гг. XX в.)
- Пятый шаг — создание химерных антител (90-е гг. XX в.)
- Шестой шаг — создание гуманизированных и человеческих моноклональных антител (конец 90-х гг. XX в. — 2000-е гг. XXI в.)
- Разработка новых моноклональных антител сегодня
- Номенклатура моноклональных антител
Моноклональные антитела для лечения мигрени
Что такое моноклональные антитела и как они помогают лечить мигрень.
О каких препаратах идет речь?
Эренумаб (Иринэкс в России, Aimovig на Западе), Фреманезумаб (Аджови, Ajovy), Галканезумаб (Эмгалити, Emgality) и Эптинезумаб (Vyepti). В России в 2020 году выходят первые два из списка, остальные должны появиться через 1-2 года.
Что такое моноклональные антитела? Это что-то связанное с иммунитетом?
И да и нет. Мы все знаем, что антитела – это особые молекулы нашей иммунной системы, которые борются с вирусами и бактериями. Их ключевая особенность – высокая специфичность (избирательность) в отношении какой-то одной мишени, против которой они были созданы организмом.
Именно поэтому мы можем болеть гриппом каждый год, даже если уже болели им раньше: вирус гриппа всегда чуть-чуть меняется от года к году, а наши старые антитела уже его не узнают. А прививка от кори или краснухи действует очень долго, так как эти вирусы не подвержены изменениям и наши антитела хорошо их узнают.
Именно избирательность антител, то есть, то, что они как ключ к замку подходят только к одной цели, позволила использовать их в медицине. Если мы знаем какую-ту особенную мишень в заболевании (например особенность раковой клетки), то можем создать антитела в лаборатории именно против этой раковой клетки и не будет необходимости «выжигать» химиотерапией все клетки подряд. Именно поэтому терапия моноклональными антителами впервые появилась в онкологии в конце 20-го века.
Затем, по мере того, как ученые стали узнавать биологические основы других болезней, этот подход к лечению стал проникать и в другие области медицины. Сейчас моноклональные антитела успешно используют в лечении псориаза, рассеянного склероза, ревматических заболеваний, астмы, а теперь – и мигрени.
И на какие мишени мы можем действовать моноклональными антителами при мигрени?
При мигрени мы можем заблокировать специальный белок CGRP или его рецептор.
Что такое CGRP?
Аббревиатура расшифровывается как Calcitonin gene-related peptide (Кальцитонин-ген родственный пептид). Это один из медиаторов боли, который выделяется в системе тройничного нерва и отвечает за головную боль при приступе мигрени. Можно сказать, что CGRP ручки громкости: чем его больше выделилось, тем сильнее и мучительнее боль.
Как связаны тройничный нерв и мигрень? Мигрень – это же изменение тонуса сосудов?
Как раз сосуды при мигрени почти или совсем ни при чем. «Сосудистая» теория мигрени была актуальна в середине прошлого века. В последние 20-30 лет стало ясно, что причина мигрени в нарушении работы головного мозга, точнее, отдельных его частей (система тройничного нерва, гипоталамус, кора головного мозга). Ученые обнаружили вещества, концентрация которых повышается при приступе мигрени (CGRP, PACAP, VIP) и придумали новые революционные препараты.
Как действуют эти препараты?
Они блокируют путь возникновения боли, в котором участвует белок CGRP. Есть две схемы: по одной работают препараты фреманезумаб, галканезумаб, эптинезумаб. Они блокируют сам белок. Эренумаб работает по-другому: влияет на рецептор, особую зону на поверхности клетки, чувствительную к этому белку. Но в целом принцип работы у препаратов общий – прервать “путь боли” с участием белка CGRP. Мы можем повлиять на этот путь или заблокировав сам белок CGRP с помощью фреманезумаба, галканезумаба и эптинезумаба, или заблокировав действие CGRP на его рецептор (особую зону на поверхности клетки) с помощью Эренумаба.
Как вводят моноклональные антитела от мигрени?
С помощью простой подкожной инъекции: (Ajovy, Иринэкс, Aimovig и Emgality) или внутривенно (Vyepti).
Какой эффект я почувствую?
Основная задача этой терапии – профилактика приступов мигрени. Мы не можем (никто в мире не может) излечить мигрень полностью, так как это врожденная особенность вашего мозга, но мы можем взять ее под контроль и сделать приступы слабее и реже. Лечение, цель которого – сократить частоту приступов, и называется профилактической терапией мигрени.
У меня полностью пройдет мигрень?
Это возможно с вероятностью примерно 20%. Именно у такого количества людей, которые участвовали в исследовании, приступы мигрени полностью заканчивались к концу года применения терапии. На 75% меньше приступов стало примерно у 45% участников исследований, а на 50% – у ⅔ пациентов. Это очень хорошие результаты по сравнению с тем лечением мигрени, которое было доступно ранее (противоэпилептические препараты, бета-блокаторы, кандесартан, антидепрессанты и ботулинический токсин).
Как часто надо применять эти лекарства?
Препараты вводят подкожно каждый месяц (Иринэкс, Аджови/Ajovy, Эмгалити/Emgality) или раз в три месяца (Аджови/Ajovy и Vyepti).
И их нужно будет колоть всю жизнь?
Конечно нет. Задача профилактической терапии мигрени: взять мигрень под контроль и сделать ее редкой, хорошо отвечающей на лечение обезболивающими. Обычно профилактику назначают на 6 или 12 месяцев – этого периода обычно достаточно, чтобы «перезагрузить» головной мозг, после чего приступов станет меньше или они совсем пропадут.
А как понять, что я в числе людей, которым это лечение помогает?
По рекомендациям европейских и американских ассоциаций по лечению головной боли мы можем оценить, работает ли лечение, через 3 месяца (если препарат вводят раз в месяц) или через 6 месяцев (если препарат вводят раз в три месяца).
А что с побочками? Наверняка что-то ужасное?
Совсем нет. Из самых частых побочных эффектов (их испытывали около 20% участников исследований) – это реакции в месте введения (покраснение, боль, жжение, отек). Это быстро проходит. В остальном серьезных нежелательных явлений исследования не показали.
Как давно появились?
Первые препараты (Аймовиг и Аджови) появились в продаже в США в 2018 году. В нашей Университетской клинике головной боли проходили исследования всех четырех препаратов еще с 2016 года.
Какие препараты есть у нас?
В России зарегистрированы два из четырех препаратов – Иринэкс (в других странах он называется Аймовиг) и Аджови.
Как получить лечение с помощью моноклональных антител к CGRP или рецептору к CGRP?
Вы можете приобрести препарат в аптеке или в специализированной клинике (такой, как наша). Препарат рекомендуют вводить под наблюдением врача.
Сколько стоит эта терапия?
Стоимость лечения с помощью препарата Иринэкс в нашей клиники составляет 17000 рублей. Стоимость лечения с помощью препарата Аджови – 20000 рублей. Перед введением необходима консультация с врачом.
Сколько стоит лечение препаратом Иринэкс?
Стоимость инъекции Иринэкса – 17.000 рублей + стоимость консультации врача.
Консультация нужна только перед первым введением. При курсовом лечении в дальнейшем вы платите только за инъекцию.
Сколько стоит лечение препаратом Аджови?
Стоимость инъекции Аджови – 20.000 рублей + стоимость консультации врача.
Консультация нужна только перед первым введением. При курсовом лечении в дальнейшем вы платите только за инъекцию.
Как записаться на прием и ввести Иринэкс или Аджови?
Если вы не наблюдаетесь в нашей клинике, записывайтесь на первичный прием к любому специалисту на удобное для вас время. Если врач подтвердит диагноз и то, что вам подходят эти препараты, ввести Иринэкс или Аджови можно будет сразу же.
Если вы уже наблюдаетесь у нас в клинике с диагнозом «мигрень» – записывайтесь на короткий повторный приём (30 минут) к докторам Нине Владимировне Ващенко или Дарье Захаровне Коробковой. При записи скажите, что вас интересует инъекция Иринэкса или Аджови. В случае, если предыдущий ваш визит был не более 2 месяцев назад, оплатить нужно будет только препарат, без консультации.
Источник
Достижения фармацевтики: моноклональные антитела
Роза Ягудина о значении моноклональных антител в современной медицине и перспективах их применения
Чудо генной инженерии — человеческие моноклональные антитела
Моноклональные антитела (МАТ) сегодня применяются при лечении заболеваний, большинство из которых еще несколько десятков лет назад считались неизлечимыми. Это онкологические, аутоиммунные, сердечно-сосудистые и инфекционные заболевания, воспалительные реакции различного генеза, системный склероз, идиопатический фиброз легких, гепатит В, СПИД, ревматоидный артрит, системная красная волчанка, аллергические реакции, мышечная дистрофия, болезнь Альцгеймера, астма, диабет и другие заболевания.
Препараты, изготовленные на основе моноклональных антител, относятся к новейшим в современной медицине. С середины 90-х годов до сегодняшнего дня на мировом фармацевтическом рынке одобрено более 30 лекарственных средств, имеющих в составе моноклональные антитела. Первоначально надежность методов и технологий производства моноклональных антител и безопасность их применения вызывали опасения у фармацевтических производителей. Однако сегодня научный и медицинский опыт показал возможность их эффективного и безопасного применения в медицине. Сейчас большинство фармацевтических компаний работают над разработкой новых препаратов и лекарственных средств на основе моноклональных антител. На этапе разработки в мире находится около 300 МАТ.
В чем же уникальность и специфика применения моноклональных антител?
Роза Исмаиловна Ягудина , доктор фармацевтических наук, профессор, зав. кафедрой организации лекарственного обеспечения и фармакоэкономики, зав. лабораторией фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова, г. Москва, главный редактор журналов «Фармакоэкономика» и «Современная организация лекарственного обеспечения».
Иллюстрации и примеры в статье взяты из: Ягудина Р.И., Тихомирова А.В. История развития моноклональных антител, их настоящее и будущее // Современная организация лекарственного обеспечения. – 2013. – №1. – 6–27
История открытия
История получения и применения моноклональных антител уходит своими корнями в исследования конца 19 века. С тех пор, за прошедшие более чем сто лет, моноклональные антитела успели несколько раз совершить революцию в медицине, полностью перевернув представления о возможностях лекарственной терапии.
Первый шаг — иммунизация антителами животных (XIX в. – начало XX в.)
Ученых с давних пор интересовал вопрос о том, каким образом организм создает множество различных антител, обладающих уникальной специфичностью в отношении чужеродных веществ (антигенов), и каким образом эти антитела работают. Один из первых шагов к ответу на этот вопрос был сделан группой ученых, работавших в Институте инфекционных болезней в Берлине и открывших методы лечения дифтерии. В конце XIX века дифтерия у детей считалась смертельным неизлечимым заболеванием. Врач иммунолог-бактериолог Эмиль Беринг (Emil Behring) предположил, что лечение дифтерии может быть успешным в случае проявления естественной защитной реакции человеческого организма, а именно, если секретируемый дифтерийными бактериями токсин нейтрализовать. В 1890 г. Беринг совместно с японским ученым Сибасабуро Китасато установили, что неиммунизированные животные могут быть защищены от токсина дифтерийных бактерий с помощью инъекции антитоксина (антитоксической сыворотки) иммунизированных животных. В 1894 г. в период эпидемии дифтерии, унесшей жизни 50 000 детей в Германии, были произведены первые 25 000 доз антитоксина для применения в лечении людей. В 1901 г. Эмилю Берингу была присуждена Нобелевская премия за работу по сывороточной терапии. Однако на тот момент эффективность сыворотки была достаточно низкой, поскольку антитела в сыворотке вырабатывались клетками животных, а не самого пациента и вызывали лишь пассивный иммунитет. Антитоксин необходимо было вводить сразу после инфицирования, иначе было слишком поздно.
Еще одним примером использования антисыворотки в терапии людей стали исследования Чарльза Ричета (Charles Richet) и Жюля Эрикура (Jules Héricourt), применявших для лечения онкологических заболеваний антисыворотку, полученную путем иммунизации животных тканями саркомы. С середины 30-х годов практика пассивной иммунизации сошла на нет в связи с открытием антибиотиков широкого спектра действия.
Второй шаг — расшифровка структуры моноклональных антител (30–70-е гг. XX в.)
В 30-х гг. появились ультрацентрифуги, позволявшие разделять антитела по размеру и форме. В 40-х гг. ученые научились сортировать антитела по электрическому заряду и размеру. Однако дальнейшая расшифровка структуры антитела была пока недоступна из-за их большого размера, в 20 раз превышавшего размер молекул белков, структуры которых к тому времени уже были расшифрованы. Только в 1962 г. на базе многочисленных исследований, проводившихся различными учеными, Родни Портер (Rodney Porter) расшифровал основную структуру антител, стало известно, что антитело состоит из легкой и тяжелой цепи. Позже Родни Портеру совместно с Джеральдом Эдельманом (Gerald Edelman) удалось определить последовательность 1300 аминокислот, входящих в белковую цепь антитела, производимого клетками раковой опухоли миеломы. В то время это была самая большая расшифровка аминокислотной последовательности, за что в 1972 году ученые получили Нобелевскую премию. В результате исследований Портера и Эдельмана стало известно, что антитело имеет форму буквы Y, в которой нижняя часть (тяжелая цепь) имеет постоянную структуру для разных антител, а плечи (легкие цепи) значительно различаются у различных антител. Именно эти плечи отвечают за связывание антитела с антигеном и его нейтрализацию.
(Рисунок 1. Структура антитела, за которую ученые Родни Портер и Джеральд Эдельман в 1972 г. получили Нобелевскую премию по физиологии и медицине)
Третий шаг — разработка первой технологии синтеза антител (70–80-е гг. XX в.)
К 1970-м годам уже были известны некоторые важные моменты о том, каким образом в организме человека вырабатываются антитела. В частности, было известно, что за продуцирование антител отвечают В-лимфоциты, причем каждый В-лимфоцит может вырабатывать только одно специфическое антитело, при этом он редуплицируется и за счет этого быстро производит большое количество идентичных по структуре антител — так называемых моноклональных, то есть произошедших от одной клетки-предшественницы.
Добиться столь же быстрой выработки антител в лабораторных условиях удалось в 1975 году ученым Георгу Кёлеру (Georges Köhler) и Сезару Мильштейну (César Milstein). На тот момент была исследована способность клеток раковой опухоли миеломы быстро производить идентичные самим себе клетки. Кроме того, существовала возможность выделения антителопродуцирующих клеток из организма животных. Технология Кёлера и Мильштейна включала несколько этапов: у мыши вырабатывался иммунитет к известному антигену, затем из ее селезенки выделялись антителопродуцирующие клетки, эти клетки с помощью особой технологии соединялись с клетками миеломы с получением гибридомы, клетки которой непрерывно в большом количестве синтезировали антитела против известного антигена. Эта методика произвела переворот в изучении антител, поскольку позволила получать антитела с удивительно точным соответствием определенной структуре. В дальнейшем технология была усовершенствована, и в 1984 году Кёлер, Мильштейн и датский иммунолог Нильс Ерне (Niels Jerne) получили Нобелевскую премию за участие в создании антител, которые можно использовать для диагностических исследований и создания лекарственных средств. В дальнейшем было разработано множество технологий, позволивших усовершенствовать синтез антител за счет развития технологий рекомбинации ДНК, технологий клонирования клеток и других достижений генной инженерии.
Четвертый шаг — применение искусственно синтезированных антител для лечения заболеваний (80-е гг. XX в.)
При первых попытках применения для лечения людей антител, искусственно синтезированных из клеток животных, ученые столкнулись с трудностями. В 1979 г. впервые в мире ученые Филип Сташенко (Philip Stashenko) и Ли Надлер (Lee Nadler) применили искусственно синтезированные моноклональные антитела, полученные из клеток мышей, против антигенов, которые вырабатываются на поверхности клеток раковых опухолей. Однако было выявлено, что мышиные антитела в незначительной степени связывались с опухолевыми антигенами и воспринимались организмом как чужеродные клетки.
С 1986 г. на фармацевтическом рынке началась реализация препарата компании Janssen «Ортоклон ОКТ3» (муромонаб), который позволяет купировать реакцию отторжения трансплантата почки, оказывая избирательное иммуноподавляющее действие. Препарат имеет полностью мышиное происхождение, то есть синтезируется мышиными гибридомами, полученными слиянием мышиной миеломы и мышиных В-лимфоцитов. Вскоре после выхода препарата на рынок стало ясно, что при длительном применении мышиных моноклональных антител в качестве лекарственных средств их эффективность снижалась. Это связано с тем, что мышиные белки являются иммуногенными для организма человека, то есть воспринимаются как чужеродные объекты. В связи с этим у пациентов, которым вводят мышиные антитела, быстро образуются человеческие антимышиные антитела (human antimurine antibody – HAMA). Образующиеся HAMA-антитела нейтрализуют эффект мышиных антител.
Пятый шаг — создание химерных антител (90-е гг. XX в.)
В начале 90-х гг. с использованием молекулярно-биологических методов, основанных на применении рекомбинантной ДНК, были созданы химерные антитела. В химерных антителах часть «мышиной» молекулы с помощью методов генной инженерии заменялась на участок человеческого происхождения, а часть оставалась фрагментом мышиного происхождения. Поскольку белковая последовательность химерных антител на 75% состояла из «человеческих» последовательностей аминокислот, то у пациентов, получавших химерные антитела, HAMA-антитела образовывались в значительно меньшем количестве, и это сделало препараты на основе химерных антител значительно более эффективными, чем на основе мышиных. В дальнейшем был выпущен целый ряд лекарственных средств на основе химерных антител: ритуксимаб, выпускаемый под брендами «Мабтера» и «Ритуксан», — для лечения раковых опухолей, «Ремикейд» (инфликсимаб) — для лечения болезни Крона, «Симулект» (базиликсимаб) — для профилактики острого отторжения трансплантата почки, «Реопро» (абциксимаб) — для профилактики стенокардии и острого инфаркта миокарда, а также другие препараты.
Разработка химерных антител позволила практически полностью отказаться от использования мышиных антител. Однако в некоторых случаях использование мышиных антител и сегодня остается оправданным. Из одобренных к применению лекарственных средств сегодня лишь три являются мышиными: «Ортоклон-ОКТ3» (муромонаб-CD3), «Зевалин» (ибритумомаб тиуксетан) и «Бексар» (тозитумомаб-йод 131). Два последних являются радиоактивно мечеными мышиными МАТ. Их функция заключается в доставке радиоизотопов к клеткам лимфомы. Наличие радиоактивной метки позволяет применять эти антитела в очень небольших количествах, поэтому иммуногенность, обусловленная мышиными последовательностями, в этом случае не так значима. То, что эти препараты включают именно мышиные, а не гуманизированные или человеческие формы делает их более эффективными, потому что гуманизированные формы могли бы связываться одновременно не только с клетками-мишенями, но и со здоровыми клетками, нанося им вред. Также к применению сегодня одобрен один препарат на основе крысино-мышиного МАТ — это препарат «Ремоваб» (катумаксомаб) для лечения злокачественного асцита.
Шестой шаг — создание гуманизированных и человеческих моноклональных антител (конец 90-х гг. XX в. — 2000-е гг. XXI в.)
В конце 90-х гг. с помощью методов генной инженерии удалось свести к минимуму процент мышиных последовательностей аминокислот в искусственно синтезируемых антителах, благодаря чему были получены гуманизированные антитела, еще в меньше степени вызывающие образование HAMA-антител у человека. Начиная с конца 90-х гг. на рынок было выпущено множество препаратов на основе гуманизированных антител.
Примеры препаратов на основе моноклональных антител:
- «Зенапакс» (даклизумаб) — для профилактики отторжения после трансплантации почки,
- «Герцептин» (трастузумаб) — для лечения рака молочной железы и рака желудка,
- «Ксолар» (омализумаб) — для лечения атопической бронхиальной астмы и сезонного аллергического ринита,
- «Раптива» (эфализумаб) — для лечения псориаза, а также многие другие.
В 2000-х годах усовершенствованные методы генной инженерии наконец позволили добиться долгожданного результата и получить человеческие МАТ. В настоящее время человеческие МАТ чаще всего получают с помощью технологии трансгенных мышей (мышей, выведенных с использованием фрагментов чужеродной ДНК) или фагового дисплея (особый метод генной инженерии с использованием вирусов-бактериофагов). Например, сегодня для клинического применения одобрены такие препараты, созданные на основе человеческих МАТ, как «Бенлиста» (белимумаб) — для лечения красной волчанки, «Ервой» (ипилимумаб) — для лечения меланомы, «Симпони» (голимумаб) — для лечения ревматоидного артрита, псориатического артрита, болезни Бехтерева, а также другие препараты.
Еще один тип веществ, созданных методами генной инженерии для лечения пациентов, — это так называемые «белки слияния», в которых искусственно соединены два отдельных белка, зачастую с различными функциями. Например, на основе такого вещества создан препарат «Амевив» (алефацепт) моноклональные антитела при псориазе, орфанный препарат «Аркалист» (рилонацепт) — для лечения редких генетических аутовоспалительных заболеваний, относящихся к группе криопинсвязанных периодических синдромов, и другие препараты.
Разработка новых моноклональных антител сегодня
Разработка лекарственного средства с использованием моноклональных антител — это очень длительный и дорогостоящий процесс. Например, первый препарат на основе мышиных антител «Ортоклон OKT3» был зарегистрирован в 1986 г., только через 11 лет после того, как мышиные антитела были впервые описаны. Первый препарат на основе химерного МАТ «Реопро» был одобрен в 1994 г., через 10 лет после первых работ по изучению химерных МАТ. Первый препарат на основе гуманизированного МАТ «Зенапакс» был утвержден в 1997 г., через 11 лет после первого доклада о конструкции гена гуманизированного антитела. Препарат «Энбрел» на основе слитых белков был одобрен в 1998 г., через 10 лет после описания «белков слияния». Препарат «Хумира» на основе человеческих МАТ был одобрен в 2002 году, через 12 лет после первой статьи о подобных МАТ.
Сегодня интерес к разработке новых препаратов на основе моноклональных антител со стороны производителей очень высок. В настоящее время на территории Российской Федерации стадию клинических исследований проходит более 10 препаратов на основе МАТ. Общее количество препаратов, находящихся на стадии разработки в мире, исчисляется сотнями.
Перед современными учеными, исследующими моноклональные антитела, стоит множество актуальных задач. В частности, поиск решения проблемы иммуногенности препаратов, изготовленных на основе МАТ. Большинство препаратов на основе МАТ, которые сегодня проходят стадию клинических исследований, включают в состав человеческие антитела. Использование этого типа антител снизило иммуногенность препаратов, однако не устранило проблему полностью, поскольку иммунная система человека способна вырабатывать антитела против любого терапевтического белка.
Еще одна проблема, связанная с применением препаратов на основе моноклональных антител, обусловлена тем, что МАТ представляют собой крупные молекулы, которые не способны проникать внутрь клетки или глубоко в ткани. Сегодня МАТ нельзя применять внутрь, так как их концентрация для достижения эффекта должна в несколько тысяч раз превышать концентрацию молекул-мишеней. В связи с этими особенностями, сегодня ученые озабочены созданием нового поколения лекарственных средств, которые объединят в себе преимущества МАТ и мелкомолекулярных препаратов. На этом пути сделано уже несколько важных научных открытий. Первое из них — создание шведской компанией Affibody особых «аффител», которые обладают свойствами обычных антител, но имеют в десятки раз меньшую молекулярную массу, что позволяет им лучше проникать в ткани. Еще одно достижение науки — разработка «нанотел» бельгийской компанией Ablynx. Эти препараты характеризуются высокой стабильностью, что позволяет использовать их внутрь и местно. Кроме того, они просты в производстве. Сейчас на стадии клинических исследований у пациентов с тромбозами и остеопорозом находятся четыре «нанотела». Наконец, еще одно сверхсовременное направление — разработка доменовых антител американской компанией Domantis. Эти антитела должны соответствовать различным отделам тяжелой и легкой цепи антител человека и быть в десять раз меньше обычного антитела, что позволит применять их внутрь и ингаляционно.
Пока что длительность и высокая стоимость производства лекарственных средств с использованием моноклональных антител делает их не всегда доступными для пациентов. Однако ученые работают над созданием новых технологий, которые позволят выпускать новые препараты быстрее и по более низкой стоимости. Благодаря современным технологиям, уже сегодня многие препараты стали доступными для большого количества пациентов и позволили излечить заболевания, ранее считавшиеся неизлечимыми. Можно надеяться, что в будущем спектр излечимых заболеваний еще более расширится, а лекарственные средства на основе моноклональных антител станут еще более эффективными.
Номенклатура моноклональных антител
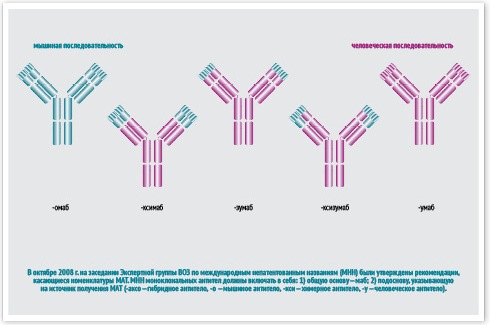
В октябре 2008 г. на заседании Экспертной группы ВОЗ по международным непатентованным названиям (МНН) были утверждены рекомендации, касающиеся номенклатуры МАТ. МНН моноклональных антител должны включать в себя:
- общую основу – маб;
- подоснову, указывающую на источник получения МАТ (-аксо — гибридное антитело, -о — мышиное антитело, -кси — химерное антитело, -у — человеческое антитело).
Источник