Виферон в лечении и профилактике острых респираторных вирусных инфекций
*Импакт фактор за 2018 г. по данным РИНЦ
Читайте в новом номере
ГУ НИИ вирусологии им. Д.И. Ивановского РАМН, Москва
И нтерфероны (ИФН) были открыты в 1957 г. английскими учеными A. Isaacs и S. Lindenmann, как белки, определяющие феномен интерференции, заключающийся в невосприимчивости организма к повторному заражению вирусом.
За полувековую историю развития учения о системе интерферона раскрыты многие важные вопросы ее функционирования, детально исследованы неспецифические и специфические механизмы резистентности. Экспериментальные работы показали, что система ИНФ, возникшая у позвоночных в процессе филогенеза, участвует в обеспечении постоянства внутренней среды организма – гомеостаза [1]. ИНФ являются активными белками, которые вырабатываются всеми клетками организма, но 99% всех ИНФ образуются клетками крови и костного мозга.
Интерфероны образуются под воздействием антигенной системы, но небольшое их количество вырабатывается без участия антигенов. Известно, например, что уровень ИНФ повышен у больных ревматоидным артритом и системной красной волчанкой [2, 3].
Медицинская значимость ИНФ определяется их антивирусной и иммунокорригирующей активностью, а также антитуморогенным и радиопротективным эффектами.
Взаимодействие ИФН с клетками начинается со связывания интерферона со специфическими интерфероновыми рецепторами на поверхности клеток. Установлено, что разные клетки чувствительны к интерферонам различных типов [4]. ИФН– a и – b на поверхности клеток имеют общий рецептор, g –ИФН – отдельный. Попадая внутрь клетки, ИФН активирует гены, кодирующие эффекторные белки, которые ответственны за противовирусный эффект. Роль ИФН в противовирусной защите подтверждается наличием строгой корреляции между уровнем продукции эндогенного ИФН и выздоровлением, усугублением тяжести болезни при подавлении активности эндогенного интерферона, и, наконец, лечение интерфероном позволяет предотвратить развитие вирусной инфекции [5].
ИФН делятся на три основных типа: a , b и g . a – и b –ИФН обладают антивирусным действием, ингибируя процессы транскрипции и трансляции, нарушают синтез вирусных белков [6].
Получены доказательства связи системы интерферона с иммунной системой: интерфероны являются важными медиаторами иммунитета, что позволяет отнести их к семейству регуляторных цитокинов, стимулирует фагоцитоз, активность естественных киллеров, усиливает экспрессию антигенов гистосовместимости 1 и 2 классов [7].
Противовирусная и иммуномодулирующая активность ИФН явилась основанием для применения в медицине лекарственных препаратов интерферона. Наиболее эффективными при большинстве инфекционных заболеваний являются интерфероны– a , которые в клинической практике применяются очень широко. Прежде всего это относится к ИНФ второго поколения – рекомбинантным интерферонам– a 2, полученным генно–инженерным путем (без использования донорской крови). Различают несколько препаратов интерферона– a 2: 2а, 2b и 2с.
Препараты интерферона обладают достаточно высокой эффективностью, однако следствием биологических процессов, которые ИФН вызывают в организме, являются побочные реакции. Наиболее частым (с большими индивидуальными колебаниями) является гриппоподобный синдром, наблюдающийся практически у всех больных, особенно в случаях применения высоких доз ИНФ. Наряду с гриппоподобным синдромом при длительных курсах могут возникать серьезные побочные явления со стороны сердечно–сосудистой системы (гипотония, нарушение сердечного ритма) и ЦНС (раздражительность, агрессивность или депрессия). Все это ограничивает применение препаратов ИФН, а при опасных побочных явлениях требует отмены.
Поиск новых форм препаратов, позволяющих избежать негативных явлений, привел к созданию Виферона – нового противовирусного иммунномодулирующего препарата, разработанного в НИИ эпидемиологии им. Н.Ф. Гамалеи РАМН (выпускается ООО «Ферон», Москва). В России Виферон зарегистрирован и разрешен для применения в 1998 г. Лекарственная форма – ректальные свечи и мазь.
Механизм действия Виферона
Виферон представляет собой комплекс рекомбинантного интерферона– a 2b в сочетании с препаратами антиоксидантного действия – a –токоферола ацетата и аскорбиновой кислоты в терапевтически эффективных дозах.
В серии экспериментальных работ В.В. Малиновской было показано, что способность к продукции ИНФ значительно повышается при добавлении (in vitro) к ИФН – индуцирующим клеткам a –токоферола ацетата и аскорбиновой кислоты, влияющих на процессы перекисного окисления липидов мембран клеток [7]. Применение формулы индекса эффективности сочетания препаратов показало, что использование Р–ИФНа с антиоксидантами оказывало синергидное действие на противовирусный эффект Р–ИФНа, многократно усиливая противовирусное действие интерферона [8].
Детальное исследование механизма действия Виферона позволило выявить его иммуномодулирующее действие на Т– и В–лимфоциты, нормализацию показателей гуморального иммунитета, содержание иммуноглобулина Е [9]. Установлена четкая корреляция между различными факторами специфической, неспецифической и антиоксидантной защиты при лечении вирусных и бактериальных инфекций [10].
Изучение фармакокинетики препарата показало, что ректальное введение Виферона позволило достичь более высокой концентрации и длительной циркуляции в крови Р–ИФН, чем при парентеральном введении [11]. Снижение уровня сывороточного интерферона через 12 часов обусловливает необходимость его повторного введения.
Побочные эффекты и переносимость
Побочные эффекты Виферона во время испытания препарата не зафиксированы.
Установлено, что при длительном применении виферона не образуются антитела, нейтрализующие антивирусную активность Р–ИФН альфа 2b.
В настоящее время Виферон является единственным зарегистрированным в России препаратом из класса рекомбинантных интерферонов, разрешенным Государственным Фармакологическим Комитетом МЗ РФ для лечения различных инфекционных заболеваний не только взрослых, но и детей, в том числе новорожденных, а также беременных женщин.
Клинико–иммунологическая эффективность Виферона
Вирусиндуцированная дисфункция иммунитета (супрессия Т–клеточного звена, угнетение фагоцитоза и др.), развивающаяся при гриппе и других ОРВЗ, позволяет отнести последние к числу тех заболеваний, течение и исход которых определяется наличием в комплексном лечении иммунных препаратов.
В нашей клинике в течение последних лет изучается клиническая эффективность Виферона при респираторных заболеваниях и их бактериальных осложнениях. В частности, нами в открытом плацебо–контролируемом исследовании показана высокая терапевтическая эффективность при гриппе и других респираторных заболеваниях, осложненных ангиной [12]. Под наблюдением находились 54 больных лакунарной ангиной и острым респираторным вирусным заболеванием, подтвержденным лабораторными методами. Получены достоверные доказательства эффективности лечения антибактериальными средствами в сочетании с Вифероном. Препарат назначали по 500 тыс. МЕ два раза в сутки в течение пяти дней. Начинали лечение не позднее 48 часов от появления первых признаков болезни. Терапевтический эффект выражался в сокращении симптомов интоксикации и продолжительности гнойных наложений на миндалинах, сокращении сроков заболевания в целом.
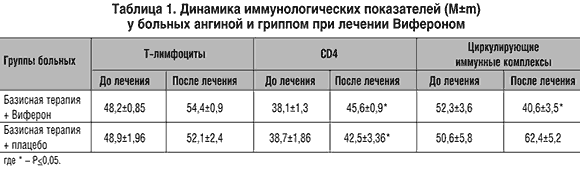
Клинический эффект, как правило, сопровождался и выраженным улучшением иммунологических показателей: нормализацией исходно сниженных СД3 и СД4, уменьшением количества циркулирующих иммунных комплексов (табл. 1). Положительная динамика циркулирующих иммунных комплексов при лечении Вифероном, с нашей точки зрения, является важным критерием, свидетельствующим об элиминации возбудителя и сокращении сроков заболевания с одной стороны [12].
По данным других клинических наблюдений за 137 больными в возрасте от 1 года до 14 лет при тяжелых формах ОРВИ, на основании клинико–катамнестического анализа авторами установлено, что при тяжелых формах инфекции достоверно чаще регистрируется низкий исходный уровень сывороточного ИФН и значительное уменьшение общего числа Т–лимфоцитов, снижение активности фагоцитов, что является основанием для назначения виферона с 1–2 дня болезни детям с тяжелыми формами ОРВИ.
Катамнестическое наблюдение за 50 детьми из числа обследованных в течение 3–6 месяцев выявило протективный эффект виферона в отношении последующих эпизодов ОРВИ [13]. Авторы рекомендуют назначать препарат часто и длительно болеющим детям 1–14 лет в течение 5 дней по 2 свечи в сутки в следующих дозах: по 500 000 МЕ в свече детям до 7 лет, и по 1 млн. МЕ – детям от 7 до 14 лет, и применять его с профилактической целью в период высокой заболеваемости ОРВИ и для адаптации детей в дошкольных учреждениях.
Клинико–иммунологические наблюдения в группе взрослых и детей, часто болеющих вирусными и бактериальными инфекциями респираторного тракта, позволили выявить нарушения в системе интерферона: снижение способности лейкоцитов к продукции a – и g –интерферонов. Выраженные изменения в системе Т–клеточного звена иммунитета требуют применения адекватных доз виферона [13,15]. Частота и длительность курсового лечения зависят от тяжести заболевания и выраженности изменений в иммунном статусе. Как правило, терапия Вифероном проводится в течение нескольких месяцев в возрастной дозировке. Пролонгированная вифероно–терапия в течение 2,5 месяцев позволила уменьшить частоту ОРВЗ примерно в 2–5 раз в год [13].
Применение Виферона–мази для лечения и профилактики гриппа и других ОРВИ
Виферон–мазь, содержащая в 1 г 40 тыс. МЕ ИФН и токоферол ацетат в терапевтической дозе, применяется при первых признаках заболевания интраназально 3–4 раза в день в течение 5 дней. В целях профилактики в очагах инфекции мазь наносится тонким слоем на слизистую оболочку носовых ходов 2 раза в день утром и вечером в течение всего опасного периода.
Согласно результатам исследования Е.С. Макаровой (2001), проведенного в дошкольном учреждении, при изучении интерферонового статуса у детей от 1 года 7 месяцев до 3 лет на фоне превентивного применения мази Виферона отмечено увеличение продукции g –интерферона, достоверное уменьшение количества циркулирующего «раннего» интерферона, сокращение заболеваемости в 4 раза, отсутствие побочных реакций. Полученные результаты, согласно заключению авторов, свидетельствуют о высокой эффективности вифероно–профилактики у часто болеющих детей раннего возраста [15].
Таким образом, удобные лекарственные формы, высокая лечебная и профилактическая эффективность Виферона, направленность воздействия на иммунитет позволяет рекомендовать данный препарат в комплексном лечении и профилактике респираторных инфекций.
В 2001 году работы по созданию новых лекарственных форм рекомбинантных интерферонов (в том числе Виферона) и внедрению их в клиническую практику удостоены премии Правительства Российской Федерации.
Из средств растительного происхождения для профилактики ОРВИ рекомендуются такие препараты, как сухой очищенный экстракт из листьев облепихи крушиновидной семейства лоховых. Препарат обладает противовирусной и интерферониндуцирующей активностью, назначается взрослым и детям при первых симптомах респираторного заболевания. Наиболее выраженный лечебный эффект достигается при сочетании лекарственных форм общерезорбтивного и местного действия.
Эффективным является иммунал сок эхинацеи пурпурной, содержащий уникальный комплекс фитокомпонентов. Препарат стимулирует выработку организмом собственного интерферона, предотвращает развитие заболевания и смягчает его симптомы; выпускается в виде капель, рекомендуется принимать курсом не менее недели. Достижение стойкого эффекта – через 8 недель.
1. Соловьев В.Д. Бектемиров Т.А. Интерфероны в теории и практике медицины. 2–е изд. – М.1981.
2. Cross J.C., Roberts R.M. Constitutive and trophoblast – specific expression if a class of bovine interferon genes. Proc. Natl. Acad. Sci USA 1991: 88, 3817 – 3824.
3. Dianzani F. The interferon system. Helth Sciences Press, 1993
4. Хесин Я.Е., Наровлянский А.Н., Амченкова А.М. Клеточные рецепторы для интерферонов. В кн. Система интерферона в норме и при патологии., Москва, 1996 : 39 – 52.
5. Dianzani F. Baron S. The interferon’s: a biological system with therapeutic potential in viral infections. In Lymphoblastoid Alpha – Interferon Carrent
Medical Literature Ltd , London ,1995.
6. Ершов Ф.И. Интерфероны (к 40–летию открытия). Вопр. вирус., 1998, № 6,т. 43, с. 247 – 252.
7. Himmler A., Hauptmann R. et al. Structure and expression in Escherichia coli of canine interferon alpha gene. J. Interferon Res, 1987: 7 , p 173 – 178.
8. Malinovskaya V.V. «Interferon a2b antivirus action modulation with the help of antioxidant action preparation» International Conference on Interferon’s Biology and Clinical Applications. 77, 1998.
9. Тареева Т. Г. и др. «Применение Виферона при внутриутробной инфекции плода и новорожденных» Тез. Докл. Росс.нац.конгр. «Человек и лекарство» М.,162,1995.
10. Кешинян Е.С. и др. «Применение генно–инженерного альфа 2–интерферона – Виферона в комплексной терапии тяжелых форм инфекционно–воспалительных заболеваний у новорожденных детей» Тез.
докл. Росс.нац.конгр. «Человек и лекарство» ,162, 1995.
11. Бабаянц А.А. Малиновская В.В. Мешкова Е.Н. «Фармакокинетика интерферона при ректальном введении» Вопр. Вирус.1:83–84, 1986
12.. Колобухина Л.В. Гатич Р.З. Меркулова Л.Н. и др. «Комплексное лечение ОРВИ, осложненных ангиной» Леч. Врач ,2003,№1 , с 32 –33.
13. Чеботарева Т.А. Тимина В.П. Малиновская В.В. Виферон: применение при гриппе и др. ОРВИ у детей в кн. « Иммуномодулирующий и противовирусный препарат виферон в лечении детей и взрослых, часто болеющих вирусно–бактериальными инфекциями», М.2003.
14. Караулов А.В. Сокуренко С.И. Бармотин Г.В. Принцип иммунотерапии и иммунореабилитации рецидивирующих респираторных заболеваний. Леч.врач, 2000 , №1 , с 44 – 45.
15. Макарова Е.С. Доскин В.А. Малиновская В.В. и др. Применение виферона у детей раннего возраста в зависимости от сезонных ритмов интерферонообразования. Тезисы докл. Росс. науч. Конгр. «Человек и лекарство» ( М ), 2 – 6 апреля 2001, с 272.
Источник
Применение рекомбинантного альфа-2b-интерферона (ВИФЕРОН®) при острых респираторных инфекциях у детей раннего возраста
Особенности онтогенеза иммунной системы определяют параметры иммунореактивности новорожденных и детей раннего возраста при острых респираторных инфекциях (ОРИ) и должны учитываться при организации профилактики и лечения инфекционных заболеваний респираторного тракта. Отягощенный преморбидный фон в сочетании с указанными физиологическими особенностями иммунной системы способствует развитию нарушений в формировании иммунного ответа на инфекционные агенты. В этой связи большое значение приобретает поиск способов универсального противоинфекционного воздействия и щадящего, неспецифического, влияния на иммунную систему ребенка для коррекции и предупреждения нарушений механизмов резистентности.
В ходе сравнительного клинико-иммунологического исследования в параллельных группах показана высокая эффективность и преимущество модифицированного режима интерферонотерапии у детей раннего возраста при ОРИ по сравнению со стандартной схемой интерферонотерапии и базисным лечением, что выразилось в сокращении продолжительности основных симптомов заболевания, предупреждении суперинфицирования и нормализации иммунного статуса ребенка. Рекомендовано включение в состав интерферонотерапии стартовых доз рекомбинантного альфа-2b-интерферона (препарат ВИФЕРОН®) 500 000 МЕ (ректально) в течение первых 5 дней с переходом на 150 000 МЕ в течение последующих 5 дней в комбинации с мазью ВИФЕРОН® (интраназально).
- КЛЮЧЕВЫЕ СЛОВА: ОРИ у детей, педиатрия, инфекции у детей, инфекционные болезни
Особенности онтогенеза иммунной системы определяют параметры иммунореактивности новорожденных и детей раннего возраста при острых респираторных инфекциях (ОРИ) и должны учитываться при организации профилактики и лечения инфекционных заболеваний респираторного тракта. Отягощенный преморбидный фон в сочетании с указанными физиологическими особенностями иммунной системы способствует развитию нарушений в формировании иммунного ответа на инфекционные агенты. В этой связи большое значение приобретает поиск способов универсального противоинфекционного воздействия и щадящего, неспецифического, влияния на иммунную систему ребенка для коррекции и предупреждения нарушений механизмов резистентности.
В ходе сравнительного клинико-иммунологического исследования в параллельных группах показана высокая эффективность и преимущество модифицированного режима интерферонотерапии у детей раннего возраста при ОРИ по сравнению со стандартной схемой интерферонотерапии и базисным лечением, что выразилось в сокращении продолжительности основных симптомов заболевания, предупреждении суперинфицирования и нормализации иммунного статуса ребенка. Рекомендовано включение в состав интерферонотерапии стартовых доз рекомбинантного альфа-2b-интерферона (препарат ВИФЕРОН®) 500 000 МЕ (ректально) в течение первых 5 дней с переходом на 150 000 МЕ в течение последующих 5 дней в комбинации с мазью ВИФЕРОН® (интраназально).
Адекватный ответ на инфекцию требует сбалансированного функционирования основных элементов защиты организма. Иммунопатогенез острых инфекций у детей имеет свои особенности, связанные с функциональной незрелостью как самой иммунной системы, так и механизмов центральной регуляции иммунного ответа. После рождения организм ребенка начинает контактировать с огромным количеством антигенов. В норме у новорожденных при физиологически протекающих беременности и родах иммунная система, несмотря на относительную «незрелость», способна контролировать бактериальную колонизацию, происходящую в течение 1-й недели после рождения [1–7]. Преждевременные роды сопровождаются недостаточным обеспечением новорожденного иммуноглобулинами, в частности иммуноглобулином (Ig) G, а также другими защитными факторами. Кроме того, отягощенный преморбидный фон новорожденного в условиях дефицита материнских антител отрицательно влияет на формирование как гуморального, так и клеточного звеньев иммунной защиты.
Известно, что чем меньше масса недоношенного ребенка, тем ниже содержание у него всех популяций Т-клеток. Недоношенные дети в большинстве случаев имеют те или иные признаки внутриутробного инфицирования, что является дополнительным фактором риска развития инфекционных заболеваний. Таким образом, недоношенность ассоциируется с более выраженной иммунологической недостаточностью и высоким риском развития инфекционных заболеваний [5, 7–9]. Уточнение факторов риска, негативно влияющих на формирование иммунного ответа у детей раннего возраста, способствует поиску способов универсального противоинфекционного воздействия и коррекции нарушений механизмов резистентности организма. С этой целью наиболее перспективным является использование препаратов на основе естественных факторов иммунитета – рекомбинантного альфа-2b-интерферона в сочетании с мембраностабилизирующими веществами (антиоксидантами, витаминами E и С) – препарата ВИФЕРОН®, выпускаемого в различных лекарственных формах (мазь, гель, суппозитории). Противовирусный эффект препарата ВИФЕРОН® реализуется уже через час после его введения через прямую кишку или нанесения местно на слизистые оболочки носо- и ротоглотки.
В зависимости от используемой дозы интерферона (ИФН) и времени применения препаратов на его основе по отношению к времени воздействия вируса на организм развивается доминирующий вируцидный (максимальный элиминирующий) или иммуномодулирующий эффект. Введение повышенных доз ИФН (детям до 6 лет 500 000 МЕ вместо 150 000 МЕ) на начальных этапах развития инфекции позволяет обеспечить элиминацию инфекционного агента задолго до того, как собственные клетки начинают синтезировать эндогенный ИФН в достаточном количестве. Кроме того, введение ИФН позволяет «разгрузить» пораженные клетки и компенсировать их неспособность к продукции собственного ИФН в необходимых количествах. Наконец, ускоренная элиминация инфекционного агента, достигнутая повышенными дозами экзогенного ИФН, позволяет сократить сроки течения инфекционного процесса, что препятствует достижению критических концентраций провоспалительных цитокинов и, как следствие, возникновению системных реакций. Обычные терапевтические дозы препарата ВИФЕРОН® оказывают положительное иммуномодулирующее влияние: происходит активация параметров иммунитета, в том числе интерферонопродукции, в случае если они снижены, и снижение их активности – в случае если она повышена [10–15].
Проведенные ранее исследования по применению препарата ВИФЕРОН® при различных инфекционных заболеваниях продемонстрировали его высокую клинико-иммунологическую эффективность и отсутствие побочных эффектов [16–19]. Однако до настоящего времени остается предметом научных дискуссий тактика выбора различных лекарственных форм препарата ВИФЕРОН® при терапии острых респираторных инфекций (ОРИ) у детей.
Исследование проведено с целью определения факторов риска, негативно влияющих на формирование противоинфекционной резистентности у детей раннего возраста, оптимизации схем и режимов дозирования препарата ВИФЕРОН® при лечении детей с ОРИ.
Пациенты и методы
Исследования проводились на базе 3-го инфекционного отделения Тушинской детской городской больницы (ТДГБ) Департамента здравоохранения города Москвы (главный врач – И.М. Османов). Под нашим наблюдением находился 91 ребенок в возрасте от 1 месяца до 3 лет с клинически установленным диагнозом ОРИ. Пациенты подбирались случайным образом (по очередности поступления) с учетом критериев включения/исключения и не позднее первых-вторых суток госпитализации. Дети, включенные в исследование, не получали лечения каким-либо иммуномодулятором в течение предшествующих четырех недель. На момент рандомизации средний возраст обследованных детей составил 15,5 ± 9,9 месяцев. Доля детей в возрасте от 1 месяца до 1 года равнялась 44 ± 5,2%, от 1 года до 3 лет – 56 ± 5,2%. Среди обследованных нами пациентов большинство было мальчиков – 53,9 ± 5,2%, количество девочек – 46,1 ± 5,2%. К моменту рандомизации (1–2-е сутки госпитализации) длительность заболевания составила от 1 до 3 суток у 60,4 ± 5,1% детей и более 3 суток у 39,6 ± 5,1% детей (р 0,05) и во 2-й группе – 2,9 ± 0,4 сут (р > 0,05) в сравнении с 3,9 ± 0,4 сут в 3-й группе). Наблюдалось также достоверное снижение продолжительности гиперемии зева: в 1-й группе – 3,3 ± 0,2 сут (р 0,05). Во 2-й и 3-й группах спектр элиминированных вирусов был представлен только вирусами гриппа (Н1N1, H3N2 и В) и парагриппа, а у пациентов 1-й группы наряду с вышеуказанными в состав элиминированных вирусов входили также респираторно-синцитиальный вирус, рино- и аденовирусы. Наиболее резистентными к проводимой терапии оказались бока- и метапневмовирусы. За время пребывания в стационаре у 46 детей отмечалось ухудшение состояния, проявляющееся повторной лихорадкой, интоксикацией и диарейным синдромом, что было расценено как развитие суперинфекции. При этом у детей 1-й группы в 1,5 раза реже регистрировалась тенденция к ухудшению состояния (23,9 ± 6,3%), чем во 2-й группе (37,1 ± 7,1%; р > 0,05), и в 1,7 раза реже, чем в 3-й группе (39,1 ± 7,2%; р > 0,05), заболевание протекало в легкой форме и непродолжительно (1,7 ± 0,2 дня против 2,3 ± 0,2 и 2,3 ± 0,4 сут соответственно) (р 0,05), в то время как в 1-й и 2-й группах повышение этих показателей было достоверно значимым (р 0,05), при этом уровень ИФН-гамма в сыворотке крови повышался в 1-й и 2-й группах (р > 0,05) и понижался в 3-й (р 0,05). При анализе уровня спонтанной продукции ИФН-альфа клетками крови не было отмечено существенных изменений, и ее значения были ниже порога чувствительности тест-систем. Уровень спонтанной продукции ИФН-гамма имел тенденцию к снижению у всех детей по сравнению с исходными значениями (р > 0,05). В связи с отсутствием достоверных различий по указанным показателям и малой информативностью полученных данных изучение спонтанной продукции ИФН нами не проводилось.
При более детальном сравнительном анализе значений сывороточных ИФН в зависимости от уровня показателей и способов проводимой терапии были получены следующие данные (см. табл. 6). В 1-й группе установлено уменьшение числа детей с низкими значениями сывороточного ИФН-альфа почти в 1,5 раза (75 ± 9,7% против исходных 55 ± 11,1%; р > 0,05), в 3-й группе – в 1,2 раза (71,4 ± 9,9% против 61,9 ± 10,6% до лечения; р > 0,05), во 2-й группе количество детей с уровнем сывороточного ИФН-альфа ниже 2 пг/мл не изменилось (61,9 ± 10,6%). Кроме того, отмечено увеличение количества детей со значениями ИФН-альфа более 6 пг/мл: в 1-й группе – в 3,5 раза (с 10 ± 6,7% до 35 ± 10,7%; р 0,05) и в 3-й группе – в 1,7 раза (с 14,3 ± 7,6% до 23,8 ± 9,3%; р > 0,05).
При оценке динамики сывороточного ИФН-гамма у детей были получены следующие результаты. На фоне проведенного лечения в 1-й группе число детей с низкими показателями сывороточного ИФН-гамма (ниже 2 пг/мл) сократилось в 1,2 раза (с 80 ± 8,9% до 70 ± 10,3%; р > 0,05), в то время как в 3-й группе отмечено повышение этого показателя (с 61,9 ± 10,6% до 95,2 ± 4,7%; р 0,05). Кроме того, в 1-й группе отмечено повышение частоты детей с уровнем ИФН-гамма в сыворотке выше 10 пг/мл (с 5 ± 4,8% до 20 ± 8,9%; р > 0,05), в 3-й группе – снижение (с 23,8 ± 9,2% до 4,8 ± 4,6%; р > 0,05), во 2-й группе изменений не зарегистрировано (14,3 ± 7,6%). По аналогии с оценкой показателей сывороточных ИФН нами был проведен подробный анализ показателей индуцированной продукции ИФН-альфа и ИФН-гамма у обследованных детей в зависимости от вида терапии. Повышение способности к продукции ИФН-альфа отмечалось чаще на фоне модифицированной схемы интерферонотерапии – 60 ± 10,9%, чем при стандартной интерферонотерапии – 38 ± 10,6% (р > 0,05) и базисном лечении – 28,5 ± 9,9% (р 0,05) и 61,9 ± 10,6% (р 0,05) и базисном лечении – 33,3 ± 10,3% (р > 0,05). Снижение уровня продукции ИФН-гамма определялось реже в 1-й группе – 35 ± 10,6% и 2-й группе – 28,6 ± 9,9%, чем в 3-й группе – 47,6 ± 10,9% (р > 0,05).
При анализе зависимости продолжительности основных клинических симптомов ОРИ от характера изменений показателей индуцированной продукции ИФН нами было установлено, что повышение исходно сниженной способности к индуцированной продукции как ИФН-альфа, так и ИФН-гамма сопровождалось более значимым сокращением продолжительности симптомов ОРИ в 1-й группе, в отличие от 2-й и 3-й группы. Кроме того, в случае понижения показателей индуцированной продукции ИФН-альфа и ИФН-гамма сроки течения заболевания при использовании модифицированной схемы интерферонотерапии были короче, чем при стандартной схеме интерферонотерапии или при применении только препаратов базисной терапии (табл. 7). Проведенный корреляционный анализ выявил наличие обратной зависимости основных симптомов заболевания от уровня индуцированной продукции ИФН при повторном обследовании. Так, коэффициент корреляции (r) между уровнем индуцированного ИФН-гамма и продолжительностью лихорадки составлял -0,32, интоксикации – -0,44 и выраженностью ринореи – -0,42. Полученные данные подтверждают, что повышение значений индуцированной продукции ИФН-гамма в более поздние сроки болезни ассоциируется с эффективным иммунным ответом против инфекционных патогенов и является признаком благоприятного течения и исхода ОРИ.
Таким образом, нами установлено, что модифицированная интерферонотерапия достоверно повышала количество лимфоцитов с маркерами CD3+ и CD3+4+, возможно, за счет усиления процессов дифференцировки и пролиферации лимфоцитов, приводила к увеличению уровня ИФН-альфа в сыворотке крови и способности к продукции ИФН-альфа и/или ИФН-гамма. Кроме того, усиление процессов антителообразования на фоне модифицированной терапии препаратом ВИФЕРОН® позволило повысить содержание сывороточного IgA и предупредить дальнейшее снижение исходно низкого значения sIgA в носоглоточных смывах в 1-й и 2-й группах наблюдения. Высокий уровень иммунологической эффективности у детей 1-й группы наблюдения способствовал достоверному уменьшению продолжительности основных клинических проявлений ОРИ у детей раннего возраста, суперинфицирования и сроков пребывания их в стационаре. Нами доказано, что усовершенствованный способ лечения ОРИ у детей раннего возраста, основанный на применении стартовых доз рекомбинантного альфа-2b-интерферона (ВИФЕРОН®) 500 000 МЕ (ректально) в течение первых 5 дней с переходом на 150 000 МЕ в течение последующих 5 дней в комбинации с мазью ВИФЕРОН® (интраназально), характеризуется хорошей переносимостью и высокой клинико-иммунологической эффективностью, а также способствует снижению вероятности суперинфицирования.
Источник