Выбираем успокоительное
Поделиться:
на правах рекламы
Виной всему как внешние факторы, которые воздействуют на нас из вне, так и внутренние – из глубин нашего организма. Мы раздражаемся, нервничаем, плохо спим. В итоге нарушается работа многих органов и систем, снижается память и внимание, слабеет иммунитет, повышается артериальное давление и учащается сердечный ритм. Поэтому очень важно разобраться в причинах стресса и по мере возможности воздействовать на них, что в дальнейшем поможет сохранить и улучшить качество нашей жизни.
Первая помощь при остром стрессе, состояниях, сопровождающихся нервным возбуждением, раздражительностью, тревожностью и нарушениями сна – это применение успокоительных средств, которые издавна успешно используются в медицине.
Успокоительные средства представлены следующими группами:
- Растительные (валериана, пустырник, мята перечная, боярышник, пион и другие);
- Синтетические (бромиды, некоторые барбитурат содержащие препараты, малые транквилизаторы);
- Комбинированные (Валемидин, Ново-Пассит).
Растительные одно- и многокомпонентные препараты имеют преимущество перед синтетическими, поскольку они малотоксичны и безопасны, хорошо переносятся, особенно пожилыми людьми, и при длительном их применении не вызывают зависимости и привыкания. Седативное действие наиболее выражено у лекарственных растений: валериана, пустырник, мелисса, мята, пион. Недостатком этих препаратов является то, что для наступления эффекта их нужно принимать длительно.
К синтетическим успокоительным средствам относятся бромиды, некоторые барбитурат содержащие препараты и малые транквилизаторы.
Препараты брома применяют при различных невротических расстройствах, они обладают также противосудорожной активностью. В настоящее время используются очень редко из-за накапливания в организме, что может стать причиной хронического отравления (бромизма).
Фенобарбитал содержащие препараты (Валокордин, Корвалол) обладают успокаивающим действием и способствуют нормализации сна. Однако их длительный приём может привести к формированию зависимости и при внезапном прекращении их приёма, иногда развивается «синдром отмены», сопровождающийся в тяжелых случаях судорогами и галлюцинациями. В большинстве стран подобные фенобарбитал содержащие препараты запрещены.
Малые транквилизаторы – это препараты снимающие тревожные состояния и страх. Они также обладают успокаивающим и снотворным эффектом. При их назначении врач тщательно анализирует клинические симптомы и индивидуально подбирает препарат и его дозировку.
Комбинированные препараты наиболее популярная группа успокоительных средств. В большинстве случаев они отпускаются без рецепта врача и их можно купить по доступным ценам. Эти препараты могут содержать или только растительные компоненты, или могут быть комбинированы с синтетическими.
Какие успокоительные наиболее безопасны и действуют быстро
По данным ВОЗ до 80% населения предпочитает лечиться препаратами растительного происхождения, как уже упоминалось выше эти препараты наименее токсичны, хорошо переносятся и не вызывают зависимости и привыкания. Что касается быстродействия, то не стоит ждать от полностью растительных препаратов моментального результата. Для развития стойкого эффекта необходимо длительное применение.
Если же нужно, чтобы успокоительное подействовало быстро (острый стресс, сдача экзаменов, эмоциональное возбуждение, повышенная раздражительность, конфликтная ситуация), то в этом случае поможет комбинированный препарат Валемидин, в его составе растительные настойки: валерианы, пустырника, боярышника, мяты перечной. Быстродействие Валемидина обеспечивает малая доза димедрола в его составе, усиливающая эффект всех настоек.
Валемидин был разработан как растительная альтернатива синтетическим препаратам Корвалолу и Валокордину. Важно, что Валемидин не вызывает зависимости и привыкания, а при длительном его применении не происходит снижения памяти, умственной работоспособности, замедления мышления.
При выборе успокоительных средств необходимо также обращать внимание на их противопоказания, которые указываются в инструкции к лекарственному препарату. Перед применением внимательно ознакомьтесь с инструкцией.
Источник
Лекарственных средств растительного происхождения это
На протяжении всей своей истории человечество соприкасалось с царством растений, используя последние для удовлетворения своих хозяйственных, пищевых и лекарственных целей. Поэтому неудивительно, что даже современные лекарственные препараты разработаны на основе природных соединений. Среди них наиболее известны витамин С, аспирин, хинин, морфин и кодеин. В последние десятилетия большое внимание уделяется изучению свойств таксола, арглабина, винбластина и некоторых других соединений, полученных на основе растительных препаратов.
Поиск новых биологически активных соединений растительного происхождения для лечения и профилактики иммуносупрессии, инфекционных заболеваний, онкологии и метаболических заболеваний остается активной частью фармацевтических исследований [15]. В последние годы на рынке появилось более 40 новых препаратов природного происхождения, прошедших полный путь от исследования до клинических испытаний [2]. Такое внимание исследователей к природным соединениям обусловлено в первую очередь меньшей токсичностью растительных препаратов и более широким спектром действия. Некоторые лекарственные соединения растительного происхождения обнаружили способность эффективно блокировать развитие различных вирусов, включая вирус простого герпеса, гриппа, вирус иммунодефицита человека, вирусы гепатита С и В и многие другие [4, 8, 17, 19,].
Целью данного сообщения является систематизация данных по действию различных соединений растительного происхождения, способных ингибировать репродукцию вирусов.
Основой противовирусной терапии является воздействие на вирус или его составляющие компоненты на той или иной стадии репродукции. Весь процесс репродукции вирусов может быть условно разделен на три фазы [15]. Первая фаза охватывает события, которые ведут к адсорбции и проникновению вируса в клетку, освобождению его внутренних структурных компонентов и модификации его таким образом, что он способен вызвать инфекцию. Вторая фаза репродукции связана со сложными процессами, в течение которых происходит экспрессия вирусного генома. Заключительной стадией репродукции является выход вирусного потомства из клетки путем почкования или за счет лизиса, причем в последнем случае клетка погибает [12]. Имеющийся на сегодняшний день арсенал противовирусных средств способен оказывать воздействие на любой из этапов репродукции вируса.
Адсорбция и проникновение вируса в клетку
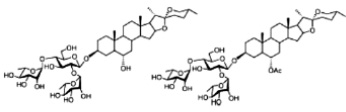
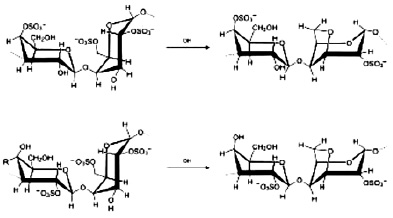
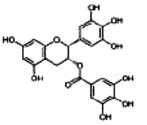
Взаимодействие вируса с клеткой начинается с процесса адсорбции, т.е. прикрепления вирусных частиц к клеточной поверхности. Этот процесс протекает при наличии соответствующих рецепторов на поверхности клетки и «узнающих» их субстанций на поверхности вируса. Прикрепление вируса к клетке происходит в два этапа, один из которых неспецифический, другой ‒ специфический. Поэтому химиотерапия этого этапа инфекции может быть также разделена на специфическую и неспецифическую. Неспецифическая стадия блокирования адсорбции вируса в первую очередь связана с электростатическими взаимодействиями между вирусом и клеткой, поэтому использование полисахаридов и некоторых пептидов, выделенных из растений и несущих большой отрицательный заряд, эффективно ингибирует адсорбцию вирусов. В подобных препаратах необходимы, как минимум, две сульфатные группы на один моносахарид. При этом противовирусная активность возрастает с возрастанием молекулярной массы в интервале от 1 до 10 kD. При меньших, а также больших массах полисахаридов противовирусная активность резко снижена. Не менее интересной группой химических соединений, подавляющих адсорбцию вирусов, можно назвать тритерпеновые сапонины, которые в силу своих структурных особенностей, связываясь с холестерином мембраны, способны изменять пространственную структуру мембраны клетки [13]. Установлено, что наличие у подобных препаратов трех сахарных остатков 3-O-β-хакотриозила увеличивает противовирусную активность соединений. Другой группой препаратов, блокирующих репликацию вирусов, являются полифенольные соединения, не только изменяющие заряд поверхности клетки, но и препятствующие специфической сорбции вируса на рецепторы (рис. 1).
Рис. 1. Соединения, блокирующие стадию адсорбции вируса [4, 8, 13]
Освобождение внутреннего компонента вируса
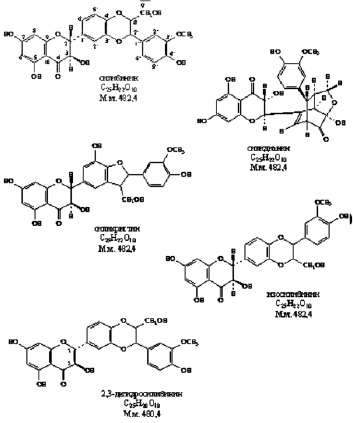
После проникновения вириона в клетку происходит целый комплекс превращений вируса, смысл которых заключается в удалении вирусных защитных оболочек, препятствующих экспрессии вирусного генома. Этот процесс сопровождается рядом характерных особенностей: исчезает инфекционность вируса, появляется чувствительность к нуклеазам, возникает устойчивость к нейтрализующему действию антител. Основной группой растительных соединений, способных подавлять репродукцию вирусов на этой стадии, являются аналоги силимарина, лютеолина и кверцетина (рис. 2) [4, 20, 21].
Рис. 2. Соединения, блокирующие освобождение внутреннего компонента вируса
Экспрессия вирусного генома и сборка вирусных частиц
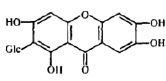
Экспрессия вирусного генома и сборка вирионов являются самыми сложными этапами, включающими транскрипцию нуклеиновых кислот, трансляцию белков, посттрансляционные модификации вирусных белков, репликацию нуклеиновых кислот, сборку вирусных частиц. Этот этап репродукции вирусов успешно блокируется 2 основными группами растительных соединений: ингибиторами РНК полимераз и ингибиторами посттрансляционных модификаций белков. К таким препаратам относятся алпизарин, госсипол, эпиген и др (рис. 3).
Механизм действия подобных препаратов связан с образованием ацил-ферментных производных и основан на блокировании одной из трех основных областей, критичных для активности аспарагиновой протеазы вируса: каталитическое ядро фермента, содержащее пару Asp-Thr/Ser-Gly триад, мобильная flap-область и домен димеризации на N- и С-концах протеазы [1, 10, 14].
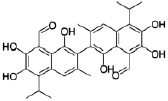
Рис. 3. Соединения, блокирующие экспрессию вирусного генома
Выход вирусного потомства
Завершающим этапом репродукции вируса является выход вирионов из инфицированной клетки. Этот процесс может протекать с помощью почкования вируса и лизиса клетки. Лизис клетки, как правило, сопровождается гибелью клетки. Блокировать такой механизм выхода вируса практически невозможно.
Выход из клетки путем почкования осуществляют вирусы с липопротеиновой оболочкой. При этом способе клетка может длительное время сохранять жизнеспособность и продуцировать вирусное потомство, пока не произойдет полное истощение ее ресурсов. Одним из механизмов блокирования этого этапа репродукции вируса является использование ингибиторов ферментативной активности вируса, участвующей в почковании вируса. Разработка препаратов группы ингибиторов фермента вируса гриппа – нейраминидазы (NA) ‒ является успешным достижением современной вирусологической науки последних лет – так называемого «рационального лекарственного дизайна», поскольку при синтезе данного препарата были использованы современные знания третичной структуры NA как антигена и фермента [3, 6].
Препараты с антинейраминидазным действием «имитируют» структуру натуральных субстратов каталитического сайта NA (рис. 4), что «привлекает» вирус к большему взаимодействию с ними [5, 18]. К подобным соединениям относятся коричные и оксикоричные кислоты, галлаты и др.
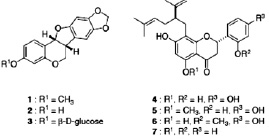
Рис. 4. Структура ингибиторов нейраминидазы [7, 9, 16]
На сегодняшний день практическая медицина обладает достаточно внушительным арсеналом противовирусных средств, способных подавлять репродукцию вируса на любой стадии процесса. Однако, несмотря на определенные успехи, достигнутые в вирусной химиотерапии, клиническая практика сталкивается с серьезной проблемой появления вариантов вируса, устойчивых к тем или иным препаратам.
Изучение растительных препаратов, обладающих антивирусными свойствами (алпизарин, эпиген, протефлазид, госсипол), показало, что за счет разных механизмов действия препаратов (противовирусное и иммуностимулирующее) появление вирусов, устойчивых к данным препаратам, не наблюдается. Большое разнообразие биологически активных соединений, находящихся в растениях, позволяет рассчитывать на возможность получения новых высокоактивных препаратов, обладающих способностью блокировать различные вирусы, в том числе, резистентные к существующим коммерческим химиопрепаратам. Подобные препараты, сочетающие в себе свойства иммуностимулирующих и противовирусных соединений, можно рекомендовать для лечения и профилактики инфекционных заболеваний, ассоциированных с иммунодефицитным состоянием, в том числе таких, как грипп, ВИЧ, гепатит С и др. [11, 17].
Рецензенты:
Саятов М.Х., д.б.н., академик НАН РК, профессор, главный научный сотрудник, РГП «Институт микробиологии и вирусологии» КН МОН РК, г. Алматы;
Жуматов К.Х., д.б.н., профессор, главный научный сотрудник, РГП «Институт микробиологии и вирусологии» КН МОН РК, г. Алматы.
Источник
Эффективность препаратов растительного происхождения в терапии тревожных расстройств
*Импакт фактор за 2018 г. по данным РИНЦ
Читайте в новом номере
Тревога, чувство внутреннего напряжения, раздражительность – жалобы, часто встречающиеся на приеме у врача [4]. В течение жизни примерно у 50% людей выявляются отдельные симптомы тревоги или синдромально очерченные тревожные расстройства [1,8]. Нередко субсиндромальные тревожные состояния скрываются за массивной вегетативной дисфункцией, формируя психовегетативный синдром, и при этом своевременно не диагностируются [3,8,9,24].
Тревога является обязательной составляющей интегративной реакции организма на стрессовое воздействие. Огромна роль дистресса (патологическая разновидность стресс–синдрома, который оказывает отрицательное влияние на организм, психическую деятельность и поведение человека, вплоть до полной их дезорганизации) в формировании психовегетативных нарушений. Вегетативные изменения, следующие за дистрессом, очень разнообразны и могут проявляться практически во всех органах и системах организма [5,8,9]. Повышенная стрессодоступность и избыточные тревожные реакции ведут к формированию психовегетативного синдрома, клинические проявления которого сопровождаются психическими и вегетативными симптомами [4,6,9], такими как усиленное или учащенное сердцебиение, потливость, ощущение нехватки воздуха, боль или дискомфорт в груди (в области сердца), тошнота (рвота) или другие желудочно–кишечные расстройства, ощущение головокружения, неустойчивости или приближающегося обморока, парестезиями, ознобом или приливами жара, учащенным мочеиспусканием, тремором [3].
При лечении тревожных расстройств широко применяют различные психотропные препараты. Для купирования остро возникшей тревоги наиболее часто используют анксиолитики – производные бензодиазепина [10,15,23], из которых чаще других – феназепам и диазепам, реже назначаются транквилизаторы и антидепрессанты [2]. Однако их использование затруднено из–за ряда побочных эффектов, возможного развития лекарственной зависимости и синдрома «отмены», затрудняющих повседневную активность пациента. В связи с этим все чаще поднимается вопрос об «альтернативной» терапии тревожных расстройств. В качестве такой «альтернативы» рассматриваются препараты растительного происхождения.
Исторически в лечении невротических расстройств, главным образом легкой степени тяжести, препаратом выбора являлись валериана и пустырник [10]. Существуют многочисленные сборы, содержащие экстракт валерианы. Добавление к экстракту валерианы других седативных средств растительного происхождения усиливает ее основные эффекты.
Давно известен вегетотропный эффект валерианы, т.е. равномерное влияние как на психические, так и на соматические (вегетативные) симптомы тревоги [6,12]. Нейробиологические механизмы эффектов валерианы включают агонистическое влияние на А1–аденозин–рецепторы [31], бензодиазепиновые рецепторы [29] и потенцирование ГАМК–ергической трансмиссии за счет облегчения выброса ГАМК и ингибиции обратного захвата ГАМК [29,30]. Множество клинических и экспериментальных исследований подтверждают, что основным механизмом действия валерианы является потенцирование ГАМК–ергической медиации, что дает основание предполагать ее нейропротективный эффект. Тестирование эффектов валерианы на гиппокампальной клеточной культуре мышей показало ее отчетливый протективный эффект. Нейропротективный эффект валерианы может рассматриваться как новая мишень для защиты мозга от стрессорных воздействий. Несмотря на то, что экстракт валерианы метаболизируется системой цитохрома Р450, он практически не влияет на метаболизм других препаратов. Спектр побочных эффектов валерианы весьма узок и практически ограничивается только аллергическими реакциями [17,18].
Клиницистам хорошо знаком препарат Персен®, который содержит экстракт валерианы (50 мг), экстракт мяты перечной (25 мг) и экстракт мелиссы (25 мг), что усиливает анксиолитический эффект валерианы и добавляет спазмолитическое действие [17,18]. Фармакологическая группа, к которой относится Персен® – седативное средство растительного происхождения [15]. Преимуществом лекарственного средства Персен® перед другими препаратами является его свойство не влиять на структуру сна и не вызывать дневной седации. Это позволяет широко использовать Персен® у лиц, ведущих активный образ жизни, в том числе выполняющих оперативную работу, управление транспортом [7]. Наряду с таблетированной формой имеется препарат в капсулах – Персен–Форте®, содержащий 125 мг экстракта валерианы, благодаря чему Персен–Форте® обеспечивает высокий анксиолитический эффект [6,17,18].
Персен–Форте® в лечении
психовегетативного синдрома
Значительная роль в развитии психовегетативных расстройств отдается снижению уровня ГАМК, являющейся одним из основных тормозных медиаторов головного мозга. Как известно, ГАМК метаболизируется в глутамат (при этом возможна как прямая, так и обратная реакции), далее глутамат под действием глутаматдегидрогеназы расщепляется до уровня a–кетоглутаровой кислоты. Для физиологических условий типична обратная реакция, то есть образование глутамата и далее ГАМК. Предполагается, что у пациентов с психовегетативными расстройствами может существовать особая форма глутаматдегидрогеназы, дающая в физиологических условиях прямую реакцию, что приводит к накоплению глутамата и снижению образования ГАМК. Дополнительную роль в формировании указанных нарушений может играть снижение чувствительности бензодиазепиновых рецепторов и изменение их способности к связыванию с соответствующими медиаторами [19].
Проведено двойное слепое рандомизированное плацебо–контролируемое исследование клинической эффективности препарата Персен–Форте®. Цель исследования – определение эффективности и переносимости средства Персен–Форте® при лечении психовегетативного синдрома с превалированием в клинической картине тревожных расстройств невротического ряда. Обследовано 93 пациента, средний возраст по группе составил 34,5 (16–62) года [4,5]. В ходе исследования пациенты были разделены на 2 группы: первая группа (n=47) – пациенты, получавшие Персен–Форте®, вторая группа (n=46) – больные, получавшие плацебо и группа контроля (n=25). Персен–Форте® назначали по 1 капсуле (125 мг) два раза в сутки. Курс лечения составил 28 дней. Оценка динамики состояния проводилась: в фоне, на 7–й день терапии и в конце лечения. Помимо клинического впечатления анкетными методами оценивались состояние вегетативной нервной системы, качество сна и качество жизни. Для оценки уровней тревожности использовали тест Спилбергера, депрессии – тест Бека, внимания – корректурную пробу Бурдона, черно–белые таблицы Шульте, стрессогенности – шкалу оценки жизненных событий Холмса–Рея.
В ходе проведенного исследования были получены положительная динамика субъективного самочувствия больных по ВАШ (4,5±1,4 б. – фон vs 3,2±1,5 б. – 28 день) и достоверное улучшение параметров тестирования: по тесту Спилбергера – снижение уровня реактивной (50,93±9,29 б. – фон vs 41,33±8,22 б. – 28 день) и личностной тревожности (52,6±7,86 б. – фон vs 45,9±7,2 б. – 28 день), по шкале Бека – снижение уровня депрессии (12,2±9,1 б. – фон vs 7,73±5,7 б. – 28 день), снижение вегетативных проявлений (34,8±12,3 б. – фон vs 28,2±10,6 б. – 28 день), нормализация сна (18,5±3,25 б. – фон vs 20,7±3,6 б. – 28 день), повышение качества жизни (37,8±19,4% – фон vs 28,7±13,3% – 28 день). Также при оценке концентрации внимания и работоспособности было показано, что Персен–Форте® не влияет на исходные показатели по данным параметров таблицы Шульте (35,6±3,4 с – фон vs 36,8±3,2 с – 28 день) и теста Бурдона (14,3±3,3 стр. – фон vs 13±2,7 стр. – 28 день). Таким образом, Персен–Форте® обладает доказанным анксиолитическим эффектом, оказывает отчетливое вегетотропное действие, не влияет на концентрацию внимания и не снижает работоспособность.
Клиническая эффективность препарата Персен– Форте® достоверно превышает эффект плацебо. Отсутствие «поведенческой токсичности» делает возможным назначение данного средства лицам пожилого возраста. Таким образом, Персен–Форте® является эффективным лекарственным средством «альтернативной» терапии транквилизаторами бензодиазепинового ряда и может быть рекомендован для лечения больных со стресс–индуцированными тревожными и психовегетативными синдромами.
Проведено другое открытое наблюдательное исследование в условиях повседневной клинической практики по оценке стресс–протективной эффективности и безопасности препарата Персен–Форте® у лиц, активно предъявляющих жалобы на повышенную нервную возбудимость и/или раздражительность [21,22]. В исследование вошли 50 амбулаторных пациентов (средний возраст по группе – 37,7±8,1 года (18–50 лет)), обратившихся к неврологу с жалобами на повышенную нервную возбудимость, раздражительность, бессонницу. Персен–Форте® назначался в дозе 2 капсулы 2 раза в сутки на протяжении трех недель. Динамика состояния оценивалась на основании общего самочувствия на момент визита к врачу по 10–балльной ВАШ, где 1 – абсолютное здоровье, 0 – предельно плохое состояние. Также оценивались уровень тревоги и депрессии по госпитальной шкале тревоги и депрессии (HADS), субъективные характеристики и степень нарушения сна. В ходе исследования были получены достоверные изменения показателей общего самочувствия по ВАШ (0,6±0,2 б. – до vs 0,9 ±1,0 б. – после), уровня тревоги (12,1±4,2 б. до vs 4,3±2,6 б. после) и депрессии (7,8±3,8 б. – до vs 4,9±2,7 б. – после) по шкале HADS.
Проведенное исследование показало, что за обыденными жалобами на раздражительность, нервную возбудимость, транзиторные нарушения сна, как правило, стоят синдромально очерченные тревожные нарушения или субсиндромальные нарушения. Улучшение общего самочувствия после курса терапии препаратом Персен–Форте® выросло в среднем на 30%. На фоне терапии данным средством изменение своего состояния как «значительное улучшение» отметили 46%, как «явное улучшение» – 54% наблюдаемых. На момент окончания терапии ни у одного из пациентов не было зарегистрировано побочных эффектов. Пациентами была дана высокая оценка эффективности («отлично» – 66%, «хорошо» – 34%) и переносимости («отлично» – 84%, «хорошо» – 16%) препарата Персен–Форте®. При развитии острой стрессовой ситуации 89% пациентов почувствовали улучшение состояния в течение часа после приема средства Персен–Форте®, 94% пациентов заявили о своем желании снова (при необходимости) прибегнуть к приему препарата. Таким образом, Персен–Форте® может назначаться как в курсовом лечении мягких и субсиндромальных тревожных расстройств, так для купирования острой стрессорной реакции.
Назначение препарата Персен®
врачом общей практики
Врачу в повседневной практике приходится сталкиваться с трудностями дифференциальной диагностики тревоги и депрессии, так как у этих патологических состояний много общих симптомов. Более того, длительное существование тревоги обусловливает развитие депрессии, которая в свою очередь усиливает симптомы тревоги, создавая порочный круг. Однако признаки депрессии возникают позднее, чем тревожные, и в 8 из 10 случаев проявления тревоги свидетельствуют о возможности развития большого депрессивного расстройства [24].
На базе кафедры неврологии ФУВ РНИМУ (2008 г.) проведено плацебо–контролируемое исследование противотревожной эффективности препарата Персен– Форте®. В исследование были включены 73 пациента (средний возраст 61,2±16,6 года), проходивших обследование и лечение в неврологическом стационаре по поводу хронической ишемии мозга (ХИМ) на разных стадиях заболевания [24]. Больные были рандомизированы в две группы: в первой (n=43) были пациенты, принимавшие Персен–Форте® по 1 капсуле дважды в сутки; во второй (n=30) – принимавшие плацебо. Курс лечения препаратом Персен–Форте® составил 4 нед. Пациенты обеих групп получали базисную терапию для лечения основного заболевания: анксиолитики, антидепрессанты, седативные средства. Динамика состояния оценивалась на основании клинико–психологического исследования (выявлялось субсиндромальное / мягкое тревожное расстройство) и с использованием шкал Гамильтона, Шихана, Цунга, общего клинического впечатления, теста запоминания 10 слов, пробы Бурдона, теста PASAT. В ходе исследования получена положительная динамика показателей: тревожности по шкале Гамильтона в группе, получавшей Персен–Форте® (13±5 б. – до vs 6±2 б. – после), по сравнению с группой плацебо (14±3 б. – до vs 12±4 б. – после), интенсивности вегетативных проявлений по шкале Шихана в группе, получавшей Персен–Форте® (37±9 б. – до vs 18±6 б. – после), по сравнению с группой плацебо (41±8 б. – до vs 32±4 б. – после).
Изменения в состоянии больных первой группы были отмечены через 2 нед. от начала терапии. Динамическая оценка когнитивных функций (тест запоминания 10 слов, проба Бурдона, тест PASAT) показала, что Персен–Форте® не вызывает торможения внимания и ослабления памяти. На фоне терапии также отмечены: положительное влияние на функциональные нарушения со стороны сердечно–сосудистой системы (тахикардия, кардиалгия, ощущение сердцебиения, колебания артериального давления), в 95,3% случаев улучшение качества сна (удлинение времени сна, уменьшение времени засыпания отмечалось у пациентов с неглубокими инсомническими расстройствами, вызванными стрессом изменения привычной обстановки). Шкала общего клинического впечатления показала, что более 4–х баллов по пункту «улучшение» и менее 3–х баллов по пункту «тяжесть заболевания» отметили 77% пациентов первой и 31% больных – второй группы. Проявлений «поведенческой токсичности» выявлено не было, признаков неблагоприятного лекарственного взаимодействия с препаратами базисной терапии не отмечалось. Таким образом, Персен–Форте® в дозировке 2 капсулы в сутки эффективен в лечении субсиндромальной тревоги и мягких проявлений симптомов тревожного расстройства.
На базе кафедры неврологии ФУВ РНИМУ (2009 г.) проведено другое плацебо–контролируемое исследование, цель которого – изучение клинической эффективности комбинированной терапии препаратами деприм и Персен–Форте® в коррекции тревожно–депрессивных симптомов и инсомнических расстройств у пациентов с ХИМ на разных стадиях заболевания [25]. В обследование были включены 49 пациентов (их средний возраст составил 63,2±11,6 года), у которых выявлено субсиндромальное или мягкое тревожно–депрессивное расстройство (ТДР) по данным шкал Гамильтона, Шихана, Цунга. Больные были рандомизированы в три группы: в первой (n=20) – получавшие деприм по 1 капсуле в сутки; во второй (n=19) – деприм по 1 капсуле в сутки + Персен–Форте® по 1 капсуле на ночь; в третьей (n=10) – плацебо. Пациенты каждой группы получали базисную терапию основного заболевания: анксиолитики, антидепрессанты, седативные средства. Курс терапии составил 3 нед.
В ходе исследования выявлено существенное (по сравнению с группой плацебо) снижение средних значений показателя тревожности и депрессии по госпитальной шкале оценки тревоги и депрессии, шкале Гамильтона в обеих группах больных, получавших фитотерапию. Изменения в состоянии больных второй группы были отмечены уже в первые дни лечения. К 10–му дню терапии положительная динамика симптомов тревоги и панических атак с акцентом на соматизированные и вегетативные компоненты (шкала Шихана) в виде снижения интенсивности вегетативных проявлений отмечена во второй группе (399 б. – до vs 266 б. – после) по сравнению с группой плацебо (426 б. – до vs 364 б. – после) и первой группой (418 б. – до vs 324 б. – после). К 5–му дню терапии улучшение качества сна (удлинение времени сна, сокращение периода засыпания) также было отмечено во второй группе.
По данным Шкалы общего клинического впечатления получено: к 10–му дню лечения улучшение состояния регистрировалось в первой группе в 20% случаев, во второй – в 55%. По завершении лечения выявлена сопоставимая эффективность: более 4 баллов по пункту «улучшение» и менее 3 баллов по пункту «тяжесть заболевания» отметили 69% пациентов первой и 77% – второй группы. К 3–й нед. лечения получено значимое снижение выраженности тревожно–депрессивных симптомов. Таким образом, комбинация фитопрепаратов деприм и Персен–Форте®, при которой уменьшение тревожных и инсомнических проявлений обнаруживается уже в первые дни терапии, а снижение выраженности тревожно–депрессивных симптомов – к 3–й неделе, может быть рекомендована в качестве старт–терапии «мягких» симптомов депрессии и тревоги разным группам больных в общемедицинской практике, в том числе лицам пожилого возраста.
Терапия субпороговых расстройств тревожного спектра у подростков
Наличие у взрослых пациентов отдельных тревожных симптомов, как правило, не рассматривается ими или их близкими как существенное патологическое состояние, поэтому мотивация обращения за медицинской помощью часто отсутствует. Тревожные расстройства у подростков, в противоположность взрослым, в большей степени приобретают характер значимой медико–социальной проблемы, поскольку нарушают семейные и школьные взаимодействия, негативно сказываются на успеваемости, могут приводить к дезадаптации детей среди сверстников. В отсутствии лечения тревожные симптомы могут подвергаться трансформации, становиться более стойкими – перманентными и достигать степени очерченных тревожных синдромов [13]. Благодаря высокому профилю безопасности Персен® может быть использован у детей [20].
Число детей с пограничными нервно–психическими расстройствами существенно увеличилось за последнее десятилетие: среди дошкольников этими расстройствами страдают до 20% детей. К концу первого класса их число возрастает до 40%, к концу школьного обучения – от 40 до 60%. К подростковому периоду возрастает число лиц с церебрально–сосудистой недостаточностью вследствие дезрегуляторного неблагополучия центров, участвующих в регуляции сосудистой и вегетативной деятельности. Это приводит к снижению адаптации организма к экзогенным и эндогенным воздействиям, включая физиологический возрастной дисбаланс [15].
На базе Детской клинической больницы № 38 ФМБА (Москва) проведено исследование по оценке влияния препарата Персен® на субпороговые расстройства тревожного спектра у подростков [13,14]. В исследования включены 48 подростков, обратившихся за консультативной амбулаторной неврологической помощью, средний возраст по группе составил 14,9±0,8 (14–16) лет. Персен® назначался в качестве монотерапии по 2 таблетки до 3–4 раз в сутки или Персен–Форте® по 1 капсуле 2–3 раза в сутки. Длительность курса лечения – 2 мес. Динамика состояния оценивалась в фоне и через 2 мес. после начала терапии. Психологическое обследование включало: клинико–психологическое обследование, тест Спилбергера (личностная и реактивная тревожность), опросник САН (самочувствие, активность, настроение), цветовой тест Люшера (эмоциональное состояние), корректурная проба и таблицы Шульте (нарушение внимания), а также ВАШ для оценки выраженности болевых проявлений. Для исключения соматических заболеваний использовали инструментальные (электрокардиография, эхокардиография, сонография органов брюшной полости, транскраниальная допплерография, эзофагогастродуоденоскопия) и лабораторные (гемограмма, урограмма, биохимические параметры сыворотки крови: общий белок, билирубин, печеночные трансаминазы, глюкоза, мочевина, креатинин, электролиты) методы исследования, для исключения неврологических расстройств пароксизмального характера проводили электроэнцефалографию.
На фоне терапии препаратом Персен® получена положительная динамика показателей: по тесту Спилбергера – снижение уровня реактивной (29,19±5,63 б. – до vs 22,69±4,6 б. – после) и личностной тревожности (28,83±5,38 б. – до vs 21,98±3,77 б. – после), по ВАШ – снижение уровня болевого синдрома (6,6±1,1 б. – до vs 3,9±1,4 б. – после), по опроснику САН – улучшение актуального самочувствия (самочувствие: 3,31 б. до vs после 5,44 б.; активность: 4,11 б. до vs после 4,6 б.; настроение: 3,88 б. до vs 4,98 б.), по цветовому тесту Люшера – выраженная обратная динамика эмоционального состояния в виде гармонизации цветового ряда. Динамика показателей параметров внимания свидетельствует об улучшении продуктивности и точности произвольного внимания, расширении его объема, снижении среднего времени, затраченного на выполнение заданий четырех таблиц Шульте, увеличении количества просмотренных букв в тесте. Корректурная проба демонстрирует уменьшение процента допущенных ошибок. Таким образом, в проведенном исследовании показана высокая эффективность препарата Персен® в отношении влияния на субпороговые расстройства тревожного спектра.
Назначение препарата Персен®
при психосоматических расстройствах у детей
Медикаментозная коррекция эмоционально–поведенческих и/или двигательных нарушений с использованием седативных средств растительного происхождения представляется немаловажным компонентом комплексного лечения нарушений психоэмоциональной сферы у детей различного возраста. Применение фитотерапевтических средств в ряде случаев позволяет избежать нежелательных «антитерапевтических» действий таких аллопатических средств, как, например, транквилизаторы/анксиолитики [15], использование которых в детском возрасте может индуцировать излишнюю седацию, снижение когнитивных функций и патологическое угнетение физической и эмоциональной активности [26].
На базе Института аллергологии и клинической иммунологии (Москва) проведено исследование по оценке терапевтического спектра действия препарата Персен® в детском возрасте при психосоматических расстройствах, связанных с бронхиальной астмой (БА) и врожденными пороками сердца (ВПС) [16]. В исследование были включены дети (n=30) и подростки (n=30) с атопической БА, проходившие курс амбулаторного лечения в Институте аллергологии и клинической иммунологии, и дети (n=30) и подростки (n=30) с ВПС, находившиеся на лечении в Институте кардиохирургии им. В.И. Бураковского НЦССХ им. А.Н. Бакулева РАМН (Москва). Длительность курса терапии препаратом Персен® составила 56 дней. Все дети с патологией сердца в раннем детском возрасте перенесли кардиохирургическое вмешательство по поводу цианотического ВПС с радикальной коррекцией дефекта.
Проведенное клинико–психологическое обследование выявило у всех детей наличие, на фоне стойкой астении, аффективных нарушений в виде тревоги невротического уровня с различной степенью выраженности тревожного аффекта. Для оценки динамики состояния использовали: проективный рисуночный тест (по Маховеру), шкалу общего клинического впечатления (дети), шкалу тревоги Гамильтона (подростки). Динамика состояния проводилась на 7–й, 14–й, 28–й и 56–й дни наблюдения. На фоне терапии препаратом Персен®, независимо от клинико–нозологической и возрастно–психологических характеристик, показатели проективных рисуночных тестов «Нарисуй человека» и «Образ себя» с использованием цветовых обозначений в группах БА и ВПС существенно не изменились. Это свидетельствует о том, что спектр терапевтической активности препарата Персен® существенно не влияет на эмоционально–личностный регистр «внутренней картины болезни» малолетнего пациента с психосоматическими расстройствами.
Динамика клинического состояния у детей–пациентов носила отставленный характер и проявлялась в виде положительных сдвигов по всем показателям к 56–му дню наблюдения, а по показателям «дифференцированные страхи, связанные с природными явлениями», «расстройства сна», «двигательное беспокойство», «вегетативные дисфункции» получено значительное улучшение к 28–му дню. Уменьшение недифференцированной тревожности, внутренного беспокойства и напряженности (на 7–14 дней) существенно не меняет оценку «общего самочувствия» во внутренней картине болезни малолетних пациентов. Положительный симптоматический спектр терапевтической активности препарата Персен® у детей с психосоматическими расстройствами полностью проявляется к концу 4–й нед. применения препарата без риска формирования психической зависимости. В конце курса терапии препаратом Персен® по шкале Общего клинического впечатления оценку «значительное улучшение» дали 56,7% пациентов в группе БА и 36,7% – в группе ВПС, «небольшое улучшение» – 40% наблюдавшихся в группе БА и 56,7% – в группе ВПС, «нет изменений» – 3,3% в группе БА и 6,7% в группе ВПС, «ухудшение» – 0% больных в обеих группах. Таким образом, можно рекомендовать безопасное назначение препарата Персен® детям с психосоматическими расстройствами.
Коррекция психоэмоциональных
расстройств во время беременности
Практически все беременные подвержены резким эмоциональным перепадам, так как ожидание ребенка сопряжено с изменениями – как физическими, так и эмоциональными. Состояние психоэмоционального напряжения с наличием тревожности различного уровня наблюдается у 40% женщин с нормально протекающей беременностью. Наиболее часто изменения психоэмоционального фона во время беременности приводят к развитию депрессивных и тревожных расстройств, и до конца патогенез этих изменений неясен [27]. Для предотвращения возможного развития, а также для лечения психоэмоциональных расстройств у беременных целесообразно применение седативных средств, действие которых смягчает повреждающее воздействие психогенных факторов. Среди фитопрепаратов, используемых клиницистами для лечения психоэмоциональных расстройств во время беременности, широкое распространение получил Персен®.
Растительные препараты при лечении соматоформных расстройств
Кроме проявлений вегетативной дисфункции, общим признаком всех невротических соматоформных расстройств является наличие у больных симптомов тревоги (тревожно–фобические и другие тревожные расстройства). Многие из этих тревожных расстройств (агорафобии, социофобии, специфические фобии) и сопровождающие их вегетативные проявления оказываются ситуационно обусловлены, в связи с чем пациенты стараются избегать соответствующих ситуаций. Нередко симптомы тревоги сочетаются с проявлениями депрессии (смешанные тревожно–депрессивные расстройства, маскированные депрессии) [11]. По результатам клинических испытаний данного препарата он был рекомендован в следующих ситуациях: при невротических расстройствах, сопровождающихся тревогой, астенией, вегетативными дисфункциями, нарушением сна; при наличии противопоказаний к назначению бензодиазепинов (молодой возраст, нарушения функций печени и почек, апноэ и др.); при отмене бензодиазепинов; при психовегетативных и посттравматических стрессовых расстройствах [10].
У больных с соматоформными расстройствами Персен® снижает уровень личностной и реактивной тревоги, уменьшает частоту и выраженность вегетативных проявлений, нормализует сон [4]. В проведенных исследованиях Персен® достоверно превосходил плацебо по влиянию на тревожные расстройства и вегетативные дисфункции. При этом он практически не вызывал побочных эффектов, в т.ч. сонливости в дневное время, не оказывал негативного влияния на концентрацию внимания и работоспособность пациентов [28]. Персен® хорошо сочетается с любыми психотропными препаратами, включая антидепрессанты. Клинически значимых взаимодействий препарата Персен с другими лекарственными средствами не выявлено.
Достоинством препарата Персен® также является возможность его применения как в качестве быстродействующего симптоматического средства для купирования симптомов тревожности и волнения, так и для длительного лечения стрессовых, тревожных и фобических расстройств. Персен® рассматривается в качестве препарата выбора для коррекции психовегетативного синдрома, сопровождающегося тревогой, в т.ч. у пациентов наиболее уязвимых групп (подростки и пожилые лица). При хронической тревоге он может быть более безопасной альтернативой бензодиазепинам, при необходимости – в сочетании с антидепрессантами. Его также можно назначать здоровым людям в качестве профилактического средства.
Заключение
Рядом проведенных исследований показана высокая эффективность и безопасность растительного препарата Персен® в лечении больных со стресс–индуцированными тревожными и психовегетативными синдромами, при лечении субсиндромальной тревоги и «мягких» проявлений симптомов тревожного расстройства, в качестве старт–терапии «мягких» симптомов депрессии и тревоги у разных групп больных в общемедицинской практике, в том числе у пожилых лиц. Также показана эффективность препарата Персен® в качестве монотерапии у подростков с субпороговыми расстройствами тревожного спектра, у детей с психосоматическими расстройствами, в коррекции психоэмоциональных расстройств во время беременности. При лечении инсомнии препаратом Персен® характерным является отсутствие дневной сонливости и влияния на концентрацию внимания, что способствует улучшению качества жизни пациентов и возвращению их к адекватной и полноценной жизни.
Источник