- Роспотребнадзор (стенд)
- Роспотребнадзор (стенд)
- Чем «контрафакт» отличается от «фальсификата» — Надзор по гигиене питания
- Чем «контрафакт» отличается от «фальсификата»
- Чем «контрафакт» отличается от «фальсификата»
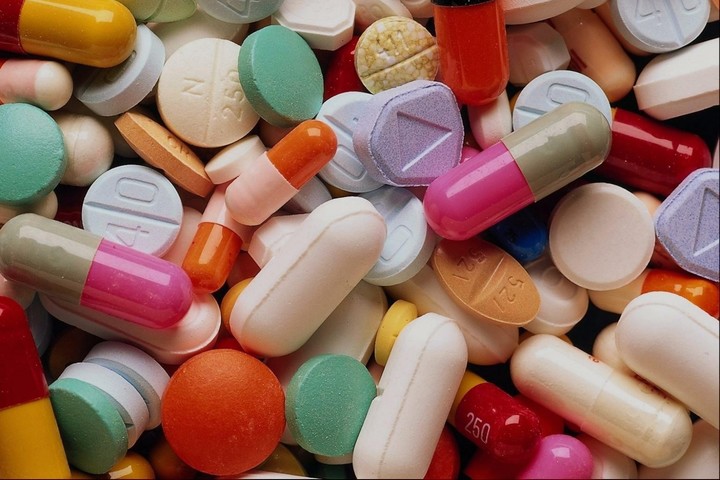
- Что такое БАДы и насколько они безопасны? Разбираемся, чем они отличаются от лекарств
- «БАД. НЕ ЯВЛЯЕТСЯ ЛЕКАРСТВЕННЫМ СРЕДСТВОМ» — эта надпись на многих упаковках в аптеке звучит довольно угрожающе. Зачем тогда это в аптеке продают, если это не лекарство? И есть ли разница? И почему какие-то лекарства нельзя купить без рецепта врача? СПИД.ЦЕНТР выяснил, чем отличаются биологически активные добавки от лекарств.
- по теме
- Лечение
- Суперсила бактерий: антибиотики наносят ответный удар
Роспотребнадзор (стенд)
Роспотребнадзор (стенд)
Чем «контрафакт» отличается от «фальсификата» — Надзор по гигиене питания
Чем «контрафакт» отличается от «фальсификата»
Чем «контрафакт» отличается от «фальсификата»
В настоящее время проблема незаконного оборота промышленной продукции актуальна как никогда. Это связано с тем, что незаконный ввоз, производство и оборот контрафактной и фальсифицированной продукции не только способствует недобросовестной конкуренции на потребительском рынке, но и наносит достаточно серьезный ущерб экономике нашей страны, вводит потребителей в заблуждение относительно потребительских свойств и происхождения продукции. Не стоит забывать о том, что контрафактная и фальсифицированная продукция может причинить вред жизни, здоровью и имуществу потребителя.
Понятие «контрафактной» продукции четко определяется в п.1 ст.1515 Гражданского кодекса Российской Федерации (ГК РФ) – «товары, этикетки, упаковки товаров, на которых незаконно размещены товарный знак или сходное с ним до степени смешения обозначение, являются контрафактными». Также в п. 3 ст.1519 ГК РФ указано следующее: «товары, этикетки, упаковки товаров, на которых незаконно использованы наименования мест происхождения товаров или сходные с ними до степени смешения обозначения, являются контрафактными».
Из этого следует, что в случаях, когда изготовление, распространение или иное использование, а также импорт, перевозка или хранение материальных носителей, в которых выражены результат интеллектуальной деятельности или средство индивидуализации, приводят к нарушению исключительного права на такой результат или на такое средство, такие материальные носители считаются контрафактными (п.4 ст.1252 ГК РФ). Кроме того, контрафактной признается продукция без маркировки, предусмотренной законом. При этом признание товара контрафактным, не всегда свидетельствует о его качестве.
Понятие «фальсификации» приводится в Федеральном законе Российской Федерации от 2 января 2000 г. №29-ФЗ «О качестве и безопасности пищевых продуктов» — «фальсифицированные пищевые продукты (в том числе биологически активные добавки), материалы и изделия — пищевые продукты (в том числе биологически активные добавки), материалы и изделия, умышленно измененные (поддельные) и (или) имеющие скрытые свойства и качество, информация о которых является заведомо неполной или недостоверной».
Исходя из анализа понятий «контрафактная» и «фальсифицированная» продукция, необходимо отметить, что контрафактная продукция всегда одновременно является и фальсифицированной, а фальсифицированная продукция может не являться контрафактной. Для признания же продукции фальсифицированной необходимо установить факт нарушения процесса ее изготовления, в том числе использование иных (не указанных в составе) компонентов.
Таким образом, фальсификат не всегда является контрафактом. Во многих случаях изготовитель товара, с целью снижения расходов по изготовлению, просто использует более дешевые компоненты. Результатом таких действий является изменение свойств и качества готовой продукции. Контрафакт и фальсификат необходимо отличать друг от друга. Контрафакт предполагает, что продукция копируется либо подделывается, при этом за основу чаще всего берется известный бренд. Фальсифицированная же продукция предполагает нарушение технологии производства и/или не использование акцизов, когда это обязательно. Целью фальсификации, как правило, является обман потребителя, заключающийся в неверном указании или сокрытии свойств товара.
Проблематика незаконного оборота промышленной продукции более всего затрагивает отрасли пищевой промышленности.
Незаконный оборот продукции может осуществляться следующими способами:
– состав и свойства продукта не соответствуют заявленным характеристикам;
– товары, выдающие себя под известные бренды;
– производство товаров под собственным товарным знаком продукции, очень схожим с известным брендом в названии и оформлении;
– несанкционированное тиражирование товара;
– импорт оригинального продукта без согласия правообладателя.
За нарушения, выявленные в сфере контрафактной продукции, предусмотрена ответственность следующими нормативно-правовыми актами:
1. Уголовным Кодексом РФ:
Статья 146 Нарушение авторских и смежных прав;
Статья 147 Нарушение изобретательских и патентных прав;
Статья 180 Незаконное использование средств индивидуализации товаров (работ, услуг).
2. Кодексом РФ об административных правонарушениях:
Статья 7.12 Нарушение авторских и смежных прав, изобретательских и патентных прав;
Статья 14.10 Незаконное использование средств индивидуализации товаров (работ, услуг).
Если у потребителя возникли подозрения, что перед вами продукция сомнительного происхождения, необходимо обратиться с заявлением в органы МВД, территориальные управления Роспотребнадзора и Россельхознадзора, органы ФТС, которые наделены полномочиями в этой сфере в пределах компетенции.
В случае приобретения товара, который оказался контрафактным (фальсифицированным), а при его покупке не была предоставлена необходимая, полная и достоверная информация о товаре, то в соответствии со ст.12 Закона Российской Федерации от 7 февраля 1992 г. № 2300-1 «О защите прав потребителей» (Закон о защите прав потребителей), вы имеете право требовать от продавца возмещения убытков, в разумный срок отказаться от исполнения договора и потребовать возврата уплаченной за товар суммы и возмещения других убытков. При причинении вреда жизни, здоровью и имуществу потребителя вследствие непредставления ему полной и достоверной информации о товаре потребитель вправе потребовать возмещения такого вреда в порядке, предусмотренном ст.14 Закона о защите прав потребителей, в том числе полного возмещения убытков, причиненных природным объектам, находящимся в собственности (владении) потребителя. В случае неудовлетворения продавцом соответствующего требования гражданина добровольно, спор должен разрешаться исключительно в рамках гражданского судопроизводства. В соответствии с частями 2, 7 и 10 ст.29 Гражданского процессуального кодекса Российской Федерации (ГПК РФ) и с п.2 ст.17 Закона о защите прав потребителей, исковое заявление в суд потребитель вправе предъявить по своему месту жительства или месту пребывания либо по месту нахождения организации либо по месту заключения или исполнения договора. Если иск к организации вытекает из деятельности её филиала или представительства, он также может быть предъявлен в суд по месту нахождения её филиала или представительства.
При обращении с иском в суд потребитель освобождается от уплаты государственной пошлины по делам, связанным с нарушением их прав (ст.11 ГК РФ, п.3 ст.17 Закона о защите прав потребителей).
Наряду с компенсацией имущественного вреда, потребитель, на основании ст.151 ГК РФ и ст.15 Закона о защите прав потребителей, вправе потребовать также возмещения морального вреда, причиненного продавцом вследствие нарушения им прав потребителя, предусмотренных законами и правовыми актами Российской Федерации, регулирующими отношения в области защиты прав потребителей.
Размер компенсации морального вреда определяется судом и не зависит от размера возмещения имущественного вреда.
Источник
Что такое БАДы и насколько они безопасны? Разбираемся, чем они отличаются от лекарств
Андрей Смирнов СПИД.ЦЕНТР
«БАД. НЕ ЯВЛЯЕТСЯ ЛЕКАРСТВЕННЫМ СРЕДСТВОМ» — эта надпись на многих упаковках в аптеке звучит довольно угрожающе. Зачем тогда это в аптеке продают, если это не лекарство? И есть ли разница? И почему какие-то лекарства нельзя купить без рецепта врача? СПИД.ЦЕНТР выяснил, чем отличаются биологически активные добавки от лекарств.
Разница действительно есть: она в регистрационном статусе и доказательной базе, но обо всем по порядку.
Быть или не быть препарату лекарством — в каждой стране решает свой государственный регулирующий орган. У нас это Минздрав, в США — FDA (Food and Drug Administration), в Европе — EMA (European Medicines Agency) и так далее. Чтобы стать лекарством, каждый кандидат должен пройти особую процедуру госрегистрации. Она долгая и сложная, основная ее задача — подтвердить две ключевые вещи:
- безопасность препарата;
- эффективность препарата.
Если сейчас вы подумали про клинические исследования — все верно, их результаты имеют важнейшее значение для регистрации препарата как лекарства. Исследования проводит производитель препарата в специальных лицензированных независимых клинических центрах. Каждое исследование до его начала должно получить одобрение Минздрава и затем тщательно контролируется на всех этапах, что исключает искажение результатов. Если в ходе исследований удалось доказать, что потенциальный препарат эффективен и безопасен, он становится лекарством.
А «слабые и некрасивые» становятся БАДами?
Не совсем. Если вещество обладает достаточно выраженным эффектом и потенциально может нанести вред человеку при неправильном применении, БАДом оно не станет. Такие вещества могут иметь статус только лекарственного средства или вообще не получат разрешения на применение, если у них плохие результаты клинических исследований.
Для БАДов (биологически активных добавок к пище) существует своя процедура государственной регистрации, но занимается этим уже Роспотребнадзор. Исследования тоже проводят, но доказывают только безопасность препарата.
по теме
Лечение
Суперсила бактерий: антибиотики наносят ответный удар
В этом принципиальное отличие БАДов от лекарств: если препарат зарегистрирован как лекарство, это значит, что его действие было подтверждено в ходе независимых испытаний и гарантировано регулирующим органом. Если речь идет о БАДе, то доказана и гарантирована только его безопасность. Это не значит, что никакого положительного эффекта не будет, его просто никто не проверял.
Конечно, производитель сам может организовать какие-то исследования, но их трудно будет назвать независимыми, а результат — гарантированным. Поэтому БАДы в этом смысле куда ближе к еде, чем к лекарствам, а с точки зрения законодательства едой и являются. В том числе поэтому их можно продавать не только в аптеках, но и в продуктовых супермаркетах. Контроль качества БАДов также значительно упрощен по сравнению с лекарствами, поэтому риск купить некачественную продукцию в случае БАДов выше.
Принимая любые БАДы, нужно четко понимать, что вреда от них с большой вероятностью не будет, но и лечебного эффекта никто не гарантирует: БАДами вообще не лечат болезни, это функциональные добавки к пище, которые могут улучшать состояние организма в некоторых случаях или применяться для профилактики. И, конечно, ни в коем случае нельзя пытаться лечить БАДами какие-либо серьезные заболевания. БАД, например, от рака может предлагать только мошенник, каким бы дорогим ни был рекламируемый препарат. Совместное применение лекарств и БАДов тоже не всегда оправдано: БАД может ухудшать всасывание лекарства или ускорять его выведение из организма, что будет снижать лечебный эффект. Поэтому при назначении любых лекарств обязательно сообщите врачу, если вы принимаете какие-то БАДы.
Отечественная регистрация
Однако есть еще один путь регистрации препаратов. Дело в том, что некоторые средства (например, витамины, пробиотики, сорбенты и тому подобные) можно регистрировать и как лекарство, и как БАД — они подходят под оба критерия, и выбор остается за производителем. Но регистрация БАДа — гораздо более простой и дешевый путь, чем регистрация лекарства. Поэтому нередко производитель сначала регистрирует и несколько лет продает такой препарат как БАД, а затем, накопив опыт применения и деньги на клинические исследования, перерегистрирует его уже как лекарство.
К сожалению, к некоторым лекарствам тоже есть вопросы по части доказательства эффективности, и речь сейчас даже не о гомеопатии. Дело в том, что российский Минздрав при оценке результатов клинических исследований использует критерии, далеко не всегда строго соответствующие принципам доказательной медицины. Поэтому у нас на рынке есть множество лекарств (Арбидол, Актовегин, Мексидол и другие), которые никогда бы не получили такого статуса в США или Европе. Это не значит, что такие лекарства «плохие» или неэффективные. Это значит, что их исследовали методами, не соответствующими критериям доказательной медицины. Применять ли такие препараты в лечении — личный выбор каждого. А проверить наличие у лекарства одобрения FDA или EMA можно на сайтах: https://www.drugs.com, или https://www.ema.europa.eu/en, или https://www.accessdata.fda.gov (поиск лучше проводить по международному непатентованному наименованию (МНН)).
В 2010 году российский Минздрав изменил правила регистрации лекарств, введя довольно неоднозначное требование об обязательном проведении клинических исследований препаратов на территории России. До этого изменения для регистрации лекарства достаточно было предоставить протоколы клинических исследований, проведенных в других странах. Мотивов введения таких изменений было несколько.
- Минздрав не мог контролировать качество исследований, проведенных в других странах.
- Некоторые лекарства по-разному действуют на представителей разных рас, что требует доказательства безопасности и эффективности препарата именно на нашей популяции.
Оба аргумента выглядят довольно слабо, потому что часть регуляторов (те же FDA и EMA) используют более жесткие критерии при оценке лекарств, поэтому сомневаться в качестве таких исследований — это дуть на воду. Что касается различий в действии лекарственных средств на людей разных рас, такие случаи встречаются нечасто и население нашей страны по этим параметрам вполне соответствует среднему европеоиду. Безусловно, огромным плюсом этой инициативы стало то, что зарубежные производители начали чаще включать Россию в мультицентровые клинические исследования, одновременно проводящиеся в нескольких странах. Что способствовало развитию всей отрасли клинических исследований в нашей стране.
Обратная сторона медали — снижение доступности некоторых новых лекарств в нашей стране. Проблема в том, что клинические исследования и вся процедура регистрации лекарств оплачиваются производителем и стоят довольно дорого. Поэтому если потенциальный рынок для нового препарата в России небольшой, производителю бессмысленно тратить деньги на исследования в России — это не окупится. А без регистрации продавать препарат нельзя. Поэтому нередко новейшие лекарства оказываются на нашем рынке с задержкой в несколько лет.
А рецепт у вас есть?
Лекарства также различаются по регистрационному статусу, образуя две большие группы:
- препараты безрецептурного отпуска (OTC от английского over-the-counter);
- препараты, отпускаемые по рецепту (Rx от латинского recipe).
Разница между этими группами понятна из названия. И здесь все дело снова в безопасности. Безрецептурный статус могут получить только давно присутствующие на рынке и хорошо изученные лекарства, не имеющие серьезных побочных эффектов при применении, не накапливающиеся в организме и с большим терапевтическим индексом.
Терапевтический индекс — это отношение средней дозы препарата, используемой для лечения заболевания, к средней дозе, в которой он проявляет токсическое действие. Чем больше значение терапевтического индекса, тем сильнее нужно превысить рекомендованную дозу, чтобы отравиться лекарством.
Источник