- Достижения и проблемы лечения гломерулонефрита
- Гломерулонефрит хронический — симптомы и лечение
- Определение болезни. Причины заболевания
- Симптомы хронического гломерулонефрита
- Патогенез хронического гломерулонефрита
- Классификация и стадии развития хронического гломерулонефрита
- Осложнения хронического гломерулонефрита
- Диагностика хронического гломерулонефрита
- Лечение хронического гломерулонефрита
- Прогноз. Профилактика
Достижения и проблемы лечения гломерулонефрита
Последняя четверть прошедшего века принесла с собой ряд важных достижений в лечении прогрессирующих почечных заболеваний, в том числе гломерулонефрита, остающегося одной из главных причин хронической почечной недостаточности (ХПН). Это касается
Последняя четверть прошедшего века принесла с собой ряд важных достижений в лечении прогрессирующих почечных заболеваний, в том числе гломерулонефрита, остающегося одной из главных причин хронической почечной недостаточности (ХПН). Это касается методов воздействия на начальные иммунно-воспалительные механизмы повреждения почечной ткани и еще в большей степени — на механизмы дальнейшего прогрессирования (развития склероза), так называемые неиммунные, часто уже не связанные с начальными путями повреждения. В связи с этим было создано новое направление в нефрологии, получившее название ренопротективной терапии.
Особенность этого периода — внедрение новых требований к качеству результатов исследований, касающихся разработки и оценки новых направлений и методов лечения (это характерно и для других областей медицины — кардиологии, гепатологии, онкологии, гематологии и т. д.), создание так называемой доказательной медицины (evidence-based medicine) — медицины, основанной на доказательствах. Суть этого подхода — организация исследований в соответствии с принципами клинической эпидемиологии. В ходе таких исследований, проводимых с использованием методов математической статистики, планируются и осуществляются клинические и экспериментальные работы, в первую очередь — контролируемые клинические исследования, посвященные роли этиологических и патогенетических факторов или эффективности лекарственной терапии.
Этот подход позволил отобрать и обобщить наиболее убедительные данные, касающиеся иммунодепрессивной и «неиммунной» (ренопротективной) терапии различных клинико-морфологических вариантов гломерулонефрита, а также дать научно обоснованные рекомендации.
Сегодня уже частично выявлены клинические и морфологические признаки, определяющие неблагоприятный прогноз, среди них быстрое развитие ХПН или тяжелые осложнения основных проявлений гломерулонефрита — нефротический синдром и артериальная гипертензия. Это позволило определить, каким пациентам в первую очередь следует проводить иммунодепрессивную терапию активными (агрессивными) методами.
Хотя арсенал иммунодепрессивных препаратов, применяемых для лечения гломерулонефрита, с начала 70-х годов практически не изменился (это по-прежнему глюкокортикоиды и две группы цитостатических препаратов: алкилирующие соединения — циклофосфамид и хлорбутин — и антиметаболиты — азатиоприн), появились новые методы и схемы их применения — так называемая ударная или пульс-терапия (pulse-therapy) — периодическое внутривенное введение сверхвысоких доз глюкокортикоидов или циклофосфамида. Одно из преимуществ этих методов — снижение частоты тяжелых осложнений, характерных для длительной пероральной терапии этими препаратами (гиперкортицизм, инфекции, токсическое повреждение гонад и т. д.).
Новые возможности лечения резистентных к иммунодепрессантам или стероидозависимых форм гломерулонефрита появились благодаря созданию циклоспорина — первого препарата из нового поколения так называемых селективных иммунодепрессантов, действующих в отличие от традиционных неселективных только на строго ограниченные звенья (точки) и молекулярные механизмы в сложных многоэтапных процессах клеточной активации, формирования и реализации иммунного ответа и воспаления. Основная область применения циклоспорина — лечение трех морфологических вариантов гломерулонефрита — «минимальных изменений» (липоидный нефроз), фокально-сегментарного гломерулосклероза и мембранозной нефропатии.
Минимальные изменения. Это заболевание исключительно редко приводит к развитию ХПН, тем не менее пациенты с таким диагнозом подвержены высокому риску тяжелых осложнений нефротического синдрома, которые могут стать причиной смерти. Это — гипергидратация (с анасаркой, водянкой полостей, отеком мозга и легких), тромбозы, белковая дистрофия, инфекции
(в том числе пневмококковый перитонит), от которых больные в прошлом нередко погибали, и, наконец, особое осложнение тяжелого нефротического синдрома — так называемый нефротический (или кининовый) криз у больных с выраженной гипоальбуминемией (с альбумином сыворотки менее 1,9 — 1,5 г%). Нефротический криз заканчивается быстронарастающей гиповолемией, приводящей к коллапсу (часто летальному) и развитию острой почечной недостаточности. Последняя также может быть следствием отека интерстиция почек, нередкого при любом тяжелом нефротическом (отечном) синдроме. Именно тяжестью и опасностью этих осложнений и обусловлена необходимость быстрой ликвидации (достижения ремиссии) нефротического синдрома.
Одна из главных проблем лечения «минимальных изменений» — единственной формы нефрита, высокочувствительной к глюкокортикоидам и столь же склонной к рецидивированию и стероидной зависимости (до 2/3 случаев у детей) — достижение длительной стойкой ремиссии нефротического синдрома. Стероидная зависимость (развитие рецидива при всякой попытке отмены, а иногда даже снижения дозы глюкокортикоидов) ведет к тяжелым проявлениям стероидной токсичности: у взрослых — к ожирению, остеопорозу, тромбозам, диабету, инфекциям, стероидной гипертонии, а у детей помимо того — к инфантилизму, задержке роста и полового созревания.
У детей «минимальные изменения» представляют собой самый распространенный вариант гломерулонефрита (до 80 — 85% случаев), что явилось основанием для проведения ряда крупных контролируемых клинических испытаний, в ходе которых были получены данные, позволяющие сформулировать четкие лечебные рекомендации. Накопленный опыт и клинические испытания позволили предложить, что существует несколько путей достижения стойкой ремиссии у этих больных. При частом рецидивировании снизить частоту обострений позволяет лечение алкилирующими препаратами в течение 8 недель. При стероидной зависимости стойкая ремиссия может быть получена после 8 — 12 недель лечения циклофосфамидом. При истинной стероидной резистентности вызвать ремиссию и восстановить чувствительность к стероидам позволяет терапия циклоспорином.
Фокально-сегментарный гломеруло-склероз (ФСГС). Разработке методов лечения этой формы нефрита в последнее 10-летие уделялось особое внимание, что позволило несколько изменить традиционное представление о неизбежно плохом прогнозе у этих больных.
ФСГС встречается не так уж редко — 7 — 20% случаев, в половине из них проявляется нефротическим синдромом (в том числе в сочетании с артериальной гипертензией и гематурией), который при отсутствии лечения у 2/3 больных приводит к развитию ХПН. Такой же исход ожидает больных, не ответивших на лечение. Отличительная особенность ФСГС — высокая частота (до 50%) рецидивов болезни в пересаженной, донорской почке, что еще раз подчеркивает необходимость достижения ремиссии уже в самом начале заболевания.
В прошлом (в 70-е годы) в результате первых попыток оценить возможности лечения ФСГС это заболевание стали классифицировать как форму нефрита, плохо поддающуюся терапии. И даже сейчас, несмотря на определенные достижения, ФСГС по-прежнему рассматривается как один из наиболее резистентных к лечению и прогностически неблагоприятных вариантов гломерулонефрита.
Результаты большого числа клинических исследований 1980 — 1990-х годов, которые включают и контролируемые клинические испытания, позволили сформулировать ряд требований к лечению больных ФСГС.
- Длительное лечение большими дозами иммунодепрессантов — более длительное, чем при «минимальных изменениях» и многих других формах гломерулонефрита. В начале заболевания основным препаратом выбора является преднизолон, который в больших дозах (60 мг в сутки) применяется в течение 4 — 6 месяцев. Только после этого больной ФСГС может быть признан резистентным к стероидной терапии. У ответивших на лечение прогноз становится благоприятным (10-летняя почечная выживаемость возрастает с 58 до 86%). У части ответивших на терапию больных, как и при «минимальных изменениях», наблюдаются рецидивы нефротического синдрома и кортикостероидная зависимость.
- Резистентным к стероидам больным назначают циклоспорин (5 мг/кг), вызывающий ремиссию у 30 — 40% из них. Еще более эффективен циклоспорин у стероидозависимых больных. Однако вероятность рецидива после отмены препарата или развития циклоспориновой зависимости (напоминающей стероидную зависимость) при снижении дозы очень высока. Ремиссия может поддерживаться длительным приемом циклоспорина, но продолжительность лечения оказывается ограничена из-за нефротоксичности препарата — способности вызывать интерстициальный фиброз с прогрессирующим ухудшением функции почек.
- Альтернативой циклоспорину являются алкилирующие препараты (циклофосфамид и хлорбутин), вызывающие у больных ФСГС (30% стероидорезистентных и 70% стероидозависимых) длительную стойкую ремиссию.
Наши собственные исследования подтверждают необходимость длительной терапии большими дозами иммунодепрессантов у пациентов с ФСГС: назначение высоких кумулятивных доз различных иммунодепрессантов (кортикостероидов, циклофосфамида, азатиоприна) сопровождалось увеличением частоты ремиссий (Шилов Е. М., Тареева И. Е. и др. // Терапевтический архив, 2000, № 6, в печати). Важно подчеркнуть, что высокие кумулятивные дозы иммунодепрессантов позволяли достичь ремиссии даже у больных с факторами резистентности к лечению (выраженной гематурией, высокой морфологической активностью почечного воспалительного процесса и склеротическими изменениями). В ходе ретроспективного исследования, в котором приняли участие 72 пациента с первичным ФСГС, было получено еще одно подтверждение преимуществ применения с самого начала болезни комбинированной терапии кортикостероидами и цитостатическими препаратами. Положительный ответ (полные или частичные ремиссии) при лечении только кортикостероидами наблюдался у 32% больных, а при комбинированном лечении — у 72% пациентов. Еще более впечатляющими оказались отдаленные результаты лечения: «почечная выживаемость» больных (креатинин
Источник
Гломерулонефрит хронический — симптомы и лечение
Что такое гломерулонефрит хронический? Причины возникновения, диагностику и методы лечения разберем в статье доктора Болгарова О. Г., педиатра со стажем в 11 лет.
Определение болезни. Причины заболевания
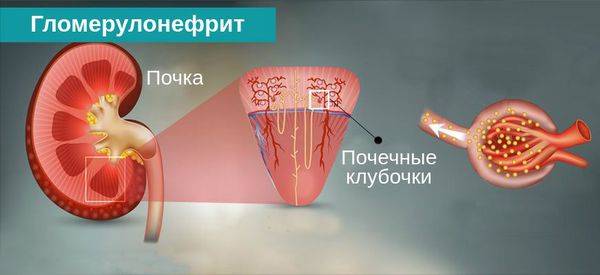
Гломерулонефрит — это двустороннее диффузное иммунное воспалительное заболевание почек, при котором в первую очередь поражаются их клубочки — гломерулы.
Хронический гломерулонефрит включает в себя группу различных заболеваний почек, отличных по своей причине, морфологической структуре и подходам к лечению, но объединённых первичным поражением гломерулов. [3]
В России заболеваемость хроническим гломерулонефритом достигает 13–50 случаев на 10 000 населения. Данные патологии чаще наблюдаются у мужчин. Они могут развиться в любом возрасте, однако наиболее часто возникают у детей 3–7 лет и взрослых 20–40 лет. [17]
На заболеваемость гломерулонефритом влияют популяционные, климатические и социально-экономические факторы. Так, фокально-сегментарный гломерулосклероз чаще встречается у афроамериканцев, ИГА-нефропатия более распространена на азиатском континенте, инфекционно-зависимые гломерулонефриты — в тропиках и развивающихся странах. [16]
Причины возникновения хронического гломерулонефрита зачастую неизвестны. В развитии части болезней установлена роль бактериальной и вирусой инфекции, в частности вирусов гепатита В и С, ВИЧ-инфекции, вирусов кори и Эпштейна — Барра. По существу, каждая редкая и новая инфекция может вызвать гломерулонефрит. [3] Также на появление хронического гломерулонефрита оказывают влияние лекарственные препараты, опухоли и другие внешние и внутренние факторы. [2]
Симптомы хронического гломерулонефрита
Первые клинические проявления хронического гломерулонефрита могут быть скудными, поэтому зачастую болезнь подкрадывается незаметно. В этом случае заподозрить заболевание можно только по изменению состава мочи: появление в ней белка (протеинурия) и изменение мочевого осадка — появление эритроцитов и лейкоцитов в моче.
Иногда болезнь дебютирует как острый нефрит. В таком случае она проявляется несколькими синдромами:
- нефритический синдром — связан с воспалением почек и проявляется гематурией (наличием крови в моче), протеинурией более 3 г/сутки, артериальной гипертонией, возникающей из-за задержки натрия, олигурией (уменьшением объёма выделяемой мочи) и снижением скорости клубочковой фильтрации;
- нефротический синдром — сочетание таких симптомов поражения почек, как массивная протеинурия более 3,5 г/сутки, отёки, дислипидемия, гипопротеинемия и гипоальбуминемия;
- мочевой синдром — включает изменения в анализах мочи, не укладывающиеся в рамки основных синдромов.
Сочетание нефротического и нефритического синдрома является наиболее неблагоприятным вариантом.
Помимо данных проявлений для гломерулонефрита характерны следующие симптомы:
- болезненные ощущения в поясничной области;
- повышение артериального давления;
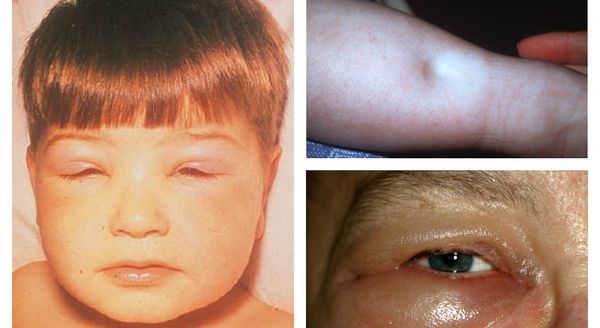
- отёки;
- суставные боли;
- слабость;
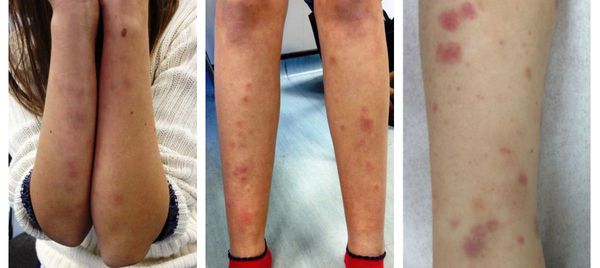
- кожная сыпь.
Все формы хронического гломерулонефрита способны периодически обостряться, при этом клиническая картина напоминает или полностью повторяет проявления острой формы заболевания. При подостром или быстро прогрессирующем гломерулонефрите функции почек снижаются на 50% меньше чем за три месяца.
Патогенез хронического гломерулонефрита
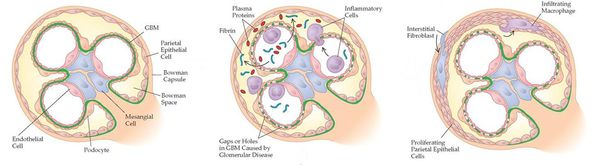
Инфекционные и другие стимулы способствуют появлению иммунного ответа с формированием и отложением антител и/или иммунных комплексов в клубочках почек (или их образованием сразу в клубочках), а также усилению клеточно-опосредованной иммунной реакции. В ответ на возникающие иммунные нарушения в почечных клубочках развиваются изменения, претерпевающие ряд стадий. Сегодня с достаточной уверенностью можно говорить о конкретных механизмах только некоторых из них.
Начало иммуновоспалительного процесса связано с активацией медиаторов тканевого повреждения, прежде всего с активацией хемотаксических факторов, способствующих миграции лейкоцитов. Одновременно активируются факторы коагуляции (сгущения), в результате чего образуются депозиты фибрина и происходит выброс факторов роста и цитокинов — гормоноподобных веществ, вырабатываемых клетками иммунной системы.
На первых этапах заболевания иммунное воспаление преобладает. Поэтому чем раньше начато иммуносупрессивное лечение, тем лучше прогноз заболевания. При стихании воспалительного процесса на первый план выходят неиммунные механизмы прогрессирования болезни:
- гиперфильтрация — неизменённые клубочки работают с повышенной нагрузкой;
- внутриклубочковая и артериальная гипертензия;
- нарушения липидного обмена и свёртывания крови;
- гиперурикемия — увеличение концентрации мочевой кислоты в крови.
При дальнейшем прогрессировании заболевания происходят вторичные изменения: процесс распространяется на другие структуры почки — канальцы и интерстиций (вид соединительной ткани).
Исход воспаления — фиброз и склероз почечной ткани, т. е. потеря почечной функции.
Классификация и стадии развития хронического гломерулонефрита
По причинам возникновения гломерулонефриты делятся на две группы:
- Первичные (идиопатические) — когда причины возникновения неизвестны.
- Вторичные — когда причины развития заболевания обусловлены:
- системными аутоиммунными заболеваниями (системной красной волчанкой, АНЦА-ассоциированными и геморрагическими васкулитами, ревматоидным артритом);
- поражениями почек в рамках паранеопластического синдрома (опухолей и лимфом) — эти гломерулонефриты устойчивы к стандартной терапии, поэтому прогноз может быть улучшен (вплоть до полного выздоровления) при полном удалении опухоли;
- инфекциями (инфекционным эндокардитом, вирусами гепатита В и С, ВИЧ-инфекцией, вирусом Эпштейна — Барра и другими);
- лекарственными болезнями (аутоиммунной реакцией на фармокологические и биологические препараты).
По клиническим проявлениям выделяют пять форм заболевания:
- Нефротическая — возникает чаще всего, сопровождается выраженными отёками (возможно скопление невоспалительной жидкости в грудной и брюшной полости, околосердечной сумке, а также отёк кожи), массивной протеинурией (более 5 г/л у взрослых и 3 г/л у детей), цилиндрурией, гипопротеинемией и дизлипидемией.
- Гипертоническая — количественные и качественные изменения мочи менее выражены по сравнению с длительным синдромом артериальной гипертензии, при котором артериальное давление повышается до 180/100-200/120 мм рт. ст. и сопровождается в течение дня серьёзными колебаниями показателей по разным причинам.
- Гематурическая (болезнь Берже) — среди прочих симптомов заболевания преобладает наличие крови в моче, причём как визуальное (заметное глазу), так и лабораторное, при котором отмечается значительное или упорное присутствие эритроцитов в осадке мочи. Данная форма чаще возникает у молодых мужчин.
- Латентная — возникает довольно часто. В связи с неявными симптомами может существовать на протяжении 10-20 лет и дольше, но в итоге всё равно приводит к уремии. Человек обычно чувствует себя удовлетворительно, возможен слабо выраженный мочевой синдром, отёки и артериальная гипертензия не наблюдаются. Из лабораторных показателей можно обнаружить протеинурию (не более 1-2 г/сутки), небольшое количество эритроцитов и цилиндров в моче, тонких, желтоватых, переплетающихся нити фибрина, удельный вес мочи в норме.
- Смешанная — включает в себя проявления нефротической и гипертонической форм.
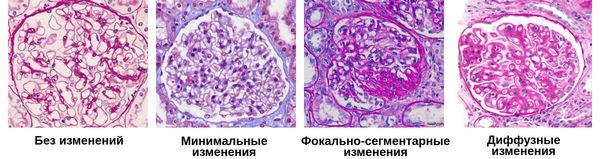
По морфологическим изменениям выделяют три хронических гломерулонефритов:
- Минимальные — на микроскопиеском уровне изменений практически нет, возможно только различить слияние ножек подоцитов, покрывающих капилляры почечных клубочков.
- Фокально-сегментарные — под микроскопом можно обнаружить не только слияние подоцитов, но и склероз и дистрофию некоторых клубочковых петель.
- Диффузные — увеличение количества клеток в клубочках почек:
- мезангиопролиферативные;
- мезангиокапиллярные. [4]
Осложнения хронического гломерулонефрита
Гломерулонефрит может осложниться инфекцией, в том числе связанной с иммунодепрессивной терапией (пиелонефрит, туберкулёз), нарушениями фосфорнокальциевого гомеостаза и остеопорозом. Причиной тому — острый воспалительный процесс или же осложнения иммунносупрессивной терапии.
Осложнения нефротической формы хронического гломерулонефрита:
- нефротический криз — самое грозное осложнение;
- внутрисосудистое свёртывание крови (ДВС-синдром);
- тромбозы вен, в том числе почечных;
- рожеподобные изменения кожи, появление которых сопровождается повышением температуры и усилением симптомов интоксикации.
Нефротический криз возникает внезапно. Его развитие может спровоцировать активная диуретическая терапия. К характерным проявлениям относятся интенсивные боли в животе, перитонитоподобный синдром, повышенная температура тела. В дальнейшем это осложнение может привести к развитию гиповолемического шока и смерти. [15]
Частые осложнения гипертонической форм связаны с гипертрофией миокарда левого желудочка (сердечная астма, отёк лёгких). Также может возникнуть острая сердечная недостаточность. [1]
Диагностика хронического гломерулонефрита
Для диагностики гломерулонефритов прежде нужно исключить целый ряд заболеваний со схожими симптомами:
- протеинурию;
- диабетическую нефропатию;
- гипертоническую болезнь с поражением почек;
- амилоидоз почек (нарушение белково-углеводного обмена в почках);
- миеломную нефропатию;
- наследственные нефропатии. [1][2]
Лабораторное или визуальное наличие крови в моче требует исключения других урологических проблем, опухолей, феномена сдавления левой почечной вены у детей, наследственных заболеваний почек — болезни тонких мембран, синдрома Альпорта (наследственного нефрита).
Для дифференциальной диагностики с системными заболеваниями необходимо исследовать их маркеры в крови:
- при системной красной волчанке — антинуклеарные антитела, волчаночный антикоагулянт, Д-димер;
- при антифосфолипидном синдроме — антитела к кардиолипину и бетта-2-гликопротеину; [1]
- при АНЦА-васкулите — антитела к цитоплазме нейтрофилов двух классов. [13]
При обострении любой формы хронического нефрита скорость оседания эритроцитов увеличивается, а также уровень иммунологических показателей, сиаловых кислот, фибрина и серомукоида в крови. При развитии хронической почечной недостаточности независимо от формы хронического нефрита уровень креатинина и мочевины в крови увеличивается. [1] [11]
Основные аспекты диагностики гломерулонефритов:
- изменения в анализах мочи — прежде всего протеинурия, гематурия ицилиндрурия;
- биохимический анализ крови — гипопротеинэмия, гипоальбуминемия, диспротеинемия, повышение альфа-2-глобулина, гаммаглобулина, креатинина и азотистых шлаков, уровня сахара и липидного спектра, гиперхолестеринэмия, дизлипидемия, гиперурикемия.
- УЗИ-почек — увеличение или уменьшение размера почек, истончение и гиперэхогенность паренхимы, нарушение кортико-медуллярной дифференциации;
- КТ и МРТ с контрастированием для исключения урологических проблем.
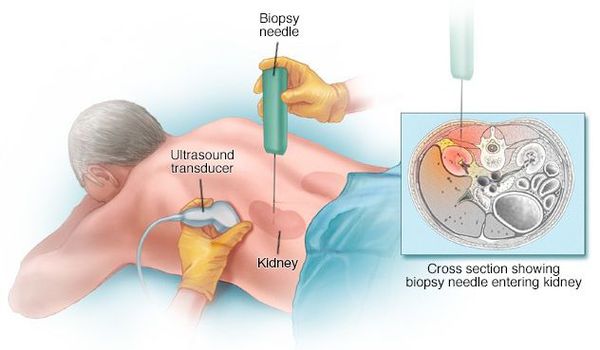
Постановка диагноза многих гломерулярных заболеваний невозможна без пункционной биопсии почки.
Показания к биопсии:
- наличие стероидрезистентного нефротического синдрома;
- признаки острого нефритического синдрома с почечной недостаточностью;
- подозрение на быстро прогрессирующий гломерулонефрит или хронический интерстициальный нефрит;
- заболевания с одновременным нарушением различных систем организма, включая почки (системная красная волчанка, геморрагический васкулит);
- длительная изолированная протеинурия или гематурия.
Противопоказания к биопсии:
- часто рецидивирующи нефротически синдром (исключение — подозрение на нефротоксичность, связанную с циклоспорином А);
- наличие только одной почти в организме (не строгое противопоказание);
- нарушение свертывания крови;
- бесконтрольная артериальная гипертензия;
- запущенные стадии формирования нефросклероза;
- терминальная почечная недостаточность.
Биопсию проводит опытный нефролог или хирург в условиях стационара. Сама процедура длится примерно 15-20 минут. Осложнения при биопсии возникают редко, кровотечение возможно всего в 5-10% случаев. [5]
Проведение биопсии почки и верификация морфологического варианта поражения почек показаны даже в тех случаях, когда имеется связь макро- гематурии с ангиной и напрашивается диагноз «острый гломерулонефрит». Исследования показали, что под маской острого «постстрептококкового» гломерулонефрита могут скрываться такие тяжёлые поражения почек, как экстракапиллярный гломерулонефрит, исход и прогноз которого зависят от своевременного начала лечения. [6]
Лечение хронического гломерулонефрита
Лечение хронических гломерулонефритов сводится к трём целям:
- подавление иммунных реакций;
- снижение темпа прогрессирования патологии;
- предупреждение появления хронической почечной недостаточности.
Этиотропная терапия проводится только при выявленной причине хронического гломерулонефрита, например, при лептоспирозе, БГСА-инфекции, вирусных гепатитах, ВИЧ-инфекции и других). В подобных случаях применяются антибиотики и противовирусные препараты.
Иммуносупрессивная терапия включает применение следующих лекарств:
- Глюкокортикостероидные препараты (ГКС). Одним из первых показаний к их применению был изолированный нефротический синдром у детей при болезни минимальных изменений. Эти препараты обладают мощным противовоспалительным и иммуносупрессивным действием, применяются в том числе для лечения аутоиммунных заболеваний почек. В последние годы были выяснены принципиально новые эффекты ГКС, в частности их защитное влияние на гломерулярные клетки — подоциты. [9]
Однако ГКС имеют множество побочных эффектов. Поэтому их стараются назначать коротким курсом в больших дозах, постепенно переходя на поддерживающую терапию минимальными дозам.
- Цитостатики. В настоящее время такой цитостатик, как циклоспорина А, является признанным методом лечения нефротических вариантов гломерулонефритов, в основе которых лежит повреждение подоцитов. При болезни минимальных изменений, фокально-сегментарном гломерулосклерозе и мембранозном гломерулонефрите данный препарат чаще всего используется в комбинации с ГКС. [7][8]
У пациентов со стероидрезистентным фокально-сегментарным гломерулосклерозом и непереносимостью циклоспорина предлагается применение другого цитостатика — микофенолата мофетила в комбинации с высокими дозами дексаметазона. [2]
- Моноклональные антитела. Использование препаратов на этой основе является новым направлением лечения хронических гломерулонефритов. Например, ритуксимаб считается эффективным препаратом. Он имеет меньше токсичных побочных эффектов и при некоторых формах заболевания позволяет добиться ремиссии. [14]
Одна из методик лечения резистентных к стандартной терапии форм является пульс-терапия — высокодозное введение лекарств коротким курсом. [12] Такой способ эффективно купирует обострения гломерулонефритов и относительно хорошо переносится пациентами.
Как правило, пульс-терапия проводится с использованием метилпреднизолонома, циклофосфамида или обоих препаратов:
- пульс-терапия метилпреднизолоном проводится 2–3 дня, после чего курс повторяются ещё 3–4 раза с перерывом в 10 дней;
- пульс-терапия циклофосфамидом проводится раз в четыре недели с повторением от 6 до 12–14 раз.
В последние десятилетия для торможения прогрессирования хронического гломерулонефрита применяется нефропротективная стратегия лечения. Так как при стихании иммунно-воспалительного процесса на первый план выходят неиммунные факторы прогрессирования заболевания (прежде всего гемодинамические), а также обменные (гиперлипидемия, дислипидемия, гиперурикемия) и коагуляционные, применяются ингибиторы АПФ и блокаторы рецепторов ангиотензина. Эти препараты восстанавливают системную и внутриклубочковую микроциркуляцию, обладают противовоспалительным и цитопротективным действием (защита клеток от вредных факторов). Они применяются для лечения всех форм гломерулонефритов и замедляют прогрессирование болезни. При некоторых формах латентных и гематурических вариантов заболевания, когда не показано иммуносупрессивное лечение, они являются препаратами выбора.
Плазмаферез (способ очищения крови) применяется для лечения быстро прогрессирующего гломерулонефрита, а также нефритов, протекающих на фоне системных заболеваний.
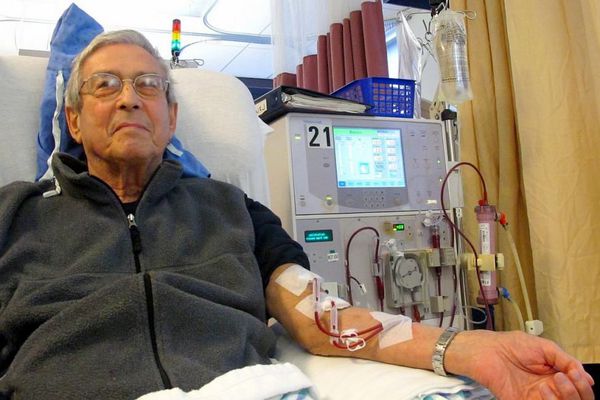
Гемосорбция и гемодиализ (способы внепочечного очищения крови) относятся к методам заместительной почечной терапии. К ним прибегают во время острого периода почечной недостаточности.
Посиндромная терапия диуретиками, антикоагулянтами, дезагрегантами, антигипертензивными препаратами, статинами, гиперлипидемическими и другими средствами проводится по показаниям. Также уделяется внимание устранению очагов хронической инфекции, лечению кариеса, профилактике вирусных инфекций, на фоне которых чаще всего возникают обострения заболевания.
При лечении нефротического синдрома у детей показана инициальная терапия в течение 4-6 недель, а также приём преднизолона, доза которого со временем снижается до поддерживающей. При благоприятном течении болезни преднизолон постепенно отменяют. В случае выявления стероидзависимости (когда на фоне снижения дозы преднизолона возникает рецидив заболевания) используются алкилирующие препараты — циклофосфамид или хлорамбуцил, а также применяется левамизол, микофенолат мофетил или такролимус.
Прогноз. Профилактика
Течение хронического гломерулонефрита зависит от причины заболевания и морфологической формы. Наиболее неблагоприятным является подострый быстро прогрессирующий вариант.
Без лечения все формы гломерулонефрита заканчиваются хронической почечной недостаточностью, разница заключается лишь в срок её наступления. А осложенения ухудшают и без того тяжёлый прогноз заболевания.
Смерть при гломерулонефрите может наступить в результате развития отёка легких, нефротического синдрома, инсульта, острой почечной недостаточности, гиповолемического шока и венозных тромбозов. Летальность при хроническом гломерулонефрите на III-V стадиях хронической болезни почек связана с сердечно-сосудистыми патологиями. [17]
Всем пациентам с хроническим гломерулонефритом важно помнить о следующих мерах профилактики обострения заболевания:
- контролирование баланса жидкости;
- соблюдение режима питания;
- отказ от курения;
- регулярное измерение артериального давления;
- недопущение переохлаждений, стрессовых ситуаций, чрезмерных физических нагрузок. [17]
Источник